急性発作時の所見
眼圧:40〜80 mmHgの急激かつ著しい上昇1)2)
角膜:実質浮腫、微小嚢胞状浮腫
結膜:強い毛様体・結膜充血
前房:中心はやや浅く、周辺部は高度に浅い
瞳孔:中等度散瞳で固定し、対光反射は減弱・消失
隅角:広範な虹彩線維柱帯接触による閉塞
水晶体:緑内障斑(glaukomflecken、水晶体前嚢下の虚血性壊死)。過去の発作を示唆する所見2)

原発閉塞隅角緑内障(primary angle closure glaucoma:PACG)は、他の要因なく遺伝的背景や加齢による前眼部形態の変化で惹起される原発性の隅角閉塞により眼圧上昇をきたし、すでに緑内障性視神経症を生じている疾患である1)。原発閉塞隅角症(primary angle closure:PAC)は、原発隅角閉塞によって眼圧上昇をきたしているか、または周辺虹彩前癒着(peripheral anterior synechia:PAS)を生じているが、緑内障性視神経症は生じていない状態である1)。原発閉塞隅角症疑い(primary angle closure suspect:PACS)は、原発性の隅角閉塞はあるが、眼圧上昇や器質的なPASはなく、緑内障性視神経症も生じていない状態を指す1)。
これら3つの病期と、急性に発症する急性原発閉塞隅角緑内障(acute PACG)・急性原発閉塞隅角症(acute PAC)を包含する総称として、原発閉塞隅角病(primary angle closure disease:PACD)という用語が用いられる1)2)。PACD という総称を用いる意義は、同一個人の病態が進行段階に応じて PACS から PAC、さらに PACG へと移行しうる連続的スペクトラムであることを強調し、切れ目のないフォローアップと早期介入を促す点にある1)2)。
隅角鏡による診断基準は以下のとおりである2)12)。
| 病期 | 180度以上の虹彩線維柱帯接触(ITC) | 眼圧上昇または PAS | 緑内障性視神経症 |
|---|---|---|---|
| PACS | あり | なし | なし |
| PAC | あり | あり | なし |
| PACG | あり | あり | あり |
2002年の Foster 分類では ITC が3象限(270度)以上を PACS と定義していたが、現在は 2021年 以降の米国 Preferred Practice Pattern 分類を踏襲し、180度以上の ITC を基準とする2)12)。
PACG・PAC には急性発症型と慢性型がある。急性原発閉塞隅角緑内障・急性原発閉塞隅角症では、眼圧がしばしば40〜80 mmHg の著しい高値となり、視力低下、霧視、虹視症、眼痛、頭痛、悪心、嘔吐、対光反射の減弱・消失などの症状を呈する1)2)。一方、慢性原発閉塞隅角緑内障(chronic angle closure glaucoma:CACG)は急性眼圧上昇の既往を持たず、20〜30 mmHg程度の中等度眼圧上昇が緩徐に進行する1)。
多治見スタディでは40歳以上の PACS が0.2%、PAC が0.5%、PACG が0.6% と報告されている13)。別の日本人集団では40歳以上の PACG 有病率を0.34〜0.6% とする報告がある2)。世界では40歳以上の約0.7% が閉塞隅角緑内障を有し、2013年時点で2,020万人、うち1,550万人がアジアに集中すると推定される2)11)。2040年には罹患者数が約50%増加して3,200万人に達し、500万人以上が失明する可能性が指摘されている2)。
民族差は顕著で、イヌイット系では2.5〜3.8%、台湾では3.0%、中国広州で1.5%、北京で1.2%、シンガポールで1.1%、モンゴルで1.4%、タイで0.9%、南インドで0.5〜0.87%、バングラデシュで0.4% と報告される2)。ヨーロッパ系では0〜0.6% と低い2)。アジア系では PACG が原発開放隅角緑内障(POAG)と同等の頻度を占める地域もある2)11)。PACG は POAG と比較して初診時の片眼失明率が高く、両眼重度視力障害リスクが約3倍に上る2)。
また、PACG の発症年齢は POAG より高い傾向にあり、50歳以上の女性で顕著に発症リスクが増加する2)。PACG・POAG の性別比をみると、POAG は男女差が軽微なのに対し、PACG は女性が男性の2〜4倍である2)。女性では男性より前房深度が浅く、眼軸長が短い傾向が観察されており、解剖学的素因として寄与している2)。日本では高齢化に伴い PACG 患者の絶対数が増加することが予想され、診療体制の整備と一次医療における狭隅角スクリーニングの強化が課題となる2)11)。
すべての PACS に対して一律にレーザー治療が必要というわけではない。中国中山での Zhongshan Angle Closure Prevention 試験(ZAP 試験)では、未治療の PACS 眼から PAC または急性発作への進行は6年で約4%、14年で約12% に留まり、予防的レーザー虹彩切開術による相対リスク低下は6年で47%、14年で70% だが絶対的利益は小さいと報告された3)。シンガポールの ANA-LIS 試験でも5年進行率は9.4%、LPI によるリスク低下は45% と同様の傾向を示した4)。これらの結果を踏まえ、欧州緑内障学会ガイドライン第6版は健常な PACS 眼へのルーチンな LPI を推奨せず、高度遠視・頻回散瞳が必要な症例・医療アクセス困難例など高リスク例のみに LPI を考慮すべきとしている5)。緑内障診療ガイドライン第5版も、暗室試験やうつむき試験の陽性例、定期検査が困難な例、急性発作時に速やかに受診できない例、家族歴陽性例、糖尿病網膜症などで頻繁に散瞳を要する例を手術適応としている1)。
PACS と慢性 PACG では自覚症状に乏しく、末期になって視力低下や視野欠損を自覚することが多い1)2)。慢性期には眼圧上昇が緩徐であるため、患者自身が気づかないうちに視神経障害が進行してしまう例も少なくない1)。また、軽度の瞳孔ブロックによる短時間の眼圧上昇(間欠性隅角閉塞)では、暗所でのかすみや軽い頭重感といった曖昧な症状を繰り返すことがあり、問診で拾い上げることが重要である2)。
一方、急性発作時には症状が劇的である。視力低下、霧視、虹視症(光の周りのハロー)、強い眼痛と同側の頭痛、悪心・嘔吐の迷走神経症状などを呈する1)2)。虹視症は角膜浮腫による光の屈折異常が原因で、電球や街灯の周りに色付きの輪が見える症状である。頭痛や嘔気が前面に立ち、神経内科や消化器内科に紛れ込むこともあるため、原因不明の強い頭痛で眼症状を伴う患者では必ず眼科的評価が必要である2)7)。また症状に乏しい急性発作(subacute attack)も存在し、明確な疼痛を欠いたまま高眼圧が持続して視神経障害が進行する場合があるため、眼底と隅角の評価を怠らない1)2)。
急性発作時の所見
眼圧:40〜80 mmHgの急激かつ著しい上昇1)2)
角膜:実質浮腫、微小嚢胞状浮腫
結膜:強い毛様体・結膜充血
前房:中心はやや浅く、周辺部は高度に浅い
瞳孔:中等度散瞳で固定し、対光反射は減弱・消失
隅角:広範な虹彩線維柱帯接触による閉塞
水晶体:緑内障斑(glaukomflecken、水晶体前嚢下の虚血性壊死)。過去の発作を示唆する所見2)
慢性PACGの所見
プラトー虹彩の所見
PACG は遺伝的・解剖学的素因の上に加齢変化が加わって発症する1)2)。主要なリスク因子を以下に示す。
| カテゴリ | 因子 | 概要 |
|---|---|---|
| 屈折 | 遠視 | 短眼軸に伴う浅前房1)2) |
| 解剖 | 短眼軸長 | 軸長20 mm未満のnanophthalmos では極めて高リスク2) |
| 解剖 | 浅前房 | 中心前房深度2.0〜2.2 mm未満は高リスク2) |
| 解剖 | 水晶体厚・前方位置 | 加齢とともに増加し瞳孔ブロックを助長1)2)10) |
| 解剖 | 小角膜径 | 水平径11 mm未満でリスク上昇2) |
| 年齢 | 50歳以上 | 高齢ほど有病率が増加1)2) |
| 性別 | 女性 | 男性より好発1)2) |
| 民族 | アジア系・イヌイット系 | 地域によりヨーロッパ系の数倍から数十倍2)11) |
| 家族歴 | 一親等に PACD 家族歴あり | 遺伝的素因2) |
| 誘発薬剤 | 抗コリン薬・散瞳薬・交感神経刺激薬 | 胃内視鏡前薬剤、睡眠薬、抗精神病薬、風邪薬、三環系抗うつ薬、SSRI、鼻炎用噴霧薬、一部吸入薬など2)7) |
原発閉塞隅角緑内障および原発閉塞隅角症の成因は、単一機序ではなく複数の機序が複合的に関与することが多い1)2)10)。
急性発作の引き金となる生活上の要因としては、暗所での読書や映画鑑賞、長時間の俯き姿勢(庭仕事、手術、長距離運転)、夜間の自然散瞳、抗コリン作用を有する薬剤の内服・吸入・点鼻、散瞳検査の影響、強いストレスなどが知られている2)7)。特に高齢女性の胃内視鏡検査前投薬、精神科薬剤、パーキンソン病治療薬、喘息・慢性閉塞性肺疾患(COPD)に対する抗コリン系吸入薬は見落とされやすく、処方医との連携が重要である2)7)。PAC 素因のある患者には、市販の総合感冒薬・鼻炎薬・乗り物酔い止め・抗ヒスタミン薬の使用前に眼科相談を行うよう指導する2)。また、50歳以上の遠視眼患者が白内障手術を先延ばしにしていると、加齢性水晶体厚増加とともに発作リスクが上昇するため、白内障手術の適応判断そのものが予防的介入となりうる6)10)。
隅角鏡検査は原発閉塞隅角病の診断における最重要検査であり、ゴールドスタンダードである1)2)5)。点眼麻酔後、まず第1眼位で圧迫を加えず、短く細いスリット光により静的隅角鏡検査を行う。瞳孔がスリット光で収縮しないよう注意して、隅角底の解剖学的構造(Schwalbe線・線維柱帯・強膜岬・毛様体帯)と微小PAS、隅角色素沈着を評価する2)。次に動的・圧迫隅角鏡検査により機能的閉塞と器質的閉塞(PAS)を鑑別する。Shaffer-Kanski 分類で2度以下(隅角20度以下)は隅角閉塞の可能性があり、1度以下では閉塞の危険が高い。
細隙灯顕微鏡のみで行える簡便なスクリーニング法で、耳側角膜輪部に60度角からスリット光を当て、周辺前房深度と角膜厚の比で評価する。角膜厚の1/4 以下(Grade 1〜2)では隅角閉塞の可能性が高く、必ず隅角鏡検査を追加する2)。
| 検査 | 特徴 | PACDでの役割 |
|---|---|---|
| 前眼部OCT | 非接触、短時間、4象限一度に撮影。AOD500・angle recess area・ITC index などを定量評価2) | 隅角閉塞の客観的定量、経過比較、暗所/明所での動的評価 |
| 超音波生体顕微鏡(UBM) | 接触式、組織深達度高く毛様体まで観察可能2)14) | プラトー虹彩の診断(毛様体前方偏位・毛様溝消失)、悪性緑内障の鑑別 |
| 全周隅角カメラ | 16面マルチミラーで360度同時撮影 | 隅角色情報のスクリーニング・フォロー |
| 眼軸長測定 | 軸長20 mm未満でnanophthalmos、水平角膜径11 mm未満で相対的前眼部マイクロフタルモス2) | 高リスク眼の同定、手術計画立案 |
| 角膜内皮細胞検査 | スペキュラマイクロスコープ | 発作眼の内皮細胞減少評価、LPI安全性判断 |
前眼部OCTは非接触で迅速に定量評価でき、縦断的な進行予測にも利用される。CASIA2 の STAR Analysis では AOD500 を360度自動解析でき、狭隅角スクリーニングに有用である2)。一方で色情報や器質的閉塞の判別は困難なため、隅角鏡検査を置換する検査ではなく補完的位置づけである2)5)。UBM は接触式で時間を要するが、毛様体と虹彩後面の解析で前眼部OCT を上回り、プラトー虹彩の確定診断には不可欠である2)14)。
暗室試験・うつむき試験・散瞳試験などの負荷試験は検出力に限界があり、ZAP 試験では暗室うつむき試験で進行リスク群を抽出できなかったと報告されている3)。従って診断は臨床所見・隅角所見・画像所見の総合評価で行う。
鑑別診断として以下を常に念頭に置く1)2)。
両眼性が原則の PACD に対し、他眼で深前房・広隅角が確認される場合は続発性を強く疑う2)7)。特に片眼性の急性発作で水晶体亜脱臼や外傷歴がある場合は外傷性水晶体脱臼、若年者で両眼性急性発作の場合はトピラマートなどのスルホンアミド誘発性を鑑別に挙げる2)。新生血管緑内障では虹彩ルベオーシスと後眼部疾患(糖尿病網膜症、網膜中心静脈閉塞症など)の既往を確認する1)。
PACG の診断には緑内障性視神経症の証明が必須である1)2)。急性期には角膜浮腫のため詳細な眼底観察が困難だが、間接検眼鏡や前眼部OCT ではなく網膜・視神経OCT を用いると、散瞳せず視神経乳頭・網膜神経線維層(RNFL)・黄斑部網膜神経節細胞複合体(GCC)の評価が可能である2)。発作時の RNFL は軸索腫脹のため一時的に肥厚し、1ヶ月後に正常値、3ヶ月後に菲薄化の順で変化するため、経時的評価が必要である2)。視野検査は発作鎮静後に Humphrey 24-2 SITA または同等の自動静的量的視野検査で施行し、POAG と同様の方法で進行を追跡する1)5)。
前眼部OCTは非接触で短時間に360度の隅角を定量評価でき、外来スクリーニングや経時比較に適する。CASIA2 の STAR Analysis では 16 方向の断面から AOD500 を自動解析し、ITC 領域をカラーマップ表示することが可能である2)。一方 UBM は接触式で時間を要するが、超音波のため毛様体や虹彩後面の構造を描出でき、毛様体の前方偏位や毛様溝消失を特徴とするプラトー虹彩の診断に不可欠である2)14)。悪性緑内障や毛様体腫瘍、水晶体後方の器質的病変が疑われる際も UBM が第一選択となる。実臨床では前眼部OCT をスクリーニングと経時評価に、UBM を毛様体評価・プラトー虹彩確定・鑑別診断に用いるのが一般的である2)5)。
治療目標は、隅角閉塞の解除、眼圧の長期コントロール、および視神経障害の予防である1)2)5)。病期(PACS/PAC/PACG)と急性・慢性の別により治療戦略が異なる。
PACS のほとんどは PAC・PACG に進行しないが、一定割合で進行するため、リスクに応じた管理が推奨される1)2)3)。
| リスク | 推奨される管理 |
|---|---|
| 低リスク(高齢女性以外、家族歴なし、医療アクセス良好) | 経過観察2)3)5) |
| 中〜高リスク(高度遠視、PACG家族歴、頻繁な散瞳必要、医療アクセス困難、抗コリン薬常用) | LPI を考慮1)2)5) |
| 白内障合併例 | 水晶体摘出も選択肢1)6) |
リスクのある例では抗コリン作用を持つ市販薬・鼻炎薬・睡眠補助薬・乗物酔い薬などで急性発作が誘発されうるため、患者教育と症状時の緊急受診指示が重要である2)7)。
緑内障診療ガイドライン第5版は、レーザー虹彩切開術あるいは水晶体摘出術による瞳孔ブロック解除を第一選択としている(推奨度1A)1)。ほとんどの例が両眼性であるため、片眼に PACG・PAC がみられた場合は他眼の狭隅角に対しても予防的 LPI(1A)あるいは水晶体摘出術(1A)を行う1)。
EAGLE(Effectiveness in Angle-Closure Glaucoma of Lens Extraction)試験は、英国を中心とする多施設共同の無作為化比較試験で、50歳以上の症候性 PAC(眼圧30 mmHg以上)または PACG 計419例を早期透明水晶体摘出(clear lens extraction:CLE)と LPI に割付けた6)。3年時点で QoL 指標(EQ-5D)、眼圧コントロール、追加治療の必要性いずれも CLE 群が優れ、薬剤なしで目標眼圧を維持できる確率は CLE 群が LPI 群の約10倍に達した6)。英国のコスト解析では3年で費用対効果良好、10年では費用節約的と推定された2)6)。これを受けて米国 AAO の Primary Angle-Closure Disease Preferred Practice Pattern も、視機能に影響を与える白内障がない症例でも、眼圧が高い PAC・PACG に対して早期水晶体摘出を初期治療の選択肢として提示している2)。欧州緑内障学会ガイドライン第6版も50歳以上の PAC・PACG に対し水晶体摘出と LPI を同等に強推奨している5)。緑内障診療ガイドライン第5版でも LPI と並ぶ第一選択として推奨度1A で明記されている1)。
急性発作は眼科救急であり、早期に眼圧を下げ瞳孔ブロックを解除することが視機能予後を決定する1)2)7)。緑内障診療ガイドライン第5版では、以下の段階的治療を推奨している1)。
初期薬物療法:
手術的治療:
緑内障診療ガイドライン第5版では、急性原発閉塞隅角緑内障・急性原発閉塞隅角症に対し水晶体再建術が第一選択として推奨されている1)。当日に緊急手術が行えない場合は、まず上記薬物療法で眼圧を下降させ、角膜透明化後に LPI を行う1)。LPI のレーザー設定例として、まず200〜400 μm、200 mW、0.2秒のアルゴンレーザーで虹彩を伸展(Stretch)し、次いで50 μm、800〜1,000 mW、0.02秒で穿孔直前まで薄くし(Thinner)、最後に Nd:YAG レーザー 2.0〜4.0 mJ で1〜2発の穿孔を加える。照射総数は角膜内皮保護の観点から100発未満が望ましい1)。角膜混濁例では観血的周辺虹彩切除術への切り替えを検討する。
アジア太平洋緑内障学会(APGS)と Academy of Asia-Pacific Professors of Ophthalmology が2025年に発表した急性原発閉塞隅角発作(APACA)に関するコンセンサスでは、従来の薬物治療のみでは発症後 50 mmHg を超える高眼圧例への効果発現が遅く、全身合併症のリスクもあるため、以下の代替治療を積極的に検討することが提案されている7)。
これらの代替治療により、従来敬遠されていた「hot and angry」な発作眼での緊急線維柱帯切除術や緊急水晶体乳化吸引術は回避することが推奨されている7)。急性発作が一旦落ち着いた後の早期水晶体乳化吸引は、網膜神経節細胞の追加的な障害を予防しうる選択肢として検討に値する7)。
対側眼の管理:
APAC 後の対側眼は予防的 LPI を行わないと5年以内に約半数が急性発作を発症しうる2)。原則として速やかに予防的 LPI を実施し、待機中は縮瞳点眼(ピロカルピン)を開始する2)7)。なお、ピロカルピンの長期投与は散瞳不良、虹彩後癒着、白内障進行、網膜剥離リスクなどを伴うため、慢性療法としては適切ではなく、LPI 実施までの橋渡しに留める2)。対側眼に予防的 LPI を行っても5〜6年で PACG を発症しうる症例が報告されており、長期フォローアップが必須である2)。
瞳孔ブロック解消後に残存する慢性眼圧上昇(残余緑内障)に対しては、原発開放隅角緑内障に準じた薬物療法、レーザー治療、観血的手術を行う1)。
プラトー虹彩では瞳孔ブロック解除のみでは眼圧コントロールが得られないことがある1)14)。
PACD の大部分は相対的瞳孔ブロックを基本機序とする1)2)。瞳孔領の虹彩-水晶体接触により、後房から前房への房水流出抵抗が上昇する。後房圧が相対的に高くなると、虹彩は前方に膨隆し、周辺部で線維柱帯をほぼ完全に覆う。これが隅角の機能的閉塞を生み出す。急性発作ではこの状態に水晶体の前方移動と虹彩実質の浮腫が加わり、瞳孔ブロックがさらに高度化して眼圧が急上昇する悪循環に陥る1)2)。
瞳孔が中等度散瞳位置にあるとき、瞳孔ブロックは最大になりやすい。暗所での読書、夜間の覚醒、抗コリン作用を持つ薬剤、俯きの姿勢などが発作の引き金となるのはこのためである2)7)。
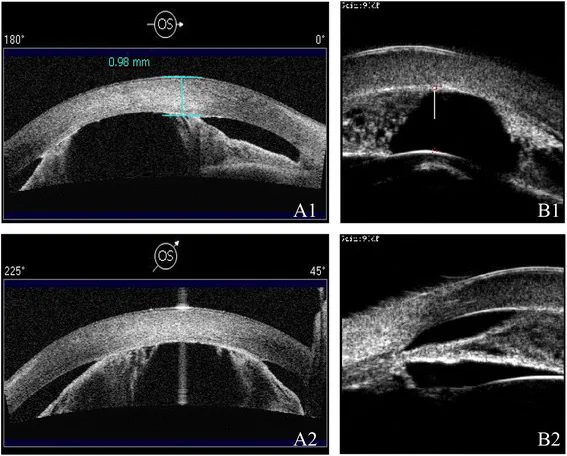
プラトー虹彩では毛様体が前方に位置し、虹彩根部を機械的に前方へ押し上げる。前房中心深度は比較的保たれているため一見正常に見えるが、散瞳時には周辺虹彩が毛様体突起に乗り上げて直接隅角を閉塞する1)14)。UBM での特徴は、毛様体の前方偏位、毛様溝の消失、厚く前方に屈曲した虹彩根部と狭い隅角底である14)。
水晶体因子は加齢性の水晶体厚増加と前方偏位によって寄与する。水晶体が厚くなると虹彩-水晶体接触面が拡大し、瞳孔ブロックを強める1)10)。また水晶体が厚いほど前房深度が浅くなり、解剖学的素因をさらに顕在化させる2)10)。水晶体摘出による隅角開大効果の理論的根拠はここにある6)10)。
長期または反復する虹彩-線維柱帯接触は線維柱帯そのものに不可逆的な機能障害を生じさせ、PAS 形成に至る1)2)。そのため瞳孔ブロックを解除しても慢性眼圧上昇が残存する例が一定割合で存在し、これを残余緑内障(residual glaucoma)と呼ぶ1)。APGS コンセンサスでは、急性発作後に LPI が成功しても最大58%の症例で慢性 PACG に移行しうると報告されている7)。線維柱帯細胞の機械的損傷、炎症メディエーターの関与、シュレム管の虚脱など複数の機序が提唱されているが、完全な病態解明には至っていない7)10)。
急性発作後の網膜神経線維層(RNFL)は、発作直後の軸索腫脹のため一過性に増厚し、約1ヶ月で正常値に戻った後、3ヶ月後には菲薄化に転じる2)。これは軸索の腫脹と続発性変性が時間的に分離して起きることを示しており、OCT による縦断評価で追跡される。未治療の APAC 例の長期転帰を4〜10年追跡した研究では、18% が法的失明に至り、58% が 20/40 未満の視力となったと報告されている2)。角膜内皮細胞密度も発作の持続時間に比例して減少し、細胞形態の多形化(変動)・多極化(大小不同)を生じる2)。高眼圧と虚血の影響は毛様体の血流にも及び、房水産生そのものが一時的に低下することで、薬物治療の反応性が悪化する場合がある7)。
急性発作時の著しい眼圧上昇は視神経乳頭と網膜への血流障害を引き起こし、発作解除後の再灌流時に酸化ストレスと炎症性サイトカインの産生が生じる7)。この虚血-再灌流障害により、眼圧が下がった後もしばらく網膜神経節細胞(RGC)の喪失が続くことが動物実験とヒトの縦断研究で示唆されている7)。この知見は、発作の眼圧を「早く」下げることの重要性を裏付けるものであり、APGS が代替治療(ALPI・LPP・ACP)による迅速な眼圧降下を推奨する理論的根拠となっている7)。
ZAP 試験はアジア人集団での大規模ランダム化試験として PACS 管理の基盤データを提供し、予防的 LPI のルーチン適応に再考を促した3)。シンガポール ANA-LIS 試験もこれを支持している4)。一方 EAGLE 試験は PAC と PACG に対する早期水晶体摘出の優位性を示し、現在の米国・欧州・日本の主要ガイドラインに採用されている1)2)5)6)。これらの成果を受け、2026年版の Primary Angle-Closure Disease Preferred Practice Pattern では水晶体摘出を PAC・PACG の有力な初期治療選択として明示している2)。
APGS/AAPPO の2025年コンセンサスでは、従来型の薬物治療単独では効果発現が遅く、高齢者や合併症を持つ患者では全身副作用のリスクもあるため、ALPI・LPP・ACP といった代替手技による迅速な眼圧降下、および発作鎮静後早期の水晶体乳化吸引を積極的に組み込む治療フローが提案されている7)。これは、発作後に RGC 損失が進行し続けうる虚血-再灌流障害を抑制する観点からも重要である7)。
前眼部OCT の縦断解析により、anterior lens vault の増加や angle width の減少が、3〜6年後の PACD 進行を予測する因子であることが報告されている2)。将来的には、これらのバイオメトリック指標を用いた個別リスク評価に基づき、LPI や水晶体摘出の適応判断が行われることが期待される。中国で行われた AI 自動診断と Markov モデルを用いた研究では、65歳以上を対象とした集団スクリーニング併用による PACG 進行抑制効果が示されているが、スクリーニング費用の回収には課題が残る2)。
MIGS は当初 PACG では禁忌とされていたが、phaco との併用により隅角へのアクセスが確保される環境で、軽〜中等度 PACG に対する低侵襲オプションとして注目されている8)。メタ解析では AIT の優位性が示されたが、試験数・追跡期間は限られており、長期成績と費用対効果のさらなる検証が求められる8)。線維柱帯切除術に比して濾過胞関連合併症や濾過胞感染のリスクが低いため、白内障合併 PACG の術式選択に大きな影響を与える可能性がある8)。
近年、PACD のリスクを増加させる遺伝子多型(PLEKHA7、COL11A1、PCMTD1-ST18 など)がゲノムワイド関連解析で同定されており、解剖学的素因の理解と個別化リスク評価が進みつつある2)。将来的には、家族歴陽性例や高リスク民族集団に対し遺伝情報とバイオメトリックデータを組み合わせたスクリーニング戦略が確立される可能性がある2)。
患者指導の観点では、PACD リスク保有者に対して急性発作の症状と速やかな受診の必要性を教育すること、市販薬・処方薬のうち瞳孔散大作用のあるものを避けるよう情報提供すること、家族(特に一親等)にも眼科検診を勧めることが長期的な視機能保全に重要である2)。
日本緑内障学会緑内障診療ガイドライン改訂委員会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
American Academy of Ophthalmology. Primary Angle-Closure Disease Preferred Practice Pattern®. San Francisco: American Academy of Ophthalmology; 2025.
He M, Jiang Y, Huang S, et al. Laser peripheral iridotomy for the prevention of angle closure: a single-centre, randomised controlled trial (Zhongshan Angle Closure Prevention Trial). Lancet. 2019;393(10181):1609-1618.
Baskaran M, Kumar RS, Friedman DS, et al. The Singapore Asymptomatic Narrow Angles Laser Iridotomy Study: Five-Year Results of a Randomized Controlled Trial. Ophthalmology. 2022;129(2):147-158.
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025.
Azuara-Blanco A, Burr J, Ramsay C, et al. Effectiveness of early lens extraction for the treatment of primary angle-closure glaucoma (EAGLE): a randomised controlled trial. Lancet. 2016;388(10052):1389-1397.
Chan PP, Zhang X, Aung T, et al. Controversies, consensuses, and guidelines for acute primary angle closure attack (APACA) by the Asia-Pacific Glaucoma Society (APGS) and the Academy of Asia-Pacific Professors of Ophthalmology (AAPPO). Asia Pac J Ophthalmol. 2025.
Paik B, Chua CH, Yip LW, Yip VCH. Outcomes and Complications of Minimally Invasive Glaucoma Surgeries (MIGS) in Primary Angle Closure and Primary Angle Closure Glaucoma: A Systematic Review and Meta-Analysis. Clin Ophthalmol. 2024;18:1573-1588.
Song BJ, Ramanathan M, Morales E, et al. Trabeculectomy and combined phacoemulsification-trabeculectomy: outcomes and risk factors for failure in primary angle closure glaucoma. J Glaucoma. 2016;25(9):763-769.
Tarongoy P, Ho CL, Walton DS. Angle-closure glaucoma: the role of the lens in the pathogenesis, prevention, and treatment. Surv Ophthalmol. 2009;54(2):211-225.
Quigley HA, Broman AT. The number of people with glaucoma worldwide in 2010 and 2020. Br J Ophthalmol. 2006;90(3):262-267.
Foster PJ, Buhrmann R, Quigley HA, Johnson GJ. The definition and classification of glaucoma in prevalence surveys. Br J Ophthalmol. 2002;86(2):238-242.
Yamamoto T, Iwase A, Araie M, et al. The Tajimi Study report 2: prevalence of primary angle closure and secondary glaucoma in a Japanese population. Ophthalmology. 2005;112(10):1661-1669.
Kumar RS, Baskaran M, Chew PT, et al. Prevalence of plateau iris in primary angle closure suspects: an ultrasound biomicroscopy study. Ophthalmology. 2008;115(3):430-434.