単純網膜症
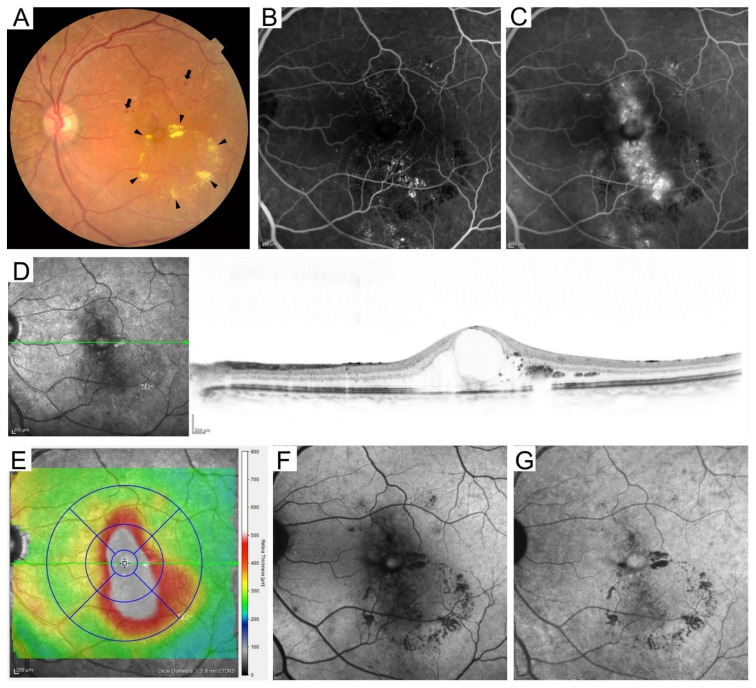
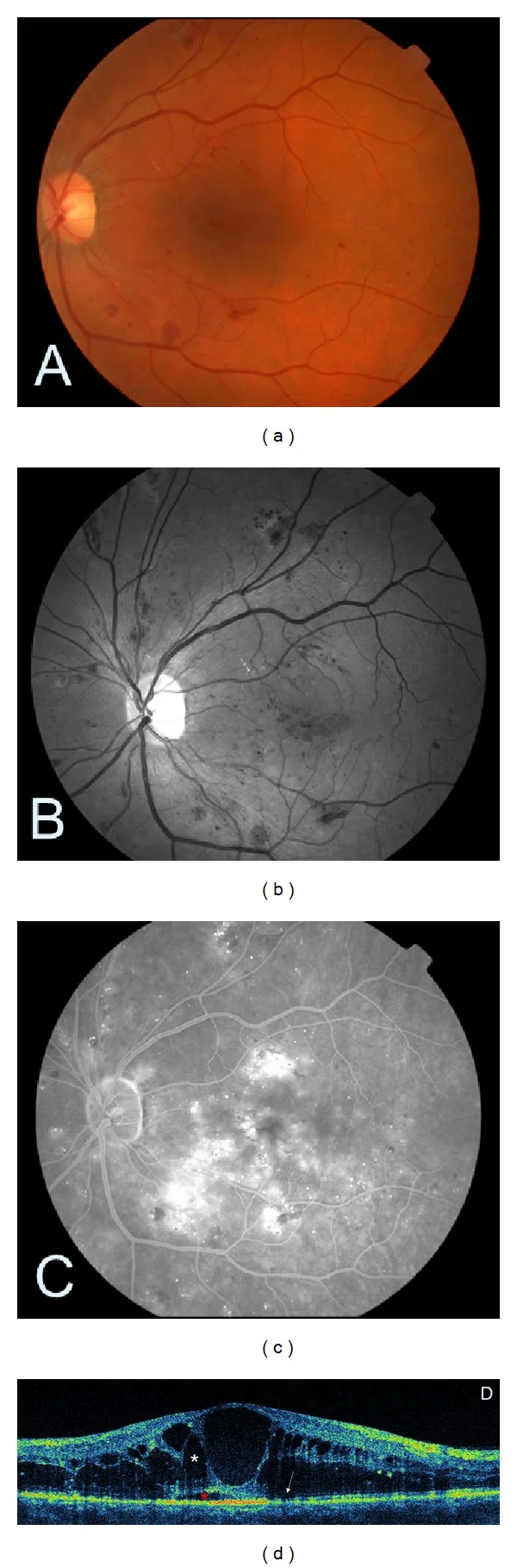
毛細血管瘤:DRの最早期所見。点状の過蛍光として蛍光眼底造影で描出される。
網膜出血:点状・斑状出血。赤血球が毛細血管から漏出して生じる。
硬性白斑:血管透過性亢進により血漿成分が漏出し、脂質が沈着したもの。

糖尿病網膜症(DR)は、高血糖に起因した代謝異常によりさまざまなサイトカインやケモカインが誘導されることで引き起こされる網膜の微小血管障害である。2次的に多様な眼底病変がもたらされ、糖尿病神経障害・糖尿病腎症とともに3大合併症と称される。近年は微小血管疾患にとどまらず「神経血管疾患」として再定義されている2)。
後天性視覚障害原因の第2位に位置し、年間約3,000人がDRにより失明している。
糖尿病黄斑浮腫(DME)は、糖尿病黄斑症の中で最も頻度が高い病型である。糖尿病黄斑症には黄斑浮腫・虚血性黄斑症・網膜色素上皮症の3型が含まれるが、黄斑浮腫の頻度が最も高く、臨床的に重要な視力低下原因となる。DMEはDRのどの病期でも発症しうる。DMEの病態は血管透過性亢進・血管閉塞による血流障害・膠質浸透圧低下・後部硝子体膜の牽引など多因子が関与する複雑なものである。
日本における主要な疫学データを以下に示す1)。
世界レベルでは、糖尿病患者の34.6%(約9,300万人)がDRを有する2)。2020年推計ではDR 1億312万人、視力を脅かすDR(VTDR)2,854万人、臨床的に重要な黄斑浮腫(CSME)1,883万人と報告されており、2045年には1億6,050万人へ増加することが予測される2)。1型DMでは発症20年後に約90%にDRが生じる11)。
日本の大規模コホートでは年3.8〜4.0%の頻度でDRが発症し、2型DM診断時にすでに約30%がDRを有する1)。世界的には糖尿病患者の34.6%(約9,300万人)がDRを有し2)、1型DM発症20年後には約90%に認める11)。
初期のDRは無症状で進行することが多い。症状が出現した時点では、すでに中等度以上の病変が存在することが多い。
病期別の主要な眼底所見を以下に示す。
単純網膜症
毛細血管瘤:DRの最早期所見。点状の過蛍光として蛍光眼底造影で描出される。
網膜出血:点状・斑状出血。赤血球が毛細血管から漏出して生じる。
硬性白斑:血管透過性亢進により血漿成分が漏出し、脂質が沈着したもの。
増殖前網膜症
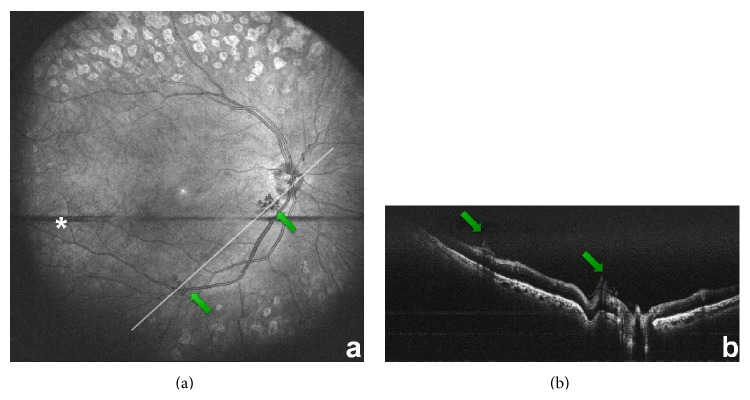
軟性白斑:視神経線維の軸索輸送が障害された局所梗塞巣。網膜虚血を反映する。
数珠状静脈拡張・ループ形成:血管閉塞領域に隣接して出現。
IRMA(網膜内細小血管異常):無灌流域周囲のシャント形成。蛍光造影でも漏出が目立たない点が新生血管との鑑別点となる。
増殖網膜症
新生血管:広範な毛細血管閉塞によるVEGF過剰産生により網膜・乳頭上に出現。蛍光造影で旺盛な蛍光漏出を示す。
線維血管性増殖膜:新生血管周囲に線維芽細胞様細胞が増殖して形成。
牽引性網膜剥離:増殖膜と網膜の癒着に硝子体牽引が加わって発生。黄斑を巻き込むと視力予後不良となる。
重症NPDRは「4-2-1ルール」で定義される2)。すなわち、以下のいずれか1つ以上を満たす場合である。
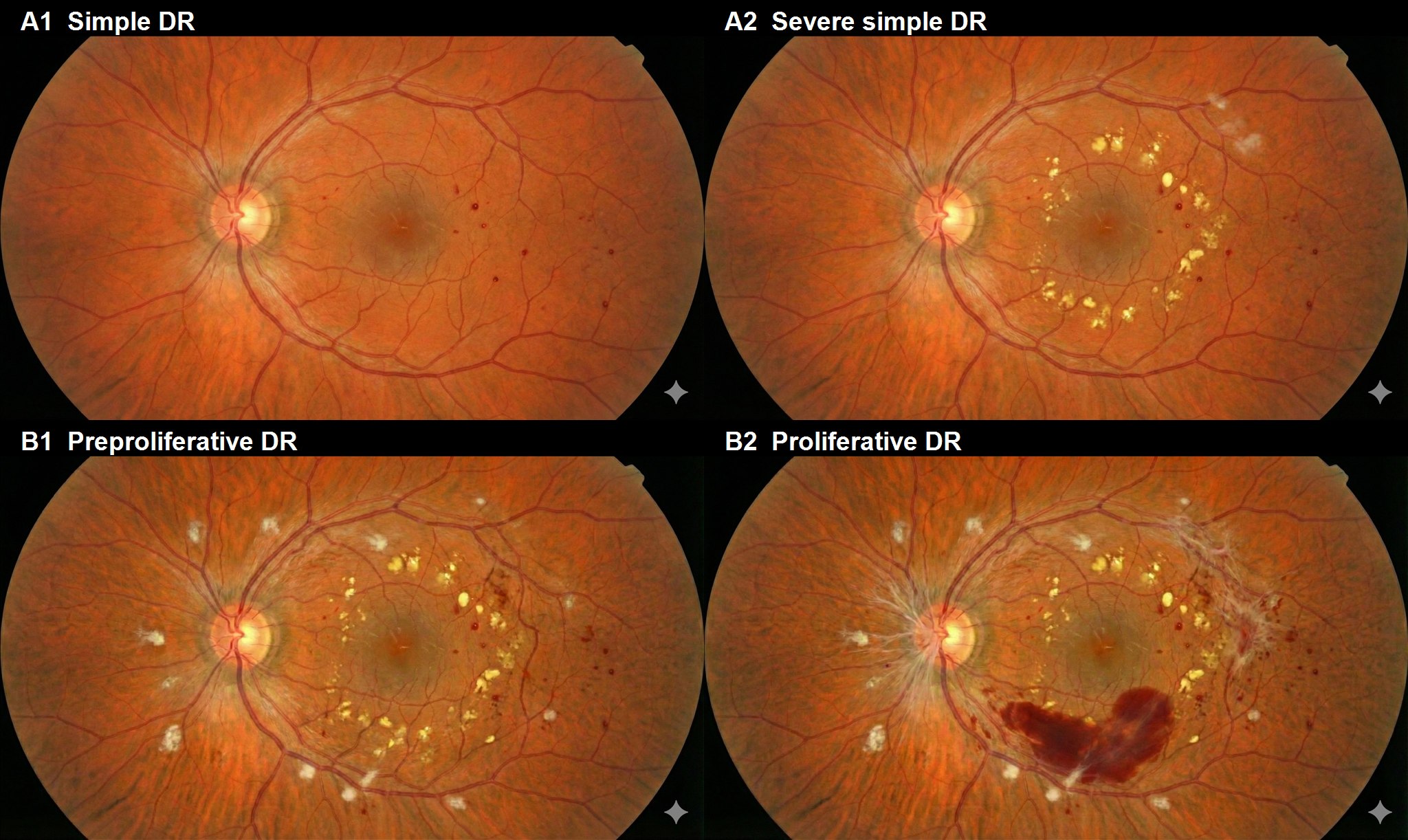
新福田分類1)は良性(A群)と悪性(B群)に大別される。
| 分類 | 病期 | 所見 |
|---|---|---|
| A1 | 軽症単純 | 毛細血管瘤・点状出血 |
| A2 | 重症単純 | しみ状出血・硬性白斑・少数の軟性白斑 |
| B1 | 増殖前 | 軟性白斑・静脈拡張・IRMA・蛍光眼底造影でNPA |
| B2 | 早期増殖 | 乳頭に直接連絡しない新生血管 |
| B3 | 中期増殖 | 乳頭に直接連絡する新生血管 |
| B4 | 末期増殖 | 硝子体出血・網膜前出血 |
| B5 | 末期増殖 | 線維血管性増殖組織 |
| A3〜A5 | 増殖停止 | 陳旧性新生血管・VH・増殖組織 |
治療により6か月間以上鎮静化すると増殖停止網膜症と称する。合併症表記として M(黄斑病変)・D(牽引性RD)・G(NVG)・N(虚血性視神経症)・P(光凝固)・V(硝子体手術)を付記する。
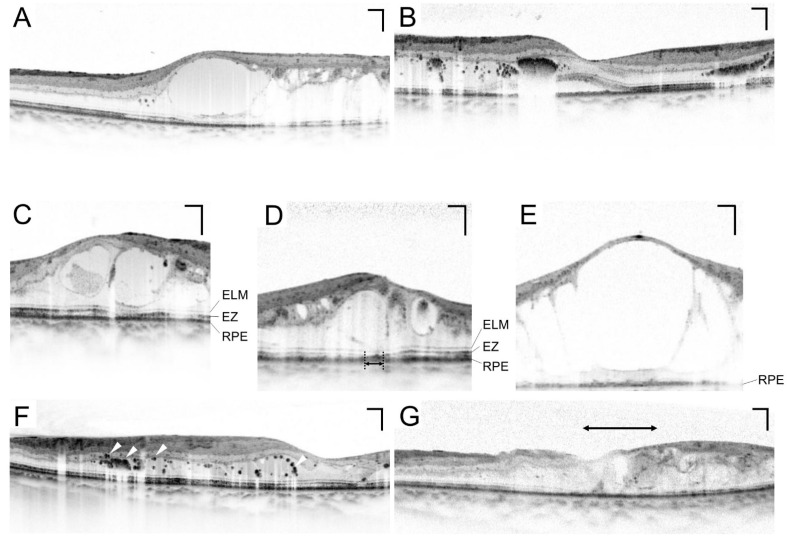
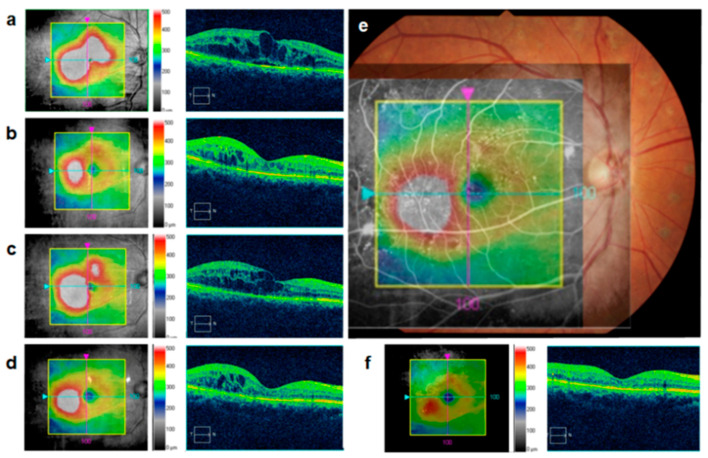
黄斑浮腫のOCT断層像は、網膜膨化・嚢胞様黄斑浮腫・漿液性網膜剥離の3基本型の組み合わせで評価する。
臨床的に重要な黄斑浮腫(CSME)はETDRS定義で以下のいずれかを満たすもの2)。
SD-OCT中心網膜厚300μm以上を中心窩を含むDMEの閾値とする(機種別: Spectralis 320/305μm、Cirrus 305/290μm、Stratus 250/250μm、男性/女性)1)。DMEの国際重症度分類は軽症(黄斑中心から離れた肥厚・硬性白斑)・中等症(中心に近いが含まない)・重症(中心窩を含む)の3段階。DMEはNPDRの進行とともに増加し、軽症NPDR 1.7〜6.3%、中等症NPDR 20.3〜63.2%に合併する1)。
DRの進行に関わる主なリスク因子を以下に示す。
| リスク因子 | 主なエビデンス |
|---|---|
| 罹患期間 | 最大のリスク因子。2型DM診断時に約30%がすでにDRを有する1) |
| 血糖コントロール | HbA1c 7.0%未満で細小血管合併症が予防される(Kumamoto Study)。HbA1c 1%低下→微小血管合併症リスク37%減少(UKPDS)1) |
| 高血圧 | WESDR: 収縮期10mmHg上昇→初期DR 10%・増殖DR/DME 15%リスク増。UKPDS: 10mmHg低下→DR進展35%減少・視力低下47%減少1) |
| 脂質異常症 | フェノフィブラート(FIELD Study): 光凝固導入31%減少、増殖DR 30%・DME 31%減少。ACCORD Eye Study: DR進行オッズ40%低下1) |
| 腎機能障害 | 蛋白尿・GFR低下がDR有病率と相関。腎症あり→PDR進行リスク29%上昇1) |
| 妊娠 | 既存DRなし→妊娠中DR発症8〜33%。既存NPDR→妊娠中悪化10〜67%1) |
| 重症低血糖 | DR発生率が約4倍に増加(JDCS)1) |
厳格な血糖コントロールがDR予防と進行抑制に有効であることが複数の大規模試験で示されている1)。
一方、長期間血糖コントロール不良の患者で急速に血糖を改善すると、一過性にDRが悪化する「early worsening」が生じることがある。視力低下が約50%の症例で遷延するため、緩やかな血糖改善が望ましく、内科との連携が重要である1)。
また、一度高血糖に曝露された網膜細胞にはエピジェネティック変化が刻まれ、血糖正常化後も病変が持続・進行する「代謝記憶(metabolic memory)」が知られている11)。SOD2のダウンレギュレーションやミトコンドリアDNAの過メチル化がそのメカニズムとして報告されている。
HbA1c 7.0%未満を目標とすることで細小血管合併症が予防される(Kumamoto Study)1)。HbA1c 1%低下で微小血管合併症リスクが37%減少する(UKPDS)1)。一度高血糖に曝露された細胞には「代謝記憶」が残るため、血糖が正常化しても長期間のフォローが必要である11)。
| 検査法 | 主な用途 | 備考 |
|---|---|---|
| 散瞳眼底検査(倒像鏡/前置レンズ) | 病期分類のゴールドスタンダード | 散瞳なしでは約50%のみ正確に分類2) |
| 細隙灯顕微鏡検査 | 角膜障害・虹彩ルベオーシス・白内障・前房炎症の確認 | 前置レンズによる黄斑の詳細観察 |
| カラー眼底写真 | 客観的記録・経時比較 | ETDRS 7方向撮影。超広角SLOで周辺部も記録可能3) |
| 蛍光眼底造影(FA) | NPA・新生血管・漏出点の同定。DMEの局所性/びまん性鑑別 | FA全副作用1.1〜11.2%、重症0.005〜0.48%、死亡0.0005〜0.002%1) |
| 光干渉断層計(OCT) | 黄斑浮腫の定量評価・経過観察 | SD-OCT深さ分解能5μm。中心網膜厚300μm以上で中心窩DME1) |
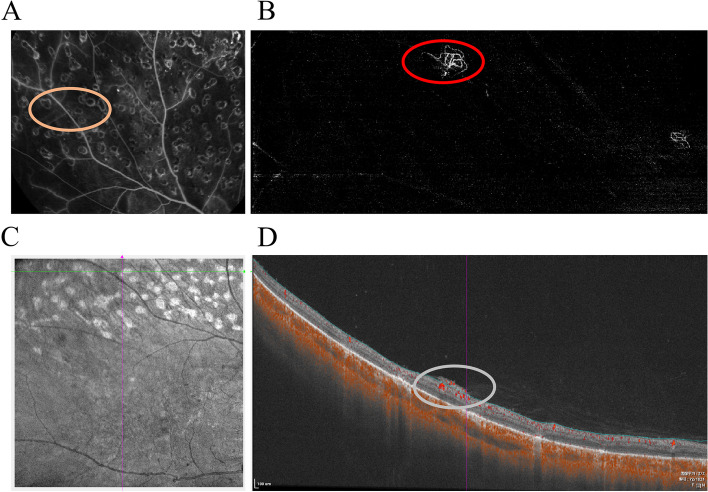
| OCTA | 造影剤不使用での毛細血管脱落・NPA・新生血管評価 | 非侵襲的。FAZの定量化も可能3) |
| 超音波検査 | 中間透光体混濁時の網膜・硝子体関係評価 | 牽引性RDの範囲・増殖膜位置の把握 |
| 網膜電図(ERG) | 網膜機能の他覚的評価 | OP潜時延長はDR早期から出現。negative ERGは術後視力不良を示唆1) |
| 病期(改変Davis分類) | 推奨間隔 |
|---|---|
| 糖尿病(網膜症なし) | 1年に1回 |
| 単純糖尿病網膜症(軽症〜中等症NPDR) | 6か月に1回 |
| 増殖前糖尿病網膜症(重症NPDR) | 2か月に1回 |
| 増殖糖尿病網膜症 | 1か月に1回 |
(AAO PPPでは重症NPDR 3〜4か月ごとを推奨しており、GL表3の値と若干異なる)1)2)
高血圧性網膜症・網膜動静脈閉塞症・Eales病・Coats病・血液疾患(貧血・白血病・Hodgkin病)・インターフェロン網膜症・放射線網膜症・Purtscher病・高安病・ぶどう膜炎(Behçet病・サルコイドーシス・SLE)が主な鑑別対象となる。
2型DMは診断時に約30%がすでにDRを有するため、診断時に眼底検査を受けることが推奨される1)。1型DMは診断後5年以内を目安とする1)。妊娠を合併している場合は第1三半期のできるだけ早期に受診し、妊娠中は3か月ごとの追跡が必要である1)。
全身の危険因子管理がDRの予防と進行抑制の根本であり、全病期を通じて継続する。
抗VEGF療法
第一選択:中心窩を含むDMEに対する標準治療1)。
ラニビズマブ(ルセンティス):0.5mg/0.05mL 硝子体内注射。視力安定まで月1回投与。
アフリベルセプト 2mg(アイリーア):2mg/0.05mL。月1回×5回導入→2か月ごと。
ファリシマブ(バビースモ):6mg/0.05mL。抗VEGF+抗Ang-2二重特異性抗体。YOSEMITE/RHINE試験で50〜70%が12〜16週間隔を維持9)。
ブロルシズマブ(ベオビュ):6mg/0.05mL。分子量26kDa。KESTREL/KITE試験で50%以上がq12w維持5)。
再投与レジメン:PRN(要時投与)・固定投与・TAE(treat and extend)の3方式1)。
ステロイド療法
トリアムシノロンアセトニド(マキュエイド):4mg/0.1mL 硝子体内投与。抗VEGF抵抗例やTenon嚢下注射として使用1)。
デキサメタゾンインプラント(オズルデックス):徐放型。偽水晶体眼や抗VEGF反応不良例に考慮5)2)。
注意点:白内障の進行(有水晶体眼)・眼圧上昇のリスクがある。
レーザー光凝固(DME)
対象:中心窩を含まないDMEに対する選択肢1)。
直接凝固:漏出源の毛細血管瘤に直接照射。
格子状凝固:びまん性漏出・NPA部位に照射。
modified ETDRS法:黄斑中心500μm以内の照射を回避し、低出力・広間隔で施行1)。
注意:atrophic creep(瘢痕拡大)・網膜下線維増殖のリスクがある1)。
| 薬剤名(商品名) | 用量 | 特徴 |
|---|---|---|
| ラニビズマブ(ルセンティス) | 0.5mg/0.05mL | Fab断片。月1回投与。視力安定まで継続 |
| アフリベルセプト 2mg(アイリーア) | 2mg/0.05mL | VEGF-A/B・PlGF結合融合蛋白。導入5回後2か月ごと |
| アフリベルセプト 8mg(アイリーア8mg) | 8mg/0.07mL | 高用量。最大16週間隔2) |
| ブロルシズマブ(ベオビュ) | 6mg/0.05mL | 分子量26kDa。50%以上がq12w。眼内炎症リスクに注意5)7) |
| ファリシマブ(バビースモ) | 6mg/0.05mL | 抗VEGF+抗Ang-2。最大q16w9) |
良好な視力(20/25以上)を有する中心窩含むDMEでは、20/30以下に低下するまで治療延期も選択肢となる2)。
中心窩を含むDMEに対しては抗VEGF療法が第一選択である1)。ラニビズマブ・アフリベルセプト・ファリシマブ・ブロルシズマブのいずれも有効であり、投与間隔延長が可能な点でファリシマブ(最大q16w)やブロルシズマブ(50%以上がq12w)が注目される5)9)。抗VEGF効果不十分な場合はトリアムシノロンやデキサメタゾンインプラントによるステロイド療法を考慮する2)。
DRの基本病態は血管透過性亢進・血管閉塞・血管新生の3つに大別され、単純網膜症・増殖前網膜症・増殖網膜症の各病期はこれら基本病態にほぼ対応している。
高血糖状態では4つの主要な代謝経路が活性化され、酸化ストレスや炎症を介して網膜障害が進行する11)。
| 経路 | 主な産物/変化 | 主要な下流障害 |
|---|---|---|
| ポリオール経路 | ソルビトール蓄積 | NADPH枯渇→グルタチオン低下→酸化ストレス増幅 |
| AGEs形成 | RAGE活性化 | NF-κB↑→VEGF↑、周細胞アポトーシス |
| PKC活性化 | PKC-β活性化 | VEGF・Nox亢進 |
| ヘキソサミン経路 | UDP-GlcNAc過剰 | TGF-β・PAI-1増加 |
内側BRB(網膜毛細血管内皮のタイトジャンクション)と外側BRB(RPE間のタイトジャンクション)の両方が障害される8)。
網膜には循環系と独立した局所RAASが発現している9)。古典的経路(ACE/AngII/AT1R軸)は周細胞アポトーシス・白血球停滞・BRB破綻を促進し、保護的経路(ACE2/Ang-(1-7)/Mas軸)がこれに拮抗する。網膜内AngII濃度は循環中より高く、DIRECT試験ではカンデサルタン投与によりDRが34%退縮した9)。
一度高血糖に曝露された網膜細胞には、血糖正常化後もエピジェネティック変化が持続する(SOD2抑制・ミトコンドリアDNA過メチル化)11)。ミトコンドリア電子伝達系Complex I/IIIからのROS産生亢進、Drp1/OPA1不均衡によるミトコンドリア過剰断片化、Nrf2/KEAP1・SIRT1を介した抗酸化応答の障害がそのメカニズムとして報告されている。
DRは「神経血管疾患」として再定義されており2)、血管病変に先行してOCTでGCIPL菲薄化が検出できる13)。黄斑NFLは年間0.25μm、GCIPLは年間0.29μmずつ菲薄化する。ミュラー細胞の膠化(GFAP上昇)とミクログリア活性化も確認されている。フラクタルカイン(CX3CL1)は網膜神経節細胞が産生し、CX3CR1受容体に作用して抗炎症・神経保護効果を発揮する10)。
糖尿病患者では硝子体中グルコース濃度が上昇し、コラーゲン線維の糖化反応が進行する。糖化反応の程度はDR進行度と相関し、コラーゲン構造変化は液化・硝子体皮質の収縮・後部硝子体剥離(PVD)を起こりやすくする。牽引を残さない完全PVDが生じると増殖DRへの進行はほぼない。一方、不完全PVD(硝子体と増殖組織の強い癒着)では硝子体牽引が持続し、牽引性網膜剥離や硝子体出血が生じやすい。
血糖コントロールはDR予防・進行抑制に最も重要であり、HbA1c 7.0%未満を目標とする1)。ただし「代謝記憶」の概念によれば、一度高血糖に曝露された細胞にはエピジェネティック変化が残存し、血糖が正常化した後も病変が持続・進行することがある11)。DCCT/EDIC追跡研究では早期の強化療法群が長期間にわたりDR進展を抑制したことが示されている。
アフリベルセプト8mgは2023年にDME適応で承認され、最大16週間隔の延長が期待されている2)。DRCR Protocol Wでは、重症NPDRへの予防的抗VEGF投与がPDR/DME発症を防ぐ一方で、長期視力転帰は初期観察と同等であることが示された2)。
LumineticsCore(旧IDx-DR)は2018年にFDAが承認した、医師の解釈を必要としない初の自律型AI眼底診断システムである3)。ディープラーニングモデルでは感度96.8%・特異度87%が報告されており3)、EyeArt・AEYE-DS等の新規システムも開発されている2)。
可溶性フラクタルカイン発現AAVベクター(rAAV-sFKN)投与により、視力改善・フィブリン漏出減少・ミクログリアの正常化が示されている10)。抗VEGF療法とは異なる神経保護・抗炎症機序を持つ。
EUROCONDOR第II-III相試験(NCT01726075)ではソマトスタチン・ブリモニジン点眼が検討されたが、全体解析では有効性を示さず、ベースラインmfERG異常サブグループで神経機能障害の進行停止が認められた13)。シチコリン+ビタミンB12点眼の36か月二重盲検RCTでは、軽度DRへの投与で機能的・構造的・血管性の進行抑制が報告されている13)。
miRNAはDR病態の複数軸(酸化ストレス・炎症・神経変性・血管機能不全)を統合的に調節する「マスターレギュレーター」として注目される14)。miR-195阻害によるSIRT1安定化、miR-497a-5pによるVEGF-A翻訳阻害の可能性が示されており、約350のmiRNAが網膜で発現し、86以上がDRモデルで異常発現している。
メトホルミンはAMPK活性化を介した抗酸化・抗炎症・抗血管新生・神経保護の多面的作用を持ち、観察研究では使用者でSTDR(sight-threatening DR)のaHR=0.29が示されている12)。ただし眼科適応のRCTデータは現時点では不十分である。
非ステロイド性MR拮抗薬フィネレノンは、前臨床モデルでBRB破綻・血管新生・炎症の軽減が示されており、DRに対する独立した治療標的としてのMRの意義が検討されている9)。