
糖尿病患者の眼科スクリーニング(Diabetic Eye Screening Guidelines)
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 糖尿病患者の眼科スクリーニングとは
Section titled “1. 糖尿病患者の眼科スクリーニングとは”糖尿病患者における眼科スクリーニングとは、糖尿病網膜症・糖尿病黄斑浮腫・新生血管緑内障・白内障・外眼筋麻痺などの眼合併症を早期に発見し、適切な治療介入につなげるための定期的な眼科的検査体制である。
糖尿病網膜症は成人の中途失明原因の第2位を占める。世界の糖尿病患者のうち約30〜40%に網膜症が存在し、視覚障害を引き起こす網膜症(視力障害性網膜症)は約10%に認められる1)。糖尿病診断時にすでに約20%の患者で網膜症が存在することも報告されており1)、スクリーニングの早期開始が重要である。
一方、適切なスクリーニングと治療介入によって失明の90%以上が予防可能とされる2)。網膜症は早期には無自覚であり、自覚症状が出現した時点では病変がかなり進行していることが多い。このため定期的な眼科検査が唯一の早期発見手段となる。
糖尿病患者数は日本国内で約1,000万人超と推定され、眼科への定期受診を継続する体制づくりが課題である。糖尿病眼手帳をはじめとした内科−眼科の連携ツールは、眼底所見・検査日・治療内容の情報共有に役立つ3)。
2型糖尿病では診断された時点で直ちに眼科検査を受けることが推奨される。糖尿病診断時にすでに約20%の患者で網膜症が存在することが報告されており1)、無症状でも網膜症が進行している可能性がある。1型糖尿病では発症または思春期から5年後を目安に眼科検査を開始する4)。いずれの型でも、視力低下などの自覚症状がない段階から定期的な眼底検査が不可欠である。
2. スクリーニングの対象と推奨頻度
Section titled “2. スクリーニングの対象と推奨頻度”対象者と開始時期
Section titled “対象者と開始時期”スクリーニングの開始時期は糖尿病の型・病態によって異なる。
- 2型糖尿病:診断時に初回眼科検査を実施する4)
- 1型糖尿病:発症(または思春期)から5年後を目安に開始し、以降は年1回の眼底検査を継続する4)
- 妊娠糖尿病(GDM):妊娠第1三半期に眼底検査を実施し、分娩後1年まで追跡する5)
- 妊娠前から糖尿病のある妊婦:妊娠前または妊娠第1三半期に検査を実施し、各三半期ごとに追跡する5)
推奨スクリーニング頻度(病期別)
Section titled “推奨スクリーニング頻度(病期別)”スクリーニング頻度は網膜症の病期とHbA1cコントロール状況を総合して決定する。
| 網膜症の病期 | 推奨スクリーニング頻度 |
|---|---|
| 網膜症なし(HbA1c < 7.0%で良好なコントロール) | 1〜2年ごと4) |
| 軽症非増殖期 | 6〜12ヵ月ごと4) |
| 中等症非増殖期 | 3〜6ヵ月ごと4) |
| 重症非増殖期(前増殖期) | 1〜3ヵ月ごと4) |
| 増殖糖尿病網膜症 | 1ヵ月ごと(治療介入と並行)4) |
HbA1cコントロールと網膜症進行
Section titled “HbA1cコントロールと網膜症進行”HbA1cコントロールはスクリーニング頻度の決定においても重要な指標となる。
UKPDS(英国前向き糖尿病研究)において、HbA1cを1%低下させることで微小血管合併症のリスクが37%減少することが示された6)。HbA1c 7.0%未満の維持が網膜症進行リスクの有意な低下につながる6)。
一方、インスリン導入などによる急激な血糖改善は、一時的に網膜症が悪化する「early worsening」を引き起こすことがある7)。DCCT(糖尿病コントロールと合併症試験)ではこの現象が確認されており、インスリン導入後の短期的な眼底悪化に注意が必要である7)。
網膜症がなくHbA1cが良好(7.0%未満)であれば1〜2年ごとの検査で可とされる。軽症非増殖期では6〜12ヵ月ごと、中等症では3〜6ヵ月ごと、重症非増殖期では1〜3ヵ月ごと、増殖期では毎月の検査と治療介入が必要になる4)。HbA1cが高い場合や血糖コントロールが不安定な場合は、より短い間隔でのフォローアップが推奨される。
3. 検査方法
Section titled “3. 検査方法”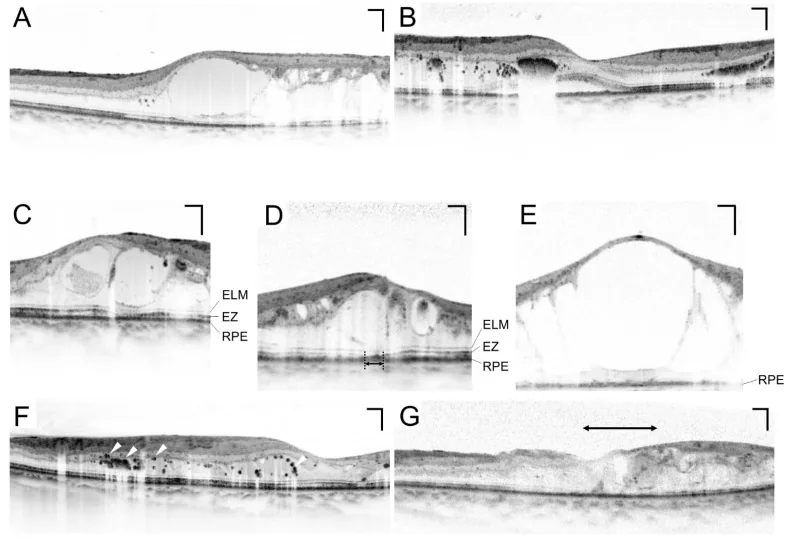
散瞳眼底検査
Section titled “散瞳眼底検査”散瞳眼底検査は糖尿病眼科スクリーニングの中心的検査である。トロピカミドとフェニレフリン(フェニレフリン塩酸塩)の点眼による散瞳後に眼底検査を行うことが標準的である4)。ETDRS(Early Treatment Diabetic Retinopathy Study)による7視野ステレオ写真撮影が参照基準とされる8)。
無散瞳眼底カメラは利便性が高くスクリーニングでの使用が広まっており、感度80〜90%が報告されている9)。英国の全国糖尿病網膜症スクリーニングプログラムでは、無散瞳デジタル眼底撮影を中核としたシステムが運用されている9)。
OCT(光干渉断層計)
Section titled “OCT(光干渉断層計)”OCTは黄斑浮腫の定量的評価において必須の検査である。中心窩網膜厚(CRT)を非侵襲的・繰り返し測定でき、治療効果判定のモニタリングに不可欠である10)。CRT > 300 μmが糖尿病黄斑浮腫(DME)の治療開始の一つの目安とされる10)。
蛍光眼底造影(FA)
Section titled “蛍光眼底造影(FA)”フルオレセインナトリウムを静脈注射して網膜血管を描出する検査であり、無灌流野の検出・新生血管の評価に使用する8)。光凝固の適応判断に用いられ、ETDRS分類の精密評価に有用である8)。
OCTアンギオグラフィ(OCTA)
Section titled “OCTアンギオグラフィ(OCTA)”造影剤を使用せずに網膜血管を三次元的に描出できる非侵襲的検査である11)。フルオレセイン造影の代替として繰り返し検査が可能であり、無灌流野や黄斑毛細血管網の評価に応用されている11)。
AIを用いた眼底スクリーニング
Section titled “AIを用いた眼底スクリーニング”ディープラーニングを用いた眼底自動解析は急速に実用段階へ移行している。Tingら(2017年)の多民族コホート研究では、糖尿病網膜症・緑内障疑い・AMDなどの自動検出において感度87〜97%が報告された12)。米国FDAが承認したAIデバイス(IDx-DR等)も実用化されており、内科・プライマリケアでのスクリーニング活用が進んでいる12)。
| 検査法 | 主な適応 | 特徴 |
|---|---|---|
| 散瞳眼底検査(7視野ステレオ) | 病期評価の参照基準 | 高精度・侵襲的散瞳が必要8) |
| 無散瞳眼底カメラ | 一次スクリーニング | 感度80〜90%・利便性高い9) |
| OCT | 黄斑浮腫の定量化・治療モニタリング | 非侵襲・CRT定量10) |
| 蛍光眼底造影(FA) | 無灌流野・新生血管評価 | 侵襲的・造影剤使用8) |
| OCTA | 非侵襲的血管評価 | 繰り返し可・造影剤不要11) |
| AI眼底スクリーニング | 一次スクリーニング自動化 | 感度87〜97%・眼科専門医不要12) |
ディープラーニングを用いたAI眼底スクリーニングは感度87〜97%という高精度が報告されており、実用段階に入っている12)。FDAが承認したAIデバイスも存在し、眼科専門医不足地域での活用が期待されている。ただしAIスクリーニングはあくまで一次スクリーニングであり、異常が検出された場合は眼科専門医による精密検査が必要である。
4. 糖尿病網膜症の分類
Section titled “4. 糖尿病網膜症の分類”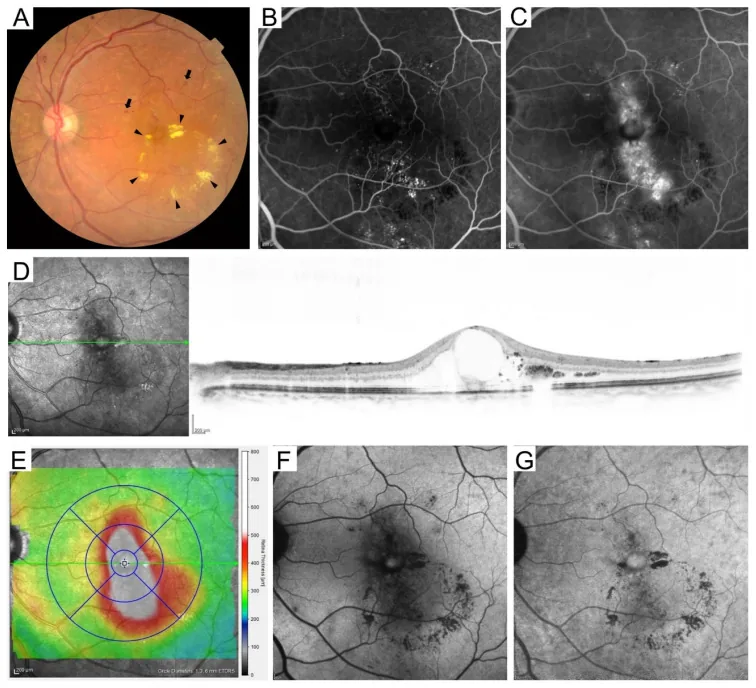
国際分類(ETDRS準拠)
Section titled “国際分類(ETDRS準拠)”糖尿病網膜症の国際分類はETDRS基準に基づく5段階で構成される8)。
| 病期 | 主な所見 | 管理方針 |
|---|---|---|
| 網膜症なし | 異常なし | 1〜2年ごとのスクリーニング4) |
| 軽症非増殖期(NPDR) | マイクロアネウリズムのみ | 6〜12ヵ月ごとの経過観察4) |
| 中等症NPDR | 軟性白斑・網膜出血・硬性白斑 | 3〜6ヵ月ごとの経過観察4) |
| 重症NPDR(4-2-1 rule) | 4象限の網膜出血・2象限の静脈数珠状拡張・1象限のIRMA8) | 早期PRP検討・1〜3ヵ月ごとの経過観察4) |
| 増殖糖尿病網膜症(PDR) | NVD・NVE・硝子体出血・牽引性網膜剥離8) | PRP・抗VEGF・手術。毎月フォロー4) |
- 重症NPDRにおける4-2-1 ruleとは、4象限の網膜出血、2象限の静脈数珠状拡張、1象限のIRMA(網膜内細小血管異常)のいずれか1項目を満たす病期を指す8)。
- 増殖糖尿病網膜症(PDR)では乳頭新生血管(NVD)や網膜新生血管(NVE)が出現し、硝子体出血・牽引性網膜剥離へと進行する8)。
糖尿病黄斑浮腫(DME)
Section titled “糖尿病黄斑浮腫(DME)”糖尿病黄斑浮腫(DME)は網膜症のどの病期にも合併しうる病態であり、糖尿病における視力低下の最も多い原因である10)。
- 中心窩に及ぶCSME(clinically significant macular edema:臨床的に有意な黄斑浮腫)が治療適応となる10)
- OCTでCRT > 300 μmが治療開始の目安の一つとされる10)
- 欧州網膜学会(EURETINA)のガイドラインでは抗VEGF療法を第一選択として推奨している10)
その他の眼合併症
Section titled “その他の眼合併症”- 新生血管緑内障:PDRの合併症として虹彩・隅角に新生血管が生じ、続発緑内障をきたす
- 糖尿病白内障:真性糖尿病白内障(若年例での急速進行型)と加齢白内障の促進の2形態がある
- 外眼筋麻痺:第III・VI脳神経麻痺による複視が急性発症することがある
5. 治療方針(スクリーニングから治療連携へ)
Section titled “5. 治療方針(スクリーニングから治療連携へ)”内科的管理の基本
Section titled “内科的管理の基本”血糖・血圧・脂質の内科的管理が糖尿病網膜症の進行抑制の基盤となる。目標値は以下のとおりである6)。
- HbA1c:7.0%未満
- 血圧:130/80 mmHg未満
- LDL-C:120 mg/dL未満
UKPDSにおいて、強化血糖管理群では通常管理群と比較して微小血管合併症のリスクが37%低下し、HbA1c 1%の低下が合併症リスクの有意な減少と関連することが示された6)。
レーザー光凝固(汎網膜光凝固:PRP)
Section titled “レーザー光凝固(汎網膜光凝固:PRP)”重症NPDRから増殖糖尿病網膜症に対して汎網膜光凝固(PRP)を実施する8)。虚血網膜を焼灼することでVEGF産生を抑制し、新生血管の退縮・予防を図る。ETDRSで確立された治療であり、高リスクPDRにおける失明予防の標準治療である8)。
抗VEGF療法
Section titled “抗VEGF療法”糖尿病黄斑浮腫(DME)に対する第一選択治療は抗VEGF硝子体内注射である。使用可能な薬剤は以下のとおりである10)。
- ラニビズマブ(Lucentis):0.5 mg/0.05 mL 硝子体内注射
- アフリベルセプト(Eylea):2 mg/0.05 mL 硝子体内注射
- ファリシマブ(Vabysmo):6 mg/0.05 mL 硝子体内注射(Ang-2/VEGF-A二重特異性抗体)
非吸収性硝子体出血・牽引性網膜剥離に対しては硝子体手術を行う8)。近年は小切開硝子体手術(25〜27ゲージ)が普及し、手術侵襲の低減が図られている。
ステロイド局所投与
Section titled “ステロイド局所投与”トリアムシノロンアセトニド(TA)4 mg/0.1 mLの硝子体内注射がDMEの補助治療として用いられる10)。抗VEGF療法への反応が不十分な症例や人工レンズ眼(白内障術後)での使用が考慮される。
フェノフィブラート
Section titled “フェノフィブラート”FIELD試験(2007年)およびACCORD Eye試験において、フェノフィブラート投与群で糖尿病網膜症の進行抑制と光凝固必要率の低下が示された13)。脂質低下作用に加えてPPARα活性化による抗炎症・抗血管新生作用が関与すると考えられている13)。
早期発見により90%以上の失明が予防可能である2)。治療法は病期と合併症の種類によって異なり、軽症〜中等症では内科的な血糖・血圧・脂質管理が主体となる。重症非増殖期〜増殖期ではレーザー光凝固(PRP)を実施し、糖尿病黄斑浮腫に対しては抗VEGF硝子体内注射(ラニビズマブ・アフリベルセプト・ファリシマブ)が第一選択となる。非吸収性硝子体出血や牽引性網膜剥離には硝子体手術が適応となる。
6. 病態生理学・スクリーニングの科学的根拠
Section titled “6. 病態生理学・スクリーニングの科学的根拠”高血糖による網膜微小血管障害
Section titled “高血糖による網膜微小血管障害”糖尿病網膜症の発症には高血糖が引き起こす複数の代謝経路が関与する14)。
- ポリオール経路の亢進:アルドース還元酵素によるグルコースのソルビトール変換が亢進し、細胞内オスモル濃度の上昇と酸化ストレスの増加をきたす
- AGE(最終糖化産物)の蓄積:血管基底膜や細胞外マトリックスへの蓄積が血管機能を障害する
- PKC(プロテインキナーゼC)の活性化:血管透過性亢進・新生血管形成に関与するVEGFの産生を促進する
- 酸化ストレスの増加:活性酸素種(ROS)の過剰産生が内皮細胞機能を障害する
周皮細胞喪失から新生血管へ
Section titled “周皮細胞喪失から新生血管へ”網膜毛細血管の周皮細胞(血管壁の支持細胞)の選択的喪失が糖尿病網膜症の最も早期の変化である14)。周皮細胞の喪失により毛細血管壁が脆弱となり、マイクロアネウリズムが形成される。血管透過性の亢進が黄斑浮腫をもたらし、毛細血管の非灌流(無灌流野)が網膜虚血を引き起こす14)。
虚血網膜からのVEGF産生増加が新生血管形成の主要なドライバーとなり、NVD・NVEが形成される。硝子体内のVEGFは硝子体出血・牽引性網膜剥離の病態にも関与する14)。
スクリーニングの費用対効果
Section titled “スクリーニングの費用対効果”糖尿病網膜症のスクリーニングプログラムの費用対効果は複数の経済分析で支持されている。Jonesらの系統的レビュー(2010年)では、スクリーニングによる早期治療は失明後の管理コストと比較して大幅に低く、費用対効果が高いことが示された15)。
DCCTとUKPDSは血糖管理の重要性を科学的に確立した。DCCTでは1型糖尿病において強化インスリン療法により網膜症の新規発症リスクが76%低下し、進行リスクが54%低下した6)。UKPDSでは2型糖尿病での強化血糖管理が微小血管合併症リスクを37%低下させることが示された6)。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”AIによる自動スクリーニングの社会実装
Section titled “AIによる自動スクリーニングの社会実装”ディープラーニングを用いた眼底自動解析の精度は眼科専門医に匹敵するレベルに達しており、社会実装が進んでいる12)。内科・プライマリケアでの非侵襲的スクリーニングへの活用で、眼科受診率の低いハイリスク患者の発見が期待される。
超広角眼底カメラの導入
Section titled “超広角眼底カメラの導入”Optosなどの超広角眼底カメラは1回の撮影で網膜の200°以上をカバーし、無散瞳スクリーニングへの応用が進んでいる9)。周辺網膜の無灌流野や新生血管を検出する精度の向上が報告されており、スクリーニングの精度向上と利便性の両立が期待される。
遠隔医療(テレオフサルモロジー)の活用
Section titled “遠隔医療(テレオフサルモロジー)の活用”テレメディシンを活用した遠隔眼底読影は、糖尿病網膜症スクリーニングを中心に実績を積んでいる12)。眼科専門医不足地域や僻地における糖尿病患者のスクリーニング受診率向上に貢献し、格差解消のツールとして注目される。
新規薬剤と網膜症リスクの研究
Section titled “新規薬剤と網膜症リスクの研究”GLP-1受容体作動薬(セマグルチド等)やSGLT2阻害薬(エンパグリフロジン等)の普及に伴い、これらの薬剤が糖尿病網膜症リスクに与える影響の研究が進んでいる16)。セマグルチドでは一部の試験で急性期の網膜症悪化リスク上昇が報告されており、特にearly worseningとの関連が注目されている16)。フェノフィブラートのDR進行抑制効果の機序解明とさらなる大規模試験への期待も継続している13)。
涙液バイオマーカー・網膜血管パラメータ
Section titled “涙液バイオマーカー・網膜血管パラメータ”非侵襲的な涙液サンプリングによるVEGF・炎症性サイトカインの定量や、網膜血管径・フラクタル解析を用いた早期網膜症リスク評価の研究が進行中である。将来的には眼底カメラ撮影のみで網膜症リスクを定量化できる可能性がある。
8. 参考文献
Section titled “8. 参考文献”- Yau JW, Rogers SL, Kawasaki R, et al. Global prevalence and major risk factors of diabetic retinopathy. Diabetes Care. 2012;35(3):556-564.
- Flaxel CJ, Adelman RA, Bailey ST, et al. Diabetic retinopathy Preferred Practice Pattern®. Ophthalmology. 2020;127(1):P66-P145.
- 日本糖尿病眼学会. 糖尿病眼手帳について. https://www.jsod.jp/techo/index.html
- Solomon SD, Chew E, Duh EJ, et al. Diabetic retinopathy: a position statement by the American Diabetes Association. Diabetes Care. 2017;40(3):412-418.
- Morrison JL, Hodgson LA, Lim LL, et al. Diabetic retinopathy in pregnancy: a review. Clin Exp Ophthalmol. 2016;44(4):321-334.
- UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet. 1998;352(9131):837-853.
- The Diabetes Control and Complications Trial Research Group. Early worsening of diabetic retinopathy in the Diabetes Control and Complications Trial. Arch Ophthalmol. 1998;116(7):874-886.
- Early Treatment Diabetic Retinopathy Study Research Group. Grading diabetic retinopathy from stereoscopic color fundus photographs — an extension of the modified Airlie House classification. ETDRS report number 10. Ophthalmology. 1991;98(5 Suppl):786-806.
- Scanlon PH. The English National Screening Programme for diabetic retinopathy 2003-2016. Acta Diabetol. 2017;54(6):515-525.
- Schmidt-Erfurth U, Garcia-Arumi J, Bandello F, et al. Guidelines for the management of diabetic macular edema by the European Society of Retina Specialists (EURETINA). Ophthalmologica. 2017;237(4):185-222.
- Spaide RF, Fujimoto JG, Waheed NK, et al. Optical coherence tomography angiography. Prog Retin Eye Res. 2018;64:1-55.
- Ting DSW, Cheung CY, Lim G, et al. Development and validation of a deep learning system for diabetic retinopathy and related eye diseases using retinal images from multiethnic populations with diabetes. JAMA. 2017;318(22):2211-2223.
- Keech AC, Mitchell P, Summanen PA, et al. Effect of fenofibrate on the need for laser treatment for diabetic retinopathy (FIELD study): a randomised controlled trial. Lancet. 2007;370(9600):1687-1697. doi:10.1016/S0140-6736(07)61607-9.
- Antonetti DA, Klein R, Gardner TW. Diabetic retinopathy. N Engl J Med. 2012;366(13):1227-1239.
- Jones S, Edwards RT. Diabetic retinopathy screening: a systematic review of the economic evidence. Diabet Med. 2010;27(3):249-256.
- Ntentakis DP, Correa VSMC, Ntentaki AM, Delavogia E, Narimatsu T, Efstathiou N, Vavvas DG. Effects of newer-generation anti-diabetics on diabetic retinopathy: a critical review. Graefes Arch Clin Exp Ophthalmol. 2024;262(3):717-752. PMID:37728754. doi:10.1007/s00417-023-06236-5.
