
Dépistage ophtalmologique chez les patients diabétiques (Directives de dépistage oculaire diabétique)
Points clés en un coup d’œil
Section intitulée « Points clés en un coup d’œil »1. Qu’est-ce que le dépistage ophtalmologique chez les patients diabétiques ?
Section intitulée « 1. Qu’est-ce que le dépistage ophtalmologique chez les patients diabétiques ? »Le dépistage ophtalmologique chez les patients diabétiques est un système d’examens ophtalmologiques réguliers visant à détecter précocement les complications oculaires telles que la rétinopathie diabétique, l’œdème maculaire diabétique, le glaucome néovasculaire, la cataracte et la paralysie des muscles oculaires externes, afin de permettre une intervention thérapeutique appropriée.
La rétinopathie diabétique est la deuxième cause de cécité évitable chez l’adulte. Environ 30 à 40 % des patients diabétiques dans le monde présentent une rétinopathie, et environ 10 % souffrent d’une rétinopathie entraînant une déficience visuelle (rétinopathie diabétique proliférante)1). Il a également été rapporté qu’environ 20 % des patients présentent déjà une rétinopathie au moment du diagnostic du diabète1), ce qui souligne l’importance d’un dépistage précoce.
D’autre part, un dépistage et un traitement appropriés peuvent prévenir plus de 90 % des cas de cécité2). La rétinopathie est asymptomatique à un stade précoce, et lorsque les symptômes subjectifs apparaissent, les lésions sont souvent déjà avancées. Par conséquent, des examens ophtalmologiques réguliers sont le seul moyen de détection précoce.
Le nombre de patients diabétiques au Japon est estimé à plus de 10 millions, et la mise en place d’un système permettant de poursuivre des consultations ophtalmologiques régulières est un défi. Les outils de collaboration entre internistes et ophtalmologistes, tels que le carnet de suivi oculaire du diabète, facilitent le partage des résultats du fond d’œil, des dates d’examen et des traitements3).
Pour le diabète de type 2, il est recommandé de subir un examen ophtalmologique immédiatement après le diagnostic. Il a été rapporté qu’environ 20 % des patients présentent déjà une rétinopathie au moment du diagnostic du diabète1), et la rétinopathie peut progresser même en l’absence de symptômes. Pour le diabète de type 1, l’examen ophtalmologique débute environ 5 ans après l’apparition de la maladie ou après la puberté4). Quel que soit le type, des examens réguliers du fond d’œil sont essentiels avant même l’apparition de symptômes subjectifs tels qu’une baisse de l’acuité visuelle.
2. Population cible et fréquence recommandée du dépistage
Section intitulée « 2. Population cible et fréquence recommandée du dépistage »Personnes concernées et moment du début
Section intitulée « Personnes concernées et moment du début »Le moment du début du dépistage varie selon le type et l’état du diabète.
- Diabète de type 2 : réaliser un premier examen ophtalmologique au moment du diagnostic4)
- Diabète de type 1 : commencer environ 5 ans après le début (ou à la puberté), puis poursuivre un examen du fond d’œil une fois par an4)
- Diabète gestationnel (DG) : réaliser un examen du fond d’œil au premier trimestre de la grossesse et suivre jusqu’à un an après l’accouchement5)
- Femmes enceintes ayant un diabète préexistant : réaliser un examen avant la grossesse ou au premier trimestre, puis suivre à chaque trimestre5)
Fréquence de dépistage recommandée (selon le stade)
Section intitulée « Fréquence de dépistage recommandée (selon le stade) »La fréquence du dépistage est déterminée en combinant le stade de la rétinopathie et le contrôle de l’HbA1c.
| Stade de la rétinopathie | Fréquence de dépistage recommandée |
|---|---|
| Absence de rétinopathie (bon contrôle avec HbA1c < 7,0%) | Tous les 1 à 2 ans4) |
| Stade non prolifératif léger | Tous les 6 à 12 mois4) |
| Rétinopathie non proliférante modérée | Tous les 3 à 6 mois4) |
| Rétinopathie non proliférante sévère (préproliférante) | Tous les 1 à 3 mois4) |
| Rétinopathie diabétique proliférante | Tous les mois (en parallèle du traitement)4) |
Contrôle de l’HbA1c et progression de la rétinopathie
Section intitulée « Contrôle de l’HbA1c et progression de la rétinopathie »Le contrôle de l’HbA1c est également un indicateur important pour déterminer la fréquence du dépistage.
L’étude UKPDS (United Kingdom Prospective Diabetes Study) a montré qu’une réduction de 1 % de l’HbA1c diminue de 37 % le risque de complications microvasculaires6). Le maintien d’une HbA1c inférieure à 7,0 % entraîne une réduction significative du risque de progression de la rétinopathie6).
En revanche, une amélioration rapide de la glycémie, par exemple par l’introduction d’insuline, peut provoquer une aggravation temporaire de la rétinopathie, appelée « early worsening »7). Ce phénomène a été confirmé dans l’étude DCCT (Diabetes Control and Complications Trial), et il faut être attentif à une détérioration rétinienne à court terme après l’introduction d’insuline7).
En l’absence de rétinopathie et avec une HbA1c bien contrôlée (inférieure à 7,0 %), un examen tous les 1 à 2 ans est considéré comme suffisant. En cas de rétinopathie non proliférante légère, tous les 6 à 12 mois ; modérée, tous les 3 à 6 mois ; sévère, tous les 1 à 3 mois ; et proliférante, un examen mensuel avec intervention thérapeutique est nécessaire4). Si l’HbA1c est élevée ou si le contrôle glycémique est instable, un suivi plus rapproché est recommandé.
3. Méthodes d’examen
Section intitulée « 3. Méthodes d’examen »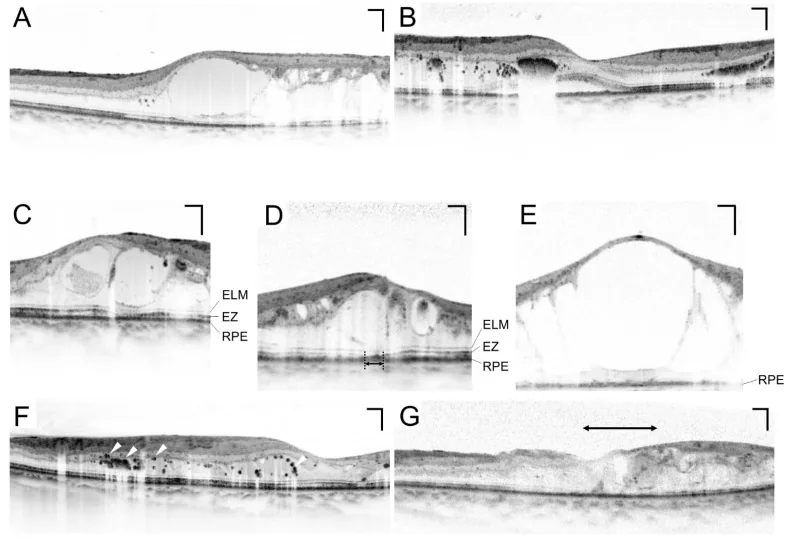
Examen du fond d’œil sous dilatation pupillaire
Section intitulée « Examen du fond d’œil sous dilatation pupillaire »L’examen du fond d’œil sous dilatation pupillaire est l’examen central du dépistage ophtalmologique du diabète. Il est standard de réaliser un examen du fond d’œil après dilatation par des gouttes de tropicamide et de phényléphrine (chlorhydrate de phényléphrine) 4). La photographie stéréoscopique à 7 champs selon l’ETDRS (Early Treatment Diabetic Retinopathy Study) est considérée comme la référence 8).
Les caméras de fond d’œil non mydriatiques sont pratiques et leur utilisation pour le dépistage se répand, avec une sensibilité rapportée de 80 à 90 % 9). Au Royaume-Uni, le programme national de dépistage de la rétinopathie diabétique utilise un système basé sur la photographie numérique non mydriatique du fond d’œil 9).
OCT (Tomographie par Cohérence Optique)
Section intitulée « OCT (Tomographie par Cohérence Optique) »L’OCT est un examen essentiel pour l’évaluation quantitative de l’œdème maculaire. Il permet de mesurer l’épaisseur rétinienne au niveau de la fovéa (CRT) de manière non invasive et répétée, et est indispensable pour le suivi de l’efficacité thérapeutique 10). Une CRT > 300 μm est considérée comme un seuil pour initier le traitement de l’œdème maculaire diabétique (OMD) 10).
Angiographie à la fluorescéine (FA)
Section intitulée « Angiographie à la fluorescéine (FA) »Cet examen consiste à injecter du fluorescéinate de sodium par voie intraveineuse pour visualiser les vaisseaux rétiniens. Il est utilisé pour détecter les zones non perfusées et évaluer les néovaisseaux 8). Il sert à déterminer l’indication de la photocoagulation et est utile pour l’évaluation précise selon la classification ETDRS 8).
Angiographie OCT (OCTA)
Section intitulée « Angiographie OCT (OCTA) »L’OCTA est un examen non invasif qui permet de visualiser en trois dimensions les vaisseaux rétiniens sans utiliser de produit de contraste 11). Il peut être répété comme alternative à l’angiographie à la fluorescéine et est utilisé pour évaluer les zones non perfusées et le réseau capillaire maculaire 11).
Dépistage du fond d’œil par IA
Section intitulée « Dépistage du fond d’œil par IA »L’analyse automatisée du fond d’œil par apprentissage profond entre rapidement en phase pratique. Dans une étude de cohorte multiethnique de Ting et al. (2017), une sensibilité de 87 à 97 % a été rapportée pour la détection automatique de la rétinopathie diabétique, de la suspicion de glaucome et de la DMLA 12). Des dispositifs d’IA approuvés par la FDA américaine (comme IDx-DR) sont également utilisés en pratique, et leur utilisation pour le dépistage en médecine interne et en soins primaires progresse 12).
| Méthode d’examen | Principales indications | Caractéristiques |
|---|---|---|
| Examen du fond d’œil sous dilatation (stéréo 7 champs) | Référence pour l’évaluation du stade | Haute précision, nécessite une dilatation invasive 8) |
| Caméra de fond d’œil sans dilatation pupillaire | Dépistage primaire | Sensibilité 80-90% · Grande commodité 9) |
| OCT | Quantification de l’œdème maculaire et suivi thérapeutique | Non invasif · Quantification CRT 10) |
| Angiographie à la fluorescéine (FA) | Évaluation des zones non perfusées et des néovaisseaux | Invasif · Utilisation de produit de contraste 8) |
| OCTA | Évaluation vasculaire non invasive | Répétable · Sans produit de contraste 11) |
| Dépistage du fond d’œil par IA | Automatisation du dépistage primaire | Sensibilité 87-97% · Pas besoin de spécialiste en ophtalmologie 12) |
Le dépistage du fond d’œil par IA utilisant l’apprentissage profond a montré une précision élevée de 87 à 97 % et est entré en phase pratique 12). Des dispositifs d’IA approuvés par la FDA existent et sont attendus dans les zones manquant de spécialistes en ophtalmologie. Cependant, le dépistage par IA n’est qu’un dépistage primaire ; si une anomalie est détectée, un examen approfondi par un ophtalmologiste est nécessaire.
4. Classification de la rétinopathie diabétique
Section intitulée « 4. Classification de la rétinopathie diabétique »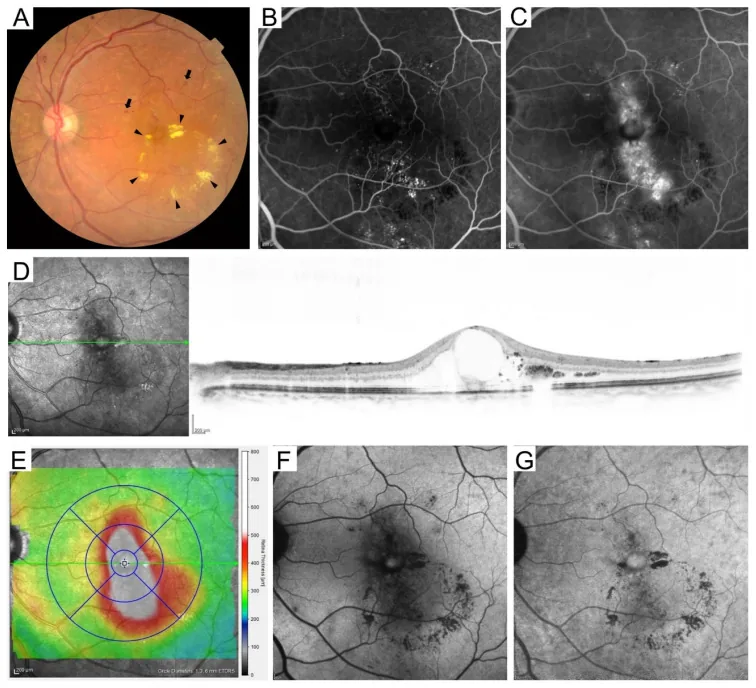
Classification internationale (basée sur l’ETDRS)
Section intitulée « Classification internationale (basée sur l’ETDRS) »La classification internationale de la rétinopathie diabétique comprend 5 stades basés sur les critères ETDRS 8).
| Stade | Principales observations | Conduite à tenir |
|---|---|---|
| Pas de rétinopathie | Aucune anomalie | Dépistage tous les 1 à 2 ans 4) |
| RDNP légère | Microanévrismes uniquement | Surveillance tous les 6 à 12 mois 4) |
| NPDR modérée | Exsudats mous, hémorragies rétiniennes, exsudats durs | Suivi tous les 3 à 6 mois4) |
| NPDR sévère (règle 4-2-1) | Hémorragies rétiniennes dans 4 quadrants, dilatations veineuses en chapelet dans 2 quadrants, IRMA dans 1 quadrant8) | Envisager une PRP précoce, suivi tous les 1 à 3 mois4) |
| Rétinopathie diabétique proliférante (RDP) | NVD, NVE, hémorragie du vitré, décollement de rétine tractionnel8) | PRP, anti-VEGF, chirurgie. Suivi mensuel4) |
- La règle 4-2-1 dans la NPDR sévère désigne un stade où au moins un des critères suivants est rempli : hémorragies rétiniennes dans 4 quadrants, dilatations veineuses en chapelet dans 2 quadrants, ou IRMA (anomalies microvasculaires intrarétiniennes) dans 1 quadrant8).
- Dans la rétinopathie diabétique proliférante (RDP), des néovaisseaux au niveau de la papille (NVD) ou de la rétine (NVE) apparaissent, évoluant vers une hémorragie du vitré et un décollement de rétine tractionnel8).
Œdème maculaire diabétique (OMD)
Section intitulée « Œdème maculaire diabétique (OMD) »L’œdème maculaire diabétique (OMD) est une pathologie pouvant survenir à tout stade de la rétinopathie et constitue la cause la plus fréquente de baisse de vision dans le diabète10).
- Un CSME (œdème maculaire cliniquement significatif) touchant la fovéa est une indication de traitement10)
- En OCT, une CRT > 300 μm est l’un des critères pour débuter le traitement10)
- Les directives de la Société européenne de la rétine (EURETINA) recommandent la thérapie anti-VEGF comme traitement de première intention 10)
Autres complications oculaires
Section intitulée « Autres complications oculaires »- Glaucome néovasculaire : En tant que complication de la PDR, des vaisseaux néoformés apparaissent dans l’iris et l’angle, entraînant un glaucome secondaire
- Cataracte diabétique : Il existe deux formes : la cataracte diabétique vraie (type à progression rapide chez les jeunes) et l’accélération de la cataracte liée à l’âge
- Paralysie des muscles extra-oculaires : Une diplopie due à une paralysie des nerfs crâniens III et VI peut survenir de manière aiguë
5. Stratégie thérapeutique (du dépistage à la coordination des soins)
Section intitulée « 5. Stratégie thérapeutique (du dépistage à la coordination des soins) »Principes de base de la prise en charge médicale
Section intitulée « Principes de base de la prise en charge médicale »La prise en charge médicale de la glycémie, de la pression artérielle et des lipides constitue la base du contrôle de la progression de la rétinopathie diabétique. Les objectifs sont les suivants 6).
- HbA1c : < 7,0 %
- Pression artérielle : < 130/80 mmHg
- LDL-C : < 120 mg/dL
Dans l’étude UKPDS, le groupe avec contrôle glycémique intensif a montré une réduction de 37 % du risque de complications microvasculaires par rapport au groupe de contrôle standard, et une diminution de 1 % de l’HbA1c était associée à une réduction significative du risque de complications 6).
Photocoagulation au laser (panphotocoagulation rétinienne : PRP)
Section intitulée « Photocoagulation au laser (panphotocoagulation rétinienne : PRP) »La panphotocoagulation rétinienne (PRP) est réalisée pour la NPDR sévère à la rétinopathie diabétique proliférante 8). En cautérisant la rétine ischémique, on supprime la production de VEGF et on favorise la régression et la prévention des néovaisseaux. Il s’agit d’un traitement établi par l’ETDRS et constitue le traitement standard pour prévenir la cécité dans la PDR à haut risque 8).
Thérapie anti-VEGF
Section intitulée « Thérapie anti-VEGF »Le traitement de première intention de l’œdème maculaire diabétique (OMD) est l’injection intravitréenne d’anti-VEGF. Les médicaments disponibles sont les suivants 10).
- Ranibizumab (Lucentis) : 0,5 mg/0,05 mL en injection intravitréenne
- Aflibercept (Eylea) : 2 mg/0,05 mL en injection intravitréenne
- Faricimab (Vabysmo) : 6 mg/0,05 mL en injection intravitréenne (anticorps bispécifique Ang-2/VEGF-A)
Vitrectomie
Section intitulée « Vitrectomie »La vitrectomie est réalisée en cas d’hémorragie vitréenne non résorbable ou de décollement de rétine tractionnel 8). Récemment, la vitrectomie par petite incision (25-27 gauge) s’est généralisée, réduisant le caractère invasif de l’intervention.
Administration locale de stéroïdes
Section intitulée « Administration locale de stéroïdes »L’injection intravitréenne de 4 mg/0,1 mL d’acétonide de triamcinolone (TA) est utilisée comme traitement adjuvant de l’OMD 10). Elle est envisagée en cas de réponse insuffisante au traitement anti-VEGF ou chez les patients pseudophakes (après chirurgie de la cataracte).
Fénofibrate
Section intitulée « Fénofibrate »Les études FIELD (2007) et ACCORD Eye ont montré que le fénofibrate ralentit la progression de la rétinopathie diabétique et réduit le besoin de photocoagulation 13). Outre son effet hypolipidémiant, il agirait via l’activation de PPARα, exerçant des effets anti-inflammatoires et anti-angiogéniques 13).
Une détection précoce permet de prévenir plus de 90 % des cas de cécité 2). Le traitement varie selon le stade et le type de complications : pour les cas légers à modérés, la prise en charge médicale du glucose, de la tension artérielle et des lipides est essentielle. Pour la phase non proliférante sévère à proliférante, une photocoagulation au laser (PRP) est réalisée, et pour l’œdème maculaire diabétique, les injections intravitréennes d’anti-VEGF (ranibizumab, aflibercept, faricimab) sont le traitement de première intention. En cas d’hémorragie intravitréenne non résorbable ou de décollement de rétine tractionnel, une vitrectomie est indiquée.
6. Physiopathologie et fondement scientifique du dépistage
Section intitulée « 6. Physiopathologie et fondement scientifique du dépistage »Microangiopathie rétinienne due à l’hyperglycémie
Section intitulée « Microangiopathie rétinienne due à l’hyperglycémie »Plusieurs voies métaboliques induites par l’hyperglycémie sont impliquées dans le développement de la rétinopathie diabétique 14).
- Augmentation de la voie des polyols : la conversion du glucose en sorbitol par l’aldose réductase est accrue, entraînant une augmentation de l’osmolarité intracellulaire et du stress oxydatif.
- Accumulation de produits de glycation avancée (AGE) : leur accumulation dans la membrane basale vasculaire et la matrice extracellulaire altère la fonction vasculaire.
- Activation de la protéine kinase C (PKC) : elle favorise la production de VEGF, impliqué dans l’augmentation de la perméabilité vasculaire et la formation de néovaisseaux.
- Augmentation du stress oxydatif : la production excessive d’espèces réactives de l’oxygène (ROS) altère la fonction des cellules endothéliales.
De la perte des péricytes aux néovaisseaux
Section intitulée « De la perte des péricytes aux néovaisseaux »La perte sélective des péricytes (cellules de soutien de la paroi vasculaire) des capillaires rétiniens est le changement le plus précoce de la rétinopathie diabétique 14). Cette perte fragilise la paroi capillaire, entraînant la formation de microanévrismes. L’augmentation de la perméabilité vasculaire provoque un œdème maculaire, et la non-perfusion capillaire (zones non perfusées) entraîne une ischémie rétinienne 14).
L’augmentation de la production de VEGF par la rétine ischémique est le principal moteur de la formation de néovaisseaux, conduisant à la formation de NVD et NVE. Le VEGF intravitréen est également impliqué dans la pathogénie de l’hémorragie intravitréenne et du décollement de rétine tractionnel 14).
Rentabilité du dépistage
Section intitulée « Rentabilité du dépistage »La rentabilité des programmes de dépistage de la rétinopathie diabétique est soutenue par plusieurs analyses économiques. Une revue systématique de Jones et al. (2010) a montré que le traitement précoce par dépistage est nettement moins coûteux que la prise en charge de la cécité après son apparition, avec un bon rapport coût-efficacité 15).
Les études DCCT et UKPDS ont établi scientifiquement l’importance du contrôle glycémique. Dans le DCCT, l’insulinothérapie intensive chez les patients atteints de diabète de type 1 a réduit de 76 % le risque de nouvelle apparition de rétinopathie et de 54 % le risque de progression 6). L’UKPDS a montré que le contrôle glycémique intensif dans le diabète de type 2 réduisait de 37 % le risque de complications microvasculaires 6).
7. Recherches récentes et perspectives futures
Section intitulée « 7. Recherches récentes et perspectives futures »Mise en œuvre sociale du dépistage automatique par IA
Section intitulée « Mise en œuvre sociale du dépistage automatique par IA »La précision de l’analyse automatique du fond d’œil utilisant l’apprentissage profond a atteint un niveau comparable à celui des ophtalmologistes spécialistes, et sa mise en œuvre sociale progresse 12). Son utilisation pour le dépistage non invasif en médecine interne et en soins primaires devrait permettre de détecter les patients à haut risque qui consultent rarement un ophtalmologiste.
Introduction de caméras de fond d’œil ultra grand angle
Section intitulée « Introduction de caméras de fond d’œil ultra grand angle »Les caméras de fond d’œil ultra grand angle comme Optos couvrent plus de 200° de la rétine en une seule prise de vue, et leur application au dépistage sans dilatation pupillaire progresse 9). Une amélioration de la précision de détection des zones non perfusées de la rétine périphérique et des néovaisseaux a été rapportée, et on attend à la fois une amélioration de la précision du dépistage et une plus grande commodité.
Utilisation de la télémédecine (téléophtalmologie)
Section intitulée « Utilisation de la télémédecine (téléophtalmologie) »La lecture à distance des images du fond d’œil via la télémédecine a fait ses preuves, notamment pour le dépistage de la rétinopathie diabétique 12). Elle contribue à améliorer le taux de participation au dépistage des patients diabétiques dans les régions manquant de spécialistes en ophtalmologie ou dans les zones isolées, et est considérée comme un outil de réduction des inégalités.
Recherche sur les nouveaux médicaments et le risque de rétinopathie
Section intitulée « Recherche sur les nouveaux médicaments et le risque de rétinopathie »Avec la généralisation des agonistes des récepteurs GLP-1 (comme le sémaglutide) et des inhibiteurs SGLT2 (comme l’empagliflozine), les recherches sur l’impact de ces médicaments sur le risque de rétinopathie diabétique progressent 16). Certaines études sur le sémaglutide ont rapporté une augmentation du risque d’aggravation aiguë de la rétinopathie, et l’association avec une aggravation précoce (early worsening) attire l’attention 16). Les recherches sur le mécanisme de l’effet inhibiteur du fénofibrate sur la progression de la rétinopathie diabétique et les attentes pour des essais à plus grande échelle se poursuivent 13).
Biomarqueurs lacrymaux et paramètres vasculaires rétiniens
Section intitulée « Biomarqueurs lacrymaux et paramètres vasculaires rétiniens »Des recherches sont en cours sur le dosage du VEGF et des cytokines inflammatoires par échantillonnage non invasif des larmes, ainsi que sur l’évaluation précoce du risque de rétinopathie par analyse du diamètre des vaisseaux rétiniens et de la fractalité. À l’avenir, il pourrait être possible de quantifier le risque de rétinopathie uniquement par une photographie du fond d’œil.
8. Références
Section intitulée « 8. Références »- Yau JW, Rogers SL, Kawasaki R, et al. Global prevalence and major risk factors of diabetic retinopathy. Diabetes Care. 2012;35(3):556-564.
- Flaxel CJ, Adelman RA, Bailey ST, et al. Diabetic retinopathy Preferred Practice Pattern®. Ophthalmology. 2020;127(1):P66-P145.
- 日本糖尿病眼学会. 糖尿病眼手帳について. https://www.jsod.jp/techo/index.html
- Solomon SD, Chew E, Duh EJ, et al. Diabetic retinopathy: a position statement by the American Diabetes Association. Diabetes Care. 2017;40(3):412-418.
- Morrison JL, Hodgson LA, Lim LL, et al. Diabetic retinopathy in pregnancy: a review. Clin Exp Ophthalmol. 2016;44(4):321-334.
- UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet. 1998;352(9131):837-853.
- The Diabetes Control and Complications Trial Research Group. Early worsening of diabetic retinopathy in the Diabetes Control and Complications Trial. Arch Ophthalmol. 1998;116(7):874-886.
- Early Treatment Diabetic Retinopathy Study Research Group. Grading diabetic retinopathy from stereoscopic color fundus photographs — an extension of the modified Airlie House classification. ETDRS report number 10. Ophthalmology. 1991;98(5 Suppl):786-806.
- Scanlon PH. The English National Screening Programme for diabetic retinopathy 2003-2016. Acta Diabetol. 2017;54(6):515-525.
- Schmidt-Erfurth U, Garcia-Arumi J, Bandello F, et al. Guidelines for the management of diabetic macular edema by the European Society of Retina Specialists (EURETINA). Ophthalmologica. 2017;237(4):185-222.
- Spaide RF, Fujimoto JG, Waheed NK, et al. Optical coherence tomography angiography. Prog Retin Eye Res. 2018;64:1-55.
- Ting DSW, Cheung CY, Lim G, et al. Development and validation of a deep learning system for diabetic retinopathy and related eye diseases using retinal images from multiethnic populations with diabetes. JAMA. 2017;318(22):2211-2223.
- Keech AC, Mitchell P, Summanen PA, et al. Effect of fenofibrate on the need for laser treatment for diabetic retinopathy (FIELD study): a randomised controlled trial. Lancet. 2007;370(9600):1687-1697. doi:10.1016/S0140-6736(07)61607-9.
- Antonetti DA, Klein R, Gardner TW. Diabetic retinopathy. N Engl J Med. 2012;366(13):1227-1239.
- Jones S, Edwards RT. Diabetic retinopathy screening: a systematic review of the economic evidence. Diabet Med. 2010;27(3):249-256.
- Ntentakis DP, Correa VSMC, Ntentaki AM, Delavogia E, Narimatsu T, Efstathiou N, Vavvas DG. Effects of newer-generation anti-diabetics on diabetic retinopathy: a critical review. Graefes Arch Clin Exp Ophthalmol. 2024;262(3):717-752. PMID:37728754. doi:10.1007/s00417-023-06236-5.
