
Guía de cribado ocular en pacientes diabéticos
Puntos clave de un vistazo
Sección titulada «Puntos clave de un vistazo»1. ¿Qué es el cribado oftalmológico para pacientes diabéticos?
Sección titulada «1. ¿Qué es el cribado oftalmológico para pacientes diabéticos?»El cribado oftalmológico para pacientes diabéticos es un sistema de exámenes oculares regulares para detectar tempranamente complicaciones oculares como retinopatía diabética, edema macular diabético, glaucoma neovascular, cataratas y parálisis de músculos extraoculares, y proporcionar una intervención terapéutica adecuada.
La retinopatía diabética es la segunda causa de ceguera adquirida en adultos. Aproximadamente el 30–40% de los pacientes diabéticos en todo el mundo tienen retinopatía, y alrededor del 10% presenta retinopatía que amenaza la visión 1). También se ha informado que alrededor del 20% de los pacientes ya tienen retinopatía en el momento del diagnóstico de diabetes 1), lo que destaca la importancia de iniciar el cribado temprano.
Por otro lado, más del 90% de la ceguera se puede prevenir con un cribado y tratamiento adecuados 2). La retinopatía es asintomática en sus etapas iniciales, y cuando aparecen los síntomas, la enfermedad suele estar bastante avanzada. Por lo tanto, los exámenes oculares regulares son el único medio de detección temprana.
Se estima que el número de pacientes diabéticos en Japón supera los 10 millones, y establecer un sistema para visitas oftalmológicas regulares continuas es un desafío. Las herramientas de colaboración entre medicina interna y oftalmología, como el cuaderno de ojos para diabetes, ayudan a compartir hallazgos de fondo de ojo, fechas de examen y detalles del tratamiento 3).
Para la diabetes tipo 2, se recomienda realizarse un examen oftalmológico inmediatamente en el momento del diagnóstico. Se ha informado que alrededor del 20% de los pacientes ya tienen retinopatía en el momento del diagnóstico 1), y la retinopatía puede estar progresando incluso sin síntomas. Para la diabetes tipo 1, los exámenes oftalmológicos deben comenzar 5 años después del inicio o desde la adolescencia 4). En ambos tipos, los exámenes regulares de fondo de ojo son esenciales incluso antes de que aparezcan síntomas como pérdida de visión.
2. Población objetivo y frecuencia recomendada de cribado
Sección titulada «2. Población objetivo y frecuencia recomendada de cribado»Población objetivo y momento de inicio
Sección titulada «Población objetivo y momento de inicio»El momento de inicio del cribado varía según el tipo y la condición de la diabetes.
- Diabetes tipo 2: Examen oftalmológico inicial en el momento del diagnóstico4)
- Diabetes tipo 1: Iniciar aproximadamente 5 años después del inicio (o en la pubertad), luego continuar con exámenes de fondo de ojo anuales4)
- Diabetes mellitus gestacional (DMG): Examen de fondo de ojo en el primer trimestre, con seguimiento hasta 1 año posparto5)
- Mujeres embarazadas con diabetes preexistente: Examen antes del embarazo o en el primer trimestre, con seguimiento cada trimestre5)
Frecuencia de cribado recomendada (por estadio de la enfermedad)
Sección titulada «Frecuencia de cribado recomendada (por estadio de la enfermedad)»La frecuencia de cribado se determina combinando el estadio de la retinopatía y el estado de control de HbA1c.
| Estadio de la retinopatía | Frecuencia de cribado recomendada |
|---|---|
| Sin retinopatía (HbA1c < 7.0% con buen control) | Cada 1–2 años4) |
| Estadio no proliferativo leve | Cada 6–12 meses4) |
| No proliferativa moderada | Cada 3–6 meses4) |
| No proliferativa grave (preproliferativa) | Cada 1–3 meses4) |
| Retinopatía diabética proliferativa | Cada 1 mes (junto con intervención terapéutica)4) |
Control de HbA1c y progresión de la retinopatía
Sección titulada «Control de HbA1c y progresión de la retinopatía»El control de HbA1c también es un indicador importante para determinar la frecuencia de detección.
El UKPDS (Estudio Prospectivo de Diabetes del Reino Unido) mostró que una reducción del 1% en HbA1c disminuye el riesgo de complicaciones microvasculares en un 37%6). Mantener HbA1c por debajo del 7.0% conduce a una reducción significativa del riesgo de progresión de la retinopatía6).
Por otro lado, la mejora rápida de la glucosa en sangre, como con la introducción de insulina, puede empeorar temporalmente la retinopatía, un fenómeno conocido como “empeoramiento temprano”7). Esto se observó en el DCCT (Estudio de Control y Complicaciones de la Diabetes), y se debe prestar atención al deterioro retiniano a corto plazo después de iniciar insulina7).
Si no hay retinopatía y la HbA1c está bien controlada (por debajo del 7.0%), un examen cada 1–2 años es aceptable. Para retinopatía no proliferativa leve, cada 6–12 meses; moderada, cada 3–6 meses; grave no proliferativa, cada 1–3 meses; y proliferativa, se necesitan exámenes mensuales e intervención terapéutica4). Si la HbA1c es alta o el control glucémico es inestable, se recomienda un seguimiento más frecuente.
3. Métodos de examen
Sección titulada «3. Métodos de examen»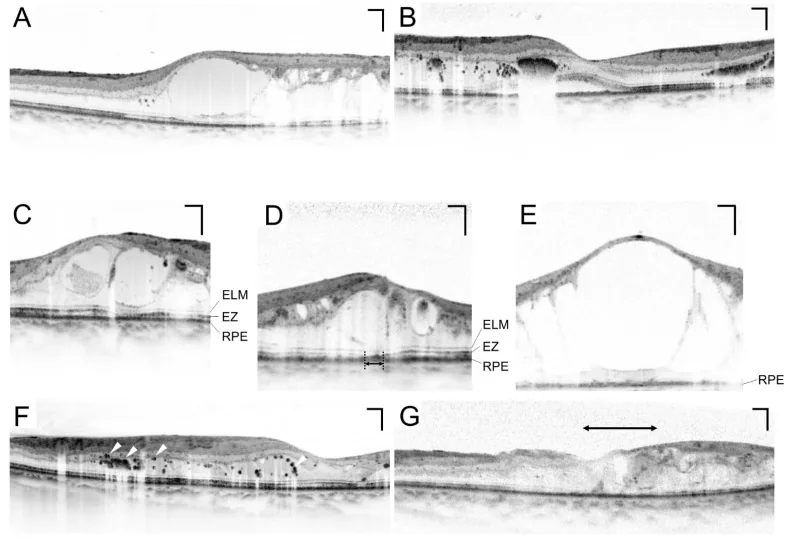
Examen de fondo de ojo con dilatación pupilar
Sección titulada «Examen de fondo de ojo con dilatación pupilar»El examen de fondo de ojo con dilatación pupilar es la prueba central en el cribado oftalmológico diabético. Es estándar realizar el examen de fondo de ojo después de la dilatación pupilar con gotas de tropicamida y fenilefrina (clorhidrato de fenilefrina) 4). La fotografía estereoscópica de 7 campos del Estudio de Tratamiento Temprano de la Retinopatía Diabética (ETDRS) se considera el estándar de referencia 8).
Las cámaras de fondo de ojo sin midriasis son convenientes y su uso en cribado está aumentando, con una sensibilidad reportada del 80–90% 9). En el Programa Nacional de Cribado de Retinopatía Diabética del Reino Unido, se opera un sistema centrado en la fotografía digital de fondo de ojo sin midriasis 9).
Tomografía de Coherencia Óptica (OCT)
Sección titulada «Tomografía de Coherencia Óptica (OCT)»La OCT es esencial para la evaluación cuantitativa del edema macular. Permite medir de forma no invasiva y repetible el grosor retiniano central (CRT) y es indispensable para monitorizar la respuesta al tratamiento 10). Un CRT > 300 μm se considera uno de los umbrales para iniciar el tratamiento del edema macular diabético (EMD) 10).
Angiografía con Fluoresceína (AF)
Sección titulada «Angiografía con Fluoresceína (AF)»Esta prueba consiste en la inyección intravenosa de fluoresceína sódica para visualizar los vasos retinianos, y se utiliza para detectar áreas de no perfusión y evaluar la neovascularización 8). Se emplea para determinar la indicación de fotocoagulación y es útil para la evaluación precisa de la clasificación ETDRS 8).
Angiografía por OCT (OCTA)
Sección titulada «Angiografía por OCT (OCTA)»La OCTA es una prueba no invasiva que puede visualizar tridimensionalmente los vasos retinianos sin usar agentes de contraste 11). Se puede repetir como alternativa a la angiografía con fluoresceína y se aplica para evaluar áreas de no perfusión y la red capilar macular 11).
Cribado de fondo de ojo basado en IA
Sección titulada «Cribado de fondo de ojo basado en IA»El análisis automatizado de fondo de ojo mediante aprendizaje profundo está avanzando rápidamente hacia la fase práctica. En un estudio de cohorte multiétnico de Ting et al. (2017), se reportó una sensibilidad del 87–97% para la detección automatizada de retinopatía diabética, sospecha de glaucoma y degeneración macular asociada a la edad 12). Dispositivos de IA aprobados por la FDA de EE. UU. (como IDx-DR) ya están en uso clínico, y su aplicación en cribado en medicina interna y atención primaria está progresando 12).
| Método de examen | Indicación principal | Características |
|---|---|---|
| Examen de fondo de ojo con dilatación (7 campos estéreo) | Estándar de referencia para estadificación | Alta precisión; requiere dilatación invasiva 8) |
| Cámara de fondo de ojo sin midriasis | Cribado primario | Sensibilidad 80–90%, alta conveniencia 9) |
| OCT | Cuantificación del edema macular y monitorización del tratamiento | No invasivo, cuantificación de CRT 10) |
| Angiografía fluoresceínica (FA) | Evaluación de áreas de no perfusión y neovascularización | Invasivo, uso de contraste 8) |
| OCTA | Evaluación vascular no invasiva | Repetible, sin necesidad de contraste 11) |
| Cribado de fondo de ojo con IA | Cribado primario automatizado | Sensibilidad 87–97%, no requiere oftalmólogo 12) |
El cribado de fondo de ojo con IA mediante aprendizaje profundo ha reportado una alta precisión con una sensibilidad del 87–97%, y ya se encuentra en fase práctica 12). Existen dispositivos de IA aprobados por la FDA, y se espera su uso en áreas con escasez de oftalmólogos. Sin embargo, el cribado con IA es solo un cribado primario; si se detecta una anomalía, es necesario un examen detallado por un oftalmólogo.
4. Clasificación de la retinopatía diabética
Sección titulada «4. Clasificación de la retinopatía diabética»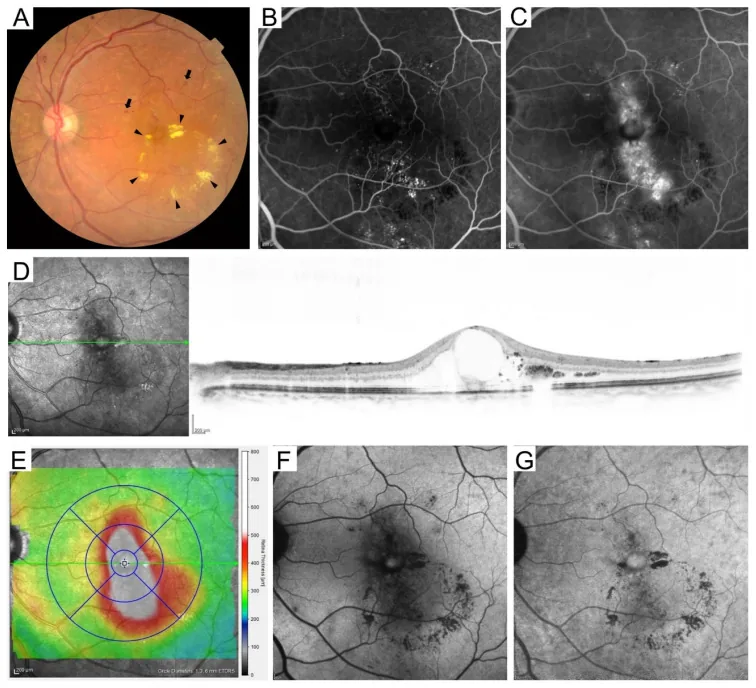
Clasificación internacional (basada en ETDRS)
Sección titulada «Clasificación internacional (basada en ETDRS)»La clasificación internacional de la retinopatía diabética consta de cinco etapas basadas en los criterios ETDRS 8).
| Estadio | Hallazgos principales | Manejo |
|---|---|---|
| Sin retinopatía | Sin anomalías | Cribado cada 1–2 años 4) |
| No proliferativa leve (RDNP) | Solo microaneurismas | Seguimiento cada 6–12 meses 4) |
| NPDR moderada | Exudados blandos, hemorragias retinianas, exudados duros | Seguimiento cada 3–6 meses4) |
| NPDR grave (regla 4-2-1) | Hemorragias retinianas en 4 cuadrantes, dilatación venosa en rosario en 2 cuadrantes, IRMA en 1 cuadrante8) | Considerar PRP temprano; seguimiento cada 1–3 meses4) |
| Retinopatía diabética proliferativa (RDP) | NVD, NVE, hemorragia vítrea, desprendimiento de retina traccional8) | PRP, anti-VEGF, cirugía. Seguimiento mensual4) |
- La regla 4-2-1 en NPDR grave se refiere a un estadio que cumple cualquiera de los siguientes: hemorragias retinianas en 4 cuadrantes, dilatación venosa en rosario en 2 cuadrantes, o IRMA (anomalías microvasculares intraretinianas) en 1 cuadrante8).
- En la retinopatía diabética proliferativa (RDP) aparecen neovascularización del disco óptico (NVD) y neovascularización retiniana (NVE), progresando a hemorragia vítrea y desprendimiento de retina traccional8).
Edema macular diabético (EMD)
Sección titulada «Edema macular diabético (EMD)»El edema macular diabético (EMD) es una afección que puede ocurrir en cualquier etapa de la retinopatía y es la causa más común de pérdida de visión en la diabetes10).
- El CSME (edema macular clínicamente significativo) que afecta la fóvea es una indicación de tratamiento10)
- En la OCT, un CRT > 300 μm se considera uno de los criterios para iniciar el tratamiento10)
- Las guías de la Sociedad Europea de Especialistas en Retina (EURETINA) recomiendan la terapia anti-VEGF como tratamiento de primera línea 10)
Otras complicaciones oculares
Sección titulada «Otras complicaciones oculares»- Glaucoma neovascular: Como complicación de la RDP, se forman nuevos vasos en el iris y el ángulo, causando glaucoma secundario
- Catarata diabética: Hay dos formas: catarata diabética verdadera (progresión rápida en pacientes jóvenes) y aceleración de la catarata relacionada con la edad
- Parálisis de músculos extraoculares: Puede ocurrir diplopía aguda debido a parálisis del tercer o sexto nervio craneal
5. Estrategia de tratamiento (del cribado a la colaboración terapéutica)
Sección titulada «5. Estrategia de tratamiento (del cribado a la colaboración terapéutica)»Fundamentos del manejo médico
Sección titulada «Fundamentos del manejo médico»El manejo médico de la glucosa en sangre, la presión arterial y los lípidos es la base para suprimir la progresión de la retinopatía diabética. Los valores objetivo son los siguientes 6).
- HbA1c: <7.0%
- Presión arterial: <130/80 mmHg
- LDL-C: <120 mg/dL
En el UKPDS, el grupo de control intensivo de glucosa redujo el riesgo de complicaciones microvasculares en un 37% en comparación con el grupo de manejo convencional, y una reducción del 1% en la HbA1c se asoció con una disminución significativa del riesgo de complicaciones 6).
Fotocoagulación con láser (panfotocoagulación retiniana: PRP)
Sección titulada «Fotocoagulación con láser (panfotocoagulación retiniana: PRP)»Se realiza panfotocoagulación retiniana (PRP) para la NPDR grave a la retinopatía diabética proliferativa 8). Al cauterizar la retina isquémica, se suprime la producción de VEGF, logrando la regresión y prevención de nuevos vasos. Este tratamiento fue establecido por el ETDRS y es el estándar para prevenir la ceguera en la RDP de alto riesgo 8).
Terapia anti-VEGF
Sección titulada «Terapia anti-VEGF»El tratamiento de primera línea para el edema macular diabético (EMD) es la inyección intravítrea de anti-VEGF. Los medicamentos disponibles son los siguientes 10).
- Ranibizumab (Lucentis): 0.5 mg/0.05 mL inyección intravítrea
- Aflibercept (Eylea): 2 mg/0.05 mL inyección intravítrea
- Faricimab (Vabysmo): 6 mg/0.05 mL inyección intravítrea (anticuerpo biespecífico Ang-2/VEGF-A)
Vitrectomía
Sección titulada «Vitrectomía»Se realiza vitrectomía para hemorragia vítrea no absorbible y desprendimiento de retina traccional 8). En los últimos años, la vitrectomía de pequeña incisión (calibre 25-27) se ha generalizado, reduciendo la invasividad quirúrgica.
Administración local de esteroides
Sección titulada «Administración local de esteroides»La inyección intravítrea de triamcinolona acetonida (TA) 4 mg/0.1 mL se utiliza como tratamiento adyuvante para el EMD 10). Se considera en casos con respuesta insuficiente a la terapia anti-VEGF o en ojos pseudofáquicos (después de cirugía de cataratas).
Fenofibrato
Sección titulada «Fenofibrato»En el estudio FIELD (2007) y el estudio ACCORD Eye, el grupo de fenofibrato mostró supresión de la progresión de la retinopatía diabética y reducción de la necesidad de fotocoagulación 13). Además de su efecto reductor de lípidos, se cree que la activación de PPARα contribuye a los efectos antiinflamatorios y antiangiogénicos 13).
La detección temprana puede prevenir más del 90% de la ceguera 2). El tratamiento varía según la etapa y el tipo de complicaciones. En casos leves a moderados, el manejo médico de la glucosa en sangre, la presión arterial y los lípidos es el pilar. En etapas no proliferativas graves a proliferativas, se realiza fotocoagulación con láser (PRP), y para el edema macular diabético, las inyecciones intravítreas anti-VEGF (ranibizumab, aflibercept, faricimab) son de primera línea. La vitrectomía está indicada para hemorragia vítrea no absorbible o desprendimiento de retina traccional.
6. Fisiopatología y base científica del cribado
Sección titulada «6. Fisiopatología y base científica del cribado»Daño microvascular retiniano por hiperglucemia
Sección titulada «Daño microvascular retiniano por hiperglucemia»El desarrollo de la retinopatía diabética involucra múltiples vías metabólicas desencadenadas por la hiperglucemia 14).
- Vía del poliol aumentada: La conversión aumentada de glucosa a sorbitol por la aldosa reductasa conduce a un aumento de la osmolaridad intracelular y estrés oxidativo.
- Acumulación de AGE (productos finales de glicación avanzada): La acumulación en la membrana basal vascular y la matriz extracelular deteriora la función vascular.
- Activación de PKC (proteína quinasa C): Promueve la producción de VEGF, contribuyendo al aumento de la permeabilidad vascular y la neovascularización.
- Aumento del estrés oxidativo: La sobreproducción de especies reactivas de oxígeno (ROS) daña la función de las células endoteliales.
De la pérdida de pericitos a la neovascularización
Sección titulada «De la pérdida de pericitos a la neovascularización»La pérdida selectiva de pericitos (células de soporte de la pared vascular) en los capilares retinianos es el cambio más temprano en la retinopatía diabética 14). La pérdida de pericitos debilita las paredes capilares, lo que lleva a la formación de microaneurismas. El aumento de la permeabilidad vascular causa edema macular, y la no perfusión capilar (áreas no perfundidas) conduce a isquemia retiniana 14).
El aumento de la producción de VEGF desde la retina isquémica es el principal impulsor de la neovascularización, formando NVD y NVE. El VEGF intravítreo también contribuye a la patología de la hemorragia vítrea y el desprendimiento de retina traccional 14).
Rentabilidad del cribado
Sección titulada «Rentabilidad del cribado»La rentabilidad de los programas de cribado de retinopatía diabética está respaldada por múltiples análisis económicos. Una revisión sistemática de Jones et al. (2010) mostró que el tratamiento temprano mediante cribado es significativamente menos costoso que los costos de manejo después de la ceguera, demostrando una alta rentabilidad 15).
DCCT y UKPDS establecieron científicamente la importancia del control glucémico. En DCCT, la terapia intensiva con insulina redujo el riesgo de retinopatía de nueva aparición en un 76% y la progresión en un 54% en diabetes tipo 1 6). UKPDS mostró que el control glucémico intensivo redujo el riesgo de complicaciones microvasculares en un 37% en diabetes tipo 2 6).
7. Investigación más reciente y perspectivas futuras
Sección titulada «7. Investigación más reciente y perspectivas futuras»Implementación social del cribado automatizado basado en IA
Sección titulada «Implementación social del cribado automatizado basado en IA»La precisión del análisis automatizado de fondo de ojo mediante aprendizaje profundo ha alcanzado un nivel comparable al de los especialistas en oftalmología, y su implementación social está avanzando 12). Se espera que su uso en cribado no invasivo en medicina interna y atención primaria ayude a identificar pacientes de alto riesgo con bajas tasas de consulta oftalmológica.
Introducción de cámaras de fondo de ojo de campo ultraamplio
Sección titulada «Introducción de cámaras de fondo de ojo de campo ultraamplio»Las cámaras de fondo de ojo de campo ultraamplio como Optos cubren más de 200° de la retina en una sola toma, y su aplicación en cribado sin midriasis está avanzando 9). Se ha informado de una mejora en la precisión para detectar áreas de no perfusión retiniana periférica y neovascularización, y se espera lograr tanto una mayor precisión del cribado como comodidad.
Uso de la telemedicina (teleoftalmología)
Sección titulada «Uso de la telemedicina (teleoftalmología)»La lectura remota de imágenes de fondo de ojo mediante telemedicina ha acumulado experiencia, principalmente en el cribado de retinopatía diabética 12). Contribuye a mejorar las tasas de cribado en pacientes diabéticos en áreas con escasez de oftalmólogos o regiones remotas, y se destaca como una herramienta para reducir las disparidades.
Investigación sobre nuevos fármacos y riesgo de retinopatía
Sección titulada «Investigación sobre nuevos fármacos y riesgo de retinopatía»Con la generalización de los agonistas del receptor GLP-1 (como semaglutida) y los inhibidores de SGLT2 (como empagliflozina), avanza la investigación sobre el impacto de estos fármacos en el riesgo de retinopatía diabética 16). En algunos ensayos con semaglutida se ha informado de un aumento del riesgo de empeoramiento agudo de la retinopatía, y se presta especial atención a su asociación con el empeoramiento temprano 16). Continúa el interés en dilucidar el mecanismo del efecto inhibidor del fenofibrato sobre la progresión de la RD y en la realización de más ensayos a gran escala 13).
Biomarcadores lagrimales y parámetros vasculares retinianos
Sección titulada «Biomarcadores lagrimales y parámetros vasculares retinianos»Se están realizando investigaciones sobre la cuantificación no invasiva de VEGF y citoquinas inflamatorias mediante muestreo de lágrimas, así como la evaluación del riesgo temprano de retinopatía mediante el diámetro de los vasos retinianos y el análisis fractal. En el futuro, podría ser posible cuantificar el riesgo de retinopatía utilizando solo la fotografía de fondo de ojo.
8. Referencias
Sección titulada «8. Referencias»- Yau JW, Rogers SL, Kawasaki R, et al. Global prevalence and major risk factors of diabetic retinopathy. Diabetes Care. 2012;35(3):556-564.
- Flaxel CJ, Adelman RA, Bailey ST, et al. Diabetic retinopathy Preferred Practice Pattern®. Ophthalmology. 2020;127(1):P66-P145.
- 日本糖尿病眼学会. 糖尿病眼手帳について. https://www.jsod.jp/techo/index.html
- Solomon SD, Chew E, Duh EJ, et al. Diabetic retinopathy: a position statement by the American Diabetes Association. Diabetes Care. 2017;40(3):412-418.
- Morrison JL, Hodgson LA, Lim LL, et al. Diabetic retinopathy in pregnancy: a review. Clin Exp Ophthalmol. 2016;44(4):321-334.
- UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet. 1998;352(9131):837-853.
- The Diabetes Control and Complications Trial Research Group. Early worsening of diabetic retinopathy in the Diabetes Control and Complications Trial. Arch Ophthalmol. 1998;116(7):874-886.
- Early Treatment Diabetic Retinopathy Study Research Group. Grading diabetic retinopathy from stereoscopic color fundus photographs — an extension of the modified Airlie House classification. ETDRS report number 10. Ophthalmology. 1991;98(5 Suppl):786-806.
- Scanlon PH. The English National Screening Programme for diabetic retinopathy 2003-2016. Acta Diabetol. 2017;54(6):515-525.
- Schmidt-Erfurth U, Garcia-Arumi J, Bandello F, et al. Guidelines for the management of diabetic macular edema by the European Society of Retina Specialists (EURETINA). Ophthalmologica. 2017;237(4):185-222.
- Spaide RF, Fujimoto JG, Waheed NK, et al. Optical coherence tomography angiography. Prog Retin Eye Res. 2018;64:1-55.
- Ting DSW, Cheung CY, Lim G, et al. Development and validation of a deep learning system for diabetic retinopathy and related eye diseases using retinal images from multiethnic populations with diabetes. JAMA. 2017;318(22):2211-2223.
- Keech AC, Mitchell P, Summanen PA, et al. Effect of fenofibrate on the need for laser treatment for diabetic retinopathy (FIELD study): a randomised controlled trial. Lancet. 2007;370(9600):1687-1697. doi:10.1016/S0140-6736(07)61607-9.
- Antonetti DA, Klein R, Gardner TW. Diabetic retinopathy. N Engl J Med. 2012;366(13):1227-1239.
- Jones S, Edwards RT. Diabetic retinopathy screening: a systematic review of the economic evidence. Diabet Med. 2010;27(3):249-256.
- Ntentakis DP, Correa VSMC, Ntentaki AM, Delavogia E, Narimatsu T, Efstathiou N, Vavvas DG. Effects of newer-generation anti-diabetics on diabetic retinopathy: a critical review. Graefes Arch Clin Exp Ophthalmol. 2024;262(3):717-752. PMID:37728754. doi:10.1007/s00417-023-06236-5.
