
Screening oculistico nei pazienti diabetici (Linee guida per lo screening oculare diabetico)
Punti chiave in sintesi
Sezione intitolata “Punti chiave in sintesi”1. Che cos’è lo screening oculistico nei pazienti diabetici?
Sezione intitolata “1. Che cos’è lo screening oculistico nei pazienti diabetici?”Lo screening oculistico nei pazienti diabetici è un sistema di esami oculistici regolari volto a rilevare precocemente le complicanze oculari come retinopatia diabetica, edema maculare diabetico, glaucoma neovascolare, cataratta e paralisi dei muscoli oculari esterni, al fine di consentire un intervento terapeutico appropriato.
La retinopatia diabetica è la seconda causa di cecità evitabile negli adulti. A livello mondiale, circa il 30-40% dei pazienti diabetici presenta retinopatia e circa il 10% presenta retinopatia che causa deficit visivo (retinopatia proliferante)1). È stato inoltre riportato che circa il 20% dei pazienti presenta già retinopatia al momento della diagnosi di diabete1), sottolineando l’importanza di iniziare precocemente lo screening.
D’altra parte, uno screening e un intervento terapeutico adeguati possono prevenire oltre il 90% dei casi di cecità2). La retinopatia è asintomatica nelle fasi iniziali e quando compaiono i sintomi soggettivi, le lesioni sono spesso già avanzate. Pertanto, esami oculistici regolari sono l’unico mezzo per la diagnosi precoce.
Il numero di pazienti diabetici in Giappone è stimato in oltre 10 milioni e la creazione di un sistema per continuare regolari visite oculistiche è una sfida. Gli strumenti di collaborazione tra internisti e oculisti, come il libretto oculistico per il diabete, facilitano la condivisione dei reperti del fondo oculare, delle date degli esami e dei trattamenti3).
Nel diabete di tipo 2, si raccomanda di sottoporsi a un esame oculistico immediatamente dopo la diagnosi. È stato riportato che circa il 20% dei pazienti presenta già retinopatia al momento della diagnosi di diabete1) e la retinopatia può progredire anche in assenza di sintomi. Nel diabete di tipo 1, si raccomanda di iniziare gli esami oculistici circa 5 anni dopo l’insorgenza della malattia o dopo la pubertà4). Indipendentemente dal tipo, esami regolari del fondo oculare sono essenziali prima ancora che compaiano sintomi soggettivi come la riduzione dell’acuità visiva.
2. Popolazione target e frequenza raccomandata dello screening
Sezione intitolata “2. Popolazione target e frequenza raccomandata dello screening”Soggetti interessati e momento di inizio
Sezione intitolata “Soggetti interessati e momento di inizio”Il momento di inizio dello screening varia in base al tipo e alla condizione del diabete.
- Diabete di tipo 2: eseguire la prima visita oculistica al momento della diagnosi4)
- Diabete di tipo 1: iniziare circa 5 anni dopo l’esordio (o la pubertà), quindi proseguire con un esame del fondo oculare annuale4)
- Diabete gestazionale (GDM): eseguire un esame del fondo oculare nel primo trimestre di gravidanza e seguire fino a un anno dopo il parto5)
- Donne in gravidanza con diabete preesistente: eseguire l’esame prima della gravidanza o nel primo trimestre, quindi seguire ogni trimestre5)
Frequenza di screening raccomandata (per stadio)
Sezione intitolata “Frequenza di screening raccomandata (per stadio)”La frequenza dello screening è determinata combinando lo stadio della retinopatia e il controllo dell’HbA1c.
| Stadio della retinopatia | Frequenza di screening raccomandata |
|---|---|
| Assenza di retinopatia (buon controllo con HbA1c < 7,0%) | Ogni 1-2 anni4) |
| Fase non proliferativa lieve | Ogni 6-12 mesi4) |
| Retinopatia non proliferante moderata | Ogni 3–6 mesi4) |
| Retinopatia non proliferante grave (preproliferante) | Ogni 1–3 mesi4) |
| Retinopatia diabetica proliferante | Mensilmente (in parallelo al trattamento)4) |
Controllo dell’HbA1c e progressione della retinopatia
Sezione intitolata “Controllo dell’HbA1c e progressione della retinopatia”Il controllo dell’HbA1c è anche un indicatore importante per determinare la frequenza dello screening.
Nello studio UKPDS (United Kingdom Prospective Diabetes Study) è stato dimostrato che una riduzione dell’1% dell’HbA1c riduce il rischio di complicanze microvascolari del 37%6). Il mantenimento di un’HbA1c inferiore al 7,0% porta a una significativa riduzione del rischio di progressione della retinopatia6).
D’altra parte, un miglioramento rapido della glicemia, ad esempio con l’introduzione dell’insulina, può causare un temporaneo peggioramento della retinopatia, noto come ‘early worsening’7). Questo fenomeno è stato confermato nello studio DCCT (Diabetes Control and Complications Trial), ed è necessario prestare attenzione a un deterioramento del fondo oculare a breve termine dopo l’introduzione dell’insulina7).
In assenza di retinopatia e con un buon controllo dell’HbA1c (inferiore al 7,0%), un esame ogni 1–2 anni è considerato sufficiente. Nella retinopatia non proliferante lieve, ogni 6–12 mesi; in quella moderata, ogni 3–6 mesi; in quella grave non proliferante, ogni 1–3 mesi; e in quella proliferante, sono necessari esami mensili e interventi terapeutici4). Se l’HbA1c è elevata o il controllo glicemico è instabile, si raccomanda un follow-up più ravvicinato.
3. Metodi di esame
Sezione intitolata “3. Metodi di esame”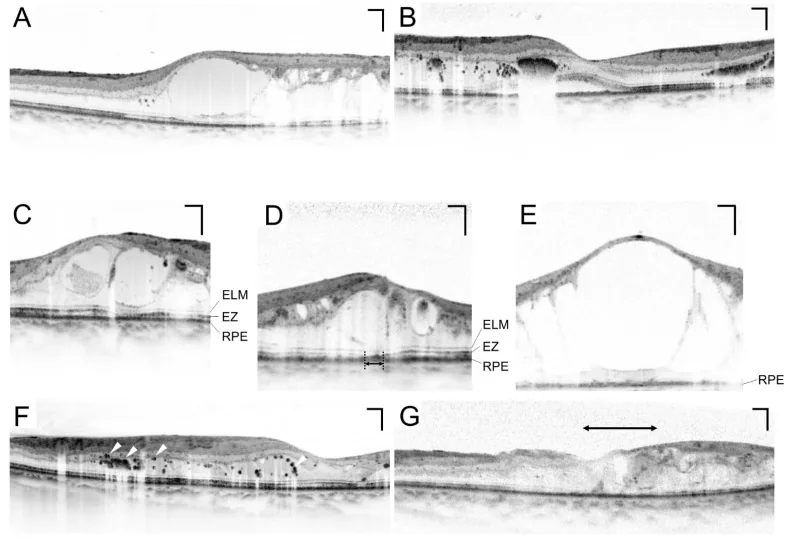
Esame del fondo oculare in midriasi
Sezione intitolata “Esame del fondo oculare in midriasi”L’esame del fondo oculare in midriasi è l’esame centrale dello screening oculistico diabetico. È standard eseguire l’esame del fondo oculare dopo dilatazione pupillare con gocce di tropicamide e fenilefrina (fenilefrina cloridrato) 4). La fotografia stereo a 7 campi secondo l’ETDRS (Early Treatment Diabetic Retinopathy Study) è considerata lo standard di riferimento 8).
Le fotocamere del fondo oculare non midriatiche sono pratiche e il loro uso nello screening si sta diffondendo, con una sensibilità riportata dell’80-90% 9). Nel programma nazionale di screening della retinopatia diabetica del Regno Unito, viene utilizzato un sistema basato sulla fotografia digitale non midriatica del fondo oculare 9).
OCT (Tomografia a Coerenza Ottica)
Sezione intitolata “OCT (Tomografia a Coerenza Ottica)”L’OCT è un esame essenziale per la valutazione quantitativa dell’edema maculare. Consente di misurare lo spessore retinico centrale (CRT) in modo non invasivo e ripetuto, ed è indispensabile per il monitoraggio dell’efficacia terapeutica 10). Un CRT > 300 μm è considerato uno dei criteri per iniziare il trattamento dell’edema maculare diabetico (DME) 10).
Angiografia con fluoresceina (FA)
Sezione intitolata “Angiografia con fluoresceina (FA)”Questo esame prevede l’iniezione endovenosa di fluoresceina sodica per visualizzare i vasi retinici. Viene utilizzato per rilevare aree di non perfusione e valutare la neovascolarizzazione 8). È impiegato per determinare l’indicazione alla fotocoagulazione ed è utile per la valutazione precisa secondo la classificazione ETDRS 8).
Angiografia OCT (OCTA)
Sezione intitolata “Angiografia OCT (OCTA)”L’OCTA è un esame non invasivo che consente di visualizzare tridimensionalmente i vasi retinici senza l’uso di mezzo di contrasto 11). Può essere ripetuto come alternativa all’angiografia con fluoresceina ed è utilizzato per valutare le aree di non perfusione e la rete capillare maculare 11).
Screening del fondo oculare con IA
Sezione intitolata “Screening del fondo oculare con IA”L’analisi automatizzata del fondo oculare mediante deep learning sta rapidamente entrando nella fase pratica. In uno studio di coorte multietnico di Ting et al. (2017), è stata riportata una sensibilità dell’87-97% per il rilevamento automatico di retinopatia diabetica, sospetto glaucoma e AMD 12). Dispositivi di IA approvati dalla FDA statunitense (come IDx-DR) sono anch’essi in uso pratico, e il loro impiego per lo screening in medicina interna e cure primarie è in aumento 12).
| Metodo di esame | Indicazioni principali | Caratteristiche |
|---|---|---|
| Esame del fondo oculare in midriasi (stereo 7 campi) | Riferimento per la valutazione dello stadio | Alta precisione, richiede midriasi invasiva 8) |
| Camera per fundus senza dilatazione pupillare | Screening primario | Sensibilità 80-90% · Alta praticità 9) |
| OCT | Quantificazione dell’edema maculare e monitoraggio terapeutico | Non invasivo · Quantificazione CRT 10) |
| Angiografia con fluoresceina (FA) | Valutazione di aree non perfuse e neovascolarizzazione | Invasivo · Uso di mezzo di contrasto 8) |
| OCTA | Valutazione vascolare non invasiva | Ripetibile · Senza mezzo di contrasto 11) |
| Screening del fundus con IA | Automazione dello screening primario | Sensibilità 87-97% · Nessun bisogno di oculista 12) |
Lo screening del fondo oculare con IA basato sul deep learning ha mostrato un’elevata sensibilità dell’87-97% ed è entrato in fase pratica 12). Esistono dispositivi IA approvati dalla FDA e si prevede il loro utilizzo in aree con carenza di oculisti. Tuttavia, lo screening con IA è solo uno screening primario; se viene rilevata un’anomalia, è necessario un esame approfondito da parte di un oculista.
4. Classificazione della retinopatia diabetica
Sezione intitolata “4. Classificazione della retinopatia diabetica”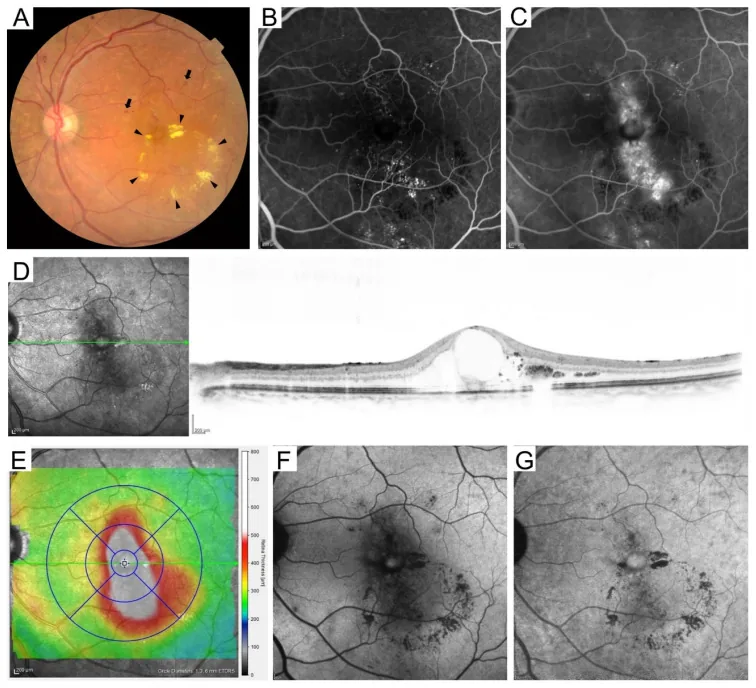
Classificazione internazionale (basata su ETDRS)
Sezione intitolata “Classificazione internazionale (basata su ETDRS)”La classificazione internazionale della retinopatia diabetica comprende 5 stadi basati sui criteri ETDRS 8).
| Stadio | Reperti principali | Gestione |
|---|---|---|
| Nessuna retinopatia | Nessuna anomalia | Screening ogni 1-2 anni 4) |
| RDNP lieve | Solo microaneurismi | Follow-up ogni 6-12 mesi 4) |
| NPDR moderata | Essudati molli, emorragie retiniche, essudati duri | Follow-up ogni 3-6 mesi4) |
| NPDR severa (regola 4-2-1) | Emorragie retiniche in 4 quadranti, dilatazioni venose a rosario in 2 quadranti, IRMA in 1 quadrante8) | Considerare PRP precoce, follow-up ogni 1-3 mesi4) |
| Retinopatia diabetica proliferante (RDP) | NVD, NVE, emorragia vitreale, distacco di retina tractionale8) | PRP, anti-VEGF, chirurgia. Follow-up mensile4) |
- La regola 4-2-1 nella NPDR severa indica uno stadio in cui è soddisfatto almeno uno dei seguenti criteri: emorragie retiniche in 4 quadranti, dilatazioni venose a rosario in 2 quadranti, o IRMA (anomalie microvascolari intraretiniche) in 1 quadrante8).
- Nella retinopatia diabetica proliferante (RDP) compaiono neovascolarizzazioni del disco ottico (NVD) o neovascolarizzazioni retiniche (NVE), che progrediscono verso emorragia vitreale e distacco di retina tractionale8).
Edema maculare diabetico (EMD)
Sezione intitolata “Edema maculare diabetico (EMD)”L’edema maculare diabetico (EMD) è una condizione che può verificarsi in qualsiasi stadio della retinopatia ed è la causa più frequente di riduzione della vista nel diabete10).
- Un CSME (edema maculare clinicamente significativo) che coinvolge la fovea è indicazione al trattamento10)
- All’OCT, un CRT > 300 μm è uno dei criteri per iniziare il trattamento10)
- Le linee guida della European Society of Retina (EURETINA) raccomandano la terapia anti-VEGF come trattamento di prima linea 10)
Altre complicanze oculari
Sezione intitolata “Altre complicanze oculari”- Glaucoma neovascolare: Come complicanza della PDR, si formano vasi neoformati nell’iride e nell’angolo, causando glaucoma secondario
- Cataratta diabetica: Esistono due forme: la cataratta diabetica vera (a rapida progressione nei giovani) e l’accelerazione della cataratta senile
- Paralisi dei muscoli extraoculari: Può insorgere acutamente diplopia dovuta a paralisi del III e VI nervo cranico
5. Strategia terapeutica (dallo screening al coordinamento delle cure)
Sezione intitolata “5. Strategia terapeutica (dallo screening al coordinamento delle cure)”Principi di base della gestione medica
Sezione intitolata “Principi di base della gestione medica”La gestione medica di glicemia, pressione arteriosa e lipidi costituisce la base per il controllo della progressione della retinopatia diabetica. I valori target sono i seguenti 6).
- HbA1c: < 7,0%
- Pressione arteriosa: < 130/80 mmHg
- LDL-C: < 120 mg/dL
Nello studio UKPDS, il gruppo con controllo glicemico intensivo ha mostrato una riduzione del 37% del rischio di complicanze microvascolari rispetto al gruppo di controllo standard, e una riduzione dell’1% dell’HbA1c è stata associata a una significativa diminuzione del rischio di complicanze 6).
Fotocoagulazione laser (panfotocoagulazione retinica: PRP)
Sezione intitolata “Fotocoagulazione laser (panfotocoagulazione retinica: PRP)”La panfotocoagulazione retinica (PRP) viene eseguita per NPDR grave fino alla retinopatia diabetica proliferante 8). La cauterizzazione della retina ischemica sopprime la produzione di VEGF e favorisce la regressione e la prevenzione dei vasi neoformati. È un trattamento stabilito dall’ETDRS ed è il trattamento standard per prevenire la cecità nella PDR ad alto rischio 8).
Terapia anti-VEGF
Sezione intitolata “Terapia anti-VEGF”Il trattamento di prima linea per l’edema maculare diabetico (DME) è l’iniezione intravitreale di anti-VEGF. I farmaci disponibili sono i seguenti 10).
- Ranibizumab (Lucentis): 0,5 mg/0,05 mL iniezione intravitreale
- Aflibercept (Eylea): 2 mg/0,05 mL iniezione intravitreale
- Faricimab (Vabysmo): 6 mg/0,05 mL iniezione intravitreale (anticorpo bispecifico Ang-2/VEGF-A)
Vitrectomia
Sezione intitolata “Vitrectomia”La vitrectomia viene eseguita in caso di emorragia vitreale non riassorbibile o distacco di retina tractionale 8). Negli ultimi anni si è diffusa la vitrectomia a piccola incisione (25-27 gauge), riducendo l’invasività chirurgica.
Somministrazione locale di steroidi
Sezione intitolata “Somministrazione locale di steroidi”L’iniezione intravitreale di 4 mg/0,1 mL di triamcinolone acetonide (TA) viene utilizzata come trattamento adiuvante del DME 10). Viene presa in considerazione in caso di risposta insufficiente alla terapia anti-VEGF o in occhi pseudofachici (dopo intervento di cataratta).
Fenofibrato
Sezione intitolata “Fenofibrato”Negli studi FIELD (2007) e ACCORD Eye è stato dimostrato che il fenofibrato rallenta la progressione della retinopatia diabetica e riduce la necessità di fotocoagulazione 13). Oltre all’effetto ipolipemizzante, si ritiene che siano coinvolti effetti antinfiammatori e antiangiogenici attraverso l’attivazione di PPARα 13).
Con una diagnosi precoce si può prevenire oltre il 90% dei casi di cecità 2). Il trattamento varia in base allo stadio e al tipo di complicanze: nei casi lievi-moderati, la gestione medica di glicemia, pressione arteriosa e lipidi è fondamentale. Nello stadio non proliferativo grave-proliferativo si esegue la fotocoagulazione laser (PRP), mentre per l’edema maculare diabetico le iniezioni intravitreali di anti-VEGF (ranibizumab, aflibercept, faricimab) sono la terapia di prima linea. In caso di emorragia vitreale non riassorbibile o distacco di retina tractionale, è indicata la vitrectomia.
6. Fisiopatologia e basi scientifiche dello screening
Sezione intitolata “6. Fisiopatologia e basi scientifiche dello screening”Microangiopatia retinica da iperglicemia
Sezione intitolata “Microangiopatia retinica da iperglicemia”Nello sviluppo della retinopatia diabetica sono coinvolte diverse vie metaboliche indotte dall’iperglicemia 14).
- Aumento della via dei polioli: la conversione del glucosio in sorbitolo da parte dell’aldoso reduttasi è aumentata, portando a un aumento dell’osmolarità intracellulare e dello stress ossidativo.
- Accumulo di AGE (prodotti finali di glicazione avanzata): il loro accumulo nella membrana basale vascolare e nella matrice extracellulare compromette la funzione vascolare.
- Attivazione della proteina chinasi C (PKC): promuove la produzione di VEGF, coinvolto nell’aumento della permeabilità vascolare e nella neovascolarizzazione.
- Aumento dello stress ossidativo: la produzione eccessiva di specie reattive dell’ossigeno (ROS) danneggia la funzione delle cellule endoteliali.
Dalla perdita dei periciti alla neovascolarizzazione
Sezione intitolata “Dalla perdita dei periciti alla neovascolarizzazione”La perdita selettiva dei periciti (cellule di supporto della parete vascolare) dei capillari retinici è il cambiamento più precoce nella retinopatia diabetica 14). La perdita dei periciti indebolisce la parete capillare, portando alla formazione di microaneurismi. L’aumento della permeabilità vascolare causa edema maculare, e la non perfusione capillare (aree non perfuse) porta a ischemia retinica 14).
L’aumento della produzione di VEGF da parte della retina ischemica è il principale motore della neovascolarizzazione, portando alla formazione di NVD e NVE. Il VEGF intravitreale è anche coinvolto nella patogenesi dell’emorragia vitreale e del distacco di retina tractionale 14).
Rapporto costo-efficacia dello screening
Sezione intitolata “Rapporto costo-efficacia dello screening”Il rapporto costo-efficacia dei programmi di screening per la retinopatia diabetica è supportato da diverse analisi economiche. Una revisione sistematica di Jones et al. (2010) ha mostrato che il trattamento precoce tramite screening è significativamente meno costoso rispetto alla gestione della cecità ed è costo-efficace 15).
DCCT e UKPDS hanno stabilito scientificamente l’importanza del controllo glicemico. Nel DCCT, la terapia insulinica intensiva nel diabete di tipo 1 ha ridotto il rischio di nuova insorgenza di retinopatia del 76% e il rischio di progressione del 54% 6). L’UKPDS ha mostrato che il controllo glicemico intensivo nel diabete di tipo 2 riduce il rischio di complicanze microvascolari del 37% 6).
7. Ricerche recenti e prospettive future
Sezione intitolata “7. Ricerche recenti e prospettive future”Implementazione sociale dello screening automatico tramite IA
Sezione intitolata “Implementazione sociale dello screening automatico tramite IA”La precisione dell’analisi automatica del fondo oculare tramite deep learning ha raggiunto un livello paragonabile a quello degli oftalmologi specialisti e la sua implementazione sociale sta progredendo 12). Il suo utilizzo per lo screening non invasivo in medicina interna e cure primarie dovrebbe consentire di individuare pazienti ad alto rischio con basso tasso di visite oculistiche.
Introduzione di fotocamere per fondo oculare ad angolo ultra-wide
Sezione intitolata “Introduzione di fotocamere per fondo oculare ad angolo ultra-wide”Le fotocamere per fondo oculare ad angolo ultra-wide come Optos coprono oltre 200° della retina in un unico scatto e la loro applicazione per lo screening senza dilatazione pupillare sta progredendo 9). È stato riportato un miglioramento della precisione nel rilevamento delle aree non perfuse della retina periferica e dei neovasi, e si prevede un miglioramento sia della precisione dello screening che della praticità.
Utilizzo della telemedicina (tele-oftalmologia)
Sezione intitolata “Utilizzo della telemedicina (tele-oftalmologia)”La lettura remota delle immagini del fondo oculare tramite telemedicina ha dimostrato la sua efficacia, in particolare nello screening della retinopatia diabetica 12). Contribuisce a migliorare il tasso di partecipazione allo screening dei pazienti diabetici in aree con carenza di oftalmologi o in zone remote ed è considerata uno strumento per ridurre le disuguaglianze.
Ricerca su nuovi farmaci e rischio di retinopatia
Sezione intitolata “Ricerca su nuovi farmaci e rischio di retinopatia”Con la diffusione degli agonisti del recettore GLP-1 (come il semaglutide) e degli inibitori SGLT2 (come l’empagliflozin), la ricerca sull’impatto di questi farmaci sul rischio di retinopatia diabetica sta progredendo 16). In alcuni studi sul semaglutide è stato riportato un aumento del rischio di peggioramento acuto della retinopatia, e in particolare viene prestata attenzione alla relazione con il peggioramento precoce (early worsening) 16). Continuano gli studi sul meccanismo dell’effetto inibitorio del fenofibrato sulla progressione della retinopatia diabetica e le aspettative per ulteriori studi su larga scala 13).
Biomarcatori lacrimali e parametri vascolari retinici
Sezione intitolata “Biomarcatori lacrimali e parametri vascolari retinici”Sono in corso ricerche sulla quantificazione del VEGF e delle citochine infiammatorie tramite campionamento non invasivo delle lacrime, nonché sulla valutazione precoce del rischio di retinopatia mediante analisi del diametro dei vasi retinici e dell’analisi frattale. In futuro, potrebbe essere possibile quantificare il rischio di retinopatia solo con una fotografia del fondo oculare.
8. Riferimenti
Sezione intitolata “8. Riferimenti”- Yau JW, Rogers SL, Kawasaki R, et al. Global prevalence and major risk factors of diabetic retinopathy. Diabetes Care. 2012;35(3):556-564.
- Flaxel CJ, Adelman RA, Bailey ST, et al. Diabetic retinopathy Preferred Practice Pattern®. Ophthalmology. 2020;127(1):P66-P145.
- 日本糖尿病眼学会. 糖尿病眼手帳について. https://www.jsod.jp/techo/index.html
- Solomon SD, Chew E, Duh EJ, et al. Diabetic retinopathy: a position statement by the American Diabetes Association. Diabetes Care. 2017;40(3):412-418.
- Morrison JL, Hodgson LA, Lim LL, et al. Diabetic retinopathy in pregnancy: a review. Clin Exp Ophthalmol. 2016;44(4):321-334.
- UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet. 1998;352(9131):837-853.
- The Diabetes Control and Complications Trial Research Group. Early worsening of diabetic retinopathy in the Diabetes Control and Complications Trial. Arch Ophthalmol. 1998;116(7):874-886.
- Early Treatment Diabetic Retinopathy Study Research Group. Grading diabetic retinopathy from stereoscopic color fundus photographs — an extension of the modified Airlie House classification. ETDRS report number 10. Ophthalmology. 1991;98(5 Suppl):786-806.
- Scanlon PH. The English National Screening Programme for diabetic retinopathy 2003-2016. Acta Diabetol. 2017;54(6):515-525.
- Schmidt-Erfurth U, Garcia-Arumi J, Bandello F, et al. Guidelines for the management of diabetic macular edema by the European Society of Retina Specialists (EURETINA). Ophthalmologica. 2017;237(4):185-222.
- Spaide RF, Fujimoto JG, Waheed NK, et al. Optical coherence tomography angiography. Prog Retin Eye Res. 2018;64:1-55.
- Ting DSW, Cheung CY, Lim G, et al. Development and validation of a deep learning system for diabetic retinopathy and related eye diseases using retinal images from multiethnic populations with diabetes. JAMA. 2017;318(22):2211-2223.
- Keech AC, Mitchell P, Summanen PA, et al. Effect of fenofibrate on the need for laser treatment for diabetic retinopathy (FIELD study): a randomised controlled trial. Lancet. 2007;370(9600):1687-1697. doi:10.1016/S0140-6736(07)61607-9.
- Antonetti DA, Klein R, Gardner TW. Diabetic retinopathy. N Engl J Med. 2012;366(13):1227-1239.
- Jones S, Edwards RT. Diabetic retinopathy screening: a systematic review of the economic evidence. Diabet Med. 2010;27(3):249-256.
- Ntentakis DP, Correa VSMC, Ntentaki AM, Delavogia E, Narimatsu T, Efstathiou N, Vavvas DG. Effects of newer-generation anti-diabetics on diabetic retinopathy: a critical review. Graefes Arch Clin Exp Ophthalmol. 2024;262(3):717-752. PMID:37728754. doi:10.1007/s00417-023-06236-5.
