
糖尿病患者眼科筛查指南
一目了然的要点
Section titled “一目了然的要点”1. 糖尿病患者的眼科筛查是什么?
Section titled “1. 糖尿病患者的眼科筛查是什么?”糖尿病患者的眼科筛查是指定期进行眼科检查,以早期发现糖尿病视网膜病变、糖尿病黄斑水肿、新生血管性青光眼、白内障、眼外肌麻痹等眼部并发症,并进行适当的治疗干预。
糖尿病视网膜病变是成人后天失明的第二大原因。全球约30-40%的糖尿病患者存在视网膜病变,约10%存在致盲性视网膜病变1)。据报道,约20%的患者在糖尿病诊断时已存在视网膜病变1),因此早期开始筛查非常重要。
另一方面,通过适当的筛查和治疗干预,90%以上的失明是可以预防的2)。视网膜病变早期无症状,当出现自觉症状时病变往往已相当进展。因此,定期眼科检查是唯一的早期发现手段。
日本国内糖尿病患者估计超过1000万人,建立持续定期就诊眼科的系统是一个挑战。糖尿病眼手册等内科-眼科协作工具有助于共享眼底所见、检查日期和治疗内容3)。
2型糖尿病建议在诊断时立即进行眼科检查。据报道,约20%的患者在诊断时已存在视网膜病变1),即使无症状也可能有视网膜病变进展。1型糖尿病在发病或青春期后5年开始眼科检查4)。无论哪种类型,在出现视力下降等症状之前,定期眼底检查都是必不可少的。
2. 筛查对象和推荐频率
Section titled “2. 筛查对象和推荐频率”对象人群和开始时间
Section titled “对象人群和开始时间”筛查的开始时间因糖尿病的类型和病情而异。
- 2型糖尿病:诊断时进行首次眼科检查4)
- 1型糖尿病:发病(或青春期)后约5年开始,之后每年进行一次眼底检查4)
- 妊娠期糖尿病(GDM):妊娠早期进行眼底检查,产后随访至1年5)
- 孕前已患糖尿病的孕妇:孕前或妊娠早期进行检查,每个孕期随访一次5)
推荐筛查频率(按病程分期)
Section titled “推荐筛查频率(按病程分期)”筛查频率根据视网膜病变的分期和HbA1c控制情况综合决定。
| 视网膜病变分期 | 推荐筛查频率 |
|---|---|
| 无视网膜病变(HbA1c < 7.0%,控制良好) | 每1~2年一次4) |
| 轻度非增殖期 | 每6~12个月一次4) |
| 中度非增殖期 | 每3~6个月4) |
| 重度非增殖期(增殖前期) | 每1~3个月4) |
| 增殖性糖尿病视网膜病变 | 每月1次(与治疗干预并行)4) |
HbA1c控制与视网膜病变进展
Section titled “HbA1c控制与视网膜病变进展”HbA1c控制也是决定筛查频率的重要指标。
UKPDS(英国前瞻性糖尿病研究)表明,HbA1c降低1%可使微血管并发症风险降低37%6)。维持HbA1c低于7.0%可显著降低视网膜病变进展风险6)。
另一方面,胰岛素导入等导致的血糖急剧改善可能会暂时加重视网膜病变,即“早期恶化”现象7)。DCCT(糖尿病控制与并发症试验)已确认此现象,需注意胰岛素导入后的短期眼底恶化7)。
若无视网膜病变且HbA1c控制良好(低于7.0%),可每12年检查一次。轻度非增殖期每612个月,中度每36个月,重度非增殖期每13个月,增殖期需每月检查并治疗干预4)。若HbA1c较高或血糖控制不稳定,建议缩短随访间隔。
3. 检查方法
Section titled “3. 检查方法”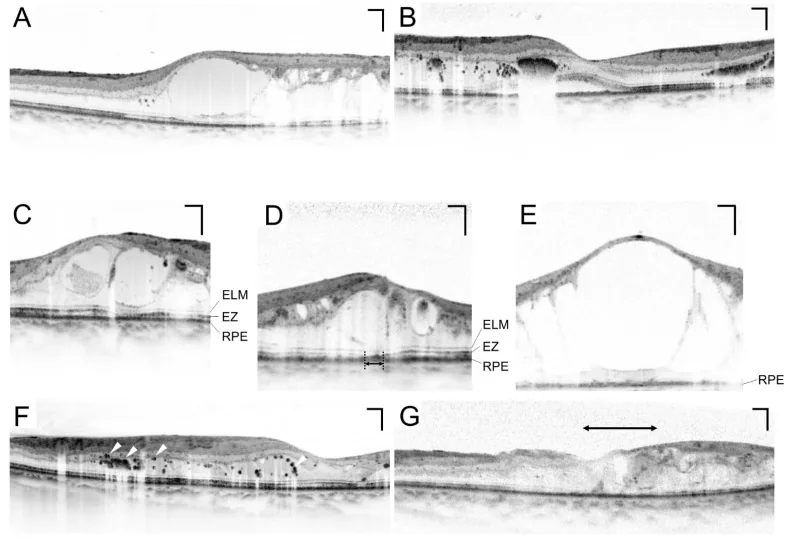
散瞳眼底检查
Section titled “散瞳眼底检查”散瞳眼底检查是糖尿病眼科筛查的核心检查。标准做法是使用托吡卡胺和去氧肾上腺素(盐酸去氧肾上腺素)滴眼液散瞳后进行眼底检查4)。早期治疗糖尿病视网膜病变研究(ETDRS)的7视野立体照相被认为是参考标准8)。
免散瞳眼底相机方便易用,在筛查中越来越广泛使用,据报道灵敏度为80-90%9)。英国国家糖尿病视网膜病变筛查项目采用以免散瞳数字眼底照相为核心的系统9)。
光学相干断层扫描(OCT)
Section titled “光学相干断层扫描(OCT)”OCT是黄斑水肿定量评估的必要检查。它可以无创、重复测量中心视网膜厚度(CRT),对监测治疗效果至关重要10)。CRT > 300 μm被认为是开始治疗糖尿病黄斑水肿(DME)的参考指标之一10)。
荧光素眼底血管造影(FA)
Section titled “荧光素眼底血管造影(FA)”该检查通过静脉注射荧光素钠来显示视网膜血管,用于检测无灌注区和评估新生血管8)。它用于判断光凝治疗的适应证,并有助于ETDRS分类的精确评估8)。
OCT血管成像(OCTA)
Section titled “OCT血管成像(OCTA)”OCTA是一种无创检查,无需使用造影剂即可三维显示视网膜血管11)。它可以作为荧光素血管造影的替代方法重复进行,用于评估无灌注区和黄斑毛细血管网11)。
基于人工智能的眼底筛查
Section titled “基于人工智能的眼底筛查”基于深度学习的眼底自动分析正迅速进入实用阶段。Ting等人(2017年)的多民族队列研究报告,在自动检测糖尿病视网膜病变、疑似青光眼和年龄相关性黄斑变性方面,灵敏度为87-97%12)。美国FDA批准的人工智能设备(如IDx-DR)已投入临床应用,在内科和初级保健中的筛查应用正在推进12)。
| 检查方法 | 主要适应证 | 特点 |
|---|---|---|
| 散瞳眼底检查(7视野立体) | 分期参考标准 | 高精度;需要侵入性散瞳8) |
| 免散瞳眼底相机 | 初步筛查 | 灵敏度80–90%,便利性高9) |
| OCT | 黄斑水肿定量及治疗监测 | 无创,CRT定量10) |
| 荧光眼底造影(FA) | 无灌注区及新生血管评估 | 有创,使用造影剂8) |
| OCTA | 无创血管评估 | 可重复,无需造影剂11) |
| AI眼底筛查 | 自动化初步筛查 | 灵敏度87–97%,无需眼科专家12) |
使用深度学习的AI眼底筛查已被报道具有87-97%的高灵敏度,现已进入实用阶段12)。存在FDA批准的AI设备,预计在眼科专家短缺地区得到应用。但AI筛查仅为初步筛查,若检测到异常,需要眼科专家进行详细检查。
4. 糖尿病视网膜病变的分类
Section titled “4. 糖尿病视网膜病变的分类”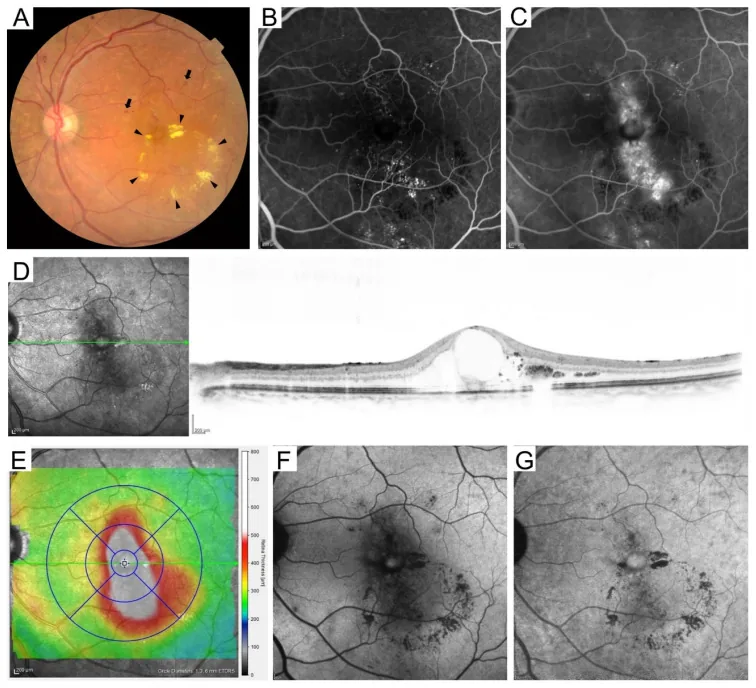
国际分类(基于ETDRS)
Section titled “国际分类(基于ETDRS)”糖尿病视网膜病变的国际分类基于ETDRS标准,分为五个阶段8)。
| 分期 | 主要表现 | 管理方案 |
|---|---|---|
| 无视网膜病变 | 无异常 | 每1-2年筛查一次4) |
| 轻度非增殖期(NPDR) | 仅微动脉瘤 | 每6-12个月随访一次4) |
| 中度NPDR | 软性渗出、视网膜出血、硬性渗出 | 每3~6个月随访一次4) |
| 重度NPDR(4-2-1法则) | 4个象限的视网膜出血、2个象限的静脉串珠样扩张、1个象限的IRMA8) | 考虑早期PRP;每1~3个月随访一次4) |
| 增殖性糖尿病视网膜病变(PDR) | NVD、NVE、玻璃体积血、牵拉性视网膜脱离8) | PRP、抗VEGF、手术。每月随访4) |
- 重度NPDR的4-2-1法则是指满足以下任一条件的阶段:4个象限的视网膜出血、2个象限的静脉串珠样扩张、或1个象限的IRMA(视网膜内微血管异常)8)。
- 增殖性糖尿病视网膜病变(PDR)出现视盘新生血管(NVD)和视网膜新生血管(NVE),并进展为玻璃体积血和牵拉性视网膜脱离8)。
糖尿病黄斑水肿(DME)
Section titled “糖尿病黄斑水肿(DME)”糖尿病黄斑水肿(DME)是可在视网膜病变任何阶段发生的病变,是糖尿病视力下降的最常见原因10)。
- 累及中心凹的CSME(临床显著性黄斑水肿)是治疗适应症10)
- OCT上CRT > 300 μm被认为是开始治疗的参考标准之一10)
- 欧洲视网膜专家学会(EURETINA)指南推荐抗VEGF治疗作为一线选择 10)
其他眼部并发症
Section titled “其他眼部并发症”- 新生血管性青光眼:作为PDR的并发症,虹膜和房角出现新生血管,导致继发性青光眼
- 糖尿病性白内障:有两种形式:真性糖尿病性白内障(年轻患者快速进展型)和加速年龄相关性白内障
- 眼外肌麻痹:第三或第六脑神经麻痹引起的复视可能急性发作
5. 治疗方针(从筛查到治疗协作)
Section titled “5. 治疗方针(从筛查到治疗协作)”内科管理基础
Section titled “内科管理基础”血糖、血压和血脂的内科管理是抑制糖尿病视网膜病变进展的基础。目标值如下 6)。
- HbA1c:<7.0%
- 血压:<130/80 mmHg
- LDL-C:<120 mg/dL
在UKPDS中,强化血糖管理组与常规管理组相比,微血管并发症风险降低37%,HbA1c降低1%与并发症风险显著减少相关 6)。
激光光凝(全视网膜光凝:PRP)
Section titled “激光光凝(全视网膜光凝:PRP)”对于重度NPDR至增殖性糖尿病视网膜病变,实施全视网膜光凝(PRP)8)。通过烧灼缺血视网膜,抑制VEGF产生,促进新生血管消退和预防。这是ETDRS确立的治疗方法,是高危PDR预防失明的标准治疗 8)。
抗VEGF治疗
Section titled “抗VEGF治疗”糖尿病黄斑水肿(DME)的一线治疗是抗VEGF玻璃体内注射。可用的药物如下10)。
- 雷珠单抗(Lucentis):0.5 mg/0.05 mL 玻璃体内注射
- 阿柏西普(Eylea):2 mg/0.05 mL 玻璃体内注射
- 法瑞西单抗(Vabysmo):6 mg/0.05 mL 玻璃体内注射(Ang-2/VEGF-A双特异性抗体)
对于非吸收性玻璃体积血和牵拉性视网膜脱离,进行玻璃体手术8)。近年来,小切口玻璃体手术(25-27G)已普及,手术创伤得以减轻。
局部类固醇给药
Section titled “局部类固醇给药”曲安奈德(TA)4 mg/0.1 mL 玻璃体内注射用作DME的辅助治疗10)。对于抗VEGF治疗反应不佳的病例或人工晶状体眼(白内障术后)可考虑使用。
在FIELD研究(2007年)和ACCORD Eye研究中,非诺贝特组显示出糖尿病视网膜病变进展的抑制和光凝需求率的降低13)。除了降脂作用外,PPARα的激活被认为参与抗炎和抗血管生成作用13)。
早期发现可预防90%以上的失明2)。治疗方法因病程和并发症类型而异,轻中度病例以血糖、血压和血脂的内科管理为主。重度非增殖期至增殖期进行激光光凝(PRP),糖尿病黄斑水肿首选抗VEGF玻璃体内注射(雷珠单抗、阿柏西普、法瑞西单抗)。对于不吸收的玻璃体出血或牵拉性视网膜脱离,适用玻璃体切除术。
6. 病理生理学与筛查的科学依据
Section titled “6. 病理生理学与筛查的科学依据”高血糖引起的视网膜微血管损伤
Section titled “高血糖引起的视网膜微血管损伤”糖尿病视网膜病变的发生涉及高血糖引发的多种代谢途径14)。
- 多元醇通路增强:醛糖还原酶将葡萄糖转化为山梨醇增加,导致细胞内渗透压升高和氧化应激增加。
- AGE(晚期糖基化终末产物)积累:在血管基底膜和细胞外基质中积累,损害血管功能。
- PKC(蛋白激酶C)激活:促进VEGF产生,参与血管通透性增加和新生血管形成。
- 氧化应激增加:活性氧(ROS)过量产生损害内皮细胞功能。
从周细胞丢失到新生血管
Section titled “从周细胞丢失到新生血管”视网膜毛细血管周细胞(血管壁支持细胞)的选择性丢失是糖尿病视网膜病变最早的变化14)。周细胞丢失使毛细血管壁脆弱,形成微动脉瘤。血管通透性增加导致黄斑水肿,毛细血管无灌注(无灌注区)导致视网膜缺血14)。
缺血视网膜产生的VEGF增加是新生血管形成的主要驱动因素,形成NVD和NVE。玻璃体内的VEGF也参与玻璃体出血和牵拉性视网膜脱离的病理过程14)。
筛查的成本效益
Section titled “筛查的成本效益”多项经济分析支持糖尿病视网膜病变筛查项目的成本效益。Jones等人(2010年)的系统评价显示,通过筛查进行早期治疗与失明后的管理成本相比显著更低,具有高成本效益15)。
DCCT和UKPDS科学地确立了血糖控制的重要性。DCCT显示,在1型糖尿病中,强化胰岛素治疗使视网膜病变的新发风险降低76%,进展风险降低54%6)。UKPDS显示,在2型糖尿病中,强化血糖控制使微血管并发症风险降低37%6)。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”基于AI的自动筛查的社会实施
Section titled “基于AI的自动筛查的社会实施”使用深度学习的眼底自动分析精度已达到与眼科专家相当的水平,社会实施正在推进中12)。在内科和初级保健中用于非侵入性筛查,有望发现眼科就诊率低的高危患者。
超广角眼底相机的引入
Section titled “超广角眼底相机的引入”Optos等超广角眼底相机一次拍摄可覆盖视网膜200°以上,其在免散瞳筛查中的应用正在推进9)。已有报告称其检测周边视网膜无灌注区和新生血管的精度有所提高,有望同时提高筛查精度和便利性。
远程医疗(远程眼科学)的应用
Section titled “远程医疗(远程眼科学)的应用”利用远程医疗进行远程眼底读片已在糖尿病视网膜病变筛查方面积累了经验12)。它有助于提高眼科专家短缺地区或偏远地区糖尿病患者的筛查就诊率,作为消除差距的工具而受到关注。
新药与视网膜病变风险的研究
Section titled “新药与视网膜病变风险的研究”随着GLP-1受体激动剂(如司美格鲁肽)和SGLT2抑制剂(如恩格列净)的普及,关于这些药物对糖尿病视网膜病变风险影响的研究正在推进16)。司美格鲁肽的一些试验报告了急性期视网膜病变恶化风险增加,特别是与早期恶化的关联受到关注16)。对非诺贝特抑制DR进展的机制阐明以及进一步大规模试验的期待仍在持续13)。
泪液生物标志物与视网膜血管参数
Section titled “泪液生物标志物与视网膜血管参数”通过非侵入性泪液采样定量VEGF和炎症细胞因子,以及利用视网膜血管直径和分形分析进行早期视网膜病变风险评估的研究正在进行中。未来可能仅通过眼底相机拍摄即可量化视网膜病变风险。
8. 参考文献
Section titled “8. 参考文献”- Yau JW, Rogers SL, Kawasaki R, et al. Global prevalence and major risk factors of diabetic retinopathy. Diabetes Care. 2012;35(3):556-564.
- Flaxel CJ, Adelman RA, Bailey ST, et al. Diabetic retinopathy Preferred Practice Pattern®. Ophthalmology. 2020;127(1):P66-P145.
- 日本糖尿病眼学会. 糖尿病眼手帳について. https://www.jsod.jp/techo/index.html
- Solomon SD, Chew E, Duh EJ, et al. Diabetic retinopathy: a position statement by the American Diabetes Association. Diabetes Care. 2017;40(3):412-418.
- Morrison JL, Hodgson LA, Lim LL, et al. Diabetic retinopathy in pregnancy: a review. Clin Exp Ophthalmol. 2016;44(4):321-334.
- UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet. 1998;352(9131):837-853.
- The Diabetes Control and Complications Trial Research Group. Early worsening of diabetic retinopathy in the Diabetes Control and Complications Trial. Arch Ophthalmol. 1998;116(7):874-886.
- Early Treatment Diabetic Retinopathy Study Research Group. Grading diabetic retinopathy from stereoscopic color fundus photographs — an extension of the modified Airlie House classification. ETDRS report number 10. Ophthalmology. 1991;98(5 Suppl):786-806.
- Scanlon PH. The English National Screening Programme for diabetic retinopathy 2003-2016. Acta Diabetol. 2017;54(6):515-525.
- Schmidt-Erfurth U, Garcia-Arumi J, Bandello F, et al. Guidelines for the management of diabetic macular edema by the European Society of Retina Specialists (EURETINA). Ophthalmologica. 2017;237(4):185-222.
- Spaide RF, Fujimoto JG, Waheed NK, et al. Optical coherence tomography angiography. Prog Retin Eye Res. 2018;64:1-55.
- Ting DSW, Cheung CY, Lim G, et al. Development and validation of a deep learning system for diabetic retinopathy and related eye diseases using retinal images from multiethnic populations with diabetes. JAMA. 2017;318(22):2211-2223.
- Keech AC, Mitchell P, Summanen PA, et al. Effect of fenofibrate on the need for laser treatment for diabetic retinopathy (FIELD study): a randomised controlled trial. Lancet. 2007;370(9600):1687-1697. doi:10.1016/S0140-6736(07)61607-9.
- Antonetti DA, Klein R, Gardner TW. Diabetic retinopathy. N Engl J Med. 2012;366(13):1227-1239.
- Jones S, Edwards RT. Diabetic retinopathy screening: a systematic review of the economic evidence. Diabet Med. 2010;27(3):249-256.
- Ntentakis DP, Correa VSMC, Ntentaki AM, Delavogia E, Narimatsu T, Efstathiou N, Vavvas DG. Effects of newer-generation anti-diabetics on diabetic retinopathy: a critical review. Graefes Arch Clin Exp Ophthalmol. 2024;262(3):717-752. PMID:37728754. doi:10.1007/s00417-023-06236-5.
