
Augenärztliches Screening bei Diabetespatienten (Diabetic Eye Screening Guidelines)
Auf einen Blick
Abschnitt betitelt „Auf einen Blick“1. Was ist das augenärztliche Screening bei Diabetikern?
Abschnitt betitelt „1. Was ist das augenärztliche Screening bei Diabetikern?“Das augenärztliche Screening bei Diabetikern ist ein System regelmäßiger augenärztlicher Untersuchungen zur Früherkennung von Augenkomplikationen wie diabetischer Retinopathie, diabetischem Makulaödem, Neovaskularisationsglaukom, Katarakt und äußerer Augenmuskellähmung, um eine geeignete therapeutische Intervention zu ermöglichen.
Die diabetische Retinopathie ist die zweithäufigste Ursache für Erblindung im Erwachsenenalter. Weltweit haben etwa 30–40 % der Diabetiker eine Retinopathie, und etwa 10 % haben eine sehbeeinträchtigende Retinopathie (proliferative Retinopathie)1). Es wurde auch berichtet, dass etwa 20 % der Patienten bereits zum Zeitpunkt der Diabetesdiagnose eine Retinopathie aufweisen1), was die Bedeutung eines frühzeitigen Screenings unterstreicht.
Andererseits können durch geeignetes Screening und therapeutische Intervention über 90 % der Erblindungen verhindert werden2). Die Retinopathie ist im Frühstadium asymptomatisch, und wenn subjektive Symptome auftreten, sind die Läsionen oft bereits fortgeschritten. Daher sind regelmäßige augenärztliche Untersuchungen das einzige Mittel zur Früherkennung.
Die Zahl der Diabetiker in Japan wird auf über 10 Millionen geschätzt, und die Einrichtung eines Systems zur Fortsetzung regelmäßiger augenärztlicher Untersuchungen ist eine Herausforderung. Kooperationsinstrumente zwischen Internisten und Augenärzten, wie der Diabetes-Augen-Pass, erleichtern den Austausch von Fundusbefunden, Untersuchungsterminen und Behandlungsinhalten3).
Bei Typ-2-Diabetes wird empfohlen, unmittelbar nach der Diagnose eine augenärztliche Untersuchung durchführen zu lassen. Es wurde berichtet, dass etwa 20 % der Patienten bereits zum Zeitpunkt der Diabetesdiagnose eine Retinopathie aufweisen1), und die Retinopathie kann auch ohne Symptome fortschreiten. Bei Typ-1-Diabetes wird empfohlen, etwa 5 Jahre nach Krankheitsbeginn oder nach der Pubertät mit den augenärztlichen Untersuchungen zu beginnen4). Unabhängig vom Typ sind regelmäßige Fundusuntersuchungen bereits vor dem Auftreten subjektiver Symptome wie Sehverschlechterung unerlässlich.
2. Zielgruppe und empfohlene Häufigkeit des Screenings
Abschnitt betitelt „2. Zielgruppe und empfohlene Häufigkeit des Screenings“Zielpersonen und Beginn
Abschnitt betitelt „Zielpersonen und Beginn“Der Zeitpunkt des Beginns des Screenings variiert je nach Art und Zustand des Diabetes.
- Typ-2-Diabetes: Erste augenärztliche Untersuchung zum Zeitpunkt der Diagnose durchführen4)
- Typ-1-Diabetes: Etwa 5 Jahre nach Beginn (oder Pubertät) beginnen, danach jährliche Fundusuntersuchung fortsetzen4)
- Gestationsdiabetes (GDM): Fundusuntersuchung im ersten Trimester der Schwangerschaft durchführen und bis ein Jahr nach der Entbindung nachverfolgen5)
- Schwangere mit vorbestehendem Diabetes: Untersuchung vor der Schwangerschaft oder im ersten Trimester durchführen, dann in jedem Trimester nachverfolgen5)
Empfohlene Screening-Häufigkeit (nach Stadium)
Abschnitt betitelt „Empfohlene Screening-Häufigkeit (nach Stadium)“Die Screening-Häufigkeit wird basierend auf dem Stadium der Retinopathie und der HbA1c-Kontrolle festgelegt.
| Stadium der Retinopathie | Empfohlene Screening-Häufigkeit |
|---|---|
| Keine Retinopathie (gute Kontrolle mit HbA1c < 7,0%) | Alle 1–2 Jahre4) |
| Leichte nicht-proliferative Phase | Alle 6–12 Monate4) |
| Mäßige nicht-proliferative Retinopathie | Alle 3–6 Monate4) |
| Schwere nicht-proliferative Retinopathie (präproliferativ) | Alle 1–3 Monate4) |
| Proliferative diabetische Retinopathie | Monatlich (parallel zur Behandlung)4) |
HbA1c-Kontrolle und Retinopathie-Progression
Abschnitt betitelt „HbA1c-Kontrolle und Retinopathie-Progression“Die HbA1c-Kontrolle ist auch ein wichtiger Indikator für die Bestimmung der Screening-Häufigkeit.
In der UKPDS (United Kingdom Prospective Diabetes Study) wurde gezeigt, dass eine Senkung des HbA1c um 1 % das Risiko für mikrovaskuläre Komplikationen um 37 % reduziert6). Die Aufrechterhaltung eines HbA1c unter 7,0 % führt zu einer signifikanten Verringerung des Risikos einer Retinopathie-Progression6).
Andererseits kann eine schnelle Blutzuckerbesserung, z. B. durch Insulinbeginn, vorübergehend eine Verschlechterung der Retinopathie verursachen, das sogenannte „Early Worsening“7). Dieses Phänomen wurde in der DCCT (Diabetes Control and Complications Trial) bestätigt, und es ist auf eine kurzfristige Fundusverschlechterung nach Insulinbeginn zu achten7).
Ohne Retinopathie und bei gutem HbA1c (unter 7,0 %) wird eine Untersuchung alle 1–2 Jahre als ausreichend angesehen. Bei leichter nicht-proliferativer Retinopathie alle 6–12 Monate, bei mäßiger alle 3–6 Monate, bei schwerer nicht-proliferativer alle 1–3 Monate und bei proliferativer Retinopathie sind monatliche Untersuchungen und Behandlungsinterventionen erforderlich4). Bei hohem HbA1c oder instabiler Blutzuckerkontrolle wird eine häufigere Nachsorge empfohlen.
3. Untersuchungsmethoden
Abschnitt betitelt „3. Untersuchungsmethoden“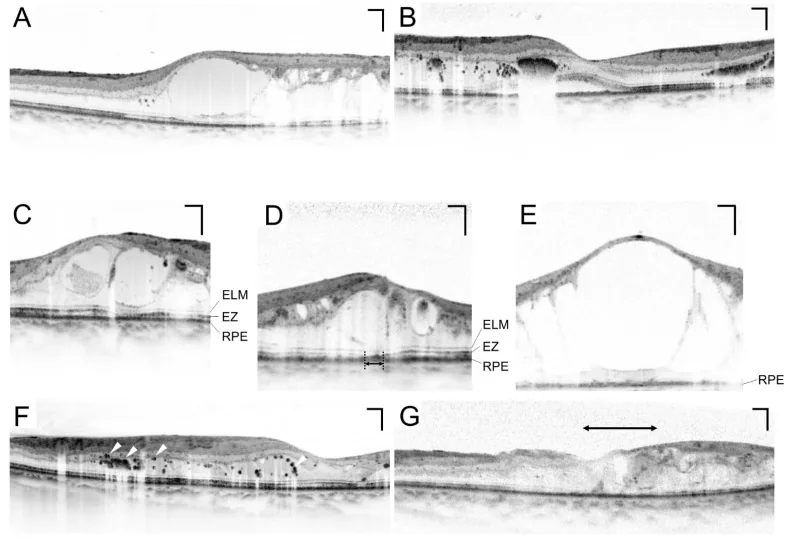
Fundusuntersuchung in Mydriasis
Abschnitt betitelt „Fundusuntersuchung in Mydriasis“Die Fundusuntersuchung in Mydriasis ist die zentrale Untersuchung des diabetischen Augenscreenings. Standardmäßig wird die Fundusuntersuchung nach Pupillenerweiterung mit Tropfen von Tropicamid und Phenylephrin (Phenylephrinhydrochlorid) durchgeführt 4). Die 7-Feld-Stereofotografie nach ETDRS (Early Treatment Diabetic Retinopathy Study) gilt als Referenzstandard 8).
Nicht-mydriatische Funduskameras sind praktisch und werden zunehmend im Screening eingesetzt, mit einer berichteten Sensitivität von 80–90 % 9). Im britischen nationalen Screening-Programm für diabetische Retinopathie wird ein System mit nicht-mydriatischer digitaler Fundusfotografie als Kern eingesetzt 9).
OCT (Optische Kohärenztomographie)
Abschnitt betitelt „OCT (Optische Kohärenztomographie)“Die OCT ist eine unverzichtbare Untersuchung zur quantitativen Beurteilung des Makulaödems. Sie ermöglicht die nicht-invasive und wiederholte Messung der zentralen Netzhautdicke (CRT) und ist für die Überwachung des Behandlungserfolgs unerlässlich 10). Eine CRT > 300 μm gilt als ein Richtwert für den Beginn der Behandlung des diabetischen Makulaödems (DME) 10).
Fluoreszenzangiographie (FA)
Abschnitt betitelt „Fluoreszenzangiographie (FA)“Bei dieser Untersuchung wird Natriumfluorescein intravenös injiziert, um die Netzhautgefäße darzustellen. Sie dient dem Nachweis von Nichtperfusionsarealen und der Beurteilung von Neovaskularisationen 8). Sie wird zur Indikationsstellung für die Photokoagulation verwendet und ist für die präzise Beurteilung nach der ETDRS-Klassifikation nützlich 8).
OCT-Angiographie (OCTA)
Abschnitt betitelt „OCT-Angiographie (OCTA)“Die OCTA ist eine nicht-invasive Untersuchung, die Netzhautgefäße ohne Kontrastmittel dreidimensional darstellen kann 11). Sie kann als Alternative zur Fluoreszenzangiographie wiederholt durchgeführt werden und wird zur Beurteilung von Nichtperfusionsarealen und des makulären Kapillarnetzwerks eingesetzt 11).
KI-basiertes Fundus-Screening
Abschnitt betitelt „KI-basiertes Fundus-Screening“Die automatisierte Fundusanalyse mittels Deep Learning befindet sich rasch in der praktischen Umsetzung. In einer multiethnischen Kohortenstudie von Ting et al. (2017) wurde eine Sensitivität von 87–97 % für die automatische Erkennung von diabetischer Retinopathie, Glaukomverdacht und AMD berichtet 12). Von der US-amerikanischen FDA zugelassene KI-Geräte (wie IDx-DR) sind ebenfalls im praktischen Einsatz, und die Nutzung für das Screening in der Inneren Medizin und der Primärversorgung nimmt zu 12).
| Untersuchungsmethode | Hauptindikationen | Merkmale |
|---|---|---|
| Fundusuntersuchung in Mydriasis (7-Feld-Stereo) | Referenzstandard für die Stadienbeurteilung | Hohe Genauigkeit, invasive Mydriasis erforderlich 8) |
| Mydriatische Funduskamera | Erstscreening | Sensitivität 80-90% · Hoher Komfort 9) |
| OCT | Quantifizierung des Makulaödems und Therapieüberwachung | Nicht-invasiv · CRT-Quantifizierung 10) |
| Fluoreszenzangiographie (FA) | Beurteilung von Nichtperfusionsarealen und Neovaskularisation | Invasiv · Kontrastmittelgebrauch 8) |
| OCTA | Nicht-invasive Gefäßbeurteilung | Wiederholbar · Kein Kontrastmittel nötig 11) |
| KI-Fundus-Screening | Automatisierung des Erstscreenings | Sensitivität 87-97% · Kein Augenarzt erforderlich 12) |
KI-Fundus-Screening mittels Deep Learning hat eine hohe Sensitivität von 87–97 % gezeigt und befindet sich in der praktischen Anwendung 12). Es gibt von der FDA zugelassene KI-Geräte, deren Einsatz in Regionen mit Augenarztmangel erwartet wird. Allerdings ist das KI-Screening nur ein primäres Screening; bei Auffälligkeiten ist eine gründliche Untersuchung durch einen Augenarzt erforderlich.
4. Klassifikation der diabetischen Retinopathie
Abschnitt betitelt „4. Klassifikation der diabetischen Retinopathie“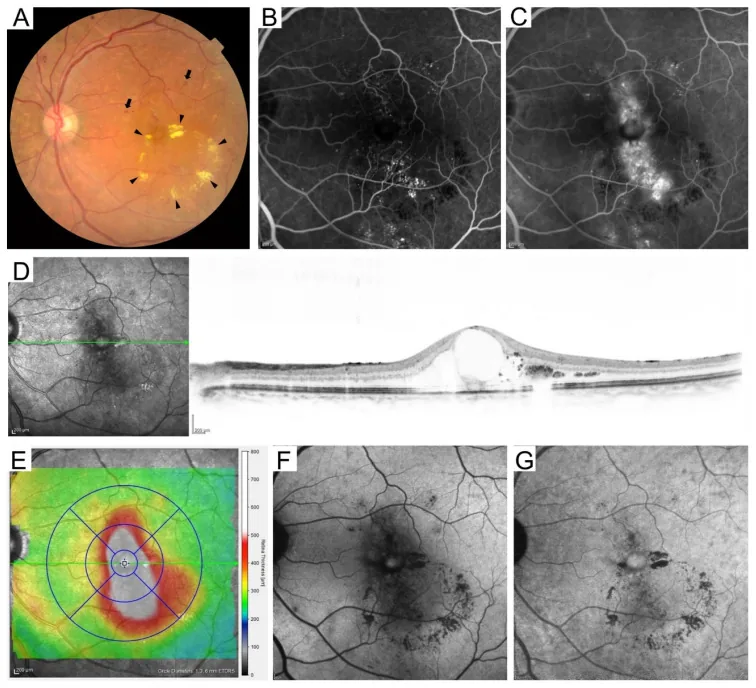
Internationale Klassifikation (basierend auf ETDRS)
Abschnitt betitelt „Internationale Klassifikation (basierend auf ETDRS)“Die internationale Klassifikation der diabetischen Retinopathie umfasst 5 Stadien basierend auf den ETDRS-Kriterien 8).
| Stadium | Hauptbefunde | Management |
|---|---|---|
| Keine Retinopathie | Keine Auffälligkeiten | Screening alle 1–2 Jahre 4) |
| Leichte NPDR | Nur Mikroaneurysmen | Nachsorge alle 6–12 Monate 4) |
| Mäßige NPDR | Weiche Exsudate, Netzhautblutungen, harte Exsudate | Nachsorge alle 3–6 Monate4) |
| Schwere NPDR (4-2-1-Regel) | Netzhautblutungen in 4 Quadranten, venöse perlschnurartige Erweiterungen in 2 Quadranten, IRMA in 1 Quadrant8) | Frühe PRP erwägen, Nachsorge alle 1–3 Monate4) |
| Proliferative diabetische Retinopathie (PDR) | NVD, NVE, Glaskörperblutung, traktive Netzhautablösung8) | PRP, Anti-VEGF, Operation. Monatliche Kontrolle4) |
- Die 4-2-1-Regel bei schwerer NPDR bezeichnet ein Stadium, in dem mindestens eines der folgenden Kriterien erfüllt ist: Netzhautblutungen in 4 Quadranten, venöse perlschnurartige Erweiterungen in 2 Quadranten oder IRMA (intraretinale mikrovaskuläre Anomalien) in 1 Quadrant8).
- Bei der proliferativen diabetischen Retinopathie (PDR) treten Papillenneovaskularisationen (NVD) oder retinale Neovaskularisationen (NVE) auf, die zu Glaskörperblutung und traktiver Netzhautablösung führen8).
Diabetisches Makulaödem (DMÖ)
Abschnitt betitelt „Diabetisches Makulaödem (DMÖ)“Das diabetische Makulaödem (DMÖ) ist eine Erkrankung, die in jedem Stadium der Retinopathie auftreten kann und die häufigste Ursache für Sehverschlechterung bei Diabetes ist10).
- Ein klinisch signifikantes Makulaödem (CSME) mit Beteiligung der Fovea ist eine Behandlungsindikation10)
- Im OCT ist eine CRT > 300 μm einer der Richtwerte für den Behandlungsbeginn10)
- Die Leitlinien der European Society of Retina (EURETINA) empfehlen die Anti-VEGF-Therapie als Erstlinienbehandlung 10)
Andere Augenkomplikationen
Abschnitt betitelt „Andere Augenkomplikationen“- Neovaskuläres Glaukom: Als Komplikation der PDR entstehen Neovaskularisationen an Iris und Kammerwinkel, die zu einem sekundären Glaukom führen
- Diabetische Katarakt: Es gibt zwei Formen: die echte diabetische Katarakt (rapid progredient bei jungen Patienten) und die Beschleunigung der altersbedingten Katarakt
- Äußere Augenmuskellähmung: Eine Diplopie aufgrund einer Lähmung des III. und VI. Hirnnervs kann akut auftreten
5. Behandlungsstrategie (vom Screening zur Behandlungskoordination)
Abschnitt betitelt „5. Behandlungsstrategie (vom Screening zur Behandlungskoordination)“Grundlagen der internistischen Behandlung
Abschnitt betitelt „Grundlagen der internistischen Behandlung“Die internistische Kontrolle von Blutzucker, Blutdruck und Lipiden bildet die Grundlage zur Hemmung des Fortschreitens der diabetischen Retinopathie. Die Zielwerte sind wie folgt 6).
- HbA1c: < 7,0 %
- Blutdruck: < 130/80 mmHg
- LDL-C: < 120 mg/dL
In der UKPDS zeigte die Gruppe mit intensiver Blutzuckerkontrolle im Vergleich zur konventionellen Gruppe eine 37%ige Risikoreduktion für mikrovaskuläre Komplikationen, und eine Senkung des HbA1c um 1% war mit einer signifikanten Verringerung des Komplikationsrisikos verbunden 6).
Laserphotokoagulation (pannetinale Photokoagulation: PRP)
Abschnitt betitelt „Laserphotokoagulation (pannetinale Photokoagulation: PRP)“Bei schwerer NPDR bis hin zur proliferativen diabetischen Retinopathie wird eine pannetinale Photokoagulation (PRP) durchgeführt 8). Durch Verödung der ischämischen Netzhaut wird die VEGF-Produktion unterdrückt und eine Regression bzw. Prävention von Neovaskularisationen angestrebt. Es handelt sich um eine durch die ETDRS etablierte Behandlung und ist die Standardtherapie zur Verhinderung von Erblindung bei Hochrisiko-PDR 8).
Anti-VEGF-Therapie
Abschnitt betitelt „Anti-VEGF-Therapie“Die Erstlinientherapie des diabetischen Makulaödems (DMÖ) ist die intravitreale Injektion von Anti-VEGF. Die verfügbaren Medikamente sind wie folgt 10).
- Ranibizumab (Lucentis): 0,5 mg/0,05 ml intravitreale Injektion
- Aflibercept (Eylea): 2 mg/0,05 ml intravitreale Injektion
- Faricimab (Vabysmo): 6 mg/0,05 ml intravitreale Injektion (Ang-2/VEGF-A bispezifischer Antikörper)
Vitrektomie
Abschnitt betitelt „Vitrektomie“Bei nicht resorbierbarer Glaskörperblutung oder traktiver Netzhautablösung wird eine Vitrektomie durchgeführt 8). In den letzten Jahren hat sich die kleinschnittige Vitrektomie (25-27 Gauge) durchgesetzt, um die operative Invasivität zu reduzieren.
Lokale Steroidgabe
Abschnitt betitelt „Lokale Steroidgabe“Die intravitreale Injektion von 4 mg/0,1 ml Triamcinolonacetonid (TA) wird als adjuvante Therapie des DMÖ eingesetzt 10). Sie wird bei unzureichendem Ansprechen auf die Anti-VEGF-Therapie oder bei Pseudophakie (nach Kataraktoperation) in Betracht gezogen.
Fenofibrat
Abschnitt betitelt „Fenofibrat“In der FIELD-Studie (2007) und der ACCORD-Eye-Studie wurde gezeigt, dass Fenofibrat das Fortschreiten der diabetischen Retinopathie verlangsamt und die Notwendigkeit einer Photokoagulation reduziert 13). Neben der lipidsenkenden Wirkung wird eine Beteiligung antiinflammatorischer und antiangiogenetischer Effekte durch PPARα-Aktivierung angenommen 13).
Durch Früherkennung können über 90 % der Erblindungen verhindert werden 2). Die Behandlung richtet sich nach Stadium und Art der Komplikationen: Bei leichten bis mittelschweren Fällen steht die internistische Kontrolle von Blutzucker, Blutdruck und Lipiden im Vordergrund. Bei schwerer nicht-proliferativer bis proliferativer Retinopathie wird eine Laserphotokoagulation (PRP) durchgeführt, und bei diabetischem Makulaödem sind intravitreale Anti-VEGF-Injektionen (Ranibizumab, Aflibercept, Faricimab) die erste Wahl. Bei nicht resorbierbarer Glaskörperblutung oder traktiver Netzhautablösung ist eine Vitrektomie indiziert.
6. Pathophysiologie und wissenschaftliche Grundlagen des Screenings
Abschnitt betitelt „6. Pathophysiologie und wissenschaftliche Grundlagen des Screenings“Mikrogefäßschäden der Netzhaut durch Hyperglykämie
Abschnitt betitelt „Mikrogefäßschäden der Netzhaut durch Hyperglykämie“An der Entstehung der diabetischen Retinopathie sind mehrere durch Hyperglykämie ausgelöste Stoffwechselwege beteiligt 14).
- Aktivierung des Polyolwegs: Die Umwandlung von Glucose in Sorbit durch Aldose-Reduktase ist gesteigert, was zu erhöhter intrazellulärer Osmolalität und oxidativem Stress führt.
- Akkumulation von AGE (fortgeschrittene Glykierungsendprodukte): Ihre Ablagerung in der vaskulären Basalmembran und extrazellulären Matrix beeinträchtigt die Gefäßfunktion.
- Aktivierung der Proteinkinase C (PKC): Sie fördert die Produktion von VEGF, das an erhöhter Gefäßpermeabilität und Neovaskularisation beteiligt ist.
- Erhöhter oxidativer Stress: Die übermäßige Produktion reaktiver Sauerstoffspezies (ROS) schädigt die Endothelzellfunktion.
Vom Perizytenverlust zu Neovaskularisationen
Abschnitt betitelt „Vom Perizytenverlust zu Neovaskularisationen“Der selektive Verlust von Perizyten (Stützzellen der Gefäßwand) der Netzhautkapillaren ist die früheste Veränderung bei der diabetischen Retinopathie 14). Der Perizytenverlust schwächt die Kapillarwand, was zur Bildung von Mikroaneurysmen führt. Die erhöhte Gefäßpermeabilität verursacht ein Makulaödem, und die kapillare Nichtperfusion (nicht perfundierte Areale) führt zu Netzhautischämie 14).
Die erhöhte VEGF-Produktion aus der ischämischen Netzhaut ist der Haupttreiber der Neovaskularisation, die zur Bildung von NVD und NVE führt. Intravitreales VEGF ist auch an der Pathogenese von Glaskörperblutung und traktiver Netzhautablösung beteiligt 14).
Kosteneffektivität des Screenings
Abschnitt betitelt „Kosteneffektivität des Screenings“Die Kosteneffektivität von Screening-Programmen für die diabetische Retinopathie wird durch mehrere Wirtschaftlichkeitsanalysen gestützt. Ein systematischer Review von Jones et al. (2010) zeigte, dass die Früherkennung und Behandlung im Vergleich zu den Kosten der Erblindungsversorgung deutlich kostengünstiger und kosteneffektiv ist 15).
DCCT und UKPDS haben die Bedeutung der Blutzuckerkontrolle wissenschaftlich belegt. Im DCCT reduzierte die intensivierte Insulintherapie bei Typ-1-Diabetes das Risiko für das Neuauftreten einer Retinopathie um 76 % und das Progressionsrisiko um 54 % 6). Die UKPDS zeigte, dass eine intensive Blutzuckerkontrolle bei Typ-2-Diabetes das Risiko für mikrovaskuläre Komplikationen um 37 % senkte 6).
7. Aktuelle Forschung und zukünftige Perspektiven
Abschnitt betitelt „7. Aktuelle Forschung und zukünftige Perspektiven“Gesellschaftliche Implementierung des automatischen Screenings durch KI
Abschnitt betitelt „Gesellschaftliche Implementierung des automatischen Screenings durch KI“Die Genauigkeit der automatischen Fundusanalyse mittels Deep Learning hat ein Niveau erreicht, das dem von Augenärzten entspricht, und die gesellschaftliche Implementierung schreitet voran 12). Der Einsatz in der nicht-invasiven Screening in der Inneren Medizin und der Primärversorgung verspricht die Erkennung von Hochrisikopatienten mit niedriger augenärztlicher Konsultationsrate.
Einführung von Ultraweitwinkel-Funduskameras
Abschnitt betitelt „Einführung von Ultraweitwinkel-Funduskameras“Ultraweitwinkel-Funduskameras wie Optos decken mit einer einzigen Aufnahme mehr als 200° der Netzhaut ab, und ihre Anwendung für das Screening ohne Pupillenerweiterung schreitet voran 9). Eine verbesserte Genauigkeit bei der Erkennung von nicht perfundierten Bereichen der peripheren Netzhaut und von Neovaskularisationen wurde berichtet, und es wird eine gleichzeitige Verbesserung der Screening-Genauigkeit und des Komforts erwartet.
Nutzung der Telemedizin (Teleophthalmologie)
Abschnitt betitelt „Nutzung der Telemedizin (Teleophthalmologie)“Die Fernbefundung von Fundusbildern mittels Telemedizin hat sich insbesondere beim Screening auf diabetische Retinopathie bewährt 12). Sie trägt zur Verbesserung der Screening-Teilnahmerate von Diabetikern in Regionen mit Augenarztmangel oder abgelegenen Gebieten bei und wird als Instrument zum Abbau von Ungleichheiten angesehen.
Forschung zu neuen Medikamenten und Retinopathierisiko
Abschnitt betitelt „Forschung zu neuen Medikamenten und Retinopathierisiko“Mit der Verbreitung von GLP-1-Rezeptoragonisten (wie Semaglutid) und SGLT2-Inhibitoren (wie Empagliflozin) schreitet die Forschung zu den Auswirkungen dieser Medikamente auf das Risiko einer diabetischen Retinopathie voran 16). Bei Semaglutid wurde in einigen Studien ein erhöhtes Risiko einer akuten Retinopathieverschlechterung berichtet, und insbesondere der Zusammenhang mit einer frühen Verschlechterung (Early Worsening) wird beachtet 16). Die Aufklärung des Mechanismus der hemmenden Wirkung von Fenofibrat auf das Fortschreiten der diabetischen Retinopathie und die Erwartung weiterer großer Studien setzen sich fort 13).
Tränen-Biomarker und retinale Gefäßparameter
Abschnitt betitelt „Tränen-Biomarker und retinale Gefäßparameter“Die Quantifizierung von VEGF und entzündlichen Zytokinen durch nicht-invasive Tränenprobenentnahme sowie die Bewertung des frühen Retinopathierisikos mittels retinaler Gefäßdurchmesser- und Fraktalanalyse werden erforscht. In Zukunft könnte es möglich sein, das Retinopathierisiko allein durch eine Funduskameraaufnahme zu quantifizieren.
8. Referenzen
Abschnitt betitelt „8. Referenzen“- Yau JW, Rogers SL, Kawasaki R, et al. Global prevalence and major risk factors of diabetic retinopathy. Diabetes Care. 2012;35(3):556-564.
- Flaxel CJ, Adelman RA, Bailey ST, et al. Diabetic retinopathy Preferred Practice Pattern®. Ophthalmology. 2020;127(1):P66-P145.
- 日本糖尿病眼学会. 糖尿病眼手帳について. https://www.jsod.jp/techo/index.html
- Solomon SD, Chew E, Duh EJ, et al. Diabetic retinopathy: a position statement by the American Diabetes Association. Diabetes Care. 2017;40(3):412-418.
- Morrison JL, Hodgson LA, Lim LL, et al. Diabetic retinopathy in pregnancy: a review. Clin Exp Ophthalmol. 2016;44(4):321-334.
- UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet. 1998;352(9131):837-853.
- The Diabetes Control and Complications Trial Research Group. Early worsening of diabetic retinopathy in the Diabetes Control and Complications Trial. Arch Ophthalmol. 1998;116(7):874-886.
- Early Treatment Diabetic Retinopathy Study Research Group. Grading diabetic retinopathy from stereoscopic color fundus photographs — an extension of the modified Airlie House classification. ETDRS report number 10. Ophthalmology. 1991;98(5 Suppl):786-806.
- Scanlon PH. The English National Screening Programme for diabetic retinopathy 2003-2016. Acta Diabetol. 2017;54(6):515-525.
- Schmidt-Erfurth U, Garcia-Arumi J, Bandello F, et al. Guidelines for the management of diabetic macular edema by the European Society of Retina Specialists (EURETINA). Ophthalmologica. 2017;237(4):185-222.
- Spaide RF, Fujimoto JG, Waheed NK, et al. Optical coherence tomography angiography. Prog Retin Eye Res. 2018;64:1-55.
- Ting DSW, Cheung CY, Lim G, et al. Development and validation of a deep learning system for diabetic retinopathy and related eye diseases using retinal images from multiethnic populations with diabetes. JAMA. 2017;318(22):2211-2223.
- Keech AC, Mitchell P, Summanen PA, et al. Effect of fenofibrate on the need for laser treatment for diabetic retinopathy (FIELD study): a randomised controlled trial. Lancet. 2007;370(9600):1687-1697. doi:10.1016/S0140-6736(07)61607-9.
- Antonetti DA, Klein R, Gardner TW. Diabetic retinopathy. N Engl J Med. 2012;366(13):1227-1239.
- Jones S, Edwards RT. Diabetic retinopathy screening: a systematic review of the economic evidence. Diabet Med. 2010;27(3):249-256.
- Ntentakis DP, Correa VSMC, Ntentaki AM, Delavogia E, Narimatsu T, Efstathiou N, Vavvas DG. Effects of newer-generation anti-diabetics on diabetic retinopathy: a critical review. Graefes Arch Clin Exp Ophthalmol. 2024;262(3):717-752. PMID:37728754. doi:10.1007/s00417-023-06236-5.
