
Офтальмологический скрининг у пациентов с диабетом (Рекомендации по скринингу диабетической ретинопатии)
Ключевые моменты с первого взгляда
Заголовок раздела «Ключевые моменты с первого взгляда»1. Что такое офтальмологический скрининг у пациентов с диабетом?
Заголовок раздела «1. Что такое офтальмологический скрининг у пациентов с диабетом?»Офтальмологический скрининг у пациентов с диабетом — это система регулярных офтальмологических обследований, направленная на раннее выявление глазных осложнений, таких как диабетическая ретинопатия, диабетический макулярный отек, неоваскулярная глаукома, катаракта и паралич наружных глазных мышц, с целью своевременного терапевтического вмешательства.
Диабетическая ретинопатия является второй по частоте причиной слепоты у взрослых. Во всем мире примерно у 30–40% пациентов с диабетом имеется ретинопатия, и примерно у 10% наблюдается ретинопатия, приводящая к нарушению зрения (пролиферативная ретинопатия)1). Также сообщается, что примерно у 20% пациентов ретинопатия уже присутствует на момент постановки диагноза диабета1), что подчеркивает важность раннего начала скрининга.
С другой стороны, при соответствующем скрининге и лечебном вмешательстве можно предотвратить более 90% случаев слепоты2). Ретинопатия на ранних стадиях протекает бессимптомно, и к моменту появления субъективных симптомов поражения часто уже значительно прогрессируют. Поэтому регулярные офтальмологические обследования являются единственным методом раннего выявления.
Число пациентов с диабетом в Японии оценивается более чем в 10 миллионов человек, и создание системы для продолжения регулярных офтальмологических осмотров является проблемой. Инструменты сотрудничества между терапевтами и офтальмологами, такие как дневник диабетического глаза, помогают обмениваться информацией о результатах осмотра глазного дна, датах обследований и лечении3).
При сахарном диабете 2 типа рекомендуется пройти офтальмологическое обследование сразу после постановки диагноза. Сообщается, что примерно у 20% пациентов ретинопатия уже присутствует на момент постановки диагноза диабета1), и ретинопатия может прогрессировать даже при отсутствии симптомов. При диабете 1 типа офтальмологическое обследование рекомендуется начинать примерно через 5 лет после начала заболевания или после полового созревания4). Независимо от типа, регулярные исследования глазного дна необходимы еще до появления субъективных симптомов, таких как снижение остроты зрения.
2. Целевая группа и рекомендуемая частота скрининга
Заголовок раздела «2. Целевая группа и рекомендуемая частота скрининга»Целевые лица и время начала
Заголовок раздела «Целевые лица и время начала»Время начала скрининга зависит от типа и состояния диабета.
- Сахарный диабет 2 типа: провести первый офтальмологический осмотр при постановке диагноза4)
- Сахарный диабет 1 типа: начать примерно через 5 лет после начала (или полового созревания), затем продолжать ежегодное исследование глазного дна4)
- Гестационный диабет (ГСД): провести исследование глазного дна в первом триместре беременности и наблюдать до одного года после родов5)
- Беременные с диабетом до беременности: провести исследование до беременности или в первом триместре, затем наблюдать каждый триместр5)
Рекомендуемая частота скрининга (по стадиям)
Заголовок раздела «Рекомендуемая частота скрининга (по стадиям)»Частота скрининга определяется на основе стадии ретинопатии и контроля HbA1c.
| Стадия ретинопатии | Рекомендуемая частота скрининга |
|---|---|
| Отсутствие ретинопатии (хороший контроль с HbA1c < 7,0%) | Каждые 1–2 года4) |
| Легкая непролиферативная стадия | Каждые 6–12 месяцев4) |
| Умеренная непролиферативная ретинопатия | Каждые 3–6 месяцев4) |
| Тяжелая непролиферативная ретинопатия (препролиферативная) | Каждые 1–3 месяца4) |
| Пролиферативная диабетическая ретинопатия | Ежемесячно (параллельно с лечением)4) |
Контроль HbA1c и прогрессирование ретинопатии
Заголовок раздела «Контроль HbA1c и прогрессирование ретинопатии»Контроль HbA1c также является важным показателем при определении частоты скрининга.
В исследовании UKPDS (Великобритания) было показано, что снижение HbA1c на 1% уменьшает риск микрососудистых осложнений на 37%6). Поддержание HbA1c ниже 7,0% приводит к значительному снижению риска прогрессирования ретинопатии6).
С другой стороны, быстрое улучшение уровня глюкозы, например, при начале инсулинотерапии, может временно ухудшить ретинопатию — так называемое «раннее ухудшение» (early worsening)7). Это явление было подтверждено в исследовании DCCT (Контроль диабета и его осложнений), и необходимо обращать внимание на краткосрочное ухудшение состояния глазного дна после начала инсулинотерапии7).
При отсутствии ретинопатии и хорошем уровне HbA1c (ниже 7,0%) обследование каждые 1–2 года считается достаточным. При легкой непролиферативной ретинопатии — каждые 6–12 месяцев, при умеренной — каждые 3–6 месяцев, при тяжелой непролиферативной — каждые 1–3 месяца, а при пролиферативной — ежемесячное обследование и лечение4). При высоком HbA1c или нестабильном контроле глюкозы рекомендуется более частое наблюдение.
3. Методы обследования
Заголовок раздела «3. Методы обследования»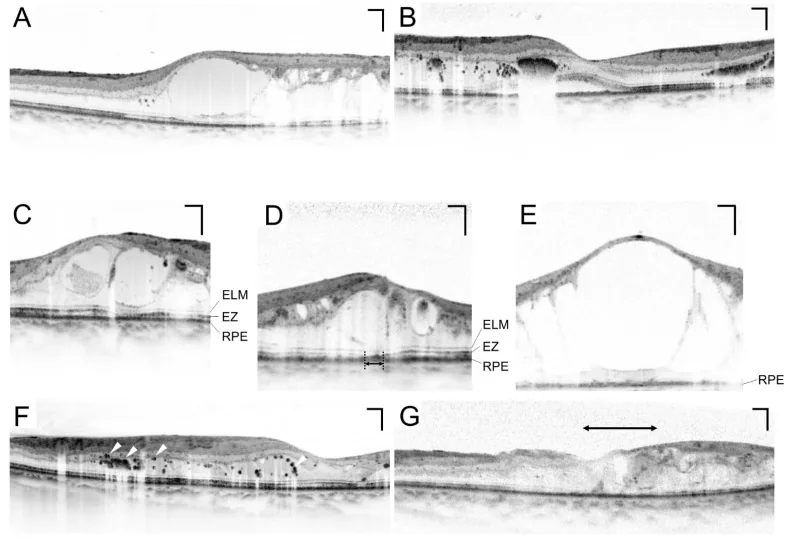
Осмотр глазного дна с расширением зрачка
Заголовок раздела «Осмотр глазного дна с расширением зрачка»Осмотр глазного дна с расширением зрачка является центральным исследованием при офтальмологическом скрининге диабета. Стандартным является проведение осмотра глазного дна после расширения зрачка каплями тропикамида и фенилэфрина (фенилэфрина гидрохлорида) 4). Эталонным стандартом считается 7-польная стереофотография по ETDRS (Early Treatment Diabetic Retinopathy Study) 8).
Бесконтактные (немидриатические) фундус-камеры удобны и все шире используются для скрининга, сообщается о чувствительности 80–90% 9). В британской национальной программе скрининга диабетической ретинопатии используется система, основанная на немидриатической цифровой фотографии глазного дна 9).
ОКТ (Оптическая когерентная томография)
Заголовок раздела «ОКТ (Оптическая когерентная томография)»ОКТ является обязательным исследованием для количественной оценки макулярного отека. Она позволяет неинвазивно и многократно измерять центральную толщину сетчатки (CRT) и незаменима для мониторинга эффективности лечения 10). CRT > 300 мкм считается одним из критериев для начала лечения диабетического макулярного отека (ДМО) 10).
Флюоресцентная ангиография (ФАГ)
Заголовок раздела «Флюоресцентная ангиография (ФАГ)»Это исследование проводится путем внутривенного введения флюоресцеина натрия для визуализации сосудов сетчатки. Оно используется для выявления зон неперфузии и оценки неоваскуляризации 8). Применяется для определения показаний к лазеркоагуляции и полезна для точной оценки по классификации ETDRS 8).
ОКТ-ангиография (ОКТА)
Заголовок раздела «ОКТ-ангиография (ОКТА)»ОКТА — это неинвазивное исследование, позволяющее трехмерно визуализировать сосуды сетчатки без использования контрастного вещества 11). Его можно повторять как альтернативу флюоресцентной ангиографии, и оно применяется для оценки зон неперфузии и макулярной капиллярной сети 11).
Скрининг глазного дна с помощью ИИ
Заголовок раздела «Скрининг глазного дна с помощью ИИ»Автоматический анализ глазного дна с использованием глубокого обучения быстро переходит в практическую фазу. В многоэтническом когортном исследовании Ting et al. (2017) сообщалось о чувствительности 87–97% для автоматического выявления диабетической ретинопатии, подозрения на глаукому и ВМД 12). Устройства ИИ, одобренные FDA США (например, IDx-DR), также используются на практике, и их применение для скрининга в терапии и первичной помощи расширяется 12).
| Метод исследования | Основные показания | Особенности |
|---|---|---|
| Осмотр глазного дна с расширением зрачка (7-польное стерео) | Эталон для оценки стадии | Высокая точность, требуется инвазивное расширение зрачка 8) |
| Безмидриатическая фундус-камера | Первичный скрининг | Чувствительность 80-90% · Высокое удобство 9) |
| ОКТ | Количественная оценка макулярного отека и мониторинг лечения | Неинвазивно · Количественное определение CRT 10) |
| Флюоресцентная ангиография (ФА) | Оценка зон неперфузии и неоваскуляризации | Инвазивно · Использование контрастного вещества 8) |
| ОКТА | Неинвазивная оценка сосудов | Повторяемо · Без контрастного вещества 11) |
| ИИ-скрининг глазного дна | Автоматизация первичного скрининга | Чувствительность 87-97% · Не требуется офтальмолог 12) |
Скрининг глазного дна с помощью ИИ на основе глубокого обучения показал высокую чувствительность 87–97% и перешел в практическую фазу 12). Существуют устройства ИИ, одобренные FDA, и ожидается их использование в регионах с нехваткой офтальмологов. Однако ИИ-скрининг является лишь первичным; при обнаружении отклонений необходимо тщательное обследование у офтальмолога.
4. Классификация диабетической ретинопатии
Заголовок раздела «4. Классификация диабетической ретинопатии»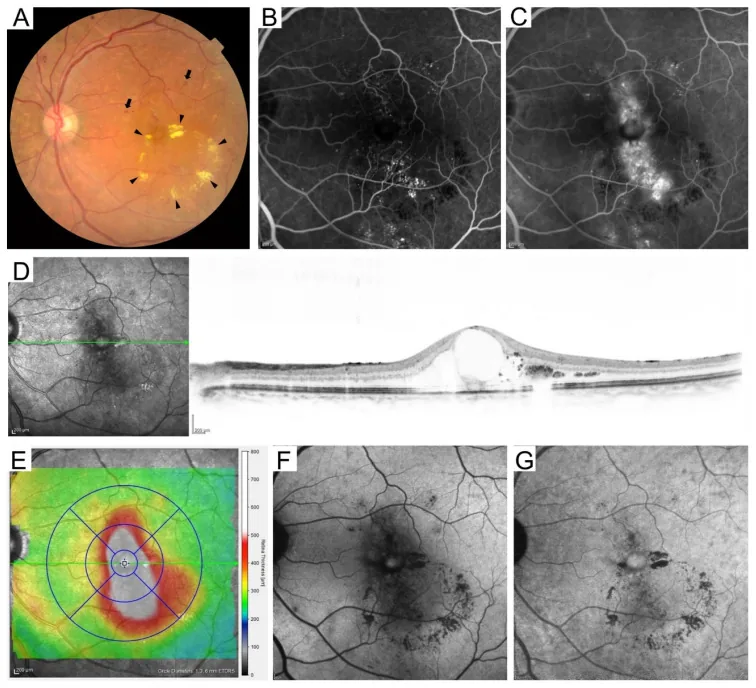
Международная классификация (на основе ETDRS)
Заголовок раздела «Международная классификация (на основе ETDRS)»Международная классификация диабетической ретинопатии включает 5 стадий на основе критериев ETDRS 8).
| Стадия | Основные находки | Тактика ведения |
|---|---|---|
| Нет ретинопатии | Нет отклонений | Скрининг каждые 1–2 года 4) |
| Легкая НПДР | Только микроаневризмы | Наблюдение каждые 6–12 месяцев 4) |
| Умеренная НПДР | Мягкие экссудаты, ретинальные геморрагии, твердые экссудаты | Наблюдение каждые 3–6 месяцев4) |
| Тяжелая НПДР (правило 4-2-1) | Ретинальные геморрагии в 4 квадрантах, венозные четкообразные расширения в 2 квадрантах, ИРМА в 1 квадранте8) | Рассмотреть раннюю ПРП, наблюдение каждые 1–3 месяца4) |
| Пролиферативная диабетическая ретинопатия (ПДР) | НВД, НВС, гемофтальм, тракционная отслойка сетчатки8) | ПРП, анти-VEGF, хирургия. Ежемесячное наблюдение4) |
- Правило 4-2-1 при тяжелой НПДР означает стадию, при которой выполняется хотя бы один из следующих критериев: ретинальные геморрагии в 4 квадрантах, венозные четкообразные расширения в 2 квадрантах или ИРМА (интраретинальные микрососудистые аномалии) в 1 квадранте8).
- При пролиферативной диабетической ретинопатии (ПДР) появляются неоваскуляризация диска зрительного нерва (НВД) или ретинальная неоваскуляризация (НВС), прогрессирующие до гемофтальма и тракционной отслойки сетчатки8).
Диабетический макулярный отек (ДМО)
Заголовок раздела «Диабетический макулярный отек (ДМО)»Диабетический макулярный отек (ДМО) — это состояние, которое может возникнуть на любой стадии ретинопатии и является наиболее частой причиной снижения зрения при диабете10).
- Клинически значимый макулярный отек (CSME) с вовлечением фовеа является показанием к лечению10)
- На ОКТ значение CRT > 300 мкм является одним из критериев для начала лечения10)
- Рекомендации Европейского общества сетчатки (EURETINA) рекомендуют анти-VEGF терапию в качестве терапии первой линии 10)
Другие глазные осложнения
Заголовок раздела «Другие глазные осложнения»- Неоваскулярная глаукома: Как осложнение ПДР, на радужке и в углу передней камеры образуются новообразованные сосуды, что приводит к вторичной глаукоме
- Диабетическая катаракта: Существует две формы: истинная диабетическая катаракта (быстро прогрессирующая у молодых) и ускорение возрастной катаракты
- Паралич наружных мышц глаза: Может остро возникнуть диплопия вследствие паралича III и VI черепных нервов
5. Лечебная тактика (от скрининга к координации лечения)
Заголовок раздела «5. Лечебная тактика (от скрининга к координации лечения)»Основы терапевтического контроля
Заголовок раздела «Основы терапевтического контроля»Терапевтический контроль уровня глюкозы, артериального давления и липидов является основой сдерживания прогрессирования диабетической ретинопатии. Целевые значения следующие 6).
- HbA1c: менее 7,0%
- Артериальное давление: менее 130/80 мм рт. ст.
- LDL-C: менее 120 мг/дл
В исследовании UKPDS в группе интенсивного контроля глюкозы риск микрососудистых осложнений был снижен на 37% по сравнению с группой стандартного контроля, и снижение HbA1c на 1% было связано со значительным уменьшением риска осложнений 6).
Лазерная фотокоагуляция (панретинальная фотокоагуляция: ПРФ)
Заголовок раздела «Лазерная фотокоагуляция (панретинальная фотокоагуляция: ПРФ)»Панретинальная фотокоагуляция (ПРФ) проводится при тяжелой НПДР и пролиферативной диабетической ретинопатии 8). Прижигание ишемизированной сетчатки подавляет продукцию VEGF и способствует регрессу и профилактике новообразованных сосудов. Это лечение, установленное ETDRS, является стандартом профилактики слепоты при ПДР высокого риска 8).
Анти-VEGF терапия
Заголовок раздела «Анти-VEGF терапия»Препаратом первой линии для лечения диабетического макулярного отека (ДМО) является интравитреальное введение анти-VEGF. Доступные препараты перечислены ниже 10).
- Ранибизумаб (Луцентис): 0,5 мг/0,05 мл интравитреально
- Афлиберцепт (Эйлеа): 2 мг/0,05 мл интравитреально
- Фарицимаб (Вабисмо): 6 мг/0,05 мл интравитреально (биспецифическое антитело к Ang-2/VEGF-A)
Витрэктомия
Заголовок раздела «Витрэктомия»Витрэктомия выполняется при нерассасывающемся кровоизлиянии в стекловидное тело или тракционной отслойке сетчатки 8). В последние годы получила распространение витрэктомия через малые разрезы (25-27 G), что позволяет снизить инвазивность операции.
Местное введение стероидов
Заголовок раздела «Местное введение стероидов»Интравитреальное введение 4 мг/0,1 мл триамцинолона ацетонида (ТА) используется в качестве вспомогательного лечения ДМО 10). Его применение рассматривается при недостаточном ответе на анти-VEGF терапию или у пациентов с артифакией (после операции по удалению катаракты).
Фенофибрат
Заголовок раздела «Фенофибрат»В исследованиях FIELD (2007) и ACCORD Eye было показано, что фенофибрат замедляет прогрессирование диабетической ретинопатии и снижает потребность в фотокоагуляции 13). Помимо снижения уровня липидов, предполагается участие противовоспалительных и антиангиогенных эффектов за счет активации PPARα 13).
При раннем выявлении можно предотвратить более 90% случаев слепоты 2). Лечение зависит от стадии и типа осложнений: при легкой и средней степени тяжести основное внимание уделяется контролю уровня глюкозы, артериального давления и липидов. При тяжелой непролиферативной и пролиферативной стадиях проводится лазерная фотокоагуляция (ПРФ), а при диабетическом макулярном отеке препаратами первой линии являются интравитреальные инъекции анти-VEGF (ранибизумаб, афлиберцепт, фарицимаб). При нерассасывающемся гемофтальме или тракционной отслойке сетчатки показана витрэктомия.
6. Патофизиология и научное обоснование скрининга
Заголовок раздела «6. Патофизиология и научное обоснование скрининга»Микрососудистое поражение сетчатки вследствие гипергликемии
Заголовок раздела «Микрососудистое поражение сетчатки вследствие гипергликемии»В развитии диабетической ретинопатии участвуют несколько метаболических путей, индуцированных гипергликемией 14).
- Активация полиолового пути: усиление превращения глюкозы в сорбитол под действием альдозоредуктазы приводит к повышению внутриклеточной осмоляльности и окислительного стресса.
- Накопление конечных продуктов гликирования (AGE): их отложение в сосудистой базальной мембране и внеклеточном матриксе нарушает функцию сосудов.
- Активация протеинкиназы C (PKC): она стимулирует продукцию VEGF, участвующего в повышении проницаемости сосудов и неоваскуляризации.
- Усиление окислительного стресса: избыточная продукция активных форм кислорода (АФК) повреждает функцию эндотелиальных клеток.
От потери перицитов к неоваскуляризации
Заголовок раздела «От потери перицитов к неоваскуляризации»Селективная потеря перицитов (опорных клеток сосудистой стенки) ретинальных капилляров является самым ранним изменением при диабетической ретинопатии 14). Потеря перицитов ослабляет капиллярную стенку, что приводит к образованию микроаневризм. Повышение проницаемости сосудов вызывает макулярный отек, а капиллярная неперфузия (неперфузируемые зоны) приводит к ишемии сетчатки 14).
Увеличение продукции VEGF ишемизированной сетчаткой является основным драйвером неоваскуляризации, приводя к образованию NVD и NVE. Интравитреальный VEGF также участвует в патогенезе гемофтальма и тракционной отслойки сетчатки 14).
Экономическая эффективность скрининга
Заголовок раздела «Экономическая эффективность скрининга»Экономическая эффективность программ скрининга диабетической ретинопатии подтверждена несколькими экономическими анализами. Систематический обзор Jones и соавт. (2010) показал, что раннее лечение на основе скрининга значительно дешевле по сравнению с затратами на ведение слепоты и является экономически эффективным 15).
Исследования DCCT и UKPDS научно обосновали важность контроля гликемии. В DCCT интенсивная инсулинотерапия при сахарном диабете 1 типа снизила риск развития ретинопатии на 76%, а риск прогрессирования — на 54% 6). UKPDS показало, что интенсивный контроль гликемии при сахарном диабете 2 типа снижает риск микрососудистых осложнений на 37% 6).
7. Новейшие исследования и перспективы на будущее
Заголовок раздела «7. Новейшие исследования и перспективы на будущее»Социальное внедрение автоматического скрининга с помощью ИИ
Заголовок раздела «Социальное внедрение автоматического скрининга с помощью ИИ»Точность автоматического анализа глазного дна с использованием глубокого обучения достигла уровня, сопоставимого с офтальмологами-специалистами, и его социальное внедрение прогрессирует 12). Его использование для неинвазивного скрининга в терапии и первичной медико-санитарной помощи позволит выявлять пациентов высокого риска с низкой частотой посещения офтальмолога.
Внедрение камер глазного дна со сверхшироким углом
Заголовок раздела «Внедрение камер глазного дна со сверхшироким углом»Камеры глазного дна со сверхшироким углом, такие как Optos, охватывают более 200° сетчатки за один снимок, и их применение для скрининга без расширения зрачка прогрессирует 9). Сообщается о повышении точности обнаружения неперфузируемых зон периферической сетчатки и новообразованных сосудов, что позволяет ожидать как повышения точности скрининга, так и удобства.
Использование телемедицины (телеофтальмологии)
Заголовок раздела «Использование телемедицины (телеофтальмологии)»Дистанционное чтение изображений глазного дна с помощью телемедицины доказало свою эффективность, особенно в скрининге диабетической ретинопатии 12). Это способствует повышению уровня участия в скрининге пациентов с диабетом в регионах с нехваткой офтальмологов или в отдаленных районах и рассматривается как инструмент для уменьшения неравенства.
Исследования новых лекарств и риска ретинопатии
Заголовок раздела «Исследования новых лекарств и риска ретинопатии»С распространением агонистов рецепторов GLP-1 (таких как семаглутид) и ингибиторов SGLT2 (таких как эмпаглифлозин) активно изучается влияние этих препаратов на риск диабетической ретинопатии 16). В некоторых исследованиях семаглутида сообщалось о повышении риска острого ухудшения ретинопатии, и особое внимание уделяется связи с ранним ухудшением (early worsening) 16). Продолжаются исследования механизма ингибирующего действия фенофибрата на прогрессирование диабетической ретинопатии и ожидания от дальнейших крупномасштабных испытаний 13).
Биомаркеры слезы и параметры сосудов сетчатки
Заголовок раздела «Биомаркеры слезы и параметры сосудов сетчатки»Проводятся исследования по количественному определению VEGF и воспалительных цитокинов с помощью неинвазивного забора слезы, а также по оценке раннего риска ретинопатии с использованием анализа диаметра сосудов сетчатки и фрактального анализа. В будущем может стать возможным количественно оценивать риск ретинопатии только по фотографии глазного дна.
8. Ссылки
Заголовок раздела «8. Ссылки»- Yau JW, Rogers SL, Kawasaki R, et al. Global prevalence and major risk factors of diabetic retinopathy. Diabetes Care. 2012;35(3):556-564.
- Flaxel CJ, Adelman RA, Bailey ST, et al. Diabetic retinopathy Preferred Practice Pattern®. Ophthalmology. 2020;127(1):P66-P145.
- 日本糖尿病眼学会. 糖尿病眼手帳について. https://www.jsod.jp/techo/index.html
- Solomon SD, Chew E, Duh EJ, et al. Diabetic retinopathy: a position statement by the American Diabetes Association. Diabetes Care. 2017;40(3):412-418.
- Morrison JL, Hodgson LA, Lim LL, et al. Diabetic retinopathy in pregnancy: a review. Clin Exp Ophthalmol. 2016;44(4):321-334.
- UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet. 1998;352(9131):837-853.
- The Diabetes Control and Complications Trial Research Group. Early worsening of diabetic retinopathy in the Diabetes Control and Complications Trial. Arch Ophthalmol. 1998;116(7):874-886.
- Early Treatment Diabetic Retinopathy Study Research Group. Grading diabetic retinopathy from stereoscopic color fundus photographs — an extension of the modified Airlie House classification. ETDRS report number 10. Ophthalmology. 1991;98(5 Suppl):786-806.
- Scanlon PH. The English National Screening Programme for diabetic retinopathy 2003-2016. Acta Diabetol. 2017;54(6):515-525.
- Schmidt-Erfurth U, Garcia-Arumi J, Bandello F, et al. Guidelines for the management of diabetic macular edema by the European Society of Retina Specialists (EURETINA). Ophthalmologica. 2017;237(4):185-222.
- Spaide RF, Fujimoto JG, Waheed NK, et al. Optical coherence tomography angiography. Prog Retin Eye Res. 2018;64:1-55.
- Ting DSW, Cheung CY, Lim G, et al. Development and validation of a deep learning system for diabetic retinopathy and related eye diseases using retinal images from multiethnic populations with diabetes. JAMA. 2017;318(22):2211-2223.
- Keech AC, Mitchell P, Summanen PA, et al. Effect of fenofibrate on the need for laser treatment for diabetic retinopathy (FIELD study): a randomised controlled trial. Lancet. 2007;370(9600):1687-1697. doi:10.1016/S0140-6736(07)61607-9.
- Antonetti DA, Klein R, Gardner TW. Diabetic retinopathy. N Engl J Med. 2012;366(13):1227-1239.
- Jones S, Edwards RT. Diabetic retinopathy screening: a systematic review of the economic evidence. Diabet Med. 2010;27(3):249-256.
- Ntentakis DP, Correa VSMC, Ntentaki AM, Delavogia E, Narimatsu T, Efstathiou N, Vavvas DG. Effects of newer-generation anti-diabetics on diabetic retinopathy: a critical review. Graefes Arch Clin Exp Ophthalmol. 2024;262(3):717-752. PMID:37728754. doi:10.1007/s00417-023-06236-5.
