血管性

囊样黄斑水肿
一目了然的要点
Section titled “一目了然的要点”1. 什么是囊样黄斑水肿?
Section titled “1. 什么是囊样黄斑水肿?”囊样黄斑水肿(Cystoid Macular Edema; CME)是由于血-视网膜屏障(BRB)破坏,黄斑部(中心凹周围)毛细血管渗漏液体,在外丛状层和内颗粒层形成囊样液体蓄积的病变。囊壁由Müller细胞和神经轴索纤维构成,液体沿Henle纤维层蓄积形成特征性的花瓣状图案。
它是发达国家中心视力障碍的主要原因之一,可由多种眼病、全身疾病和药物引起。CME的病理机制包括三种基本类型:①渗出性(BRB破坏导致血管渗漏)、②变性性(Müller细胞功能障碍导致细胞内液体积聚)、③牵拉性(玻璃体黄斑牵拉或视网膜前膜引起的机械变形)。3)
OCT上液体的分层定位有助于推断病因。局限于内颗粒层提示变性机制,局限于外颗粒层提示急性Müller细胞水肿或牵拉性,累及两层则提示渗出性。3)
多数病例在3~4个月内自行消退。但如果慢性化(持续6~9个月以上),可能导致光感受器永久性损伤。明确病因并进行适当治疗干预很重要,详情请参阅“标准治疗方法”一节。
2. 主要症状与临床所见
Section titled “2. 主要症状与临床所见”- 视力下降:早期常无自觉症状。随着水肿扩大,视力下降变得明显。
- 视物变形:由于Henle纤维层变形,直线看起来扭曲。
- 小视症:物体看起来变小。
- 中心暗点:中心凹水肿严重时,中心视野出现视物困难。
- 对比敏感度和色觉下降:常与视力下降同时出现。
荧光素眼底血管造影(FA)中的渗漏程度与视力下降程度并不一定相关。
裂隙灯显微镜下中心凹反射消失是早期重要体征。中心凹厚度≥300μm时被认为是临床上有意义的水肿。绿色光(无赤光)照射可增强囊肿轮廓。
眼底检查可见以中心凹为中心的花瓣状囊肿排列,常呈蜂窝状图案。严重病例囊肿融合形成大囊肿。
3. 原因与风险因素
Section titled “3. 原因与风险因素”CME的主要原因可通过助记符“DEPRIVENS”整理:Diabetes(糖尿病视网膜病变)、Epinephrine(肾上腺素)、Pars planitis(中间葡萄膜炎)、Retinitis pigmentosa(视网膜色素变性)、Irvine-Gass综合征(白内障术后)、Vein occlusion(静脉阻塞)、Nicotinic acid(烟酸)、External beam radiation(外照射放疗)、Surgery(手术)。
术后CME(Irvine-Gass综合征)
Section titled “术后CME(Irvine-Gass综合征)”白内障术后CME是最常见的术后CME。IOL植入眼中多达20%发生,但伴有视力下降的仅1-20%。后囊破裂是高危因素。发病多在术后6-10周,95%在6个月内自行消退。黄斑裂孔术后CME发生率低于10%。14)
药物性CME
Section titled “药物性CME”以下药物的相关报告已积累。
| 药物 | 适应症 | 特点 |
|---|---|---|
| 拉坦前列素 | 青光眼 | 有晶状体眼也可发生。使用22年后首次报告1) |
| 芬戈莫德 | 多发性硬化 | 0.5mg时ME 0.4%。白内障手术为触发因素8) |
| 西波尼莫德 | 多发性硬化 | EXPAND试验中CME 2%。开始后1周内发病4) |
| 白蛋白结合型紫杉醇 | 乳腺癌 | 无FA渗漏(Müller细胞毒性)2) |
| 伊布替尼 | 慢性淋巴细胞白血病 | 中心凹视网膜厚度600μm。停药6个月后消退7) |
| 戊聚糖多硫酸酯(PPS) | 间质性膀胱炎 | 停药10年后仍可发病。17%的黄斑病变合并此症10) |
前列腺素相关药物(PGA)通过破坏血-房水屏障诱发CME。Warwar等人关于拉坦前列素的综述中,94名患者中有2.1%发生CME;Hu等人的综述中,48只眼中47只为假晶状体眼或无晶状体眼。1)有晶状体眼中发病罕见,但也有长期使用22年后发病的报道。1)
- 视网膜静脉阻塞(RVO):分支和中央静脉阻塞均常合并CME。高同型半胱氨酸血症(超过正常值5~13 μmol/L的23.3 μmol/L)通过高凝状态增加RVO风险,并可直接破坏血-视网膜屏障(BRB)导致CME。6)
- 视网膜中央动脉阻塞(CRAO):急性期可出现局限于外核层的CME,并在两周内自行消退。慢性期出现局限于内核层的退行性CME,无荧光素渗漏。3)
- 葡萄膜炎:免疫恢复性葡萄膜炎(IRU)使CME风险增加20倍。5)
- 青光眼装置:有报道Hydrus Microstent弯曲→虹膜摩擦→急性虹膜睫状体炎→CME的机制。9)
炎症性
药物性
PGA滴眼液:即使在有晶状体眼也可能发生。1)
S1P受体调节剂:芬戈莫德、西波尼莫德。4, 8)
抗癌药物:紫杉烷类、BTK抑制剂、PPS。2, 7, 10)
术后/牵拉性
IOL植入眼中最多20%会发生CME(Irvine-Gass综合征),但实际导致视力下降的只有1-20%。后囊破裂时风险更高。95%在术后6个月内自行消退,但建议对高风险病例预防性使用NSAIDs。12)
芬戈莫德和西波尼莫德(多发性硬化症治疗药)、白蛋白结合型紫杉醇(抗癌药)、伊布替尼(血液肿瘤治疗药)、戊聚糖多硫酸酯(间质性膀胱炎治疗药)等有报道。停用致病药物是最有效的治疗方法,详情请参阅“标准治疗方法”一节。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”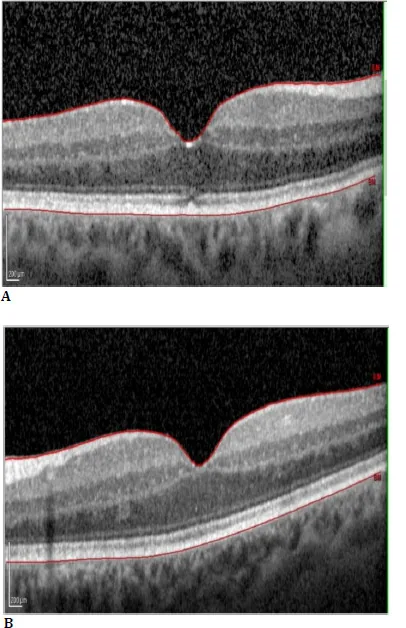
诊断CME需使用多种影像学检查。以下为主要检查方法。
| 检查方法 | 特点 | 主要用途 |
|---|---|---|
| OCT | 无创、定量评估 | 确诊、疗效判断 |
| 荧光素眼底血管造影(FA) | 使用造影剂 | 确认渗漏模式 |
| 眼底自发荧光(FAF) | 无创 | 评估RPE损伤 |
OCT(光学相干断层扫描)
Section titled “OCT(光学相干断层扫描)”最重要的检查方法。可以定量评估囊肿的位置、分布和视网膜厚度,对于治疗效果的纵向监测不可或缺。CME的基本OCT表现有三种类型:①视网膜肿胀(弥漫性)、②囊样水肿(囊肿形成)、③浆液性视网膜脱离。
分层定位有助于推断病因:内颗粒层局限提示退行性机制,外颗粒层局限提示急性Müller细胞水肿。3)En face OCT有助于可视化CME的分布模式。3)
关于治疗反应的OCT生物标志物的系统评价显示如下:13)
视网膜下液在67%的病例中改善,视网膜内囊肿在76%中改善,而EZ(椭圆体带)损伤在64%中不变或恶化,ELM(外界膜)损伤在67%中不变或恶化,高反射灶在63%中不变或恶化,DRIL(视网膜内层紊乱)在50%中不变或恶化。13)
EZ和ELM损伤的存在是预后不良的生物标志物,表明治疗后视功能恢复不佳。13)
荧光素眼底血管造影(FA)
Section titled “荧光素眼底血管造影(FA)”晚期(10-20分钟)沿Henle纤维层的花瓣状渗漏是特征性的。然而,在紫杉烷类抗癌药诱发的CME中,FA渗漏常不出现(由于退行性机制),因此FA阴性也不能排除CME。2)
眼底自发荧光(FAF)
Section titled “眼底自发荧光(FAF)”在戊聚糖多硫酸酯(PPS)相关黄斑病变中,观察到特征性的FAF异常模式,常被误诊为AMD。10)FAF对于评估RPE损伤比CME本身更有用。
可以定量评估囊肿的位置、分布、大小和视网膜厚度,对于治疗效果的纵向判断不可或缺。分层定位(内颗粒层还是外颗粒层)为推断病因提供线索。EZ和ELM损伤作为影响视功能预后的生物标志物进行评估。13)
5. 标准治疗方法
Section titled “5. 标准治疗方法”根据原发疾病和病理选择治疗。对于药物性CME,停用致病药物是首选治疗。
NSAIDs滴眼液
Section titled “NSAIDs滴眼液”使用酮咯酸0.5%、奈帕芬胺0.1%、溴芬酸0.07%等。通过抑制环氧化酶(COX),抑制前列腺素产生,稳定血-视网膜屏障(BRB)。
建议对术后高风险眼(如后囊破裂、单眼、糖尿病病例等)进行NSAIDs围手术期预防性给药。术前开始给药并术后立即持续给药可促进视力恢复。12)
在Hydrus Microstent弯曲导致的CME病例中,据报道使用酮咯酸+泼尼松龙滴眼液2个月后完全消退(视力20/60→20/25)。9)
- Tenon囊下曲安奈德注射:局部抗炎作用。通常需要多次给药。
- 玻璃体内曲安奈德注射:更直接的药物递送。需注意眼压升高和白内障进展。
- 全身类固醇:用于严重炎症性CME,但长期给药时副作用管理很重要。
类固醇被认为通过刺激Müller细胞的腺苷信号来降低VEGF产生。在IRU相关CME中,当类固醇禁忌(如股骨头坏死)时,托珠单抗可作为替代(后述)。
抗VEGF玻璃体内注射
Section titled “抗VEGF玻璃体内注射”糖尿病黄斑水肿和RVO相关CME的主要治疗。使用贝伐珠单抗1.25 mg/0.05 mL、雷珠单抗0.5 mg、阿柏西普2 mg等。
据报道,两次注射贝伐珠单抗1.25 mg/0.05 mL后,PPS相关CME完全消退。在该病例中,NSAIDs和类固醇滴眼液无效,但获得了良好结局。10)
在伴有高同型半胱氨酸血症的双侧静脉淤滞和CME病例中,两次抗VEGF注射也获得了改善。6)
碳酸酐酶抑制剂(CAI)
Section titled “碳酸酐酶抑制剂(CAI)”增强RPE泵功能并促进视网膜下液吸收。通过滴眼液(多佐胺、布林佐胺)或口服(乙酰唑胺)给药。在拉坦前列素诱发的CME中,将拉坦前列素更换为多佐胺后一个月内消退(CMT 319→218 μm,326→227 μm)。1)
停用致病药物
Section titled “停用致病药物”在药物性CME中,停用致病药物是最有效的治疗。
- 拉坦前列素:停药或换药后1个月内消退。1)
- 芬戈莫德:因多发性硬化恶化风险,有时会继续用药等待自然消退。有报告称13个月后自然消退。8)
- 西波尼莫德:停药1周明显改善,1个月完全消退。4)
- 白蛋白结合型紫杉醇:化疗停药2个月后改善。Tenon囊下曲安奈德无效。2)
- 伊布替尼:停药6个月完全消退(视力6/15→6/12)。NSAIDs+类固醇滴眼液2年仅部分有效。7)
- PPS:停药后仍可能发生CME,甚至有10年后发病的病例。10)
玻璃体手术(PPV)
Section titled “玻璃体手术(PPV)”伴有VMT的牵引性CME,玻璃体切除术可使80-92%的CME改善。奥克纤溶酶(酶促玻璃体剥离剂)在2/3期试验中显示58%的患者在1个月内解除VMT。
根据病因,可选择NSAIDs滴眼液、类固醇(Tenon囊下/玻璃体内注射)、抗VEGF玻璃体内注射、碳酸酐酶抑制剂、玻璃体手术等。药物性CME中,停用致病药物是最有效的首选治疗。治疗方法详见“标准治疗”章节。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”血-视网膜屏障(BRB)的结构
Section titled “血-视网膜屏障(BRB)的结构”BRB由两层结构组成:内层BRB(视网膜血管内皮细胞间的紧密连接)和外层BRB(视网膜色素上皮细胞间的紧密连接),维持视网膜的水分稳态。炎症、缺血或毒性物质导致紧密连接减弱时,血清蛋白和脂质漏出,引起渗透压升高。11)
Müller细胞通过水通道蛋白-4和Kir4.1通道的排水机制,正常情况下防止液体蓄积。当BRB严重破坏时,这种代偿性排出机制饱和,CME显现。11)
CME的三种机制
Section titled “CME的三种机制”渗出性
变性性
牵拉性
特殊发病机制
Section titled “特殊发病机制”S1P受体调节剂(芬戈莫德、西波尼莫德):抑制血管内皮钙黏蛋白的调节,增加血管通透性,从而破坏血-视网膜屏障。4)EXPAND试验中,西波尼莫德组2%出现CME(安慰剂组<1%)。4)
伊布替尼(BTK抑制剂):由于其能够穿过血脑屏障的特性,推测也可能破坏血-视网膜屏障。在3期试验中,伊布替尼组10%报告视力模糊(奥法妥木单抗组3%)。7)
急性CRAO:缺血导致细胞外离子稳态破坏,引起离子快速流入Müller细胞。结果水通道蛋白-4和Kir4.1通道表达增加,导致Müller细胞水肿(局限于外核层)。3)
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”托珠单抗(抗IL-6受体抗体)治疗IRU相关CME
Section titled “托珠单抗(抗IL-6受体抗体)治疗IRU相关CME”已有病例报告显示托珠单抗对免疫恢复性葡萄膜炎(IRU)继发的CME有效。
Nguyen等人(2024)对一名17岁女性(T细胞急性淋巴细胞白血病治疗后出现CMV视网膜炎→IRU导致CME,全身类固醇因股骨头坏死禁忌)给予托珠单抗8mg/kg静脉注射,每月一次,共2个周期。2个周期后CME显著改善。5)
STOP-UVEITIS试验显示托珠单抗可改善CME,有望成为类固醇禁忌病例的替代治疗。这一发现提示IL-6直接参与CME的发病机制。5)
PPS相关黄斑病变和CME的长期病程
Section titled “PPS相关黄斑病变和CME的长期病程”PPS相关性黄斑病变是一种相对较新的疾病概念,于2018年首次被认识。停用PPS后,病变可能进展并在10年以上发生CME,凸显了长期随访的重要性。10)
Szelog等人(2023)报告了一名57岁女性,在使用PPS 3年并停药10年后发生CME。初诊时被误诊为AMD,NSAIDs和类固醇滴眼液无效,但两次贝伐珠单抗1.25mg/0.05mL注射后完全消退。5个月后对侧眼也发生CME。10)
据报道,17%的PPS相关性黄斑病变合并CME,累计使用500g以上时超过10%的患者发生黄斑病变。10)
OCT生物标志物预测预后
Section titled “OCT生物标志物预测预后”系统评估OCT表现治疗反应性的研究表明,以下生物标志物对预后预测有用。13)
2025年发表在《Survey of Ophthalmology》上的一项系统综述报告,视网膜内囊肿(76%改善)和视网膜下液(67%改善)治疗反应性高,而EZ破坏(64%不变/恶化)、ELM破坏(67%不变/恶化)、高反射灶(63%不变/恶化)和DRIL(50%不变/恶化)提示预后不良。13)
将EZ和ELM破坏的有无纳入治疗决策的进展正在推进。
利用En face OCT进行病因诊断
Section titled “利用En face OCT进行病因诊断”利用En face OCT分析CME分布模式,正在确定有助于鉴别病因疾病的图像特征。3)特别是CRAO合并CME中急性和慢性期分层分布的差异,作为无创病因推断手段备受关注。
8. 参考文献
Section titled “8. 参考文献”- Lin WC, Hsieh JW, Tsai SH, Lan YW. Latanoprost-associated cystoid macular edema in a patient with phakic eyes. Taiwan J Ophthalmol. 2023;13:242-244.
- Yamane H, Itagaki T, Kajitani K, et al. Cystoid macular edema following treatment with nanoparticle albumin-bound paclitaxel and atezolizumab for metastatic breast cancer. Case Rep Oncol. 2023;16:1121-1128.
- Estawro R, Abraham N, Fouad Y, Bousquet E, Sarraf D. Cystoid macular edema as a complication of central retinal artery occlusion. Am J Ophthalmol Case Rep. 2024;33:101998.
- Kim MY, Alkhabaz A, Smith SJ, Liao YJ. Siponimod-associated cystoid macular edema without known risk factors. Am J Ophthalmol Case Rep. 2024;36:102124.
- Nguyen BT, Hung JH, Thng ZX, et al. Tocilizumab for cystoid macular edema secondary to immune recovery uveitis in a patient with contraindications to long-term systemic corticosteroid. Yale J Biol Med. 2024;97:423-430.
- Chaloulis SK, Tsaousis KT. Cystoid macular edema associated with venous stasis in a patient with previously undiagnosed hyperhomocysteinemia. Cureus. 2021;13(12):e20782.
- Ben-Avi R, Dori D, Chowers I. Cystoid macular edema secondary to ibrutinib. Am J Ophthalmol Case Rep. 2022;26:101436.
- Fukuoka H, Kojima K, Iwama A, Okumura T, Sotozono C. Fingolimod-associated severe bilateral cystoid macular edema. Am J Ophthalmol Case Rep. 2022;26:101553.
- Karaca I, Korot E, Ghoraba H, et al. Acute iridocyclitis and cystoid macular edema related to kinked Hydrus Microstent in advanced glaucoma. Saudi J Ophthalmol. 2022;36:390-393.
- Szelog JT, Shah NS, Camejo MD. Cystoid macular edema arising 10 years after cessation of pentosan polysulfate sodium successfully treated with bevacizumab. J Vitreoret Dis. 2023;7(1):83-86.
- Cunha-Vaz J, et al. Blood-retinal barrier. Prog Retin Eye Res. 2024. [出典: 1-s2.0-S1350946224000107-main.pdf]
- American Academy of Ophthalmology. Cataract in the Adult Eye Preferred Practice Pattern. Ophthalmology. 2022. [出典: PIIS0161642021007508.pdf]
- OCT biomarkers systematic review. Surv Ophthalmol. 2025. [出典: PIIS0039625725001766.pdf]
- Royal College of Ophthalmologists. DRAFT Clinical Guideline on Idiopathic Full-Thickness Macular Holes. 2024.
