혈관성

낭포황반부종
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 낭포황반부종이란?
섹션 제목: “1. 낭포황반부종이란?”낭포황반부종(Cystoid Macular Edema; CME)은 혈액-망막 장벽(BRB)의 파괴로 인해 황반부(중심와 주변) 모세혈관에서 액체가 누출되어 외망상층과 내과립층을 중심으로 낭포성 액체 저류를 초래하는 병태입니다. 낭포 격벽은 뮐러 세포와 신경 축삭 섬유로 구성되며, 헨레 섬유층을 따라 액체가 저류되어 특징적인 꽃잎 모양 패턴을 형성합니다.
선진국에서 중심 시력 장애의 주요 원인 중 하나이며, 다양한 안과 질환, 전신 질환, 약물이 원인이 될 수 있습니다. CME는 병태에 따라 세 가지 기본 메커니즘이 있습니다: ①삼출성(BRB 파괴로 인한 혈관 누출), ②변성성(뮐러 세포 장애로 인한 세포 내 액체 저류), ③견인성(유리체황반견인 또는 망막전막으로 인한 기계적 변형)입니다. 3)
OCT에서 액체의 층별 국소화가 원인 추정의 단서가 됩니다. 내과립층에 국한된 경우 변성성 기전을, 외과립층에 국한된 경우 급성 뮐러 세포 부종 또는 견인성을, 두 층에 걸친 분포는 삼출성을 시사합니다. 3)
대부분 34개월 이내에 자연 소실됩니다. 그러나 만성화(69개월 이상)되면 광수용체의 영구 손상이 발생할 수 있습니다. 원인 확인과 적절한 치료 중재가 중요하며, 자세한 내용은 「표준적 치료법」 항을 참조하십시오.
2. 주요 증상과 임상 소견
섹션 제목: “2. 주요 증상과 임상 소견”자각 증상
섹션 제목: “자각 증상”- 시력 저하: 초기에는 자각하지 못하는 경우가 많습니다. 부종이 확대됨에 따라 저하가 현저해집니다.
- 변시증(왜곡): 헨레 섬유층의 변형으로 인해 직선이 왜곡되어 보입니다.
- 소시증: 물체가 작게 보입니다.
- 중심 암점: 중심와의 부종이 심해지면 중심부가 잘 보이지 않게 됩니다.
- 대비 감도 및 색각 저하: 시력 저하와 함께 나타나는 경우가 많습니다.
형광 안저 혈관 조영술(FA)에서의 누출 정도는 시력 저하 정도와 반드시 상관관계가 있지는 않습니다.
임상 소견
섹션 제목: “임상 소견”세극등 현미경에서 중심와 반사 소실은 초기 중요 소견입니다. 중심와 두께 ≥300μm이면 임상적으로 유의한 부종으로 인식됩니다. 녹색광(무적색광) 조사로 낭종 윤곽이 강조됩니다.
안저 검사에서 중심와를 중심으로 꽃잎 모양 배열의 낭종이 형성되며, 벌집 모양 패턴으로 관찰되는 경우가 많습니다. 심한 경우 낭종이 융합하여 큰 낭종을 형성합니다.
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”CME의 주요 원인은 두문자어 “DEPRIVENS”로 정리됩니다: Diabetes(당뇨망막병증), Epinephrine(에피네프린), Pars planitis(중간부 포도막염), Retinitis pigmentosa(망막색소변성), Irvine-Gass 증후군(백내장 수술 후), Vein occlusion(정맥 폐쇄), Nicotinic acid(니코틴산), External beam radiation(방사선), Surgery(수술).
수술 후 CME (Irvine-Gass 증후군)
섹션 제목: “수술 후 CME (Irvine-Gass 증후군)”백내장 수술 후 CME는 가장 흔한 수술 후 CME입니다. IOL 삽입안의 최대 20%에서 발생하지만 시력 저하를 동반하는 경우는 120%입니다. 후낭 파열은 고위험 인자입니다. 발병은 수술 후 610주에 가장 많으며, 95%가 6개월 이내에 자연 소실됩니다. 황반원공 수술 후 CME 발생률은 10% 미만입니다. 14)
약물 유발 CME
섹션 제목: “약물 유발 CME”다음 약물에 대한 보고가 축적되고 있습니다.
| 약물 | 적응증 | 특징 |
|---|---|---|
| 라타노프로스트 | 녹내장 | 수정체안에서도 발생합니다. 22년 사용 후 첫 보고 1) |
| 핑골리모드 | 다발성 경화증 | 0.5mg에서 ME 0.4%. 백내장 수술이 유발 요인8) |
| 시포니모드 | 다발성 경화증 | EXPAND 시험에서 CME 2%. 시작 1주 내 발병4) |
| 나브-파클리탁셀 | 유방암 | FA 누출 없음 (뮐러 세포 독성)2) |
| 이브루티닙 | 만성 림프구성 백혈병 | 중심와 망막 두께 600μm. 중단 6개월 후 소실7) |
| 펜토산 폴리설페이트 (PPS) | 간질성 방광염 | 중단 10년 후에도 발병. 황반병증의 17%에서 합병10) |
프로스타글란딘 유사체(PGA)는 혈액-방수 장벽을 손상시켜 CME를 유발합니다. 라타노프로스트에 대한 Warwar 등의 리뷰에서는 94명 중 2.1%에서 CME가 발생했고, Hu 등의 리뷰에서는 48안 중 47안이 인공수정체안 또는 무수정체안이었습니다. 1) 유수정체안에서의 발병은 드물지만, 22년간 장기 사용 후 발병한 사례도 보고되었습니다. 1)
기타 원인
섹션 제목: “기타 원인”- 망막정맥폐쇄(RVO): 분지 및 중심정맥폐쇄 모두에서 CME가 빈번하게 합병됩니다. 고호모시스테인혈증(정상 범위 5~13 μmol/L를 초과하는 23.3 μmol/L)은 응고항진을 통해 RVO 위험을 높이고, 직접적으로 BRB를 손상시켜 CME를 유발할 수 있습니다. 6)
- 망막중심동맥폐쇄(CRAO): 급성기에는 외과립층에 국한된 CME가 발생하여 2주 이내에 자연 소실될 수 있습니다. 만성기에는 내과립층에 국한된 퇴행성 CME가 발생하며 형광누출을 동반하지 않습니다. 3)
- 포도막염: 면역회복포도막염(IRU)은 CME 위험을 20배 증가시킵니다. 5)
- 녹내장 장치: Hydrus Microstent의 굽힘 → 홍채 마찰 → 급성 홍채모양체염 → CME의 기전이 보고되었습니다. 9)
염증성
약물성
수술 후/견인성
IOL 삽입안의 최대 20%에서 CME(Irvine-Gass 증후군)가 발생하지만, 실제로 시력 저하를 초래하는 경우는 1~20%로 알려져 있습니다. 후낭 파손이 있는 경우 위험이 높아집니다. 95%는 수술 후 6개월 이내에 자연 소실되지만, 고위험군에는 예방적 NSAIDs 투여가 권장됩니다. 12)
핑골리모드 및 시포니모드(다발성 경화증 치료제), Nab-파클리탁셀(항암제), 이브루티닙(혈액암 치료제), 펜토산 폴리황산염(간질성 방광염 치료제) 등에서 보고되었습니다. 원인 약물 중단이 가장 효과적인 치료이며, 자세한 내용은 「표준적 치료법」 항을 참조하십시오.
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”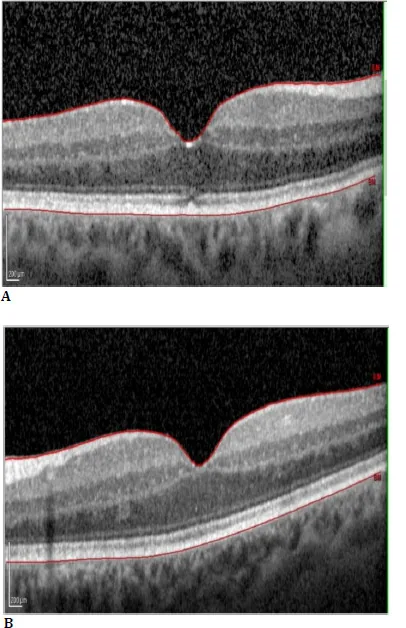
CME 진단에는 여러 영상 검사가 사용됩니다. 주요 검사법은 다음과 같습니다.
| 검사법 | 특징 | 주요 용도 |
|---|---|---|
| OCT | 비침습적·정량적 평가 | 확진·치료 효과 판정 |
| 형광안저혈관조영술(FA) | 조영제 사용 | 누출 패턴 확인 |
| 안저자가형광(FAF) | 비침습적 | RPE 손상 평가 |
OCT(광간섭단층촬영)
섹션 제목: “OCT(광간섭단층촬영)”가장 중요한 검사법입니다. 낭종의 위치, 분포 및 망막 두께를 정량적으로 평가할 수 있으며, 치료 효과의 경과 모니터링에 필수적입니다. CME의 기본 OCT 소견에는 3가지 유형이 있습니다: ① 망막 팽창(미만성), ② 낭포성 부종(낭종 형성), ③ 장액성 망막박리.
층별 국소화는 원인 추정에 유용하며, 내과립층 국한은 변성 기전을, 외과립층 국한은 급성 뮐러 세포 부종을 시사합니다. 3)En face OCT는 CME의 분포 패턴 시각화에 유용합니다. 3)
치료 반응성 OCT 바이오마커에 대한 체계적 문헌고찰에서는 다음이 제시되었습니다. 13)
망막하액은 67%의 증례에서 개선, 망막내 낭종은 76%에서 개선된 반면, EZ(타원체대) 장애는 64%가 불변 또는 악화, ELM(외경계막) 장애는 67%가 불변 또는 악화, 고반사 병소는 63%가 불변 또는 악화, DRIL(망막내층 구조 붕괴)은 50%가 불변 또는 악화되었습니다. 13)
EZ 및 ELM 장애의 존재는 치료 후에도 시기능 회복이 불량함을 나타내는 예후 불량 바이오마커입니다. 13)
형광안저조영술(FA)
섹션 제목: “형광안저조영술(FA)”후기상(10~20분)에 Henle 섬유층을 따라 꽃잎 모양의 누출이 특징적입니다. 그러나 탁산계 항암제 유발 CME에서는 FA 누출이 보이지 않는 경우가 많으며(변성 기전에 의함), FA 음성이어도 CME를 배제할 수 없습니다. 2)
안저자가형광(FAF)
섹션 제목: “안저자가형광(FAF)”펜토산 폴리황산염(PPS) 관련 황반병증에서는 특징적인 FAF 이상 패턴이 관찰되며, 처음에 AMD로 오진되기 쉽습니다. 10)FAF는 CME 자체보다 RPE 손상 평가에 유용합니다.
낭종의 위치, 분포, 크기 및 망막 두께를 정량적으로 평가할 수 있으며, 치료 효과의 경과 판정에 필수적입니다. 층별 국소화(내과립층 또는 외과립층)가 원인 추정의 단서가 됩니다. EZ 및 ELM 장애는 시기능 예후에 영향을 미치는 바이오마커로 평가됩니다. 13)
5. 표준적 치료법
섹션 제목: “5. 표준적 치료법”치료는 원인 질환과 병태에 따라 선택합니다. 약물 유발 CME에서는 원인 약물 중단이 일차 선택입니다.
NSAIDs 점안액
섹션 제목: “NSAIDs 점안액”케토롤락 0.5%, 네파페낙 0.1%, 브롬페낙 0.07% 등이 사용됩니다. 사이클로옥시게나제(COX) 억제를 통해 프로스타글란딘 생성을 억제하고, 혈액-망막 장벽(BRB)을 안정화시킵니다.
수술 후 고위험안(후낭 파열, 단안, 당뇨병 사례 등)에 대한 NSAIDs 주술기 예방 투여가 권장됩니다. 수술 전 투여 시작과 수술 직후부터 지속 투여가 시력 회복을 촉진합니다. 12)
Hydrus Microstent 굴곡으로 인한 CME 사례에서 케토롤락 + 프레드니솔론 점안액 2개월 사용으로 완전 소실(시력 20/60→20/25)이 보고되었습니다. 9)
스테로이드
섹션 제목: “스테로이드”- 테논낭하 트리암시놀론 주사: 국소 항염 효과. 여러 번 투여가 필요한 경우가 많습니다.
- 유리체내 트리암시놀론 주사: 보다 직접적인 약물 전달. 안압 상승, 백내장 진행에 주의가 필요합니다.
- 전신 스테로이드: 중증 염증성 CME에 사용되지만, 장기 투여 시 부작용 관리가 중요합니다.
스테로이드는 뮐러 세포의 아데노신 신호를 자극하여 VEGF 생성을 감소시키는 기전이 제시됩니다. IRU 관련 CME에서 대퇴골두 괴사 등으로 스테로이드가 금기인 경우 토실리주맙이 대안이 될 수 있습니다(후술).
항VEGF 유리체내 주사
섹션 제목: “항VEGF 유리체내 주사”당뇨병성 황반 부종 및 RVO 관련 CME의 주요 치료법. 베바시주맙 1.25mg/0.05mL, 라니비주맙 0.5mg, 애플리버셉트 2mg 등이 사용됩니다.
베바시주맙 1.25mg/0.05mL 2회 투여로 PPS 관련 CME가 완전 소실된 사례가 보고되었습니다. NSAIDs 및 스테로이드 점안액이 효과가 없었던 해당 사례에서 좋은 결과를 얻었습니다. 10)
고호모시스테인혈증을 동반한 양안 정맥 울혈 및 CME 사례에서도 항VEGF 2회 투여로 개선이 얻어졌습니다. 6)
탄산탈수효소 억제제 (CAI)
섹션 제목: “탄산탈수효소 억제제 (CAI)”RPE 펌프 기능을 강화하고 망막하액 흡수를 촉진합니다. 점안(도르졸아미드, 브린졸아미드) 또는 경구(아세타졸아미드)로 투여됩니다. 라타노프로스트 유발 CME에서 라타노프로스트를 도르졸아미드로 전환하여 1개월 이내 소실이 보고되었습니다(CMT 319→218μm, 326→227μm). 1)
원인 약물 중단
섹션 제목: “원인 약물 중단”약물 유발 CME에서는 원인 약물 중단이 가장 효과적인 치료입니다.
- 라타노프로스트: 중단 또는 전환 후 1개월 이내 소실. 1)
- 핑골리모드: MS 악화 위험 때문에 지속하면서 자연 소실을 기다리는 경우도 있음. 13개월 후 자연 소실 보고. 8)
- 시포니모드: 중단 1주에 현저한 개선, 1개월에 완전 소실. 4)
- Nab-파클리탁셀: 항암치료 중단 2개월 후 개선. 테논낭하 트리암시놀론은 무효. 2)
- 이브루티닙: 중단 6개월에 완전 소실(시력 6/15→6/12). NSAIDs+스테로이드 점안 2년간 부분 반응만. 7)
- PPS: 중단 후에도 CME 발생 가능, 10년 후 발병 사례도 존재. 10)
유리체절제술(PPV)
섹션 제목: “유리체절제술(PPV)”VMT를 동반한 견인성 CME에서 유리체절제술로 80~92%에서 CME가 개선됨. 옥크리플라스민(효소적 유리체박리제)은 2/3상 시험에서 58%에서 1개월 이내 VMT 해소를 보임.
원인에 따라 NSAIDs 점안, 스테로이드(테논낭하/유리체내 주사), 항VEGF 유리체내 주사, 탄산탈수효소 억제제, 유리체절제술 등이 선택됨. 약물성 CME에서는 원인 약물 중단이 가장 효과적인 일차 치료. 치료법의 자세한 내용은 “표준적 치료법” 항목을 참조.
6. 병태생리학 및 상세 발병 기전
섹션 제목: “6. 병태생리학 및 상세 발병 기전”혈액-망막 장벽(BRB)의 구조
섹션 제목: “혈액-망막 장벽(BRB)의 구조”BRB는 두 층으로 구성됩니다. 내측 BRB(망막 혈관 내피 세포 간의 치밀 결합)와 외측 BRB(망막 색소 상피 세포 간의 치밀 결합)가 망막의 수분 항상성을 유지합니다. 염증, 허혈, 독성 물질 등으로 치밀 결합이 약화되면 혈청 단백질과 지질이 누출되어 삼투압이 상승합니다. 11)
Müller 세포는 aquaporin-4와 Kir4.1 채널을 이용한 배수 기전으로 정상적으로 액체 축적을 방지합니다. BRB 파괴가 심해지면 이 보상적 배출 기전이 포화되어 CME가 현저해집니다. 11)
CME의 세 가지 기전
섹션 제목: “CME의 세 가지 기전”삼출성
BRB 파괴: 혈관 내피 및 RPE 치밀 결합 약화.
액체 성분: 혈청 단백질 및 지질 누출. FA에서 꽃잎 모양 누출을 보임.
대표 질환: 당뇨망막병증, 망막정맥폐쇄, 포도막염. 11)
변성성
견인성
특수 발병 기전
섹션 제목: “특수 발병 기전”S1P 수용체 조절제(핑골리모드, 시포니모드): 혈관내피 카드헤린 조절을 억제하고 혈관 투과성을 증가시켜 BRB를 손상시킴. 4)EXPAND 시험에서 시포니모드군의 2%에서 CME 발생(위약군 <1%). 4)
이브루티닙(BTK 억제제): 혈액뇌장벽(BBB)을 통과하는 약물 특성으로 인해 BRB도 손상시킬 가능성이 시사됨. 3상 시험에서 이브루티닙군의 10%가 시야 흐림 보고(오파투무맙군 3%). 7)
급성 CRAO: 허혈로 인해 세포외 이온 항상성이 파괴되고 Müller 세포로 급격한 이온 유입이 발생. 그 결과 aquaporin-4와 Kir4.1 채널 발현이 증가하여 Müller 세포 부종(외과립층 국한)이 발생. 3)
7. 최신 연구와 향후 전망(연구 단계 보고)
섹션 제목: “7. 최신 연구와 향후 전망(연구 단계 보고)”토실리주맙(항IL-6 수용체 항체)에 의한 IRU 관련 CME 치료
섹션 제목: “토실리주맙(항IL-6 수용체 항체)에 의한 IRU 관련 CME 치료”면역회복성 포도막염(IRU)에 속발한 CME에 대해 토실리주맙이 효과적이었던 증례가 보고되었다.
Nguyen 등(2024)은 T세포 급성 림프구성 백혈병 치료 후 CMV 망막염 → IRU로 인한 CME가 발생한 17세 여성(전신 스테로이드가 대퇴골두 괴사로 금기)에게 토실리주맙 8mg/kg 정맥주사를 월 1회 × 2사이클 투여했다. 2사이클 후 CME의 현저한 개선이 관찰되었다. 5)
STOP-UVEITIS 시험에서 토실리주맙이 CME 개선을 가져오는 것으로 나타났으며, 스테로이드 금기 예에서 대체 치료로서의 위치가 기대된다. IL-6가 CME 병태에 직접 관여함을 시사하는 소견이다. 5)
PPS 관련 황반병증 및 CME의 장기 경과
섹션 제목: “PPS 관련 황반병증 및 CME의 장기 경과”PPS 관련 황반병증은 2018년에 처음 인식된 비교적 새로운 질환 개념입니다. PPS 중단 후에도 10년 이상 병변이 진행되고 CME가 발생할 수 있어 장기 추적 관찰의 중요성이 강조됩니다. 10)
Szelog 등(2023)은 PPS를 3년 사용하고 중단한 지 10년 후에 CME가 발생한 57세 여성을 보고했습니다. 초진 시 AMD로 오진되어 NSAIDs 및 스테로이드 점안액이 효과가 없었으나, 베바시주맙 1.25mg/0.05mL 2회 투여로 완전히 소실되었습니다. 5개월 후 반대쪽 눈에도 CME가 발생했습니다. 10)
PPS 관련 황반병증의 17%에서 CME가 동반되며, 누적 500g 이상 사용 시 10% 초과에서 황반병증이 발생하는 것으로 보고됩니다. 10)
OCT 바이오마커를 통한 예후 예측
섹션 제목: “OCT 바이오마커를 통한 예후 예측”OCT 소견의 치료 반응성을 체계적으로 평가한 연구에서 다음 바이오마커가 예후 예측에 유용한 것으로 나타났습니다. 13)
2025년 Survey of Ophthalmology에 게재된 체계적 검토에서는 망막 내 낭종(76% 호전) 및 망막하액(67% 호전)은 치료 반응성이 높은 반면, EZ 장애(64% 불변/악화), ELM 장애(67% 불변/악화), 고반사 병소(63% 불변/악화), DRIL(50% 불변/악화)은 예후가 불량함을 시사했습니다. 13)
EZ 및 ELM 장애 유무를 치료 방침 결정에 포함시키는 움직임이 진행되고 있습니다.
En face OCT를 통한 원인 진단
섹션 제목: “En face OCT를 통한 원인 진단”En face OCT를 이용한 CME 분포 패턴 분석을 통해 원인 질환 감별에 유용한 영상 특징이 확인되고 있습니다. 3) 특히 CRAO 동반 CME에서 급성 및 만성기의 층별 분포 차이는 비침습적 원인 추정 수단으로 주목받고 있습니다.
8. 참고문헌
섹션 제목: “8. 참고문헌”- Lin WC, Hsieh JW, Tsai SH, Lan YW. Latanoprost-associated cystoid macular edema in a patient with phakic eyes. Taiwan J Ophthalmol. 2023;13:242-244.
- Yamane H, Itagaki T, Kajitani K, et al. Cystoid macular edema following treatment with nanoparticle albumin-bound paclitaxel and atezolizumab for metastatic breast cancer. Case Rep Oncol. 2023;16:1121-1128.
- Estawro R, Abraham N, Fouad Y, Bousquet E, Sarraf D. Cystoid macular edema as a complication of central retinal artery occlusion. Am J Ophthalmol Case Rep. 2024;33:101998.
- Kim MY, Alkhabaz A, Smith SJ, Liao YJ. Siponimod-associated cystoid macular edema without known risk factors. Am J Ophthalmol Case Rep. 2024;36:102124.
- Nguyen BT, Hung JH, Thng ZX, et al. Tocilizumab for cystoid macular edema secondary to immune recovery uveitis in a patient with contraindications to long-term systemic corticosteroid. Yale J Biol Med. 2024;97:423-430.
- Chaloulis SK, Tsaousis KT. Cystoid macular edema associated with venous stasis in a patient with previously undiagnosed hyperhomocysteinemia. Cureus. 2021;13(12):e20782.
- Ben-Avi R, Dori D, Chowers I. Cystoid macular edema secondary to ibrutinib. Am J Ophthalmol Case Rep. 2022;26:101436.
- Fukuoka H, Kojima K, Iwama A, Okumura T, Sotozono C. Fingolimod-associated severe bilateral cystoid macular edema. Am J Ophthalmol Case Rep. 2022;26:101553.
- Karaca I, Korot E, Ghoraba H, et al. Acute iridocyclitis and cystoid macular edema related to kinked Hydrus Microstent in advanced glaucoma. Saudi J Ophthalmol. 2022;36:390-393.
- Szelog JT, Shah NS, Camejo MD. Cystoid macular edema arising 10 years after cessation of pentosan polysulfate sodium successfully treated with bevacizumab. J Vitreoret Dis. 2023;7(1):83-86.
- Cunha-Vaz J, et al. Blood-retinal barrier. Prog Retin Eye Res. 2024. [出典: 1-s2.0-S1350946224000107-main.pdf]
- American Academy of Ophthalmology. Cataract in the Adult Eye Preferred Practice Pattern. Ophthalmology. 2022. [出典: PIIS0161642021007508.pdf]
- OCT biomarkers systematic review. Surv Ophthalmol. 2025. [出典: PIIS0039625725001766.pdf]
- Royal College of Ophthalmologists. DRAFT Clinical Guideline on Idiopathic Full-Thickness Macular Holes. 2024.
