신생혈관형 AMD

연령 관련 황반변성 (AMD)
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 연령 관련 황반변성이란?
섹션 제목: “1. 연령 관련 황반변성이란?”연령 관련 황반변성(AMD)은 황반부의 노화 관련 변화로 인해 위축성 또는 삼출성 변화를 일으키는 질환입니다. 유전적 소인 외에도 노화, 흡연, 햇빛 노출, 비만, 고지방 식이 등의 환경 요인이 관여하는 다인자 질환으로 생각됩니다.
50세 이상에서 중심와를 중심으로 직경 6,000μm 범위에 나타나는 노화에 기반한 황반 이상으로 정의되며, 전구 병변, 신생혈관형, 위축형으로 크게 나뉩니다. 시각 장애의 원인으로 4위를 차지합니다.
Hisayama 연구(2012년)에 따르면 진행성 AMD의 유병률은 1.6%(삼출형 1.5%, 위축형 0.1%)이며, Nagahama 연구(2008년~)에서는 전구 병변의 유병률이 22.8%(드루젠 39.4%)로 보고되었습니다. 50세 이상 남녀(남:여 = 3:1)에서 발생하며, 한쪽 눈 또는 양쪽 눈(약 40%)에 발병합니다. 전구 병변과 진행성 AMD 모두 증가 추세에 있습니다. Hisayama 연구(9년 추적)에서는 흡연 습관이 후기 AMD 발병을 4배 증가시켰다고 보고되었습니다1).
인종 차이가 있어 백인과 아시아인에서 유병률이 높고, 히스패닉과 아프리카계에서는 낮습니다2). 위축형 AMD의 유병률은 서양 연구에서 0.661.34%로 보고되며, 85세 이상에서는 삼출형보다 4배 빈번하다는 보고도 있습니다. 고령화가 진행되는 우리나라에서도 향후 큰 문제가 될 가능성이 높습니다. 전 세계적으로 AMD 환자는 약 2억 명에 이르며, 2040년에는 약 2억 8,800만 명으로 증가할 것으로 예측됩니다2). 후기 AMD의 유병률은 5059세에서 0.1%, 80세 이상에서 4.3%로 연령에 따라 지수 함수적으로 상승합니다2).
병기 분류
섹션 제목: “병기 분류”최신 일본 진료 가이드라인(2024년)에서는 Beckman 분류를 참고하여 다음과 같은 4단계로 분류하고 있습니다1).
| 병기 | 특징 |
|---|---|
| 초기 AMD | 중형 연성 드루젠(63~125μm 미만) 1개 이상 |
| 중기 AMD | 대형 드루젠(125μm 이상), RPE 이상, 망막하 드루젠양 침착물 |
| 후기 AMD | 황반 신생혈관(MNV)(PNV 포함) 또는 지도상 위축 |
| 말기 AMD | 섬유성 반흔 또는 낭포성 황반 변성에 동반된 심한 시력 저하 |
소형(경성) 드루젠(<63 μm)은 생리적 노화 변화로 간주되며 조기 AMD에 포함되지 않습니다. 그러나 다수(20개 이상)의 경성 드루젠이 관찰되는 경우 AMD 발병 위험이 높습니다1). 중기 AMD의 5년 진행률은 약 18%이지만, 망상 가성드루젠이 존재하는 경우 위험이 현저히 증가합니다(색소 이상 + 대형 드루젠 + 망상 가성드루젠에서 5년 위험 72%)2).
위축형 AMD
2. 주요 증상과 임상 소견
섹션 제목: “2. 주요 증상과 임상 소견”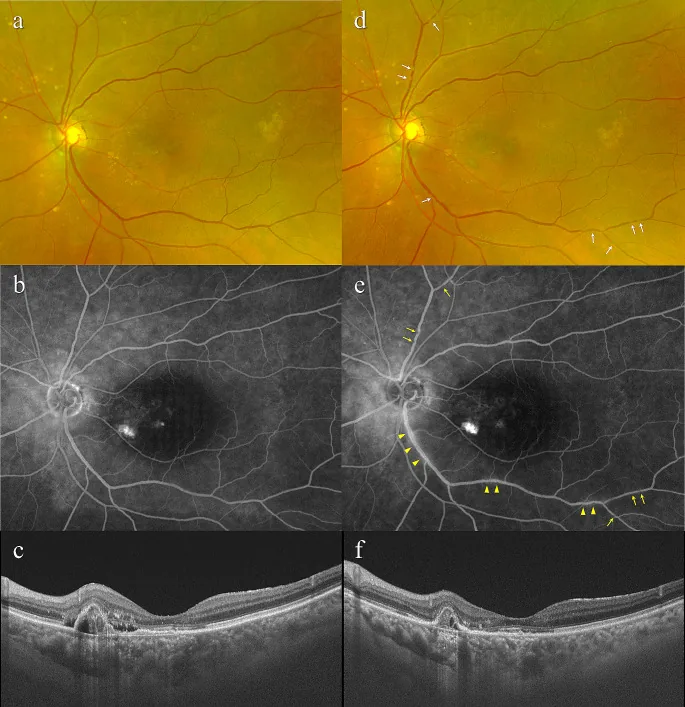
자각 증상
섹션 제목: “자각 증상”초기에는 변시증(왜곡되어 보임)과 중심암점으로 시작됩니다. 진행되면 0.1 미만의 시력 저하에 이릅니다. 대량 출혈의 경우 갑작스러운 심한 시력 저하가 발생할 수 있습니다.
- 변시증(메타모르프시아): 직선이 물결쳐 보입니다. MNV 발병의 초기 증상으로 중요합니다2).
- 중심암점: 중심에서 중심와 주변의 시야 결손입니다. 지도상 위축에서는 위축 영역에 일치하는 절대암점이 발생합니다.
- 시력 저하: 신생혈관형에서는 급격한 저하가 나타납니다. 위축형은 서서히 진행되지만, 중심와에 위축이 미치면 0.1 이하로 저하됩니다.
- 대비 감도 저하: 중심와가 보존된 위축형에서도 초기에 발생하며, 시력 검사로는 포착할 수 없는 기능 장애입니다8).
- 암순응 곤란: 어두운 곳에 적응하는 데 시간이 걸립니다. 시력 저하에 선행하여 나타날 수 있습니다2).
- 독서 및 원거리 시기능 장애: 중심와 외부의 지도상 위축에서도 삶의 질에 영향을 미칩니다8). 지도상 위축 환자의 약 절반이 급속한 질병 진행을 경험하며, 삶의 질에 큰 부정적 영향을 미친다고 알려져 있습니다3).
- 광시증(포톱시아): 번쩍이는 느낌입니다. 빈도는 낮지만 신생혈관 발병 초기에 호소될 수 있습니다2).
한쪽 눈 발병의 경우 일상생활에서 자각하지 못하는 경우가 많습니다. 증상의 정도는 MNV의 위치, 크기, 망막하액, 출혈, 섬유성 반흔의 정도에 따라 다양합니다. 신생혈관형에서는 법적 실명에 이르는 기간이 위축형보다 짧은 경향이 있으며, 변시증이 나타날 때는 신속한 진료가 권장됩니다.
임상 소견 (의사가 진찰로 확인하는 소견)
섹션 제목: “임상 소견 (의사가 진찰로 확인하는 소견)”드루젠
섹션 제목: “드루젠”황반부에 보이는 황백색의 작은 원형 융기 병변으로, RPE의 기저막과 브루크막 내콜라겐층 사이에 축적된 다형성 물질(막양 잔해물, 비에스테르화 콜레스테롤, 보체 등)입니다. AMD 병태의 근간인 만성 염증의 기원으로 생각됩니다.
- 경성 드루젠: 장경 63μm 미만. 경계가 명확합니다. 단순한 노화 변화로 AMD 발병과 관련되지 않습니다.
- 연성 드루젠: 장경 63μm 이상. 경계가 불명확합니다. AMD 발병과 밀접하게 관련됩니다.
- 망막하 드루젠양 침착물(망상 가성 드루젠): RPE 위에 존재하며, 위축형 AMD 및 RAP(3형 MNV)와 밀접하게 관련됩니다1).
MNV 관련 소견 (신생혈관형)
섹션 제목: “MNV 관련 소견 (신생혈관형)”- 1형 MNV: OCT에서 이중층 징후(double layer sign, RPE의 불규칙 융기와 내부 중등도 반사)를 보입니다. 낮고 편평한 형태와 RPE가 돔 모양으로 융기된 섬유혈관성 PED로 나뉩니다. 후자는 특히 치료에 저항성이 있습니다1).
- 2형 MNV: OCT에서 RPE 위의 중~고반사 구조물로 검출됩니다. 피브린 삼출을 동반하는 경우가 많습니다1).
- 3형 MNV (RAP): 양안에 연성 드루젠이 다발하는 환자에서 흔합니다. OCT에서 낭포성 황반부종과 bump sign을 동반한 PED가 관찰됩니다1).
- PCV: 1형 MNV의 가장자리에 용종상 병변이 동반됩니다. 검안경에서 주황색-적색 융기 병변으로 관찰되며, ICGA로 확진합니다1).
지도상 위축
섹션 제목: “지도상 위축”맥락막 혈관이 투시되는 경계가 명확한 RPE 위축 영역입니다. 병변은 중심와 주변(중심와 주위)에서 시작하여 말굽형 → 고리형으로 확대되고 중심와로 진행됩니다. 중심와 침범까지의 중앙값은 2.5년으로 알려져 있습니다3). 성장 속도는 1.28~2.6 mm²/년이며, 라니비주맙 임상시험 데이터에서 GA 면적이 2년 동안 평균 8.07에서 12.05 mm²로 확대되었습니다3). 다병소성 GA는 단일 병소보다 성장 속도가 빠릅니다3). 반대안의 GA 전환율은 12개월에 약 30%에 이르고, CNV 전환율도 6.7%로 보고되었습니다.
큰 드루젠양 PED가 퇴축할 때 급속히 위축이 진행될 수도 있습니다. 안저자가형광에서 위축 영역 경계부에서 관찰되는 과형광 패턴은 진행 속도 예측에 유용합니다.
기타 소견
섹션 제목: “기타 소견”- 망막하/RPE하 출혈: MNV로 인한 출혈. 대량인 경우 황반하 혈종이 되고, 유리체 출혈까지 이를 수도 있습니다.
- 장액성 망막박리/장액성 PED: MNV의 액체 누출로 인해 발생합니다.
- 경성 백반: 만성 삼출에 따라 황반 주위에 침착됩니다.
- 섬유성 반흔: 말기 AMD의 소견. 섬유혈관성 반흔 조직이 황반에 형성됩니다1).
3. 원인과 위험 요인
섹션 제목: “3. 원인과 위험 요인”AMD는 다인자 질환으로, 유전적 소인에 환경 및 행동 요인이 더해져 발병합니다.
- 나이: 가장 큰 위험 요인입니다. 75세 이상에서 유병률이 급격히 증가합니다2).
- 흡연: 가장 중요한 수정 가능한 위험 요인입니다. Hisayama 연구에서는 흡연이 후기 AMD 발병 위험을 4배 증가시킨다고 보고했습니다1). 용량-반응 관계가 있으며, 간접 흡연도 관련됩니다2).
- 유전적 소인: 보체인자 H(CFH) Y402H 돌연변이와 ARMS2/HTRA1이 주요 위험 유전자좌입니다. C2/CFB, C3, CFI 등의 보체계 유전자와 APOE, CETP 등의 지질 대사 유전자도 관여합니다1).
- 두꺼운 맥락막(pachychoroid): 맥락막 대혈관 확장 및 혈관 투과성 증가가 신생혈관성 AMD 발병 배경으로 중요시됩니다. 일본인에서는 서양인보다 드루젠이 적고(약 30%), 두꺼운 맥락막이 발병에 크게 관여합니다1).
- 심혈관 질환, 고혈압, 비만: AMD 발병 위험과 관련됩니다2).
- 식습관: 고지방 식이는 위험을 높이고, 장쇄 오메가-3 지방산과 녹황색 채소 섭취는 위험을 낮춥니다1). 지중해식 식단을 준수하면 진행성 AMD 위험이 41% 감소합니다2).
- 햇빛 노출: 자외선 및 가시광선 노출도 위험 요인으로 지적됩니다.
- 성별: 남성에게 더 흔합니다(남녀 비율 3:1). 그러나 고령 여성에서도 빈번하게 나타납니다.
- 홍채 색: 홍채 색이 옅은(파란색 또는 회색) 사람에서 위험이 더 높은 경향이 있습니다.
- 가족력: 1촌 친족에 AMD 환자가 있는 경우 발병 위험이 증가합니다.
- 원시: 원시안에서 AMD 발병 위험이 높다는 보고가 있습니다.
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”진단 기준
섹션 제목: “진단 기준”신생혈관형 AMD의 진단 기준은 다음과 같습니다 1):
- 황반부(중심와를 중심으로 직경 6,000μm 이내)에 드루젠, 두꺼운 맥락막 또는 RPE 이상과 관련하여 발생한 MNV가 존재함
- 확진을 위해서는 MNV 확인이 바람직하나, 출혈성 변화나 섬유성 반흔으로부터 MNV 존재를 충분한 확신으로 의심할 수 있으면 진단 가능
- 제외: 고도 근시, 망막 색소 선조, 염증성 질환, 외상 등으로 인한 병변
위축형 AMD(지도상 위축)의 진단 기준은 다음 모두를 충족해야 합니다 1):
| 항목 | 기준 |
|---|---|
| 크기 | 직경 ≥250μm |
| 형태 | 원형, 난원형, 소엽상 또는 지도상 |
| 경계 | 선명함 |
| RPE 변화 | 저색소 또는 탈색소 변화 |
| 맥락막 | 중대형 혈관이 명확하게 보임 |
주요 검사법
섹션 제목: “주요 검사법”- OCT(광간섭단층촬영): AMD 진단 및 경과 관찰의 중심 검사. 1형 MNV의 이중층 징후, 2형 MNV의 망막하 고반사 구조물, 3형 MNV의 범프 징후, 지도상 위축의 외층 망막 위축 등을 검출합니다1).
- OCTA(광간섭단층혈관조영): MNV 검출 메타분석에서 민감도 0.87, 특이도 0.972). 비침습적이며, FA보다 1형 MNV 검출력이 높을 수 있습니다1).
- FA(형광안저혈관조영): MNV 유형(고전적/잠복) 분류에 유용합니다. 변시증이나 원인 불명의 시력 저하 등의 적응증이 있을 때 시행합니다2).
- ICGA(인도시아닌그린혈관조영): PCV 진단 확정에 유용합니다. 1형 MNV 주변의 폴립양 병소를 동맥류상 과형광으로 묘사합니다1). 아나필락시스 위험이 있으므로 다른 검사로 진단 가능한 경우 생략을 고려합니다.
- 안저자가형광(FAF): 지도상 위축을 경계가 선명한 자가형광 감소 영역으로 검출합니다. 경계부의 과자가형광은 진행 예측에 유용합니다.
- Amsler 격자: 변시증 및 암점 선별검사. 정기적인 자가 점검이 권장됩니다2).
- 미세시야계: 망막 민감도 정량화. 지도상 위축으로 인한 절대 암점 및 민감도 저하를 측정할 수 있으며, BCVA로는 포착할 수 없는 기능 장애를 평가합니다8).
활동성 평가(신생혈관형)
섹션 제목: “활동성 평가(신생혈관형)”MNV로부터의 삼출성 변화(IRF, SRF, RPE하액, 피브린, 출혈 등)가 관찰되면 ‘활동성’으로 판단합니다1). OCT를 이용한 비침습적 평가가 주류가 되고 있습니다. MNV의 질병 활동성이 높은 부위가 반드시 중심와에 있는 것은 아니므로, 황반 전체를 스캔하여 평가하는 것이 권장됩니다1).
감별 진단
섹션 제목: “감별 진단”MNV를 동반한 황반 이상은 다음 질환과의 감별이 필요합니다.
- 고도 근시: 근시성 맥락망막 위축, MNV
- 중심성 장액성 맥락망막병증(CSC): 후포도막 관련 질환의 연속체로 중복될 수 있음
- 유전성 망막 이영양증: 젊은 나이에 발병 시 적극적으로 의심
- 염증성 질환: 안구 히스토플라스마증 증후군, 다초점 맥락막염 등
- 혈관모양 줄무늬: Bruch막 파열로 인한 MNV
5. 표준 치료법
섹션 제목: “5. 표준 치료법”전구 병변(초기/중기 AMD)에 대한 치료
섹션 제목: “전구 병변(초기/중기 AMD)에 대한 치료”초기 AMD에 대한 근거 기반 치료법은 없습니다2). 중기 AMD 이상에서는 금연 지도, 식생활 개선에 더해 AREDS2 처방에 따른 보충제 섭취가 권장됩니다1).
AREDS2에서 사용된 보충제 처방1):
- 비타민 C 500mg
- 비타민 E 400 IU
- 루테인/제아잔틴 10 mg/2 mg
- 산화아연 25 mg
- 산화구리 2 mg
베타카로틴은 흡연자의 폐암 위험을 증가시키므로 루테인/제아잔틴으로 대체되었습니다1). AREDS2 처방은 중기 AMD에서 후기 AMD로의 진행 위험을 약 25% 감소시킵니다.
신생혈관성 AMD의 치료
섹션 제목: “신생혈관성 AMD의 치료”유리체내 항VEGF 주사 (1차 치료)
섹션 제목: “유리체내 항VEGF 주사 (1차 치료)”신생혈관성 AMD의 1차 치료는 항VEGF 약제의 유리체내 주사입니다1). 중심와하 MNV에 대해 초기 치료로 항VEGF 단독 요법이 권장됩니다.
라니비주맙
용량: 0.5 mg 유리체내 투여
도입기: 1개월 간격으로 3회
유지기: 필요시 투여(PRN). MARINA 연구에서 위약군 14.9글자 감소 대비 6.6글자의 시력 개선1).
바이오시밀러: 라니비주맙 BS 사용 가능.
아플리버셉트
용량: 2.0 mg 유리체내 투여
도입기: 1개월 간격으로 3회 주사
유지기: 2개월마다 고정 투여 또는 treat-and-extend 방식. 삼출 재발이 없으면 2주씩 연장(최대 3개월), 재발 시 2주 단축 1).
PCV: 폴립 퇴축률 4050%로 라니비주맙(2030%)보다 우수.
브롤루시주맙 / 파리시맙
브롤루시주맙: 6mg 투여. 8~12주마다 투여 가능. 망막혈관염 및 혈관폐쇄를 포함한 안내 염증에 주의 필요 1).
파리시맙: VEGF-A + Ang-2 이중특이항체. 8~16주마다 투여. TENAYA/LUCERNE 연구에서 아플리버셉트에 비해 비열등성 입증 1)10).
투여 방법
섹션 제목: “투여 방법”다음 세 가지 투여 요법이 있다 1).
- 고정 투여법: 일정 간격으로 지속 투여.
- 필요시 투여법(PRN): 매월 경과 관찰 후 질환 활성도가 보이면 투여. CATT 연구 및 HARBOR 연구에서 PRN군은 매월 투여군에 비해 2년째 시력이 저하되었다고 보고됨 11).
- treat-and-extend(TAE)법: 질환 활성도에 따라 투여 간격 조정. TREX-AMD 연구에서 매월 투여와 동등한 시력 개선 효과가 입증됨. ALTAIR 연구(일본인 대상)에서는 2주/4주 조정 TAE로 96주에 걸친 효과가 확인됨 1). 메타분석에서도 TAE는 고정 투여와 동등한 2년 시력 성적을 보였고, PRN보다 유의하게 우수함 1).
중심와를 포함하지 않는 MNV에 대한 레이저 광응고술
섹션 제목: “중심와를 포함하지 않는 MNV에 대한 레이저 광응고술”2형 MNV 또는 PCV에 대해 MNV 전체에 레이저 광응고술을 시행하는 방법이 있다. 노란색 이상 파장, 스팟 크기 200300μm, 출력 150250mW, 응고 시간 0.2~0.5초로, MNV 주변에 100μm의 안전 여백을 포함하여 중등도 이상의 광응고를 시행한다. 단, 레이저 광응고술은 RPE를 비가역적으로 손상시키므로 중심와에 가까운 MNV 치료에는 적합하지 않다 1).
PCV(폴립양 맥락막 혈관병증)의 치료
섹션 제목: “PCV(폴립양 맥락막 혈관병증)의 치료”PCV에 대한 치료 선택지는 다음과 같다 1).
- 항VEGF 약물 병용 광역학치료(PDT): EVEREST II 연구에서 라니비주맙과 PDT 병용이 라니비주맙 단독에 비해 유의하게 높은 폴립 퇴축 효과를 보였습니다. 안전성 측면에서 항VEGF 약물과의 병용이 권장됩니다.
- 항VEGF 약물 단독요법: 아플리버셉트의 폴립 퇴축률이 40~50%로 양호하여, 최근 단독요법의 기회가 증가하고 있습니다.
PDT 처방: 베르테포르핀 6mg/m²를 10분간 정맥 투여합니다. 투여 시작 15분 후 레이저 조사(689nm, 600mW/cm², 83초)를 시행합니다. 조사 크기는 병변 최대 직경 + 1,000μm입니다. 치료 후 2일간 직사광선을 피해야 합니다.
장기적으로 PDT는 황반 위축을 악화시킬 수 있으며, 맥락막이 얇은 경우나 이미 황반 위축이 있는 경우에는 피하는 것이 바람직합니다. 3형 MNV에 대한 PDT는 권장되지 않습니다 1).
치료 저항성 사례 및 약제 전환
섹션 제목: “치료 저항성 사례 및 약제 전환”항VEGF 약물 치료 중 효과가 부족한 경우(치료 저항성)나 효과가 감소한 경우(내성 획득)에는 다른 약제로의 전환이 효과적일 수 있습니다 1). 또한 치료 부담(내원 빈도, 주사 빈도)을 고려하여 약제를 변경하기도 합니다. 말기 AMD에서 질환 활동성이 낮은 섬유성 반흔이나 위축성 변화가 보이는 경우에는 적극적인 치료 적응이 되지 않으며 경과 관찰을 고려합니다 1).
RAP(망막혈관종성 증식)의 치료
섹션 제목: “RAP(망막혈관종성 증식)의 치료”시력이 양호한 눈에서는 항VEGF 단독요법, 치료 횟수 감소가 필요한 경우 PDT-VEGF 억제제 병용요법이 선택지가 됩니다. 실제 임상에서는 항VEGF 단독요법이 주류입니다.
황반하 혈종의 대응
섹션 제목: “황반하 혈종의 대응”대량의 황반하 출혈은 급격한 시력 저하를 초래합니다. 발병 초기라면 혈종 이동술로 시력 개선을 얻을 수 있습니다.
- 보존적 치료: 소량 출혈, 비교적 양호한 시력인 경우. 아도나정 30mg×3(분할 3회), 트라넥삼산캡슐 250mg×3(분할 3회) 경구 투여. 삼출을 동반하면 항VEGF 약물 투여.
- 유리체강내 가스 주입술: 육불화황(SF₆) 또는 퍼플루오로프로판(C₃F₈) 0.3~0.5mL 주입 및 수술 후 엎드린 자세 유지로 혈종 이동. tPA 병용도 시행됩니다 1).
- 유리체절제술: tPA 망막하 주입이나 퍼플루오로카본액을 이용한 혈종 압출.
위축형 AMD(지도상 위축)의 치료
섹션 제목: “위축형 AMD(지도상 위축)의 치료”현 시점에서 중심와를 포함한 지도상 위축이 확립된 증례에 대한 치료법은 아직 없습니다. 보체계가 강하게 관여하는 것으로 생각되며, 보체 경로를 표적으로 하는 여러 분자표적약물이 개발 및 임상시험 단계에 있습니다.
중심와 외부의 지도모양 위축에 대해 AREDS2 보충제 섭취와 생활습관 개선이 권장됩니다. 경과 중 MNV가 발생한 경우(10~15%) 항VEGF 약물 치료가 표준이 됩니다.
시력 저하가 진행된 환자에게는 차광 안경, 확대경 등의 시각 보조기구 제안 및 일상생활 지원 등 저시력 관리가 중요합니다 1).
도입기에는 보통 1개월 간격으로 3회 주사합니다. 이후 유지기에는 treat-and-extend 방법(간격을 점차 연장)이 권장됩니다. ALTAIR 연구(일본인 대상)에서 96주에 걸친 효과가 확인되었습니다 1). 파리시맙에서는 최대 16주 간격 유지가 가능한 증례도 있습니다 10).
6. 병태생리학·상세한 발병 기전
섹션 제목: “6. 병태생리학·상세한 발병 기전”RPE-브루크막-맥락막 복합체의 변성
섹션 제목: “RPE-브루크막-맥락막 복합체의 변성”AMD의 병태는 RPE 세포의 손상에서 시작됩니다. RPE의 기저막과 브루크막의 내콜라겐층 사이에 드루젠이 축적됩니다. 드루젠의 구성 성분에는 막양 잔해물, 비에스테르화 콜레스테롤, 보체 등이 포함되어 만성 염증의 기원이 됩니다. 산화 스트레스, 지질 대사 이상, 자연 면역계의 활성화가 복합적으로 관여하여 RPE-브루크막-맥락막 모세혈관 복합체의 항상성이 파괴됩니다. 이후 경로는 두 가지로 분기됩니다.
- 위축형 경로: 염증과 산화 스트레스로 인해 RPE 변성 위축이 진행되어 광수용체-RPE-맥락막모세혈관 복합체에 지도상 위축이 발생합니다. 먼저 외층 망막(RPE 및 타원체대)이 소실되고, 진행된 경우에는 맥락막모세혈관도 위축됩니다3).
- 삼출형 경로: 망막 외층 또는 RPE 아래에 신생혈관(MNV)이 발생하여 출혈과 삼출을 일으킵니다. 안내액에서 IL-6, IL-8, MCP-1 및 VEGF가 상승합니다5).
RPE 세포의 노화
섹션 제목: “RPE 세포의 노화”노화된 RPE 세포는 세포 노화 관련 분비 표현형(SASP)을 나타내며, SA-β-gal, p53, p21 및 p16의 발현이 증가합니다7). 이 노화 RPE 표현형은 위축형 AMD 환자의 소견과 일치하며, 세노리틱스(senolytics)를 통한 선택적 제거가 치료 표적으로 주목받고 있습니다.
보체계의 관여
섹션 제목: “보체계의 관여”CFH, C3 및 ARMS2의 유전자 다형성이 AMD 발병 감수성에 관여합니다2). 보체 경로(고전적 경로, 대체 경로, 렉틴 경로)의 조절 이상이 지도상 위축의 확장을 유발합니다3). 보체 C3를 억제하면 C5 이후의 전체 말단 경로를 억제하고, C5를 억제하면 막공격복합체(MAC) 형성을 방지할 수 있을 것으로 기대됩니다.
Anegondi 등(2025)은 람팔리주맙(lampalizumab) 시험 데이터 분석에서 지도상 위축의 성장률이 빠를수록 BCVA 감소가 빠르며, 2년 동안 약 75%가 5글자 이상, 약 50%가 10글자 이상, 약 25%가 15글자 이상의 시력 저하를 보인다고 보고했습니다3).
파키코로이드(pachychoroid)와 신생혈관성 AMD
섹션 제목: “파키코로이드(pachychoroid)와 신생혈관성 AMD”파키코로이드는 맥락막 대혈관의 확장(pachyvessel)과 맥락막 혈관 투과성 항진을 특징으로 하는 병태입니다1). 중심성 장액성 맥락망막병증(CSC)이 파키코로이드 질환의 대표이며, CSC나 파키코로이드 색소상피병증(PPE)을 배경으로 MNV가 발생한 것을 파키코로이드 신생혈관병증(PNV)이라고 합니다. CFH 유전자는 파키코로이드와 CSC의 발병에도 관여하는 것으로 보고되었습니다1).
비만 세포와 염증
섹션 제목: “비만 세포와 염증”Ribatti 등(2024)은 맥락막 비만 세포가 분비하는 트립타제(tryptase)에 의한 Bruch막 분해가 RPE 사멸을 유도하고, VEGF-A, FGF-2, IL-8 및 NGF의 방출이 혈관 신생을 촉진한다고 보고했습니다5).
비삼출성 MNV의 생물학적 활성
섹션 제목: “비삼출성 MNV의 생물학적 활성”비삼출성 MNV는 무증상이더라도 생물학적으로 활성이며, 면적 증가가 지속됩니다4).
Wang 등(2023)은 45안의 SS-OCTA 연구에서 성장형 MNV(면적 50% 이상 증가)는 비성장형 MNV보다 삼출 전환까지의 기간이 유의하게 짧았으며(13.60개월 vs 31.11개월, HR 12.51), 흡연력과 고중성지방혈증이 성장과 유의하게 상관관계가 있었다(P=0.021)고 보고했습니다4).
중심와의 보호 기전
섹션 제목: “중심와의 보호 기전”지도상 위축은 종종 중심와 주변에서 시작되며, 중심와는 위축에 대해 상대적 내성을 보입니다3). 이로 인해 말굽 모양 또는 고리 모양의 GA가 형성됩니다. 중심와 침범까지의 중앙값은 2.5년이며, 그 동안 고대비 시력은 유지되지만 암순응 감도, 읽기 속도 등의 일상 시각 기능은 조기에 손상됩니다8).
7. 최신 연구 및 향후 전망 (연구 단계 보고)
섹션 제목: “7. 최신 연구 및 향후 전망 (연구 단계 보고)”보체 억제제 (미국 FDA 승인, 일본 미승인)
섹션 제목: “보체 억제제 (미국 FDA 승인, 일본 미승인)”2023년에 지도상 위축에 대해 두 가지 보체 억제제가 미국에서 FDA 승인을 받았습니다.
- 페그세타코플란 (SYFOVRE): C3 억제제. 15mg/0.1mL, 25~60일마다 유리체내 주사. OAKS 시험 (637명) 및 DERBY 시험 (621명)에서 지도상 위축의 성장률을 최대 21% 감소시켰습니다9).
- 아바신캅타드 페골 (Izervay): C5 억제제. 2mg, 월 1회 유리체내 주사. GATHER 2 시험 (448명)에서 14~19%의 성장률 감소를 보였습니다.
그러나 두 약물 모두 시력 개선을 사전 설정 평가 항목으로 한 시험에서 유의한 차이를 얻지 못하여, ‘구조-기능 괴리’가 과제로 남아 있습니다3)8). 유럽 의약품청(EMA)은 기능적 이점의 입증을 요구하며 페그세타코플란의 승인을 인정하지 않았습니다8).
보체 D 인자 억제제 람팔리주맙의 3상 CHROMA (906명) 및 SPECTRI (975명) 시험은 GA 면적 억제를 보여주지 못해 중단되었습니다. 시각 사이클 억제제 에믹스스타트의 SEATTLE 시험 (580명)도 유효성을 입증하지 못했습니다.
기능적 시각 평가의 과제
섹션 제목: “기능적 시각 평가의 과제”Dinah 등 (2025)의 리뷰에서는 BCVA가 지도상 위축의 기능적 영향을 충분히 포착하지 못하며, 미세시야계, 저휘도 시력(LLVA), 읽기 속도가 대체 지표로 권장되었습니다8). 복합적·다중 모드 기능 평가의 확립이 향후 임상 시험의 핵심이 될 것입니다.
신규 항VEGF 약물 및 지속 방출 장치
섹션 제목: “신규 항VEGF 약물 및 지속 방출 장치”- 고용량 아플리베르셉트 (8mg): PULSAR 시험에서 최대 16주 간격 투여가 가능함을 입증했습니다2). 치료 부담 감소가 기대됩니다.
- 라니비주맙 지속 방출 임플란트(port delivery system): Archway 시험에서 24주마다 리필 교체로 매월 주사와 동등한 효과가 보고되었습니다2).
- 바이오시밀러: 라니비주맙 및 애플리버셉트의 여러 바이오시밀러가 승인되었습니다2).
광생물조절 요법
섹션 제목: “광생물조절 요법”Ji 등(2025)은 광생물조절 치료(적색근적외선 6501,300nm)를 받은 건성 AMD 사례를 보고했습니다6). 8개월 동안 우안의 드루젠 면적이 58% 감소했고 좌안에서는 완전히 소실되었습니다. 시력은 양안 모두 20/30에서 20/20으로 개선되었습니다. Lightsite III 3상 시험에서도 드루젠 부피 감소 및 시력 개선이 확인되었습니다.
세노리틱스
섹션 제목: “세노리틱스”Chung과 Kim(2022)은 MDM2 억제제 Nutlin-3a가 노화 RPE 세포를 선택적으로 제거하는 새로운 접근법으로 유망하다고 보고했습니다7). 미토콘드리아 특이적 세노리틱스의 개발이 향후 과제입니다.
줄기세포 치료 및 유전자 치료
섹션 제목: “줄기세포 치료 및 유전자 치료”RPE 세포 이식을 이용한 줄기세포 치료가 연구 단계에 있으며, 여러 임상시험이 진행 중입니다. 보체 인자를 표적으로 하는 유전자 치료도 검토되고 있습니다.
8. 예후와 경과
섹션 제목: “8. 예후와 경과”위축형 AMD의 예후
섹션 제목: “위축형 AMD의 예후”위축형 AMD는 서서히 진행되지만, 지도상 위축이 중심와에 도달하면 시력이 0.1 이하로 저하됩니다. 법적 실명(ETDRS 20글자 미만)까지의 중앙값은 6.2년으로 보고되었습니다3). 람팔리주맙 시험 데이터 분석에 따르면 2년 동안 평균 BCVA가 66자에서 57자(약 20/50에서 20/80 상당)로 감소했습니다3).
지도상 위축의 성장 속도가 빠를수록 BCVA 감소도 빠르며, 특히 중심와하 단일 병변을 가진 눈에서는 최속 성장군에서 2년 동안 약 4줄(17.75자)의 감소가 나타납니다3). 반면, 최완 성장군에서는 2년 동안 단 1.69자만 감소합니다. 중심와가 보존되는 동안에도 암소 감도, 대비 감도, 읽기 속도는 조기에 손상되므로 시력값만으로는 기능적 영향을 과소평가하게 됩니다8).
또한 일정 확률로 MNV가 발생하여 신생혈관성 AMD로 이행되며, 더 심각한 시력 저하를 초래할 수 있습니다.
신생혈관성 AMD의 예후
섹션 제목: “신생혈관성 AMD의 예후”항VEGF 약물을 통한 MNV 조절로 시력 예후가 크게 개선되었습니다. CATT 연구 5년 추적 관찰에서 50%의 눈이 시력 20/40 이상을 달성했습니다11). 그러나 방치할 경우 약 90%의 눈에서 시력이 0.1 이하로 저하되고, 황반부에 섬유성 또는 위축성 반흔이 남습니다. MNV로 인해 대량 출혈이 발생한 경우, 광범위한 시야 결손을 동반하여 완전 실명을 포함한 더 심각한 시기능 장애를 초래할 수 있습니다.
MNV의 완치는 불가능하며, 적절한 치료와 장기 관리 없이는 비가역적인 시력 저하가 쉽게 발생합니다1). MNV의 활동성이 일시적으로 안정되더라도 장기 경과 중 재발할 수 있으며, 반복적인 삼출로 인해 위축성 변화나 섬유성 반흔이 합병될 수 있습니다. 반대안에도 MNV가 높은 비율로 발생한다는 점을 염두에 두고, 치료 지속과 정기적인 모니터링이 필수적입니다1). 심각한 시기능 저하를 겪는 환자에게는 적극적인 저시력 재활이 권장됩니다.
9. 참고문헌
섹션 제목: “9. 참고문헌”-
日本網膜硝子体学会 新生血管型加齢黄斑変性診療ガイドライン作成ワーキンググループ. 新生血管型加齢黄斑変性の診療ガイドライン. 日眼会誌. 2024;128(9):680-696.
-
Flaxel CJ, Adelman RA, Bailey ST, et al. Age-Related Macular Degeneration Preferred Practice Pattern. Ophthalmology. 2024;131(8):S1-S50.
-
Anegondi N, Steffen V, Sadda SR, et al. Visual loss in geographic atrophy: learnings from the lampalizumab trials. Ophthalmology. 2025;132(4):420-430.
-
Wang Y, Sun J, Wu J, et al. Growth of nonexudative macular neovascularization in age-related macular degeneration: an indicator of biological lesion activity. Eye (Lond). 2023;37(10):2048-2054.
-
Ribatti D, Dammacco R. Mast cells in human choroid and their role in age-related macular degeneration (AMD). Clin Exp Med. 2024;24(1):98.
-
Ji PX, Pickel L, Berger AR, Sivachandran N. Improvement in dry age-related macular degeneration with photobiomodulation. Case Rep Ophthalmol. 2025;16(1):155-162.
-
Chung H, Kim C. Nutlin-3a for age-related macular degeneration. Aging (Albany NY). 2022;14(14):5613-5616.
-
Dinah C, Esmaeelpour M, Rachitskaya AV, De Salvo G, Munk MR. Functional endpoints in patients with geographic atrophy: what to consider when designing a clinical trial. Surv Ophthalmol. 2025. doi:10.1016/j.survophthal.2025.02.004.
-
Heier JS, Lad EM, Holz FG, et al. Pegcetacoplan for the treatment of geographic atrophy secondary to age-related macular degeneration (OAKS and DERBY): two multicentre, randomised, double-masked, sham-controlled, phase 3 trials. Lancet. 2023;402:1434-1448.
-
Khanani AM, Kotecha A, Chang A, et al. TENAYA and LUCERNE: two-year results from the phase 3 neovascular age-related macular degeneration trials of faricimab. Ophthalmology. 2024;131:914-926.
-
Martin DF, Maguire MG, Ying GS, et al; CATT Research Group. Ranibizumab and bevacizumab for neovascular age-related macular degeneration. N Engl J Med. 2011;364:1897-1908.
