新生血管型AMD
黃斑新生血管(MNV):源自脈絡膜或視網膜血管的新生血管出現在黃斑,導致視力急劇下降。
分型:分為1型MNV(RPE下)、2型MNV(RPE上)、3型MNV(視網膜內血管來源,RAP)和PCV(1型MNV+息肉狀病灶)1)。
日本的特點:約半數新生血管型AMD為厚脈絡膜新生血管病變(PNV),僅約30%可見玻璃膜疣1)。

年齡相關性黃斑部病變(AMD)是由於黃斑部的年齡相關性變化導致萎縮性或滲出性變化的疾病。除遺傳易感性外,還涉及年齡、吸菸、日光暴露、肥胖、高脂飲食等環境因素,被認為是一種多因素疾病。
定義為50歲以上人群在中心凹為中心、直徑6000μm範圍內出現的基於年齡的黃斑異常,大致分為前驅病變、新生血管型和萎縮型。是視覺障礙的第四大原因。
久山町研究(2012年)顯示,晚期AMD的盛行率為1.6%(滲出型1.5%,萎縮型0.1%),長濱研究(2008年至今)報告前驅病變的盛行率為22.8%(玻璃膜疣39.4%)。該病見於50歲及以上男女(男:女=3:1),單眼或雙眼(約40%)發病。前驅病變和晚期AMD均呈增加趨勢。久山町研究(9年追蹤)報告,吸菸使晚期AMD的發生率增加4倍1)。
存在種族差異,白種人和亞洲人盛行率較高,西班牙裔和非洲裔較低2)。萎縮型AMD的盛行率在西方研究中為0.66%1.34%,85歲以上人群中其頻率是滲出型的4倍。隨著日本人口老化,這很可能成為一個重大問題。全球約有2億AMD患者,預計到2040年將增至約2.88億2)。晚期AMD的盛行率隨年齡呈指數增長,5059歲為0.1%,80歲以上為4.3%2)。
最新的日本診療指引(2024年)參考Beckman分類,將AMD分為以下四期1)。
| 分期 | 特徵 |
|---|---|
| 早期AMD | 1個或多個中型軟性玻璃膜疣(63~<125 μm) |
| 中期AMD | 大型玻璃膜疣(≥125 μm)、RPE異常、視網膜下玻璃膜疣樣沉積物 |
| 晚期AMD | 黃斑新生血管(MNV)(包括PNV)或地圖狀萎縮 |
| 末期AMD | 纖維性疤痕或囊樣黃斑變性伴嚴重視力下降 |
小型(硬性)玻璃膜疣(<63 μm)被認為是生理性老化變化,不包括在早期AMD中。但如果存在大量(20個以上)硬性玻璃膜疣,則AMD的發生風險較高1)。中期AMD的5年進展率約為18%,但存在網狀假性玻璃膜疣時風險顯著升高(色素異常+大型玻璃膜疣+網狀假性玻璃膜疣時5年風險為72%)2)。
新生血管型AMD
黃斑新生血管(MNV):源自脈絡膜或視網膜血管的新生血管出現在黃斑,導致視力急劇下降。
分型:分為1型MNV(RPE下)、2型MNV(RPE上)、3型MNV(視網膜內血管來源,RAP)和PCV(1型MNV+息肉狀病灶)1)。
日本的特點:約半數新生血管型AMD為厚脈絡膜新生血管病變(PNV),僅約30%可見玻璃膜疣1)。
萎縮型AMD
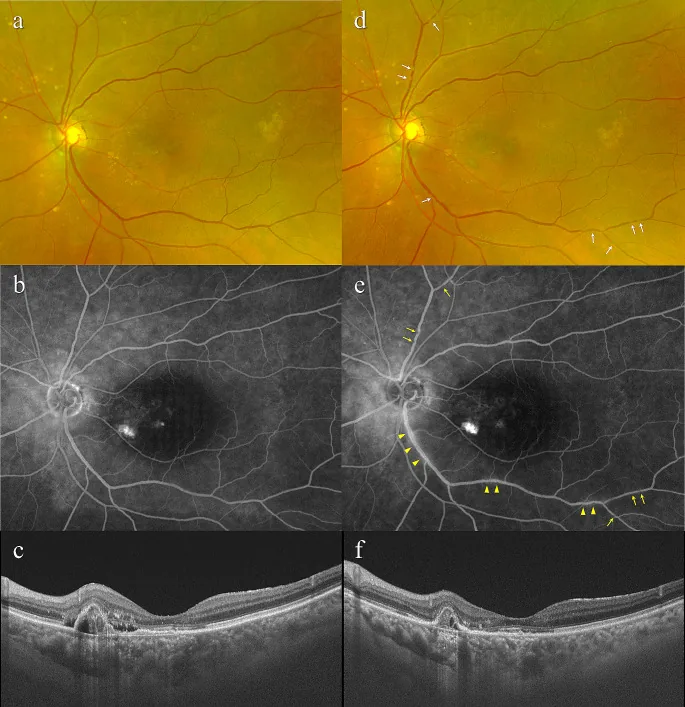
初期表現為變視(扭曲)和中心暗點。隨著病情進展,視力下降至0.1以下。大量出血病例可能出現突然的嚴重視力下降。
單眼發病時,日常生活中常無自覺症狀。症狀的嚴重程度因MNV的部位、大小以及視網膜下液、出血、纖維性疤痕的程度而異。新生血管型從發病到法定失明的時間往往比萎縮型短,出現變視時建議及時就診。
黃斑部可見的黃白色小圓形隆起病灶,是積聚在RPE基底膜和Bruch膜內膠原層之間的多形性物質(膜樣碎片、非酯化膽固醇、補體等)。被認為是AMD病理核心——慢性發炎的起源。
地圖狀萎縮是邊界清晰的RPE萎縮區,可見脈絡膜血管。病變始於中心凹周圍(近中心凹),呈馬蹄形→環形擴大,並向中心凹進展。累及中心凹的中位時間為2.5年3)。生長速度為1.28~2.6 mm²/年;在蘭尼單抗試驗數據中,GA面積在2年內從平均8.07 mm²擴大到12.05 mm²3)。多灶性GA比單灶性GA生長速度更快3)。對側眼在12個月時轉化為GA的比例約為30%,轉化為CNV的比例為6.7%。
大的玻璃膜疣樣PED消退時,萎縮也可能快速進展。眼底自發螢光上萎縮邊界處的強自發螢光模式有助於預測進展速度。
使用Amsler方格表(方格紙狀自查表)可自行檢查視物變形和暗點。但早期常無症狀,定期眼科檢查必不可少。尤其是單眼發病時,日常生活中常不易察覺。
AMD是一種多因素疾病,由遺傳易感性與環境和行為因素共同作用而發病。
新生血管型AMD的診斷標準如下 1):
萎縮型AMD(地圖狀萎縮)的診斷標準需滿足以下所有條件 1):
| 項目 | 標準 |
|---|---|
| 大小 | 直徑≥250μm |
| 形態 | 圓形、卵圓形、小葉狀或地圖狀 |
| 邊界 | 清晰 |
| RPE變化 | 低色素或脫色素變化 |
| 脈絡膜 | 中大型血管清晰可見 |
如果觀察到來自MNV的滲出性變化(IRF、SRF、RPE下液、纖維蛋白、出血等),則判斷為「活動性」1)。使用OCT進行非侵入性評估已成為主流。由於MNV疾病活動性高的部位不一定位於中心凹,建議掃描整個黃斑進行評估1)。
伴有MNV的黃斑異常需要與以下疾病進行鑑別。
早期AMD尚無基於證據的治療方法2)。對於中期AMD及以上,除戒菸指導和飲食改善外,建議根據AREDS2配方補充營養素1)。
AREDS2中使用的補充劑配方1):
β-胡蘿蔔素因增加吸菸者肺癌風險而被葉黃素/玉米黃素取代1)。AREDS2配方可將中期AMD進展為晚期AMD的風險降低約25%。
新生血管性AMD的第一線治療是玻璃體內注射抗VEGF藥物1)。對於中心凹下MNV,建議初始治療採用抗VEGF單一療法。
雷珠單抗
阿柏西普
劑量:2.0 mg 玻璃體內注射
導入期:每月1次,共3次注射
維持期:每2個月固定給藥或治療-延長方案。若無滲出復發,注射間隔每2週延長一次(最長3個月);復發時縮短2週1)。
PCV:息肉消退率40-50%,優於雷珠單抗(20-30%)。
布羅魯珠單抗 / 法瑞西單抗
布羅魯珠單抗:6mg劑量。可每8-12週給藥一次。需注意眼內炎症,包括視網膜血管炎和血管閉塞1)。
法瑞西單抗:VEGF-A + Ang-2雙特異性抗體。每8-16週給藥一次。TENAYA/LUCERNE研究顯示其非劣效於阿柏西普1)10)。
有以下三種給藥方案1)。
對於2型MNV或PCV,可對整個MNV進行雷射光凝。使用黃色或更長波長,光斑大小200-300μm,功率150-250mW,持續時間0.2-0.5秒,在MNV周圍包含100μm安全邊界進行中度或以上光凝。但雷射光凝會不可逆地損傷RPE,因此不適用於靠近中心凹的MNV1)。
PCV的治療選擇如下1)。
PDT處方:verteporfin 6mg/m²靜脈輸注10分鐘。輸注開始後15分鐘進行雷射照射(689nm,600mW/cm²,83秒)。照射大小為病灶最大直徑+1000μm。治療後2天需避免直射陽光。
長期PDT可能惡化黃斑部萎縮,對於脈絡膜較薄或已有黃斑部萎縮的病例應避免使用。不建議對第3型MNV使用PDT 1)。
抗VEGF藥物治療效果不佳(治療頑固)或效果減弱(抗藥性)時,轉換其他藥物可能有效 1)。也可根據治療負擔(就診頻率、注射頻率)考慮更換藥物。在末期AMD出現不活躍的纖維疤痕或萎縮性變化時,不積極治療,考慮觀察 1)。
視力良好的眼睛可選擇抗VEGF單一療法;如需減少治療次數,可選擇PDT-VEGF抑制劑合併療法。臨床實務中以抗VEGF單一療法為主。
大量黃斑部下出血會導致視力急遽下降。早期進行血腫移位術可能改善視力。
目前對於已確立的累及中心凹的地圖狀萎縮尚無治療方法。補體系統被認為密切相關,多種針對補體路徑的分子標靶藥物正在開發或臨床試驗階段。
對於中心凹外的地圖狀萎縮,建議服用AREDS2補充劑並改善生活習慣。如果在病程中出現MNV(10-15%),則標準治療是抗VEGF藥物。
對於視力下降進展的患者,提供遮光眼鏡、放大鏡等視覺輔助器具的建議以及日常生活支持等低視力護理非常重要1)。
導入期通常每月注射一次,共三次。維持期推薦採用treat-and-extend方法(逐漸延長間隔)。ALTAIR研究(日本受試者)證實了96週內的療效1)。使用法瑞西單抗,部分病例可維持最長16週的間隔10)。
目前尚無確立的治療方法。美國於2023年批准了兩種補體抑制劑9),但在日本尚未核准。AREDS2補充劑可降低進展為晚期AMD的風險,但尚未顯示能抑制地圖狀萎縮本身的進展。當視力下降進展時,低視力護理變得重要。
AMD的病理始於RPE細胞的損傷。玻璃膜疣積聚在RPE基底膜和布魯赫膜內膠原層之間。玻璃膜疣的成分包括膜樣碎片、非酯化膽固醇和補體,成為慢性炎症的起源。氧化壓力、脂質代謝異常和先天免疫系統的活化複雜地參與其中,破壞了RPE-布魯赫膜-脈絡膜毛細血管複合體的穩態。隨後,通路分為兩個分支。
老化的RPE細胞表現出細胞老化相關分泌表現型(SASP),SA-β-gal、p53、p21和p16的表現增加7)。這種老化RPE表現型與萎縮型AMD患者的發現一致,透過senolytics選擇性清除作為治療標靶受到關注。
CFH、C3和ARMS2的基因多型性與AMD發病易感性相關2)。補體路徑(經典路徑、替代路徑和凝集素路徑)的調節異常驅動地圖狀萎縮的擴大3)。抑制補體C3有望抑制C5下游的整個終末路徑,抑制C5有望防止膜攻擊複合物(MAC)的形成。
Anegondi等人(2025)分析lampalizumab試驗數據表明,地圖狀萎縮生長速度越快,BCVA下降越快,2年內約75%的患者視力下降≥5個字母,約50%下降≥10個字母,約25%下降≥15個字母3)。
厚脈絡膜是一種以脈絡膜大血管擴張(pachyvessel)和脈絡膜血管通透性增加為特徵的疾病1)。中心性漿液性脈絡膜視網膜病變(CSC)是厚脈絡膜疾病的代表,在CSC或厚脈絡膜色素上皮病變(PPE)背景下產生的MNV稱為厚脈絡膜新生血管病變(PNV)。CFH基因也被報導參與厚脈絡膜和CSC的發生1)。
Ribatti等人(2024)報導,脈絡膜肥大細胞分泌的類胰蛋白酶降解Bruch膜,誘導RPE死亡,VEGF-A、FGF-2、IL-8和NGF的釋放促進血管新生5)。
非滲出性MNV即使無症狀也具有生物學活性,面積持續增大4)。
Wang等人(2023)對45隻眼進行SS-OCTA研究,報告生長型MNV(面積增加≥50%)轉化為滲出性的時間顯著短於非生長型MNV(13.60個月 vs 31.11個月,HR 12.51),吸菸史和高三酸甘油酯血症與生長顯著相關(P=0.021)4)。
地圖狀萎縮通常從中心凹周圍開始,中心凹對萎縮表現出相對耐受性3)。這形成了馬蹄形或環形GA。中心凹受累的中位時間為2.5年,在此期間高對比度視力得以保留,但暗適應敏感度、閱讀速度等日常視覺功能早期即受損8)。
2023年,兩種針對地圖狀萎縮的補體抑制劑在美國獲得FDA核准。
然而,這兩種藥物在以視力改善為預設終點的試驗中均未達到統計顯著性,「結構-功能分離」仍是一個挑戰3)8)。歐洲藥品管理局(EMA)要求證明功能性益處,因此未核准佩格塞塔科普蘭8)。
補體D因子抑制劑蘭帕利珠單抗的III期CHROMA試驗(906名患者)和SPECTRI試驗(975名患者)未能顯示對GA面積的抑制,因此終止。視覺循環抑制劑艾米克斯塔特的SEATTLE試驗(580名患者)也未能顯示療效。
Dinah等人(2025)的綜述指出,BCVA不足以捕捉地圖狀萎縮的功能性影響,微視野計、低亮度視力(LLVA)和閱讀速度被推薦作為替代終點8)。建立複合、多模式的功能評估將是未來臨床試驗的關鍵。
Ji等人(2025)報告了一例接受光生物調節治療(紅色至近紅外光650–1,300 nm)的乾性AMD病例6)。8個月內,右眼玻璃膜疣面積減少58%,左眼完全消失。雙眼視力從20/30改善至20/20。Lightsite III第3期試驗也證實了玻璃膜疣體積減少和視力改善。
Chung和Kim(2022)報告,MDM2抑制劑Nutlin-3a作為一種選擇性清除衰老RPE細胞的新方法具有前景7)。粒線體特異性衰老細胞清除藥物的開發是未來的挑戰。
利用RPE細胞移植的幹細胞治療處於研究階段,多項試驗正在進行中。針對補體因子的基因治療也在探索中。
萎縮性AMD進展緩慢,但地圖狀萎縮累及中心凹時,視力降至0.1以下。據報告,達到法定失明(ETDRS <20個字母)的中位時間為6.2年3)。對蘭帕珠單抗試驗數據的分析顯示,2年內平均BCVA從66個字母降至57個字母(約相當於20/50至20/80)3)。
地圖狀萎縮生長速度越快,BCVA下降也越快;在最快生長組中,中心凹下單一病灶的眼在2年內視力下降約4行(17.75個字母)3)。相反,最慢生長組在2年內僅下降1.69個字母。即使中心凹得以保留,暗適應敏感度、對比敏感度和閱讀速度早期即受損,因此僅憑視力值會低估功能影響8)。
此外,有一定機率發生MNV並轉變為新生血管型AMD,可能導致更嚴重的視力下降。
透過抗VEGF藥物控制MNV,視力預後已大幅改善。CATT研究5年追蹤中,50%的眼睛視力達到20/40或更好11)。然而,若放任不管,約90%的眼睛視力會降至0.1或以下,並在黃斑部留下纖維性或萎縮性疤痕。在MNV導致大量出血的病例中,可能伴有廣泛的視野缺損,導致包括完全失明在內的更嚴重的視功能障礙。
MNV無法完全治癒,若未進行適當治療與長期管理,很容易導致不可逆的視力下降1)。即使MNV活動性暫時穩定,長期過程中仍可能復發,反覆滲出會導致萎縮性變化和纖維性疤痕。考慮到對側眼也高機率發生MNV,持續治療與定期監測是必不可少的1)。對於出現嚴重視功能低下的患者,建議積極進行低視力復健。
日本網膜硝子体学会 新生血管型加齢黄斑変性診療ガイドライン作成ワーキンググループ. 新生血管型加齢黄斑変性の診療ガイドライン. 日眼会誌. 2024;128(9):680-696.
Flaxel CJ, Adelman RA, Bailey ST, et al. Age-Related Macular Degeneration Preferred Practice Pattern. Ophthalmology. 2024;131(8):S1-S50.
Anegondi N, Steffen V, Sadda SR, et al. Visual loss in geographic atrophy: learnings from the lampalizumab trials. Ophthalmology. 2025;132(4):420-430.
Wang Y, Sun J, Wu J, et al. Growth of nonexudative macular neovascularization in age-related macular degeneration: an indicator of biological lesion activity. Eye (Lond). 2023;37(10):2048-2054.
Ribatti D, Dammacco R. Mast cells in human choroid and their role in age-related macular degeneration (AMD). Clin Exp Med. 2024;24(1):98.
Ji PX, Pickel L, Berger AR, Sivachandran N. Improvement in dry age-related macular degeneration with photobiomodulation. Case Rep Ophthalmol. 2025;16(1):155-162.
Chung H, Kim C. Nutlin-3a for age-related macular degeneration. Aging (Albany NY). 2022;14(14):5613-5616.
Dinah C, Esmaeelpour M, Rachitskaya AV, De Salvo G, Munk MR. Functional endpoints in patients with geographic atrophy: what to consider when designing a clinical trial. Surv Ophthalmol. 2025. doi:10.1016/j.survophthal.2025.02.004.
Heier JS, Lad EM, Holz FG, et al. Pegcetacoplan for the treatment of geographic atrophy secondary to age-related macular degeneration (OAKS and DERBY): two multicentre, randomised, double-masked, sham-controlled, phase 3 trials. Lancet. 2023;402:1434-1448.
Khanani AM, Kotecha A, Chang A, et al. TENAYA and LUCERNE: two-year results from the phase 3 neovascular age-related macular degeneration trials of faricimab. Ophthalmology. 2024;131:914-926.
Martin DF, Maguire MG, Ying GS, et al; CATT Research Group. Ranibizumab and bevacizumab for neovascular age-related macular degeneration. N Engl J Med. 2011;364:1897-1908.