活動性病變
黃白色脈絡膜視網膜病變:後極部可見小型、邊界清晰的黃灰色斑點。視乳頭周圍不受侵犯。
無眼內發炎:點狀內層脈絡膜病變的特徵是不伴有前房發炎和玻璃體炎3)。
神經感覺層視網膜剝離:活動性病變上方可能伴有漿液性視網膜剝離。

點狀內層脈絡膜病變(punctate inner choroidopathy)是1984年由Watzke等人首次報告的特發性發炎性脈絡膜疾病。它被歸類為白點症候群之一,屬於侵犯外視網膜、脈絡膜微血管層和脈絡膜的發炎性疾病群7)。根據葡萄膜炎診療指引(日眼會誌 2019;123(6):635-696),它被定位為非感染性、以眼底病變為主的後部葡萄膜炎,具有緩慢發病、單眼或雙眼性的特點8)。
主要發生於近視的年輕女性(約90%為女性)5)。大規模研究報告平均發病年齡為36歲,平均近視度數為-4.5屈光度5)。好發於中度近視眼的年輕女性,急性期在後極部可見數個小型黃白色病灶,隨時間推移變為萎縮病灶。
點狀內層脈絡膜病變與多灶性脈絡膜炎(MFC)在侵犯脈絡膜、視網膜色素上皮(RPE)和外視網膜方面有共同點,提示可能屬於同一疾病譜7)。兩者的鑑別關鍵在於有無玻璃體炎和病變分布範圍。點狀內層脈絡膜病變無玻璃體炎,病變局限於後極部;而MFC伴有玻璃體炎,病變可延伸至周邊部6)。
點狀內層脈絡膜病變無玻璃體炎,病變局限於後極部;而MFC伴有玻璃體炎和前房發炎,病變可延伸至中周邊部。兩者可能屬於同一疾病譜。
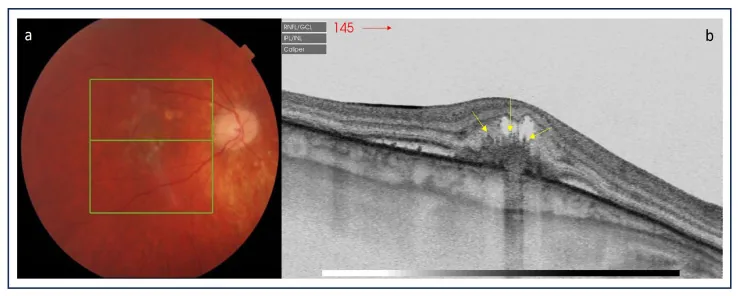
點狀內層脈絡膜病變最常見的初發症狀是單眼暗點和視力下降。
眼底所見:後極部侷限分布12至25個100–300μm大小的黃白色小斑點,呈隨機模式。病變發生在外層視網膜、RPE和內層脈絡膜層級。80%為雙眼性,但常左右不對稱1)。
點狀內層脈絡膜病變的特徵總結如下。
活動性病變
黃白色脈絡膜視網膜病變:後極部可見小型、邊界清晰的黃灰色斑點。視乳頭周圍不受侵犯。
無眼內發炎:點狀內層脈絡膜病變的特徵是不伴有前房發炎和玻璃體炎3)。
神經感覺層視網膜剝離:活動性病變上方可能伴有漿液性視網膜剝離。
瘢痕期病變
SD-OCT描述了點狀內層脈絡膜病變的五階段演變過程2)。
點狀內層脈絡膜病變的病因不明,但被認為是一種多基因易感性基礎上的自體免疫疾病,由感染、疫苗接種或壓力等環境刺激誘發。
| 因子 | 詳細 |
|---|---|
| 性別 | 女性約佔90–93% |
| 年齡 | 18–40歲(平均36歲) |
| 近視 | −3.25至−10.0 D |
已有報導COVID-19感染後點狀內層脈絡膜病變的發病和再活化。SARS-CoV-2感染可能在有遺傳易感性的個體中誘發自體免疫失調。此外,也有報導COVID-19疫苗接種後點狀內層脈絡膜病變復發3)。
Scott等人(2024)報告了一例38歲女性在接種輝瑞-BioNTech COVID-19疫苗7天後點狀內層脈絡膜病變復發,並伴有發炎性脈絡膜新生血管膜(iCNVM)。在免疫抑制狀態下接種疫苗未出現復發,但在非免疫抑制狀態下接種第四劑後復發3)。
已有報導在COVID-19疫苗接種後點狀內層脈絡膜病變復發3)。但疫苗的益處遠大於眼內炎症復發的風險。有病史者應在接種前後諮詢眼科醫師進行追蹤觀察。
點狀內層脈絡膜病變的診斷基於臨床發現。結合輔助影像學檢查進行確診。組織胞漿菌素皮膚試驗為陰性。
FA中,活動性病變在動脈早期顯示高螢光,晚期出現滲漏和染色7)。比臨床檢查發現更多病變。CNVM表現為不規則的網狀新生血管網絡。
ICG在後極部和視盤周圍顯示中期低螢光病變7)。在32%的患眼中檢測到亞臨床低螢光斑點,提高診斷能力。
SD-OCT對點狀內層脈絡膜病變的診斷和追蹤有用。活動性病變顯示RPE局部高反射隆起和橢圓體帶(EZ)中斷7)。脈絡膜新生血管(CNV)陽性病變的高度、寬度和體積大於CNV陰性病變,伴有EZ和Bruch膜中斷以及外層視網膜模糊。
深度增強成像OCT(EDI-OCT)顯示活動性病變正下方的脈絡膜厚度增加,治療後減少(「海綿徵」)。這有助於與近視性脈絡膜新生血管鑑別。
OCTA是點狀內層脈絡膜病變診斷中的重要影像學工具。它能以高檢出率識別傳統FA或SD-OCT難以發現的續發性脈絡膜新生血管。
使用OCTA檢查,可以在許多點狀內層脈絡膜病變患者中證明脈絡膜新生血管的存在,包括FA未能得出結論的病例。
Leclaire等人(2021)報告了在FAG和SD-OCT中未檢測到、僅在OCT-A中發現的續發性脈絡膜新生血管病例,提示臨床上無症狀的續發性脈絡膜新生血管可能有很多未被發現5)。
Stattin等人(2021)報告使用SS-OCTA監測點狀內層脈絡膜病變續發脈絡膜新生血管的血管密度變化,並將其作為抗VEGF治療決策的指導依據4)。
活動性點狀內層脈絡膜病變表現為低自發螢光1)。圍繞活動性病變的高自發螢光暈環可能是發炎未受控制的間接徵象。萎縮性疤痕病變也表現為低自發螢光斑1)。
眼底自發螢光是一種非侵入性、快速的檢查方法,有助於評估病變分佈、監測治療效果和檢測復發1)。
約41%的患者出現生理盲點擴大,也可見中心暗點和旁中心暗點。45%的患者視野正常。
需要鑑別的疾病如下:
如果沒有脈絡膜新生血管的證據,視力預後良好,大多數病例無需治療。唯一的例外是當存在非常接近固視點的活动性炎症病變時,可考慮藥物治療。
對於中心凹附近的活动性病變,可採用曲安奈德後Tenon囊下注射或口服類固醇(潑尼松龍40-60mg/天逐漸減量)8)。如果中心凹外的脈絡膜新生血管對類固醇無反應,可嘗試光凝治療。
合併脈絡膜新生血管的病例需要積極治療。
這是治療合併脈絡膜新生血管的點狀內層脈絡膜病變的主要方法。使用貝伐珠單抗、雷珠單抗和阿柏西普。
Stattin等人(2021)在SS-OCTA監測下,對點狀內層脈絡膜病變續發的脈絡膜新生血管按需給予雷珠單抗(0.5mg),共注射6次,最終視力達到20/204)。
抗VEGF藥物與類固醇的雙向方法被認為是有效的4)。對於合併CNV的病例,玻璃體內注射貝伐珠單抗有時被用作一線治療8)。
全身性類固醇通常以1mg/kg/天(60-80mg/天)開始,持續3-5天,然後逐漸減量4)。有報告稱口服類固醇可將iCNVM發生風險降低一半3)。
玻璃體內類固醇製劑包括以下:
在合併脈絡膜新生血管的病例中,PDT的有效性已有報導。與口服潑尼松龍(1mg/kg/天)聯合使用時,平均2次PDT後視力改善15個字母。
因病例而異。在SS-OCTA指導下的按需給藥中,有報告稱進行了6次注射4)。需要定期進行影像檢查評估脈絡膜新生血管的活動性,復發時可能需要追加給藥。
點狀內層脈絡膜病變的病理生理學尚未完全闡明。主流假說認為它是一種起源於內層脈絡膜的炎症性疾病。
對點狀內層脈絡膜病變繼發CNVM的病理研究表明,脈絡膜毛細血管層得以保留,而內層脈絡膜水平存在淋巴細胞浸潤。這一發現從超微結構上支持了點狀內層脈絡膜病變是一種起源於脈絡膜的炎症性疾病的假說。
在ICG檢查中,低螢光區域對應局灶性脈絡膜低灌注,血管壁上的局灶性高螢光點可能提示血管炎。由於大的脈絡膜血管穿過這些低螢光區域,因此認為血管炎過程局限於小血管和脈絡膜毛細血管層。
點狀內層脈絡膜病變相關的脈絡膜新生血管為2型(視網膜色素上皮下),通過破壞Bruch膜和視網膜色素上皮而發生。周細胞稀少的新生血管單元對抗VEGF藥物高度敏感,表明周細胞可能是一個重要的治療靶點。
在OCT-A上,活動性炎症性脈絡膜視網膜病變在脈絡膜毛細血管層水平顯示血流信號不可檢測7)。脈絡膜毛細血管層的原發性受累是否先於外層視網膜改變,還是相反,仍存在爭議7)。
白點症候群患者及其家屬中全身性自體免疫疾病的患病率較高6)。據報導,點狀內層脈絡膜病變患者攜帶IL-10單倍型和HLA-DRB1*15等位基因,提示遺傳易感性與環境因素共同作用導致發病6)。
Jampol和Becker(2003)提出將MEWDS、MCP、PIC和AZOOR整合為一個單一的臨床概念,稱為「AZOOR複合體」。該假說認為遺傳易感性與多種環境觸發因素相結合,導致不同的臨床表型6)。
Liu等人(2024)報告了一例孤立性點狀脈絡膜視網膜炎(SPC)的91個月追蹤病例,SPC是點狀內層脈絡膜病變的一個亞型,表現為單一病灶出現在黃斑中心凹附近,其脈絡膜新生血管的繼發發生率低於點狀內層脈絡膜病變(16% vs 約50%)。在91個月的病程中,病灶保持孤立性,OCTA上的血管樣結構自然消退。最終視力恢復到0.8,無需抗VEGF治療2)。
Stattin等人(2021)通過SS-OCTA的en face影像顯示,可以隨時間追蹤脈絡膜新生血管的血管結構變化(分支、環、吻合),並且即使SD-OCT沒有間接活動性表現,SS-OCTA也能捕捉到新生血管的變化4)。基於OCTA結果的脈絡膜新生血管活動性評估和治療決策,可能成為未來點狀內層脈絡膜病變管理的標準方法。
Scott等人(2024)的報告顯示,在免疫抑制狀態下接種COVID-19疫苗時,未觀察到點狀內層脈絡膜病變的復發3)。對於高風險患者,疫苗接種時預防性免疫抑制的作用是未來需要探討的課題。
Walters等人(2021)報告了一例罕見病例,一名長期患有點狀內層脈絡膜病變的患者急性發作多發性消失性白點症候群。點狀內層脈絡膜病變與多發性消失性白點症候群的共存支持了AZOOR複合體的概念,並提示存在共同的遺傳基礎6)。