1기

망막혈관종성증식(RAP)
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 망막 혈관종성 증식(RAP)이란?
섹션 제목: “1. 망막 혈관종성 증식(RAP)이란?”망막 혈관종성 증식(RAP)은 연령 관련 황반변성(AMD)의 특수한 아형이다. 맥락막 혈관에서 유래한 신생혈관을 가진 다른 AMD와 달리, 망막 내 심부 모세혈관총(deep retinal capillary plexus)에서 신생혈관이 발생하고, 진행되면 맥락막 신생혈관과 문합한다.
2001년 Yannuzzi 등이 독립적인 질환 개념으로 제안하였고, 처음에는 1~3기의 3단계로 분류하였다 3). 이후 2010년 Yannuzzi 자신이 4기를 추가하여 4단계 병기 분류를 보고하였다. 한편, Freund 등은 ‘3형 신생혈관’이라는 통일된 명명을 제안하고 병기 분류는 불필요하다는 입장을 취하였다 4).
일본의 신생혈관성 AMD 진료 가이드라인(2024년)에서는 황반부의 신생혈관을 ‘황반 신생혈관(MNV)‘으로 총칭하고, RAP를 ‘3형 MNV’로 공식 분류하고 있다 1). 기존의 ‘맥락막 신생혈관(CNV)‘이라는 용어는 망막 혈관 유래 신생혈관을 포함하지 않으므로, 현재는 MNV로의 전환이 진행되고 있다.
용어의 변천
섹션 제목: “용어의 변천”전통적으로 황반부의 신생혈관은 ‘맥락막 신생혈관(CNV)‘이라고 불렸으나, 망막 혈관 유래 신생혈관도 포함되므로 2020년 이후 국제적으로 ‘황반 신생혈관(MNV)‘이라는 용어가 사용되고 있다 1). RAP에 해당하는 3형 MNV는 망막 혈관에서 발생한 신생혈관이며, 맥락막 유래의 1형 MNV 및 2형 MNV와 발생 기원이 명확히 다르다.
서구의 신생혈관성 AMD 환자에서 RAP는 15~20%를 차지한다. 일본에서는 아시아인에서 빈도가 낮아 약 5%로 보고된다. 고령 여성에 호발하는 점이 특징적이며, 발병 연령은 70세 이상이 많다.
양안 발병률이 매우 높으며, 한쪽 눈이 발병하면 반대쪽 눈의 발병 위험이 현저히 증가합니다. 따라서 반대안의 경과 관찰이 임상적으로 매우 중요합니다. 다른 AMD 아형에 비해 진행이 빠르고, 치료에 반응하더라도 재발률이 높습니다. 장기 경과에서는 위축 병변이 생기기 쉬우며, AMD 중에서도 시력 예후가 나쁜 병형으로 인식되고 있습니다.
2. 주요 증상과 임상 소견
섹션 제목: “2. 주요 증상과 임상 소견”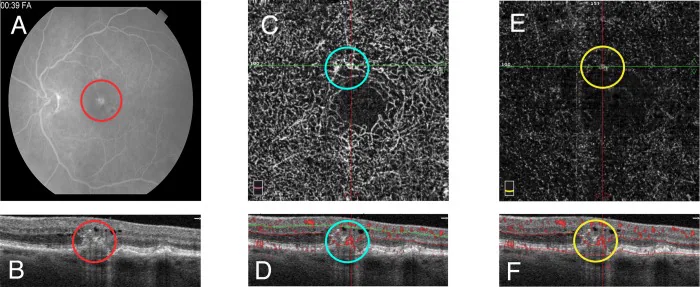
자각 증상
섹션 제목: “자각 증상”초기부터 중기까지 다음과 같은 자각 증상이 나타납니다.
- 변시증(물체가 왜곡되어 보임): 황반부 망막 부종이나 삼출에 동반되어 발생합니다. 초기 주된 호소로 많습니다.
- 중심 암점: 병변이 황반 중심와에 미치면 중심 시야의 결손을 자각합니다.
- 시력 저하: 낭포황반부종이나 신생혈관의 활동성이 높은 시기에 급속히 진행됩니다.
증상의 진행은 비교적 빠르며, 다른 AMD 아형에 비해 조기에 심한 시력 저하를 일으키기 쉽습니다. 낭포황반부종이 현저한 경우 급격한 시력 저하를 나타낼 수도 있어, 조기 내원과 진단이 시각 기능 유지에 중요합니다.
임상 소견(의사가 진찰로 확인하는 소견)
섹션 제목: “임상 소견(의사가 진찰로 확인하는 소견)”후극부에 다발하는 연성 드루젠의 집락과 망상 가성 드루젠(RPD)이 기반 소견으로 특징적입니다. RPD는 망막색소상피(RPE) 위에 위치하는 망상 내지 점상 침착물로, RAP의 전구 병변으로 중요시됩니다1).
활동기에는 다음과 같은 소견이 인정됩니다.
- 망막 표층 출혈 및 망막 내 출혈: 후극부에 소량에서 중등도의 출혈을 동반합니다. 특히 1기에서는 결절성 적점으로 관찰되는 신생혈관 주위에 소량의 표층 출혈이 보입니다.
- 낭포황반부종: RAP의 특징적인 소견으로, 다른 AMD 아형에 비해 중증도가 높고 조기에 나타나는 경향이 있습니다.
- 망막하 삼출액 및 장액성 망막박리: 2기 이후에 나타납니다.
- 색소상피박리(PED): 진행된 경우(3기 이후)에 합병됩니다. 섬유혈관성 PED 또는 드루젠양 PED의 형태를 취합니다.
RAP 병기 분류(Yannuzzi 4단계 분류)에 따른 임상 소견은 다음과 같습니다3).
2기
3기
4기
망막-맥락막 혈관 문합(RCA): 망막 신생혈관과 맥락막 신생혈관이 문합되는 최종 단계입니다.
IA 소견: RCA 및 RRA 검출에 IA가 유용하며, 과형광은 핫스팟으로 나타납니다.
반흔화: 원판형 반흔이 형성되면 중심 시력의 비가역적 저하가 발생합니다.
영상 검사 소견
섹션 제목: “영상 검사 소견”3형 MNV는 검안경이나 안저 사진으로 관찰이 어려우므로 영상 검사를 통한 확인이 필수적입니다1). 주요 검사법과 소견을 아래에 요약합니다.
| 검사 | 특징적 소견 |
|---|---|
| FA | 핫스팟(결절상 과형광), 후기에 형광 누출이 현저함 |
| IA (ICGA) | hot spot, RRA/RCA 시각화 |
| OCT | bump sign, IRF, SRF, PED, 낭포황반부종 |
| OCTA | 망막 내 및 망막하 신생혈관의 비침습적 시각화 |
OCT는 RAP의 병기 평가와 치료 효과 판정의 주축입니다. bump sign은 RPE 바로 위의 소돌기 병변으로, 3형 MNV에 비교적 특이적인 소견으로 간주됩니다. OCT에서는 발병 초기부터 낭포황반부종이 나타나며, 병기가 진행됨에 따라 PED가 동반됩니다1).
OCTA의 B-스캔 영상에서는 망막 표층 혈관과 문합된 망막 내 신생혈관이 망막하로 또는 RPE를 관통하여 RPE 아래로 확장되는 모습을 포착할 수 있습니다1). RAP는 망막 내에 신생혈관이 발생하기 때문에 AMD 중에서도 특히 OCTA에서 이상 혈관이 잘 묘사됩니다. 고령자에서 반복적인 조영 검사가 어려운 경우 OCTA를 통한 비침습적 병변 평가가 유용합니다10).
질환 활동성 판단 지표로 IRF(망막 내액)와 SRF(망막하액)를 사용합니다. 3형 MNV의 병소가 반드시 중심와에 발생하는 것은 아니므로, 황반 전체 또는 병변 전체를 스캔하여 액체를 정확히 평가하는 것이 권장됩니다1).
3. 원인과 위험 요인
섹션 제목: “3. 원인과 위험 요인”RAP의 주요 위험 요인은 다음과 같습니다.
- 노화: 가장 큰 위험 인자입니다. 나이가 많을수록 발병 위험이 높습니다.
- 성별: 여성에 호발합니다.
- 후극부 연성 드루젠: 황반부에 대형 연성 드루젠(장경 125μm 이상)이 다발하는 눈은 AMD 진행의 중요한 전구 소견이다1).
- 망상 가성 드루젠(RPD): RAP 발병과 가장 밀접하게 관련된 전구 병변으로 인식된다. RPD는 일반적인 드루젠(RPE 아래에 존재)과 달리 RPE 위에 위치하는 망상~점상 침착물로, 3형 MNV 및 위축형 AMD로의 진행 위험 인자로 널리 알려져 있다1).
- 유전적 소인: ARMS2 유전자 다형성 및 CFH(보체 H 인자) 유전자 다형성이 AMD 전체의 감수성에 관여한다11). 대규모 게놈 전체 연관 분석에서 이들 유전자 좌위가 AMD 발병 위험의 주요 결정 인자임이 확인되었다.
- 흡연: AMD 전체의 위험 인자이며, 수정 가능한 위험 인자 중 가장 중요하다. 일본인을 대상으로 한 Funagata 연구, Hisayama 연구, Nagahama 연구 모두에서 흡연과 AMD의 연관성이 보고되었으며, Hisayama 연구에서는 흡연 습관으로 인해 후기 AMD 발병이 4배 증가한다고 알려져 있다12).
양안 발병률이 높은 것도 중요한 특징이며, 한쪽 눈의 발병이 확인되면 반대쪽 눈의 정기적인 경과 관찰이 필수적이다. 반대쪽 눈에도 연성 드루젠이나 RPD가 보이는 경우 발병 위험이 더욱 높아지므로 짧은 간격으로 정밀 검사가 필요하다.
성비에 관해서는 신생혈관형 AMD 전체에서는 남성이 많지만(남:여 = 3:1), RAP는 여성에서 더 많이 발병하는 특징이 있다. 발병 연령은 AMD 전체와 동일하거나 약간 높으며, 70세 이상이 대부분을 차지한다.
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”확진의 핵심 포인트
섹션 제목: “확진의 핵심 포인트”3형 MNV는 검안경이나 안저 사진으로 관찰하기 어렵기 때문에 확진을 위해서는 여러 영상 검사를 조합한 체계적인 평가가 필수적이다1).
진단 절차는 다음과 같다.
- 임상적 의심: 양안에 연성 드루젠이 다발하는 고령 환자에서 후극부에 망막내 출혈이 보일 때 3형 MNV를 의심한다.
- OCT 검사: 발병 초기부터 낭포황반부종이 나타나고, bump sign(RPE 파열양 덩어리 반사)이 보이면 강력히 시사된다. PED의 합병은 진행을 나타낸다.
- OCTA 검사: B-스캔 영상에서 망막 표층 혈관에서 bump sign으로 향하는 연속적인 혈류 신호를 확인한다. 비침습적이며 조영검사가 어려운 고령자에게 특히 유용하다.
- FA/ICGA 검사: FA에서는 결절상 과형광(핫스팟)과 후기의 왕성한 형광 누출을 보인다. ICGA에서는 hot spot으로 RRA/RCA가 묘사되어 병기 확정에 기여한다.
활동성 평가는 OCT가 주축이 되며, IRF, SRF, sub-RPE fluid의 유무를 비침습적으로 판정한다1). 장액성 PED와 출혈성 PED의 감별은 OCT 내용물 밝기로 하며, 중간 밝기면 드루젠, 낮은 밝기면 장액성으로 판단한다.
감별 진단
섹션 제목: “감별 진단”황반부 모세혈관확장증 2형(MacTel type 2)과의 감별
섹션 제목: “황반부 모세혈관확장증 2형(MacTel type 2)과의 감별”MacTel 2형은 RAP와 마찬가지로 황반부에 병변을 일으키고 망막하 신생혈관을 합병할 수 있으므로 감별이 중요하다5).
| 감별점 | RAP(3형 MNV) | MacTel type 2 |
|---|---|---|
| 발병 연령 | 고령(70세 이상 많음) | 중장년(50~60대) |
| 배경 소견 | 연성 드루젠 및 RPD 다발 | 중심와 이측 망막 투명도 저하 |
| OCT | 범프 사인(bump sign), PED, 낭포성 부종 | 타원체대 결손, 망막 공동(비후 없음) |
| 진행 속도 | 빠름(삼출/출혈 위주) | 느림(망막 위축 위주) |
MacTel 2형에서는 직각 소정맥(right-angled venule, 망막 심층 방향으로 직각으로 꺾여 끌려 들어가는 소정맥)과 크리스탈린 유사 침착물이 특징적인 소견이다. 무적색광 이미지(특히 공초점 청색광 반사)에서는 황반부에 고리 모양 또는 가로 타원형의 고반사 소견을 보이며, 질병 초기부터 나타나므로 진단에 유용하다5). 또한 OCT에서는 망막 비후를 동반하지 않는 망막 내 공동 소견(retinal cavity)이 특징적이며, 진행하면 외층 분층 원공이나 황반 원공을 형성할 수 있다5).
반면, RAP에서는 IA상의 핫스팟(hot spot)과 연성 드루젠의 집락을 동반하며, OCT에서는 범프 사인과 낭포성 황반 부종이 주체인 점에서 MacTel과 명확히 구별된다. MacTel은 망막 위축이 주체로 느리게 진행하는 반면, RAP은 삼출·출혈이 전면에 나와 빠르게 진행하는 경향이 있다.
폴립양 맥락막 혈관병증(PCV)과의 감별
섹션 제목: “폴립양 맥락막 혈관병증(PCV)과의 감별”PCV는 IA에서 폴립양 병소(결절상 과형광)와 이상 혈관망(branching vascular network)을 보이며, OCT에서는 내부에 저반강을 동반한 급격한 RPE 융기가 특징적이다1). 안저 사진에서는 등적색 융기 병소가 관찰된다. RAP에서는 IA상의 핫스팟이 주체이고 낭포성 황반 부종이 전면에 나타나는 점에서 감별된다. PCV에서는 맥락막 비후(두꺼운 맥락막 소견)를 동반하는 경우가 많은 반면, RAP에서는 연성 드루젠이나 RPD의 집락이 배경 소견이 된다.
전형적인 AMD(1형·2형 MNV)와의 감별
섹션 제목: “전형적인 AMD(1형·2형 MNV)와의 감별”전형적인 AMD에서는 맥락막 유래 신생혈관이 주체이다. 1형 MNV는 RPE 아래에 존재하며 OCT에서 이중층 징후(double layer sign)를 보인다. 2형 MNV는 RPE 위(망막하 공간)에 존재하며, OCT에서는 망막하 중등도 반사 덩어리로 검출된다1). RAP에서는 망막 혈관 유래 신생혈관이 망막 내에 존재하므로 낭포성 황반 부종이 조기에 나타나고 범프 사인을 동반하는 점에서 구별할 수 있다. 또한 RAP에서는 양안 발병이 많고 연성 드루젠의 다발을 동반하는 경향이 강하다.
5. 표준 치료법
섹션 제목: “5. 표준 치료법”항VEGF 약물 유리체강내 주입(일차 선택)
섹션 제목: “항VEGF 약물 유리체강내 주입(일차 선택)”신생혈관성 AMD에 대한 치료의 일차 선택은 항VEGF 약물 유리체강내 주입이다1). 3형 MNV에 대해서도 모든 항VEGF 약물에서 시력 개선 효과가 입증되었다.
현재 신생혈관성 AMD에 사용 가능한 항VEGF 약물은 다음과 같습니다1).
- 라니비주맙 (루센티스/라니비주맙 BS): MARINA 연구에서 24개월째 가짜 주사군은 14.9글자 시력 저하를 보인 반면, 라니비주맙 월간 주사군은 6.6글자 시력 개선을 보였습니다14). ANCHOR 연구에서도 PDT군에 대한 우월성이 입증되었습니다15).
- 아플리버셉트 2mg (아일리아): VIEW 1/2 연구에서 초기 3회 주사 후 8주 간격 주사가 라니비주맙 월간 주사와 비교하여 시력 유지율에서 비열등성을 보였습니다6).
- 브롤루시주맙 6mg (베오뷰): HAWK/HARRIER 연구에서 초기 3회 주사 후 8~12주 간격 주사가 아플리버셉트와 비교하여 시력 개선량에서 비열등성을 보였고, 중심망막두께 감소 효과에서는 우월성이 인정되었습니다7).
- 파리시맙 (바비스모): VEGF와 안지오포이에틴-2에 대한 이중특이항체입니다. TENAYA/LUCERNE 연구에서 초기 4회 주사 후 8~16주 간격 주사가 아플리버셉트와 비열등성을 보였습니다8).
투여 방법
섹션 제목: “투여 방법”도입기는 한 달에 한 번, 보통 연속 3회(파리시맙은 4회) 투여하여 시력 개선을 도모합니다1).
유지기의 투여 방법에는 다음과 같은 선택지가 있습니다.
- 고정 투여법: 임상시험에서 사용된 방법입니다. 일정 간격(예: 8주마다)으로 투여합니다.
- 필요시 투여법(PRN): 매월 경과를 관찰하고 질환 활성도가 보일 때만 투여합니다. 그러나 장기적으로 PRN법은 시력이 악화된다는 보고가 있습니다1, 13).
- 치료-연장(T&E) 투여법: 질환 활성도에 따라 투여 간격을 단계적으로 연장하는 방식으로, 현재 가장 권장되는 유지 요법입니다. 메타분석에서 월간 투여와 동등한 시력 개선을 유지하면서 PRN법보다 우수한 시력 결과를 얻을 수 있는 것으로 나타났습니다1).
일본인을 대상으로 한 ALTAIR 연구에서는 아플리버셉트의 T&E법(2주 간격 또는 4주 간격으로 투여 간격 조정)으로 96주 동안 시력과 망막 두께 개선이 유지되었다고 보고되었습니다9). T&E법을 언제까지 지속할지에 대해서는 일정한 견해가 없으며, 환자의 병태나 사회적 상황을 고려하여 판단합니다1).
치료 중 질환 활성도 평가
섹션 제목: “치료 중 질환 활성도 평가”치료 효과 판정에는 OCT가 주축이 됩니다. MNV 주변의 fluid(IRF, SRF, sub-RPE fluid)의 잔존이나 재출현으로 활성도가 있다고 판단합니다1). 3형 MNV의 망막내 신생혈관은 반드시 중심와에 국한되지 않으므로, 황반 전체 또는 병변 전체를 스캔하여 평가하는 것이 권장됩니다.
약제 전환
섹션 제목: “약제 전환”치료 중 효과가 부족한 경우(치료 저항성 예)나 효과가 감소한 경우(내성 획득)에는 다른 항VEGF 약물로의 전환이 효과적일 수 있습니다1). RAP는 치료 저항성을 보이기 쉬운 병형이므로, 반응이 불량할 때 조기 전환이 중요합니다. 치료 부담을 고려하여 약물 전환을 검토하는 경우도 있습니다.
광역학 치료(PDT)
섹션 제목: “광역학 치료(PDT)”3형 MNV에 대한 PDT 단독은 현재 권장되지 않습니다1). 항VEGF 약물에 저항하는 증례에서는 PDT 병용을 고려할 수 있지만, 장기적으로 PDT는 황반 위축을 악화시킬 가능성이 있습니다. 맥락막이 얇은 증례나 이미 황반 위축이 있는 증례에서는 피하는 것이 바람직합니다1).
PDT 병용 시 처방은 다음과 같습니다.
- 베르테포르핀(비스다인) : 6mg/체표면적(m²), 10분간 정맥 주입
- 레이저 조사 : 주입 시작 15분 후 조사(689nm, 600mW/cm², 83초)
- 조사 범위 : 조영 소견에 기반한 병변 최대 직경 + 1,000μm의 스팟 크기
- 항VEGF 약물 병용 시기 : PDT 전 1주 이내 또는 PDT 당일(차광 하) 투여
- 술후 관리 : 치료 후 2일간 직사광선 차광 필요
장기 관리
섹션 제목: “장기 관리”신생혈관성 AMD의 완치는 현재 불가능하며, 적절한 치료와 장기 관리를 하지 않으면 비가역적인 시력 저하가 발생합니다1). RAP는 특히 다음 점에서 장기적인 주의가 필요합니다.
- MNV의 활동성이 안정되어 있어도 장기 경과 중 재발할 수 있음
- 삼출이 반복되면 위축성 변화나 섬유성 반흔이 합병됩니다. 장기 경과에서는 망막 위축(지도상 위축)이 발생하기 쉬우며, 이것이 비가역적 시력 저하의 주된 원인이 됩니다
- 반대안에도 높은 비율로 MNV가 발생함
심각한 시기능 저하가 발생한 경우에는 확대경, 확대 독서기 등을 통한 저시력 관리 도입도 적극적으로 검토합니다. 신생혈관성 AMD의 완치는 불가능하므로, 환자의 사회적 상황이나 반대안의 상태도 고려하면서 지속 가능한 관리 계획을 환자와 공유하는 것이 바람직합니다1).
6. 병태생리학 및 상세한 발병 기전
섹션 제목: “6. 병태생리학 및 상세한 발병 기전”신생혈관 발생의 기원
섹션 제목: “신생혈관 발생의 기원”RAP의 본질은 망막 심층 모세혈관총에서 기원하는 망막 내 신생혈관입니다. 이것이 ‘3형 MNV’로 명명된 근거이며, 맥락막에서 기원하는 1형 및 2형 MNV와 발생 기전이 근본적으로 다릅니다1).
MNV 분류에서 3형 MNV의 위치는 다음과 같습니다.
- 1형 MNV: RPE 아래에 존재하는 맥락막 유래 신생혈관(occult CNV에 해당)
- 2형 MNV: RPE 위(망막하 공간)에 존재하는 맥락막 유래 신생혈관(classic CNV에 해당)
- 3형 MNV: 망막 혈관에서 발생한 신생혈관(RAP) 1)
전구 병변과 RAP 형성 과정
섹션 제목: “전구 병변과 RAP 형성 과정”연성 드루젠의 집적과 망상 가성 드루젠(RPD)이 전구 병변으로 중요합니다. RPD는 일반적인 드루젠(RPE 아래에 존재하는 침착물)과 달리 RPE 위쪽에 위치한 삼각뿔 모양의 침착물입니다. OCT에서는 RPE층에서 망막 내로 돌출되는 형태로 나타나며, 타원체대를 넘어 외경계막까지 도달하는 경우도 있습니다. RPD는 위축형 AMD 및 3형 MNV(RAP)와 밀접하게 관련되어 있으며, RAP 발병 예측 인자로서 임상적으로 중요하게 간주됩니다1).
RPD 및 연성 드루젠 축적을 배경으로 RPE와 광수용체의 기능 장애가 진행됩니다. 만성 저산소 환경에서 VEGF를 비롯한 혈관신생 촉진 인자가 생성 및 축적되어, 심부 모세혈관총에서 신생혈관의 발아가 유도됩니다. 신생혈관은 다음 과정을 통해 단계적으로 진행됩니다.
- 1단계: 심부 모세혈관총 내 신생혈관 형성 (망막 내 신생혈관)
- 2단계: 망막하 공간으로의 확장
- 3단계: 색소상피박리 합병
- 4단계: 맥락막 신생혈관과의 문합 형성 (망막-맥락막 혈관 문합)
발병 경로에 관한 논의
섹션 제목: “발병 경로에 관한 논의”2001년 Yannuzzi 등의 원보에서는 망막 측에서 맥락막 방향으로 진행하는 모델이 제안되었습니다3). 그러나 최근 OCT의 발전에 따라 맥락막 측에서 신생혈관이 발생하여 망막 혈관과 문합하는 형태도 보고되었습니다. Freund 등은 망막-맥락막 혈관 문합을 일으키는 신생혈관을 ‘3형 신생혈관’이라고 부르며, 병기 분류는 불필요하다는 입장을 취하고 있습니다4).
현재는 다음과 같은 세 가지 경로가 가정되고 있습니다.
- 망막 혈관 → 망막 외층 → RPE → 맥락막 (고전적 경로)
- 맥락막 신생혈관 → RPE → 망막 (역행 경로)
- 양방향 진행
어느 경로에서든 RPE와 광수용체의 손상이 VEGF 생성 증가의 출발점입니다. 망막-맥락막 문합이 완성되면 치료 저항성이 더욱 증가하고 섬유성 반흔으로의 진행이 가속화되므로, 가능한 한 조기 단계에서 신생혈관 활성을 억제하는 것이 중요합니다.
7. 최신 연구와 향후 전망 (연구 단계의 보고)
섹션 제목: “7. 최신 연구와 향후 전망 (연구 단계의 보고)”파리시맙의 장기 성적
섹션 제목: “파리시맙의 장기 성적”TENAYA 및 LUCERNE 시험의 2년 성적(Khanani 외, 2024년 보고)에서 파리시맙(항VEGF/항Ang-2 이중특이항체)은 아플리베르셉트 2mg과 비교하여 시력 및 해부학적 결과에서 비열등성을 유지했으며, 환자의 약 절반이 최대 16주 간격의 유지 투여를 달성했습니다8). Ang-2 억제를 통한 혈관 안정화와 삼출 억제의 상승 효과가 기대됩니다.
아플리베르셉트 8mg 고용량 제제
섹션 제목: “아플리베르셉트 8mg 고용량 제제”아플리베르셉트 8mg(고용량 제제)는 기존 2mg 제제보다 고농도이며, PULSAR 시험에서 최대 16~20주 간격의 유지 투여가 검토되고 있습니다2). RAP와 같이 여러 번의 주사가 필요한 병형에서는 투여 간격 연장을 통한 치료 부담 감소에 대한 기대가 큽니다.
OCTA를 이용한 추적 관찰의 진보
섹션 제목: “OCTA를 이용한 추적 관찰의 진보”OCTA는 비침습적으로 망막 내 신생혈관의 활동성을 평가할 수 있는 방법으로 급속히 임상 도입이 진행되고 있습니다10). RAP는 망막 내에 신생혈관이 존재하므로 OCTA로 시각화하기 적합하며, 고령자에서 반복적인 조영 검사가 어려운 경우 대체 수단으로 기대됩니다. 향후 OCTA의 정량적 분석을 통한 치료 결정 알고리즘 개발이 과제입니다.
유전자 개별화 치료와 예방 전략
섹션 제목: “유전자 개별화 치료와 예방 전략”ARMS2 및 CFH 유전자 다형성에 기반한 발병 위험 계층화와 개별화 치료 전략에 대한 연구가 진행되고 있습니다11). 유전자 프로파일에 따른 치료 선택 및 예방 중재의 실현이 향후 과제로 여겨집니다. 중기 AMD 단계에서 유전적 위험이 높은 환자를 식별하고 조기에 치료 개입함으로써 시력 예후를 개선할 가능성이 모색되고 있습니다.
황반하 혈종에 대한 외과적 중재
섹션 제목: “황반하 혈종에 대한 외과적 중재”RAP를 포함한 신생혈관성 AMD에서는 대량의 황반하 출혈로 인해 급격한 시력 저하가 발생할 수 있습니다. 발병 초기에는 유리체내 가스 주입술(SF6 또는 C3F8 0.3~0.5mL 주입 후 엎드린 자세 유지) 또는 유리체 절제술을 통한 혈종 이동술이 시력 개선에 효과적인 경우가 있습니다. 조직 플라스미노겐 활성화 인자(tPA) 병용도 시도되고 있지만, 적응증에 대해서는 추가 검토가 필요합니다1).
8. 참고문헌
섹션 제목: “8. 참고문헌”- 日本網膜硝子体学会新生血管型加齢黄斑変性診療ガイドライン作成ワーキンググループ. 新生血管型加齢黄斑変性の診療ガイドライン. 日眼会誌. 2024;128(9):680-695.
- Flaxel CJ, Adelman RA, Bailey ST, et al. Age-Related Macular Degeneration Preferred Practice Pattern. Ophthalmology. 2024;131(1):P1-P49.
- Yannuzzi LA, Negrão S, Iida T, et al. Retinal angiomatous proliferation in age-related macular degeneration. Retina. 2001;21(5):416-434.
- Freund KB, Ho IV, Barbazetto IA, et al. Type 3 neovascularization: the expanded spectrum of retinal angiomatous proliferation. Retina. 2008;28(2):201-211.
- 飯田知弘ほか(黄斑部毛細血管拡張症2型診療ガイドライン作成ワーキンググループ). 黄斑部毛細血管拡張症2型診療ガイドライン(第1版). 日眼会誌. 2022;126(4):463-470.
- Heier JS, Brown DM, Chong V, et al. Intravitreal aflibercept (VEGF trap-eye) in wet age-related macular degeneration: VIEW 1 and VIEW 2 study results. Ophthalmology. 2012;119(12):2537-2548.
- Dugel PU, Koh A, Ogura Y, et al. HAWK and HARRIER: phase 3, multicenter, randomized, double-masked trials of brolucizumab for neovascular age-related macular degeneration. Ophthalmology. 2020;127(1):72-84.
- Khanani AM, Kotecha A, Chang A, et al. TENAYA and LUCERNE: 2-year results of faricimab for neovascular age-related macular degeneration. Ophthalmology. 2024;131(7):914-926.
- Ohji M, Takahashi K, Okada AA, et al. Efficacy and safety of intravitreal aflibercept treat-and-extend regimens in exudative age-related macular degeneration: 52- and 96-week findings from ALTAIR. Adv Ther. 2020;37(3):1173-1187.
- Spaide RF, Fujimoto JG, Waheed NK, et al. Optical coherence tomography angiography. Prog Retin Eye Res. 2018;64:1-55.
- Fritsche LG, Igl W, Bailey JN, et al. A large genome-wide association study of age-related macular degeneration highlights contributions of rare and common variants. Nat Genet. 2016;48(2):134-143.
- Klein R, Klein BE, Knudtson MD, et al. Fifteen-year cumulative incidence of age-related macular degeneration: the Beaver Dam Eye Study. Ophthalmology. 2007;114(2):253-262.
- Martin DF, Maguire MG, Fine SL, et al. Ranibizumab and bevacizumab for treatment of neovascular age-related macular degeneration: two-year results. Ophthalmology. 2012;119(7):1388-1398.
- Rosenfeld PJ, Brown DM, Heier JS, et al. Ranibizumab for neovascular age-related macular degeneration. N Engl J Med. 2006;355:1419-1431.
- Brown DM, Kaiser PK, Michels M, et al. Ranibizumab versus verteporfin for neovascular age-related macular degeneration. N Engl J Med. 2006;355:1432-1444.
