활동기

근시성 맥락막 신생혈관
1. 근시성 맥락막 신생혈관이란?
섹션 제목: “1. 근시성 맥락막 신생혈관이란?”근시성 맥락막 신생혈관(myopic choroidal neovascularization; 근시성 CNV)은 병적 근시안의 후극부에 발생하는 맥락막 유래 신생혈관입니다. 최근에는 맥락막 유래뿐만 아니라 망막 혈관 유래 신생혈관도 포함하는 개념으로 국제적으로 ‘근시성 MNV(myopic neovascularization)‘라는 명칭이 사용되고 있습니다. 6)
연령 관련 황반변성 다음으로 맥락막 신생혈관의 두 번째로 흔한 원인이며, 50세 이하의 맥락막 신생혈관에서는 가장 큰 원인 질환입니다. 병적 근시 환자 전체의 약 10%에서 발생합니다. 7)
고도 근시는 등가 구면 도수 -6.0 D 이하 또는 안축장 26.5 mm 이상으로 정의됩니다. 병적 근시는 안저에 미만성 위축 이상의 위축성 변화가 있거나 후부 포도종이 있는 눈으로 정의됩니다(META-PM 분류, 2015년). 10)
근시성 MNV는 Gass 분류의 type 2 CNV(CNV가 RPE 위에 존재)인 경우가 대부분입니다. 비교적 소형이고 삼출성 변화도 경미한 경우가 많습니다.
- 근시성 MNV는 고도 근시안의 5~11%에서 발생합니다
- 8년 추적 관찰에서 MNV 병력이 없는 병적 근시 환자의 약 6%가 발병합니다
- 한쪽 눈에 MNV 병력이 있는 환자의 약 35%에서 반대쪽 눈에도 발생합니다.
- 50세 미만 환자에서 MNV의 약 60%는 근시성 MNV입니다7).
- 병적 근시는 교정시력 0.1 이하의 시각 장애의 13%를 차지하며, 녹내장 다음으로 두 번째로 흔한 실명 원인입니다.
2. 주요 증상 및 임상 소견
섹션 제목: “2. 주요 증상 및 임상 소견”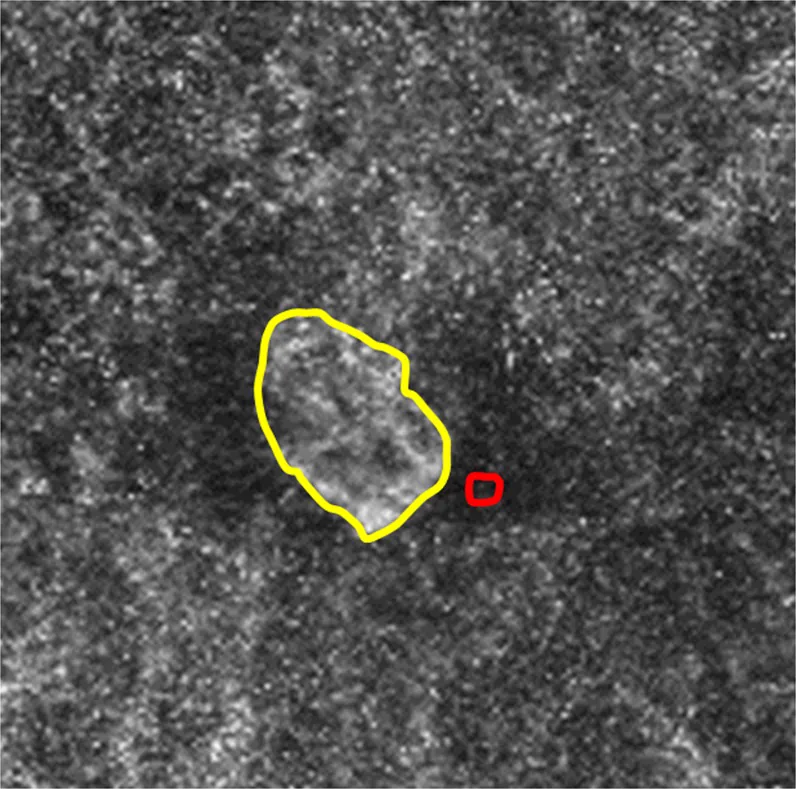
자각 증상
섹션 제목: “자각 증상”근시성 MNV가 중심와에 영향을 미칠 경우 다음과 같은 증상이 나타납니다. 제2형 CNV이므로 삼출이 망막 외층에 직접 작용하여 증상이 일찍 나타나고 빠르게 진행됩니다. 6)
- 변시증: 직선이 왜곡되어 보입니다. 근시 환자에서 새로운 변시증의 출현은 근시성 MNV를 의심하는 중요한 징후입니다. 근시성 견인 황반병증을 동반한 경우 왜곡 악화를 알아차리기 어려울 수 있습니다. 6)
- 중심 암점: 시야 중심에 어두운 점이 나타납니다.
- 시력 저하: 병변이 중심와로 확장되면 빠르게 진행됩니다. CNV가 퇴축되어도 반흔이 중심와에 남아 있으면 비가역적인 시력 저하가 됩니다.
황반 영역 외부에 위치하는 경우 무증상일 수도 있습니다. 환자의 자각 증상 호소에 주의 깊게 대응하는 것이 중요합니다. 6)
임상 소견
섹션 제목: “임상 소견”근시성 MNV는 활동기, 반흔기, 위축기의 3단계로 분류됩니다.
반흔기 및 위축기
OCT 혈관조영술에서 활동기는 “레이스 모양의 네트워크, 넓은 문합, 병변 주변의 저강도 후광”을 보이고, 정지기는 “긴 선형 성숙 혈관, 드문 문합(고목 모양 외관)“을 보입니다. 활동기 외에도 내부 혈류는 높은 빈도로 유지됩니다(활동기 100%, 반흔기 약 80%, 위축기 약 90%). 그러나 OCTA는 MNV의 활동성 평가에는 적합하지 않습니다. 6)
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”근시성 MNV의 발생에는 Bruch막의 기계적 파열과 맥락막 순환 장애의 두 가지 기전이 관여하는 것으로 생각됩니다.
발병 기전
섹션 제목: “발병 기전”안축의 진행성 연장으로 인해 맥락망막의 신전 및 얇아짐이 발생합니다.
- Bruch막 파열(래커 균열): 기계적 파열 부위가 MNV를 동반한 결합 조직의 발판이 됩니다.
- 맥락막 순환 장애: 맥락막 모세혈관판의 폐쇄 및 소실로 인해 VEGF 생성이 촉진됩니다.
- 패치 위축과 래커 균열은 MNV 발생의 예측 인자입니다7).
위험 인자
섹션 제목: “위험 인자”- 국소 맥락망막 위축: 특히 중심와 주변 1유두 직경 범위의 위축.
- 래커 균열: Bruch막의 선형 균열. CNV 발생 오즈비 2.56.
- 돔형 황반(DSM): CNV 발생 오즈비가 4.95로 높음5).
- 후부 포도종: 고도 근시 자체가 위험 인자입니다.
- 긴 안축장: 근시성 황반병증 진행의 위험 인자.
- 여성: 근시성 맥락망막 위축 병변의 유병률 오즈비가 3.29배 높음.
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”근시성 MNV의 진단에는 병적 근시에 동반된 안저 변화와 MNV의 존재 확인이 필요합니다. 6) 단순형 황반부 출혈과의 감별이 가장 중요하며, MNV의 존재가 확인되지 않은 증례에 대한 항VEGF 약물 요법은 권장되지 않습니다. 6)
형광안저혈관조영술(FA)
섹션 제목: “형광안저혈관조영술(FA)”가이드라인에서 가장 중시되는 검사입니다. 6)
- 근시성 MNV는 FA 조기부터 명확한 과형광을 보이며, 활동성 MNV에서는 중기부터 후기까지 형광 누출을 보입니다.
- 검안경 소견이나 OCT에서 명확하지 않은 병변도 검출 가능합니다.
- 단순형 황반부 출혈에서는 형광 차단(저형광)으로만 관찰되며 과형광을 동반하지 않습니다 → 감별에 결정적입니다.
- 판단이 어려운 경우 적극적으로 FA를 시행해야 합니다. 6)
광간섭단층촬영(OCT)
섹션 제목: “광간섭단층촬영(OCT)”- 활동기: RPE 위의 돔형 고반사 융기 병소. 주변에 망막하액 및 피브린 삼출. 6)
- 반흔기: RPE에 의한 포위(encapsulation)의 고반사선. 포위의 명확성은 MNV 활동성 평가에 매우 유용합니다. 6)
- 재발 시: 선이 불명확해짐(이전 OCT 이미지와의 비교가 중요). 6)
- 단순형 황반부 출혈과의 감별: OCT에서 Henle 섬유층을 따른 고반사로 관찰됩니다. 6)
- OCT만으로 감별이 어려운 경우 FA가 필수입니다. 6)
OCT 혈관조영술(OCTA)
섹션 제목: “OCT 혈관조영술(OCTA)”- 비침습적으로 혈류 유무 평가 가능 6)
- MNV 식별에 유용 (단순형 황반부 출혈과의 감별) 6)
- 민감도 90.48%, 특이도 93.75%로 보고됨 3)
- Angio-B 모드에서 구조 OCT로 검출 어려운 조기 MNV 검출 가능 3)
- 활동성 평가에는 부적합 (반흔기/위축기에서도 내부에 혈류 신호를 보이기 때문) 6), 14)
IA (인도시아닌그린 형광 안저 조영)
섹션 제목: “IA (인도시아닌그린 형광 안저 조영)”- 근시성 MNV는 IA에서 반드시 과형광을 보이지 않음 6)
- MNV 활동성 평가에는 FA 우선 6)
- lacquer cracks 검출 성능이 높으며, IA 후기상에서 선상 저형광으로 나타남 6)
FAF (안저 자가형광)
섹션 제목: “FAF (안저 자가형광)”- 황반부 위축은 저형광으로 명확하게 나타나므로 진단 및 확대 평가에 FAF 유용 6)
- MNV 안정 후 경과 관찰에 권장 6)
감별 진단
섹션 제목: “감별 진단”근시성 MNV와 감별이 필요한 질환은 다음과 같습니다.
| 감별 질환 | 감별 포인트 |
|---|---|
| 단순형 황반부 출혈 | FA에서 형광 누출 없음(형광 차단만 있음). OCT에서 Henle 섬유층을 따른 고반사. 출혈은 2~3개월 내 자연 흡수됨 6), 15) |
| 연령 관련 황반변성 | 드루젠 및 RPE 박리 동반. MNV가 크고 삼출성 변화가 심함 |
| 점상 맥락막 내층증 (PIC) | 근시안의 젊은 여성에 호발. 후극부에 다발하는 소형(500μm 미만) 경계가 명확한 황백색 병소. 염증에 따른 맥락막 비후 6) |
| 다초점 맥락막염 (MFC) | PIC의 유사 질환 6) |
| Dome-shaped macula에 동반된 MNV | OCT에서 황반부의 내측으로의 볼록 돌출. MNV가 없어도 삼출성 변화 있음 6) |
| 경사 시신경 유두 증후군 (하부 포도종) | 하부 포도종 가장자리에 MNV가 발생할 수 있음 6) |
단순형 황반부 출혈은 lacquer cracks 형성 시 맥락막 모세혈관이 손상되어 발생하는 출혈로, 2~3개월 내 자연 흡수되어 치료가 필요하지 않습니다. OCT에서는 Henle 섬유층을 따른 고반사로 관찰됩니다. 반면, 근시성 MNV는 MNV에 동반된 출혈이며, FA에서 과형광(형광 누출)을 보여 감별할 수 있습니다. OCT만으로 감별이 어려운 경우 FA 검사가 필수적입니다. 6)
5. 표준적 치료법
섹션 제목: “5. 표준적 치료법”항VEGF 약제 유리체강내 주입 (1차 선택)
섹션 제목: “항VEGF 약제 유리체강내 주입 (1차 선택)”다기관 전향적 무작위 대조 시험에서 유효성이 유일하게 입증된 치료법입니다. 6)
2024년 8월 현재 일본 승인 약물: 라니비주맙(루센티스®) 및 그 바이오시밀러, 아플리버셉트(아일리아®). 6)
Glachs 등(2024)의 네트워크 메타분석(34개 연구, 2,098안)에서 항VEGF 약제는 6개월 내에 무치료군 대비 +14.1글자(95% CI 10.8
17.4), PDT군 대비 +12.1글자(95% CI 8.315.8)의 시력 개선을 보였습니다(모두 p<0.0001). 1)
투여 요법:
- 도입기 1회 투여 후 PRN법(1+PRN)이 표준입니다 6), 11)
- 3+PRN과 시력 개선에 유의한 차이 없음. 1+PRN군이 주사 횟수가 적음(12개월에 1.8회 vs 3.2회) 1)
Cheung 2017 국제 컨센서스 치료 원칙: 11)
- 근시성 MNV에 대해 지체 없이 항VEGF 약제 요법 시행
- 항VEGF 약제 요법이 불가능한 경우 PDT 고려(동등한 시력 예후 기대 불가)
- 도입기 투여는 1회만 하고 이후 PRN법
- OCT에서 망막하액, 시력 저하, FA에서 형광 누출이 있으면 재투여 고려
- MNV가 안정되면 최대 3개월까지 투여 간격 연장 11)
주요 임상 시험:
- MYRROR 시험: 아플리버셉트의 다기관 RCT. 유의한 시력 개선 입증. 8)
- RADIANCE 시험: 라니비주맙의 다기관 RCT. 유효성 입증. 9)
약물 간 비교:
베바시주맙, 라니비주맙, 애플리버셉트 간 시력 개선에 유의한 차이는 없음. 1) 애플리버셉트는 중심 망막 두께 감소가 더 크지만 시력에 미치는 영향은 차이 없음. 1)
기타 치료법
섹션 제목: “기타 치료법”- 광역학치료(PDT): 항VEGF 약물에 비해 시력 개선 효과가 떨어짐. 1) 장기적으로 황반 위축 악화 가능성. 보험 적용 없음. 6)
- 트리암시놀론 아세토니드 유리체강내 주사: 항VEGF 약물에 비해 효과가 떨어지며, 안압 상승 및 백내장 진행 위험. 1)
- 레이저 광응고: 런오프 현상으로 MNV 재발 유발 가능. 현재는 권장되지 않음.
경과 관찰
섹션 제목: “경과 관찰”- 활동성 MNV에서는 1~3개월 간격으로 OCT와 안저 검사 시행 6)
- MNV 안정화 후 수개월~1년 간격으로 경과 관찰 6)
- 재발 확인은 OCT 중심. MNV 확대·새로운 MNV 의심 시 OCTA 시행 6)
- 활동성 평가에 FA는 유용하지만 침습적이므로 검사 간격·전신 상태 고려 6)
- 황반부 위축 평가에는 FAF가 유용 6)
- 젊은 환자·소형 MNV에서는 반흔 형성이 작고 예후 양호. 발병 후 가능한 조기에 적극적 중재 중요 6)
1회 주사 후 필요 시 재치료(1+PRN)가 표준 요법이며, 12개월 동안 평균 1.8회라는 보고가 있습니다. 1) 연령 관련 황반변성에 비해 필요한 주사 횟수는 일반적으로 적습니다. 그러나 재발이나 위축 확대에 대한 장기 추적 관찰은 필수적이며, 조기 재치료가 권장됩니다. 6)
6. 병태생리학 및 상세한 발병 기전
섹션 제목: “6. 병태생리학 및 상세한 발병 기전”Bruch막 파열과 창상 치유 반응
섹션 제목: “Bruch막 파열과 창상 치유 반응”안축 연장에 따른 맥락막 위축과 Bruch막의 탄력 섬유 감소로 인해 Bruch막이 기계적으로 파열되어 lacquer cracks가 발생합니다. 이 파열 부위를 발판으로 창상 치유 반응으로서 MNV를 동반한 결합 조직이 망막하로 증식합니다. Patchy atrophy와 lacquer cracks는 MNV 발병의 예측 인자입니다. 7)
맥락막 순환 장애와 VEGF
섹션 제목: “맥락막 순환 장애와 VEGF”병적 근시안에서는 맥락막 모세혈관판과 혈관층이 거의 소실되고, 맥락막 대혈관만 남아 있는 경우가 있습니다. EDI-OCT를 이용한 연구에서 MNV를 발생시키는 고도 근시안에서는 맥락막이 유의하게 얇아져 있다고 보고되었습니다. 얇아진 맥락막 조직의 순환 장애가 VEGF 생성을 촉진하여 비정상적인 혈관망 형성으로 이어집니다.
CNV 유래 혈관 (짧은 후섬모체동맥)
섹션 제목: “CNV 유래 혈관 (짧은 후섬모체동맥)”Swept source OCT와 ICGA를 이용한 연구에서 짧은 후섬모체동맥이 근시성 MNV 근처에서 공막을 관통하여 MNV에 인접하는 소견이 75.0%에서 확인되었습니다. 짧은 후섬모체동맥 유래 혈관이 MNV에 환류한다고 생각되는 증례는 활동기 100%, 반흔기 87.9%, 위축기 73.8%로 높은 빈도입니다.
근시성 견인 황반병증과의 합병
섹션 제목: “근시성 견인 황반병증과의 합병”근시성 MNV와 근시성 황반분리증(MF)의 합병은 드물지만 중요한 임상적 의의를 가집니다.
Sayanagi 등(2023)은 근시성 MNV 주변에 MF를 동반한 3예를 보고하였다. 2) 모든 예에서 추적 관찰 중 황반부 망막박리가 악화되었다. MNV로 인한 망막하액이 구심성 및 원심성 견인 균형을 파괴하여 MF 진행을 촉진할 가능성이 시사된다.
Pereira 등(2023)은 근시성 황반분리증을 동반한 병적 근시안에서 발생한 MNV가 전층 황반원공의 원인이 된 증례를 보고하였다. 4) MNV 삼출로 인한 기계적 거상이 약화된 중심와의 뮐러 세포에 응력을 가하여 열공 형성에 이르렀을 것으로 추정된다.
7. 최신 연구와 향후 전망 (연구 단계 보고)
섹션 제목: “7. 최신 연구와 향후 전망 (연구 단계 보고)”근시성 황반병증의 장기 자연 경과
섹션 제목: “근시성 황반병증의 장기 자연 경과”Carlà 등(2025)은 1,228안의 유럽 코호트를 대상으로 한 장기 연구에서 근시성 황반병증의 57%가 10년 이상의 추적 관찰 중 진행되었음을 보고하였다. 5) 국소 위축을 가진 안의 47%가 황반부 위축으로 진행되었고(OR 4.21), 활동성 MNV는 15%의 안에서 평균 4.5년에 발생하였다. MNV 발생은 시력 저하(p=0.001) 및 황반부 위축으로의 진행(OR 5.81)과 유의하게 상관관계가 있었다.
항VEGF 약물의 장기 과제
섹션 제목: “항VEGF 약물의 장기 과제”항VEGF 약물로 단기적으로는 양호한 시력 개선을 얻을 수 있지만, 5년 이상의 장기 성적은 단기 성적에 비해 떨어진다. 치료하지 않은 자연 경과에서는 5년에 89%, 10년에 96%가 소수시력 0.1 이하가 된다. 12) 5년간 라니비주맙 투여는 시력 유지의 유용성이 보고되었다. 13) 위축 진행을 억제하는 치료법 개발이 향후 과제이다.
OCTA를 통한 조기 진단 가능성
섹션 제목: “OCTA를 통한 조기 진단 가능성”OCT-A Angio-B 모드는 구조 OCT나 형광 혈관 조영술로 검출하기 어려운 조기 MNV를 검출할 수 있을 가능성이 있다. 3) 비침습적이고 고감도인 검사법으로서 고도 근시안의 선별 검사에 응용이 기대된다.
8. 참고문헌
섹션 제목: “8. 참고문헌”- Glachs L, Embacher S, Berghold A, et al. Treatment of myopic choroidal neovascularization: a network meta-analysis and review. Graefes Arch Clin Exp Ophthalmol. 2024;262:1693-1722.
- Sayanagi K, Hara C, Fukushima Y, et al. Three cases of macular retinal detachment exacerbated during follow-up with myopic foveoschisis around myopic choroidal neovascularization. Am J Ophthalmol Case Rep. 2023;32:101899.
- Rico S, Sher I, Lavinkfy F, et al. Optical coherence tomography Angio-B mode for early detection of myopic choroidal neovascularization and treatment with Bevacizumab. Am J Ophthalmol Case Rep. 2024;34:102041.
- Pereira A, Ballios BG, Sarraf D, Yan P. Full-thickness macular hole due to choroidal neovascularization in the setting of pathologic myopia. J VitreoRetinal Dis. 2023;7(1):65-69.
- Carlà MM, Boselli F, Giannuzzi F, et al. Longitudinal Progression of Myopic Maculopathy in a Long-Term Follow-Up of a European Cohort: Imaging Features and Visual Outcomes. Ophthalmol Retina. 2025;9(8):774-786. doi:10.1016/j.oret.2025.02.015. PMID:40010496.
- 大野京子, 三宅正裕, 柳靖雄, ほか. 近視性黄斑部新生血管の診療ガイドライン. 日眼会誌. 2024;128:719-729.
- Ohno-Matsui K, Yoshida T, Futagami S, et al. Patchy atrophy and lacquer cracks predispose to the development of choroidal neovascularisation in pathological myopia. Br J Ophthalmol. 2003;87:570-573.
- Ikuno Y, Ohno-Matsui K, Wong TY, et al; MYRROR Investigators. Intravitreal aflibercept injection in patients with myopic choroidal neovascularization: the MYRROR Study. Ophthalmology. 2015;122:1220-1227.
- Wolf S, Balciuniene VJ, Laganovska G, et al; RADIANCE Study Group. RADIANCE: a randomized controlled study of ranibizumab in patients with choroidal neovascularization secondary to pathologic myopia. Ophthalmology. 2014;121:682-692.
- Ohno-Matsui K, Kawasaki R, Jonas JB, et al; META-PM Study Group. International photographic classification and grading system for myopic maculopathy. Am J Ophthalmol. 2015;159:877-883.
- Cheung CMG, Arnold JJ, Holz FG, et al. Myopic choroidal neovascularization: review, guidance, and consensus statement on management. Ophthalmology. 2017;124:1690-1711.
- Yoshida T, Ohno-Matsui K, Yasuzumi K, et al. Myopic choroidal neovascularization: a 10-year follow-up. Ophthalmology. 2003;110:1297-1305.
- Onishi Y, Yokoi T, Kasahara K, et al. Five-year outcomes of intravitreal ranibizumab for choroidal neovascularization in patients with pathologic myopia. Retina. 2019;39:1289-1298.
- Miyata M, Ooto S, Hata M, et al. Detection of myopic choroidal neovascularization using optical coherence tomography angiography. Am J Ophthalmol. 2016;165:108-114.
- Goto S, Sayanagi K, Ikuno Y, et al. Comparison of visual prognosis between natural course of simple hemorrhage and choroidal neovascularization treated with intravitreal bevacizumab in highly myopic eyes: a 1-year follow-up. Retina. 2015;35:429-434.
