เยื่อบุโพรงจอประสาทตา เจริญผิดปกติจากสายตาสั้น (CNV สายตาสั้น ) คือเส้นเลือดใหม่ที่เกิดจากคอรอยด์ ในจอประสาทตา ของดวงตาที่มีสายตาสั้น ทางพยาธิวิทยา ในระดับสากล มีการเปลี่ยนชื่อจาก CNV เป็น MNV (myopic neovascularization) 6)
เกิดขึ้นใน 5-11% ของดวงตาที่มีสายตาสั้น รุนแรง และเป็นสาเหตุใหญ่ที่สุดของเยื่อบุโพรงจอประสาทตา เจริญผิดปกติในผู้ที่มีอายุต่ำกว่า 50 ปี
อาการหลักคือ เห็นภาพบิดเบี้ยว จุดบอดกลาง และการมองเห็น ลดลง เนื่องจากเป็น CNV type 2 อาการที่ผู้ป่วยรู้สึกได้จึงปรากฏเร็วและดำเนินไปอย่างรวดเร็ว
หากไม่รักษา 89% ของผู้ป่วยจะมีการมองเห็นที่แก้ไขแล้ว ลดลงเหลือ 0.1 หรือน้อยกว่าภายใน 5 ปี ทำให้เป็นโรคที่มีการพยากรณ์โรคไม่ดี
การรักษาทางเลือกแรกคือการฉีดยา anti-VEGF เข้าไปในน้ำวุ้นตา โดยสูตรมาตรฐานคือ 1 ครั้ง + ฉีดซ้ำเมื่อจำเป็น (1+PRN) 1), 6)
การตรวจฟลูออเรสซีน แองจิโอกราฟี (FA ) มีความสำคัญที่สุดในการวินิจฉัย และจำเป็นในการแยกจากเลือดออกในจอประสาทตา ธรรมดา 6)
ในระยะยาว การขยายตัวของจอประสาทตา ฝ่อที่เกี่ยวข้องกับ MNV สายตาสั้น มีผลต่อการพยากรณ์การมองเห็น
เยื่อบุโพรงจอประสาทตา เจริญผิดปกติจากสายตาสั้น (myopic choroidal neovascularization; CNV สายตาสั้น ) คือเส้นเลือดใหม่ที่เกิดจากคอรอยด์ ที่ขั้วหลังของดวงตาที่มีสายตาสั้น ทางพยาธิวิทยา ในช่วงไม่กี่ปีที่ผ่านมา มีการใช้คำว่า “MNV สายตาสั้น ” (myopic neovascularization) ในระดับสากลเพื่อรวมเส้นเลือดใหม่ที่มาจากคอรอยด์ และจอประสาทตา 6)
เป็นสาเหตุที่พบบ่อยเป็นอันดับสองของเยื่อบุโพรงจอประสาทตา เจริญผิดปกติรองจากจอประสาทตา เสื่อมตามอายุ และเป็นสาเหตุใหญ่ที่สุดในผู้ที่มีอายุต่ำกว่า 50 ปี เกิดขึ้นในประมาณ 10% ของผู้ป่วยสายตาสั้น ทางพยาธิวิทยาทั้งหมด 7)
สายตาสั้น รุนแรงถูกกำหนดให้มีค่าสายตาเทียบเท่าทรงกลม -6.0 D หรือน้อยกว่า หรือความยาวแกนตา 26.5 มม. หรือมากกว่า สายตาสั้น ทางพยาธิวิทยาถูกกำหนดให้มีการเปลี่ยนแปลงฝ่อในอวัยวะรับภาพเกินกว่าการฝ่อแบบกระจาย หรือมีสตาฟิโลมา หลัง (การจำแนก META-PM, 2015) 10)
MNV สายตาสั้น ส่วนใหญ่เป็น CNV type 2 ตามการจำแนกของ Gass (CNV อยู่เหนือเยื่อบุผิวเม็ดสีจอประสาทตา ) มักมีขนาดค่อนข้างเล็กและการเปลี่ยนแปลงแบบมีน้ำซึมน้อย
MNV สายตาสั้น เกิดขึ้นใน 5-11% ของดวงตาที่มีสายตาสั้น รุนแรง
ระหว่างการติดตามผล 8 ปี ประมาณ 6% ของผู้ป่วยสายตาสั้น ทางพยาธิวิทยาที่ไม่มีประวัติ MNV มาก่อนเกิดภาวะนี้
ในผู้ป่วยที่มีประวัติ MNV ในตาข้างเดียว ประมาณ 35% จะเกิดในตาอีกข้าง
หากจำกัดเฉพาะผู้ที่มีอายุต่ำกว่า 50 ปี ประมาณ 60% ของ MNV เป็น MNV จากสายตาสั้น 7)
สายตาสั้น ทางพยาธิวิทยาคิดเป็น 13% ของความบกพร่องทางการมองเห็น ที่มีค่าสายตาแก้ไข ≤0.1 และเป็นสาเหตุอันดับสองของการตาบอดรองจากต้อหิน
Q
เส้นเลือดใหม่ในคอรอยด์จากสายตาสั้นเริ่มเกิดขึ้นเมื่ออายุเท่าใด?
A
แตกต่างจากจอประสาทตา เสื่อมตามอายุ CNV จากสายตาสั้น สามารถเริ่มได้ตั้งแต่อายุน้อย (ตั้งแต่วัยรุ่น) เป็นสาเหตุใหญ่ที่สุดของเส้นเลือดใหม่ในคอรอยด์ ในผู้ที่มีอายุต่ำกว่า 50 ปี และเป็นโรคสำคัญที่ทำลายการมองเห็น ส่วนกลางของทั้งสองตาในวัยทำงาน การตรวจพบตั้งแต่เนิ่นๆ และการรักษาตั้งแต่เนิ่นๆ ส่งผลต่อการพยากรณ์โรคอย่างมาก
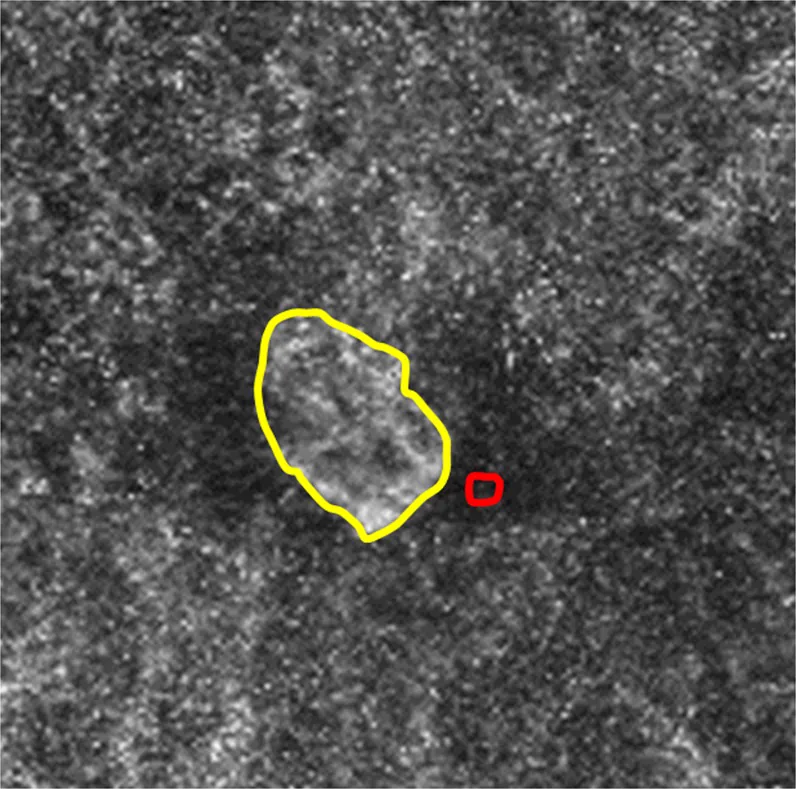
ภาพ OCTA ของเส้นเลือดใหม่ในคอรอยด์จากสายตาสั้น Sawai Y, et al. Usefulness of Denoising Process to Depict Myopic Choroidal Neovascularisation Using a Single Optical Coherence Tomography Angiography Image. Sci Rep. 2020. Figure 3. PM
CI D: PMC7148361. License: CC BY.
เมื่อ MNV จากสายตาสั้น ลามไปถึงโฟเวีย จะมีอาการดังต่อไปนี้ เนื่องจากเป็น CNV ชนิด 2 สารน้ำจะออกฤทธิ์โดยตรงต่อชั้นนอกของจอประสาทตา ทำให้อาการปรากฏเร็วและดำเนินไปอย่างรวดเร็ว6)
ภาพบิดเบี้ยว ภาพบิดเบี้ยว ใหม่ในผู้ป่วยสายตาสั้น เป็นสัญญาณสำคัญที่บ่งชี้ถึง MNV จากสายตาสั้น ในกรณีที่มีภาวะจอประสาทตา ถูกดึงจากสายตาสั้น ร่วมด้วย อาจสังเกตเห็นการแย่ลงของภาพบิดเบี้ยว ได้ยาก6) จุดบอดกลาง การมองเห็น ลดลงCNV จะยุบตัวลง หากมีแผลเป็นที่โฟเวีย การมองเห็น ที่ลดลงจะกลายเป็นแบบถาวร
หากอยู่บริเวณนอกจอประสาทตา อาจไม่มีอาการ การตอบสนองต่อข้อร้องเรียนที่ผู้ป่วยรู้สึกได้อย่างระมัดระวังเป็นสิ่งสำคัญ6)
MNV ในสายตาสั้น แบ่งออกเป็น 3 ระยะ: ระยะ active, ระยะ scar, และระยะ atrophy
ระยะ active
รอยโรคใต้จอประสาทตา สีเทาขาว : ปรากฏเป็นรอยโรคขนาดเล็กที่มีขอบมีเม็ดสี มีขนาดเล็กกว่า MNV ในจอประสาทตา เสื่อมตามอายุ 6)
เลือดออกใต้จอประสาทตา : มักพบรอบๆ CNV
ผล OCT : รอยโรคนูนสูงสะท้อนแสงเหนือ RPE อาจมีน้ำใต้จอประสาทตา เลือดออกใต้จอประสาทตา จอประสาทตา บวมน้ำแบบถุงน้ำ หรือ fibrin deposition แต่การเปลี่ยนแปลงแบบ serous ไม่รุนแรง 6)
ระยะ scar และ atrophy
Fuchs spot : หลังจาก MNV ยุบตัว จะเกิดรอยโรคแผลเป็นที่มีเม็ดสีจากการ hyperplasia ของ RPE และ basement membrane
จอประสาทตา ฝ่อที่เกี่ยวข้องกับ MNV ในสายตาสั้น การมองเห็น อย่างรุนแรง สังเกตได้จากการขยายของรอยฉีกของ Bruch membrane และการฝ่อของ retinal pigment epithelium, choriocapillaris และชั้นนอกของจอประสาทตา หลังจาก 5 ปี 88.9% หลังจาก 10 ปี 96.3% มีสายตาที่แก้ไขแล้ว ≤ 0.1 12)
ในการตรวจ OCT angiography ระยะ active จะแสดง “เครือข่ายคล้ายลูกไม้, anastomosis กว้าง, และ halo ความเข้มต่ำรอบรอยโรค” ส่วนระยะสงบจะแสดง “หลอดเลือดที่โตเต็มที่ยาวเป็นเส้นตรง, anastomosis น้อย (ลักษณะคล้ายต้นไม้แห้ง)” แม้จะอยู่นอกระยะ active การไหลเวียนเลือดภายในมักคงอยู่ (ระยะ active 100%, ระยะ scar ประมาณ 80%, ระยะ atrophy ประมาณ 90%) อย่างไรก็ตาม OCTA ไม่เหมาะสำหรับการประเมินกิจกรรมของ MNV 6)
จอประสาทตา เสื่อมตามอายุ
MNV ในสายตาสั้น แตกต่างจากจอประสาทตา เสื่อมตามอายุในประเด็นต่อไปนี้: การเปลี่ยนแปลงแบบ exudative เล็กน้อย ไม่มี drusen หรือ RPE detachment ส่วนใหญ่เป็น type 2 CNV (classic CNV ) พบบ่อยในคนอายุน้อย และจำนวนครั้งที่ต้องฉีด anti-VEGF โดยทั่วไปน้อยกว่า
เชื่อว่ากลไกสองอย่างเกี่ยวข้องกับการเกิด MNV ในสายตาสั้น : การฉีกขาดเชิงกลของ Bruch membrane และความผิดปกติของการไหลเวียนของคอรอยด์
การยืดตัวของแกนลูกตาอย่างต่อเนื่องทำให้คอรอยด์ และจอประสาทตา ยืดและบางลง
การฉีกขาดของเยื่อบรูค (รอยร้าวแลคเกอร์) : บริเวณที่ฉีกขาดเชิงกลกลายเป็นโครงสร้างเนื้อเยื่อเกี่ยวพันที่มาพร้อมกับเส้นเลือดใหม่คอรอยด์ ความผิดปกติของการไหลเวียนเลือดคอรอยด์ : การอุดตันและการหายไปของแผ่นเส้นเลือดฝอยคอรอยด์ ส่งเสริมการผลิต VEGFการฝ่อแบบปื้นและรอยร้าวแลคเกอร์เป็นปัจจัยทำนายการเกิดเส้นเลือดใหม่คอรอยด์ 7)
การฝ่อของคอรอยด์ และจอประสาทตา เฉพาะที่ : โดยเฉพาะบริเวณรอบรอยบุ๋มจอตา ในระยะเส้นผ่านศูนย์กลางจานประสาทตา รอยร้าวแลคเกอร์ : รอยแตกเชิงเส้นบนเยื่อบรูค ค่า OR สำหรับ CNV เท่ากับ 2.56จุดรับภาพทรงโดม (DSM) : ค่า OR สำหรับ CNV สูงถึง 4.955) สตาฟิโลมา หลังสายตาสั้น สูงในตัวเองเป็นปัจจัยเสี่ยงความยาวแกนตา ยาว : ปัจจัยเสี่ยงต่อการดำเนินของจอประสาทตา เสื่อมจากสายตาสั้น เพศหญิง : ความชุกของรอยโรคฝ่อคอรอยด์ และจอประสาทตา จากสายตาสั้น สูงกว่าโดยมี OR 3.29
Q
สายตาสั้นสูงจะทำให้เกิดเส้นเลือดใหม่คอรอยด์เสมอหรือไม่?
A
ไม่ใช่ทุกตาที่มีสายตาสั้น สูงจะเกิด MNV จากสายตาสั้น อุบัติการณ์ประมาณ 5-11% และความเสี่ยงสูงกว่าในตาที่มีรอยร้าวแลคเกอร์หรือการฝ่อแบบปื้น7) การตรวจพบแต่เนิ่นๆ ด้วยการตรวจตาเป็นประจำเป็นสิ่งสำคัญ
ในการวินิจฉัย MNV จากสายตาสั้น จำเป็นต้องยืนยันการเปลี่ยนแปลงของจอประสาทตา ที่เกี่ยวข้องกับสายตาสั้น ทางพยาธิวิทยาและการมีอยู่ของ MNV 6) การแยกความแตกต่างที่สำคัญที่สุดคือระหว่างเลือดออกในจอประสาทตา แบบธรรมดากับ MNV และไม่แนะนำให้ใช้การรักษาด้วยยาต้าน VEGF ในกรณีที่ไม่สามารถยืนยันการมีอยู่ของ MNV ได้ 6)
การตรวจที่ให้ความสำคัญมากที่สุดในแนวทางปฏิบัติ 6)
MNV จากสายตาสั้น แสดงการเรืองแสงมากเกินไปอย่างชัดเจนตั้งแต่ระยะแรกของ FA และใน MNV ที่ยังทำงานอยู่ จะพบการรั่วของฟลูออเรสซีน ตั้งแต่ระยะกลางถึงปลาย
สามารถตรวจพบรอยโรคที่ไม่ชัดเจนจากการตรวจด้วยกล้องตรวจตา หรือ OCT ได้
ในเลือดออกในจอประสาทตา แบบธรรมดา จะสังเกตได้เฉพาะเป็นรอยบดบังการเรืองแสง (การเรืองแสงน้อย) โดยไม่มีการเรืองแสงมากเกินไป → ชี้ขาดในการแยกความแตกต่าง
หากมีข้อสงสัยในการประเมิน ควรทำ FA อย่างจริงจัง 6)
ระยะทำงาน : รอยโรคยกตัวรูปโดมสะท้อนแสงสูงเหนือ RPE มีของเหลวใต้จอประสาทตา และไฟบรินสะสมรอบๆ 6) ระยะแผลเป็น : เส้นสะท้อนแสงสูงของการห่อหุ้ม MNV โดย RPE ความชัดเจนของการห่อหุ้มมีประโยชน์มากในการประเมินการทำงานของ MNV 6) เมื่อกลับมาเป็นซ้ำ : เส้นจะไม่ชัดเจน (การเปรียบเทียบกับภาพ OCT ก่อนหน้ามีความสำคัญ) 6) การแยกความแตกต่างจากเลือดออกในจอประสาทตา แบบธรรมดา : ใน OCT จะสังเกตเป็นเส้นสะท้อนแสงสูงตามแนวชั้นเส้นใยเฮนเล 6) หากแยกความแตกต่างได้ยากด้วย OCT เพียงอย่างเดียว จำเป็นต้องทำ FA 6)
ประเมินการมีอยู่ของการไหลเวียนเลือดแบบไม่รุกล้ำ6)
มีประโยชน์ในการระบุ MNV (แยกจากเลือดออกในจอประสาทตา แบบธรรมดา)6)
มีรายงานความไว 90.48% และความจำเพาะ 93.75%3)
โหมด Angio-B สามารถตรวจพบ MNV ระยะเริ่มต้นที่ตรวจพบได้ยากด้วย OCT โครงสร้าง3)
ไม่เหมาะสำหรับการประเมินกิจกรรม (เนื่องจากแสดงสัญญาณการไหลภายในแม้ในระยะแผลเป็นและฝ่อ)6), 14)
MNV สายตาสั้น ไม่จำเป็นต้องแสดงการเรืองแสงมากเกินไปใน IA6)
FA ถูกจัดลำดับความสำคัญสำหรับการประเมินกิจกรรมของ MNV6) มีความสามารถสูงในการตรวจจับรอยแตกแลคเกอร์ ปรากฏเป็นเส้นเรืองแสงต่ำในระยะปลายของ IA6)
การฝ่อของจุดรับภาพชัดเจนปรากฏเป็นบริเวณเรืองแสงต่ำ ดังนั้น FAF จึงมีประโยชน์สำหรับการวินิจฉัยและการประเมินการขยายตัว6)
แนะนำสำหรับการติดตามผลหลังจาก MNV คงที่6)
โรคที่ต้องแยกจาก MNV สายตาสั้น แสดงไว้ด้านล่าง
โรคที่ต้องแยก จุดที่ใช้แยก เลือดออกจอประสาทตา ชนิดธรรมดา ไม่มีการรั่วของฟลูออเรสซีน ในการตรวจ FA (เฉพาะการอุดกั้นฟลูออเรสซีน ) ใน OCT พบการสะท้อนสูงตามแนวชั้นเส้นใยเฮนเล เลือดออกจะถูกดูดซึมเองภายใน 2-3 เดือน6), 15) จอประสาทตา เสื่อมตามอายุร่วมกับดรูเซน และการหลุดลอกของเยื่อบุผิวเม็ดสีจอตา MNV มีขนาดใหญ่และมีการเปลี่ยนแปลงแบบมีน้ำซึมรุนแรง โรคคอรอยด์ อักเสบแบบจุดใน (PIC ) พบบ่อยในหญิงสาวสายตาสั้น รอยโรคสีเหลือง-ขาวหลายจุดขนาดเล็ก (<500 ไมครอน) ขอบเขตชัดเจนที่ขั้วหลัง คอรอยด์หนา ขึ้นเนื่องจากการอักเสบ6) คอรอยด์ อักเสบหลายจุด (MFC)โรคที่เกี่ยวข้องกับ PIC 6) MNV ร่วมกับจอประสาทตารูปโดม ใน OCT พบการนูนเข้าด้านในของจอประสาทตา อาจมีการเปลี่ยนแปลงแบบมีน้ำซึมแม้ไม่มี MNV6) กลุ่มอาการจานประสาทตา เอียง (สตาฟิโลมา ด้านล่าง) MNV อาจเกิดขึ้นที่ขอบของสตาฟิโลมา ด้านล่าง6)
Q
อะไรคือความแตกต่างระหว่างเลือดออกจอประสาทตาชนิดธรรมดากับเส้นเลือดใหม่คอรอยด์จากสายตาสั้น?
A
เลือดออกจอประสาทตา ชนิดธรรมดาคือเลือดออกที่เกิดจากความเสียหายของเส้นเลือดฝอยคอรอยด์ ขณะเกิดรอยแตกแลกเกอร์ และจะถูกดูดซึมเองภายใน 2-3 เดือนโดยไม่ต้องรักษา ใน OCT จะเห็นเป็นการสะท้อนสูงตามแนวชั้นเส้นใยเฮนเล ในทางตรงกันข้าม MNV จากสายตาสั้น คือเลือดออกร่วมกับ MNV ซึ่งแสดงการเรืองแสงเกิน (การรั่วของฟลูออเรสซีน ) ในการตรวจ FA ทำให้แยกได้ หาก OCT เพียงอย่างเดียวแยกได้ยาก จำเป็นต้องตรวจ FA 6)
นี่คือการรักษาเพียงอย่างเดียวที่พิสูจน์ประสิทธิภาพในการทดลองแบบสุ่มและมีกลุ่มควบคุมแบบหลายศูนย์ 6)
ยาที่ได้รับการอนุมัติ ณ เดือนสิงหาคม 2024 (ญี่ปุ่น): ranibizumab (Lucentis®) และไบโอซิมิลาร์ , aflibercept (Eylea®) 6)
ในการวิเคราะห์อภิมานเครือข่ายโดย Glachs และคณะ (2024) (34 การศึกษา, 2098 ตา) anti-VEGF แสดงการปรับปรุงการมองเห็น +14.1 ตัวอักษร (95% CI 10.8–17.4) เทียบกับไม่รักษา และ +12.1 ตัวอักษร (95% CI 8.3–15.8) เทียบกับ PDT (ทั้งคู่ p<0.0001) 1)
สูตรการให้ยา:
การให้ยาโหลดครั้งเดียวแล้วตามด้วย PRN (1+PRN) เป็นมาตรฐาน 6), 11)
ไม่มีความแตกต่างอย่างมีนัยสำคัญในการปรับปรุงการมองเห็น เมื่อเทียบกับ 3+PRN กลุ่ม 1+PRN มีจำนวนการฉีดน้อยกว่า (1.8 ครั้ง เทียบกับ 3.2 ครั้งใน 12 เดือน) 1)
หลักการรักษาตามฉันทามติระหว่างประเทศ Cheung 2017: 11)
ควรทำการรักษาด้วย anti-VEGF โดยไม่ชักช้าสำหรับ MNV สายตาสั้น
หากไม่สามารถรักษาด้วย anti-VEGF ได้ ให้พิจารณา PDT (ไม่สามารถคาดหวังการพยากรณ์การมองเห็น ที่ใกล้เคียงกัน)
ให้ยาโหลดเพียงครั้งเดียว จากนั้น PRN
หากมีของเหลวใต้จอประสาทตา ใน OCT , การมองเห็น ลดลง หรือการรั่วของฟลูออเรสซีน ใน FA ให้พิจารณาฉีดซ้ำ
หาก MNV คงที่ สามารถขยายระยะห่างการฉีดได้สูงสุด 3 เดือน 11)
การทดลองทางคลินิกหลัก:
การทดลอง MYRROR: RCT แบบหลายศูนย์ของ aflibercept พิสูจน์การปรับปรุงการมองเห็น อย่างมีนัยสำคัญ 8)
การทดลอง RADIANCE: การทดลองแบบสุ่มและมีกลุ่มควบคุมแบบหลายศูนย์ของ ranibizumab แสดงให้เห็นประสิทธิผล 9)
การเปรียบเทียบระหว่างยา :
ไม่พบความแตกต่างที่มีนัยสำคัญทางสถิติในการปรับปรุงการมองเห็น ระหว่าง bevacizumab, ranibizumab และ aflibercept 1) Aflibercept ทำให้ความหนาของจอประสาทตา ส่วนกลางลดลงมากกว่า แต่ไม่มีผลต่อการมองเห็น ที่แตกต่างกัน 1)
การรักษาด้วยแสงไดนามิก (PDT )การมองเห็น ด้อยกว่ายาต้าน VEGF 1) อาจทำให้จอประสาทตา ฝ่อแย่ลงในระยะยาว ไม่ครอบคลุมโดยประกัน 6) การฉีด triamcinolone acetonide เข้าแก้วตา : ด้อยกว่ายาต้าน VEGF มีความเสี่ยงต่อความดันลูกตา สูงและต้อกระจก ที่แย่ลง 1) การจี้ด้วยเลเซอร์ : อาจกระตุ้นให้ MNV กลับมาเป็นซ้ำเนื่องจากปรากฏการณ์ run-off ปัจจุบันไม่แนะนำ
ใน MNV ที่ยังทำงานอยู่ ให้ทำ OCT และตรวจอวัยวะทุก 1-3 เดือน 6)
หลังจาก MNV คงที่ ให้ติดตามทุกสองสามเดือนถึง 1 ปี 6)
การตรวจหาการกลับเป็นซ้ำส่วนใหญ่ใช้ OCT หากสงสัยว่า MNV ขยายใหญ่ขึ้นหรือมี MNV ใหม่ ให้ทำ OCTA 6)
การตรวจหลอดเลือดด้วยฟลูออเรสซีน (FA ) มีประโยชน์ในการประเมินกิจกรรม แต่เป็นการรุกล้ำ ดังนั้นควรพิจารณาช่วงเวลาการตรวจและสภาพร่างกายโดยรวม 6)
การถ่ายภาพเรืองแสงอัตโนมัติของจอตา (FAF ) มีประโยชน์ในการประเมินการฝ่อของจอประสาทตา 6)
ในผู้ป่วยอายุน้อยและ MNV ขนาดเล็ก การเกิดแผลเป็นมีขนาดเล็กกว่าและการพยากรณ์โรคดีกว่า การแทรกแซงเชิงรุกโดยเร็วที่สุดหลังเริ่มมีอาการเป็นสิ่งสำคัญ 6)
ใน MNV สายตาสั้น สารน้ำจะหายไปในหลายกรณีหลังฉีดครั้งเดียว แต่อาจกลับมาเป็นซ้ำได้ แม้จะมีการหุ้ม (encapsulation) ก็อาจกลับมาเป็นซ้ำได้ ดังนั้นจำเป็นต้องติดตาม OCT ในระยะยาว 6)
หากมีจอประสาทตา ผิดปกติจากการดึงรั้งในสายตาสั้น (จอประสาทตา แยกชั้น) จอประสาทตาลอก อาจแย่ลงหลังฉีด anti-VEGF 2)
มีรายงานภาวะแทรกซ้อนที่พบได้ยากคือการเกิดหรือขยายของรูจอประสาทตา หลังฉีด anti-VEGF 4)
ในบางกรณี จอประสาทตา ฝ่อขยายตัวในระยะยาวและการมองเห็น ลดลง การประเมินการฝ่อเป็นประจำด้วย FAF มีความสำคัญ
Q
ต้องฉีดกี่ครั้งในการรักษาหลอดเลือดใหม่ในคอรอยด์จากสายตาสั้น?
A
สูตรมาตรฐานคือฉีดครั้งเดียว + ฉีดซ้ำเมื่อจำเป็น (1+PRN) โดยมีรายงานเฉลี่ย 1.8 ครั้งใน 12 เดือน 1) จำนวนครั้งที่ฉีดโดยทั่วไปน้อยกว่าเมื่อเทียบกับจอประสาทตา เสื่อมตามอายุ อย่างไรก็ตาม การติดตามระยะยาวเพื่อดูการกลับเป็นซ้ำและการขยายตัวของการฝ่อเป็นสิ่งจำเป็น และแนะนำให้รักษาซ้ำตั้งแต่เนิ่นๆ 6)
การฝ่อของคอรอยด์ และการลดลงของเส้นใยยืดหยุ่นในเยื่อบรูค เนื่องจากการยืดของแกนลูกตาทำให้เกิดการฉีกขาดทางกลของเยื่อบรูค และเกิดรอยร้าวแลคเกอร์ (lacquer cracks) ที่บริเวณที่ฉีกขาด เนื้อเยื่อเกี่ยวพันที่มี MNV จะเจริญเติบโตใต้จอประสาทตา เพื่อตอบสนองต่อการสมานแผล การฝ่อแบบปื้น (patchy atrophy) และรอยร้าวแลคเกอร์เป็นปัจจัยทำนายการเกิด MNV 7)
ในตาที่มีสายตาสั้น ทางพยาธิวิทยา ชั้นเส้นเลือดฝอยคอรอยด์ และชั้นหลอดเลือดเกือบหายไป เหลือเพียงหลอดเลือดคอรอยด์ ขนาดใหญ่ การศึกษาโดยใช้ EDI-OCT รายงานว่าคอรอยด์ บางลงอย่างมีนัยสำคัญในตาสายตาสั้น สูงที่เกิด MNV ความผิดปกติของการไหลเวียนในเนื้อเยื่อคอรอยด์ ที่บางจะกระตุ้นการผลิต VEGF นำไปสู่การสร้างเครือข่ายหลอดเลือดที่ผิดปกติ
โดยใช้ swept source OCT และ ICGA พบว่าหลอดเลือดแดงซิลิอารีส่วนหลังสั้นเจาะทะลุตาขาว ใกล้กับ MNV สายตาสั้น และเข้าใกล้ MNV ใน 75.0% ของกรณี ในกรณีที่เชื่อว่าหลอดเลือดที่มาจากหลอดเลือดแดงซิลิอารีส่วนหลังสั้นไหลเวียนไปยัง MNV ความถี่สูง: 100% ในระยะ active, 87.9% ในระยะแผลเป็น และ 73.8% ในระยะฝ่อ
การเกิดร่วมของ MNV สายตาสั้น กับจอประสาทตา แยกชั้นในสายตาสั้น (MF) พบได้น้อยแต่มีความสำคัญทางคลินิก
Sayanagi และคณะ (2023) รายงานผู้ป่วย 3 รายที่มี MF รอบๆ MNV สายตาสั้น 2) ทุกรายมีจอประสาทตาลอก บริเวณจุดรับภาพแย่ลงระหว่างการติดตามผล มีการเสนอว่าของเหลวใต้จอประสาทตา จาก MNV ทำลายสมดุลแรงดึงเข้าสู่ศูนย์กลางและออกจากศูนย์กลาง ส่งเสริมการดำเนินของ MF
Pereira และคณะ (2023) รายงานผู้ป่วย MNV ในตาสายตาสั้น ทางพยาธิวิทยาที่มีจอประสาทตา หลุดลอกแบบสายตาสั้น ซึ่งทำให้เกิดรูจุดรับภาพทะลุตลอดความหนา 4) การยกตัวเชิงกลจากการรั่วซึมของ MNV สันนิษฐานว่า施加แรงกดต่อเซลล์ Müller ที่บริเวณรอยบุ๋มซึ่งอ่อนแอ นำไปสู่การเกิดรู
เนื้อหาต่อไปนี้อยู่ในระยะวิจัยหรือการทดลองทางคลินิกในปัจจุบัน และไม่ใช่การรักษามาตรฐานที่ได้รับในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับความก้าวหน้าทางการแพทย์ในอนาคต
Carlà และคณะ (2025) ในการศึกษาระยะยาวในตา 1228 ตาจากกลุ่มประชากรยุโรป รายงานว่า 57% ของจอประสาทตา เสื่อมจากสายตาสั้น ดำเนินไประหว่างการติดตามผลมากกว่า 10 ปี 5) 47% ของตาที่มีฝ่อเฉพาะที่ดำเนินไปเป็นฝ่อจุดรับภาพ (OR 4.21) และ MNV ที่ทำงานเกิดขึ้นใน 15% ของตาโดยเฉลี่ย 4.5 ปี การเกิด MNV สัมพันธ์อย่างมีนัยสำคัญกับการลดลงของการมองเห็น (p=0.001) และการดำเนินไปเป็นฝ่อจุดรับภาพ (OR 5.81)
ยาต้าน VEGF ให้การมองเห็น ดีขึ้นในระยะสั้น แต่ผลระยะยาวมากกว่า 5 ปีด้อยกว่าผลระยะสั้น ในประวัติธรรมชาติที่ไม่ได้รับการรักษา 89% ของตาที่ 5 ปีและ 96% ที่ 10 ปีมีการมองเห็น 0.1 หรือน้อยกว่า 12) การให้ ranibizumab เป็นเวลา 5 ปีมีรายงานว่ามีประโยชน์ในการรักษาการมองเห็น 13) การพัฒนาการรักษาที่ยับยั้งการดำเนินของฝ่อเป็นความท้าทายในอนาคต
โหมด OCT -A Angio-B สามารถตรวจพบ MNV ระยะแรกที่ตรวจพบได้ยากด้วย OCT เชิงโครงสร้างหรือการถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน 3) ในฐานะวิธีการตรวจที่ไม่รุกรานและมีความไวสูง คาดว่าจะนำไปประยุกต์ใช้ในการคัดกรองตาสายตาสั้น สูง
Glachs L, Embacher S, Berghold A, et al. Treatment of myopic choroidal neovascularization: a network meta-analysis and review. Graefes Arch Clin Exp Ophthalmol. 2024;262:1693-1722.
Sayanagi K, Hara C, Fukushima Y, et al. Three cases of macular retinal detachment exacerbated during follow-up with myopic foveoschisis around myopic choroidal neovascularization. Am J Ophthalmol Case Rep. 2023;32:101899.
Rico S, Sher I, Lavinkfy F, et al. Optical coherence tomography Angio-B mode for early detection of myopic choroidal neovascularization and treatment with Bevacizumab. Am J Ophthalmol Case Rep. 2024;34:102041.
Pereira A, Ballios BG, Sarraf D, Yan P. Full-thickness macular hole due to choroidal neovascularization in the setting of pathologic myopia. J VitreoRetinal Dis. 2023;7(1):65-69.
Carlà MM, Boselli F, Giannuzzi F, et al. Longitudinal Progression of Myopic Maculopathy in a Long-Term Follow-Up of a European Cohort: Imaging Features and Visual Outcomes. Ophthalmol Retina. 2025;9(8):774-786. doi:10.1016/j.oret.2025.02.015. PMID:40010496.
大野京子, 三宅正裕, 柳靖雄, ほか. 近視性黄斑部新生血管の診療ガイドライン. 日眼会誌. 2024;128:719-729.
Ohno-Matsui K, Yoshida T, Futagami S, et al. Patchy atrophy and lacquer cracks predispose to the development of choroidal neovascularisation in pathological myopia. Br J Ophthalmol. 2003;87:570-573.
Ikuno Y, Ohno-Matsui K, Wong TY, et al; MYRROR Investigators. Intravitreal aflibercept injection in patients with myopic choroidal neovascularization: the MYRROR Study. Ophthalmology. 2015;122:1220-1227.
Wolf S, Balciuniene VJ, Laganovska G, et al; RADIANCE Study Group. RADIANCE: a randomized controlled study of ranibizumab in patients with choroidal neovascularization secondary to pathologic myopia. Ophthalmology. 2014;121:682-692.
Ohno-Matsui K, Kawasaki R, Jonas JB, et al; META-PM Study Group. International photographic classification and grading system for myopic maculopathy. Am J Ophthalmol. 2015;159:877-883.
Cheung CMG, Arnold JJ, Holz FG, et al. Myopic choroidal neovascularization: review, guidance, and consensus statement on management. Ophthalmology. 2017;124:1690-1711.
Yoshida T, Ohno-Matsui K, Yasuzumi K, et al. Myopic choroidal neovascularization: a 10-year follow-up. Ophthalmology. 2003;110:1297-1305.
Onishi Y, Yokoi T, Kasahara K, et al. Five-year outcomes of intravitreal ranibizumab for choroidal neovascularization in patients with pathologic myopia. Retina. 2019;39:1289-1298.
Miyata M, Ooto S, Hata M, et al. Detection of myopic choroidal neovascularization using optical coherence tomography angiography. Am J Ophthalmol. 2016;165:108-114.
Goto S, Sayanagi K, Ikuno Y, et al. Comparison of visual prognosis between natural course of simple hemorrhage and choroidal neovascularization treated with intravitreal bevacizumab in highly myopic eyes: a 1-year follow-up. Retina. 2015;35:429-434.