活動期

近視性脈絡膜新生血管
1. 近視性脈絡膜新生血管とは
Section titled “1. 近視性脈絡膜新生血管とは”近視性脈絡膜新生血管(myopic choroidal neovascularization; 近視性CNV)は、病的近視眼の後極部に発生する脈絡膜由来の新生血管である。近年は脈絡膜由来のみならず網膜血管由来の新生血管も含めた概念として、国際的に「近視性MNV(myopic neovascularization)」の呼称が用いられるようになっている。6)
加齢黄斑変性に次いで脈絡膜新生血管の2番目に多い原因であり、50歳以下の脈絡膜新生血管では最大の原因疾患である。病的近視患者全体の約10%に生じる。7)
強度近視は等価球面度数−6.0 D以下または眼軸長26.5 mm以上と定義される。病的近視はびまん性萎縮以上の萎縮性変化を眼底に有するか、後部ぶどう腫を有する眼と定義される(META-PM分類、2015年)。10)
近視性MNVはGass分類のtype 2 CNV(CNVがRPE上に存在)であることがほとんどである。比較的小型で滲出性変化も軽度であることが多い。
- 近視性MNVは強度近視眼の5〜11%に生じる
- 8年の経過観察で、MNV既往のない病的近視患者の約6%が発症する
- 片眼にMNV既往がある患者では約35%が僚眼にも発症する
- 50歳未満に限るとMNVの約6割が近視性MNVである7)
- 病的近視は矯正視力0.1以下の視覚障害の13%を占め、緑内障に次ぐ第2位の失明原因である
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”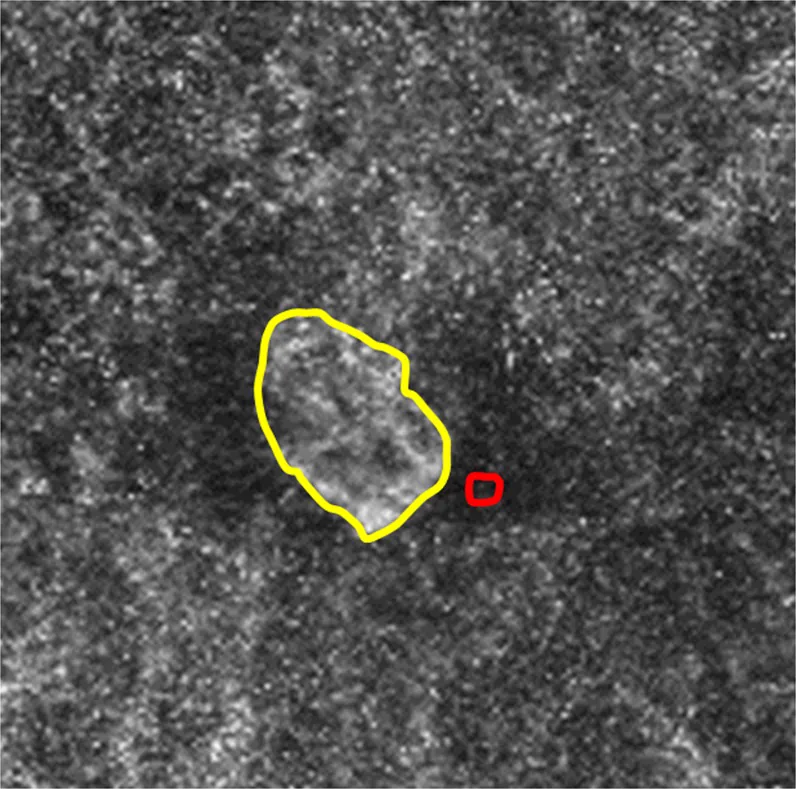
近視性MNVが中心窩に及ぶ場合、以下の症状を呈する。type 2 CNVのため滲出が網膜外層に直接作用し、症状が早めに出現し急速に進行する。6)
- 変視症:直線が歪んで見える。近視患者における変視症の新たな出現は近視性MNVを疑う重要な徴候である。近視性牽引黄斑症を合併する症例では歪視の増悪に気づきにくい場合がある。6)
- 中心暗点:視野の中心部に暗い点が出現する。
- 視力低下:病変が中心窩に進展すると急速に進行する。CNVが退縮しても瘢痕が中心窩に存在すれば不可逆性の視力低下となる。
黄斑領域外に位置する場合は無症状のこともある。患者の自覚症状の訴えに注意深く対応することが重要である。6)
近視性MNVは活動期・瘢痕期・萎縮期の3期に分類される。
瘢痕期・萎縮期
Fuchs斑:MNV退縮後にRPEと基底膜の過形成からなる色素沈着を伴った瘢痕病巣を形成する。
近視性MNV関連黄斑部萎縮:長期経過で比較的急速に拡大し、高度の視力障害に至る。Bruch膜の断裂拡大と色素上皮・脈絡毛細血管板・網膜外層の萎縮として観察される。5年以上で88.9%、10年で96.3%が矯正視力0.1以下。12)
OCTアンギオグラフィーでは、活動期は「レース状のネットワーク・広い吻合・病変周囲の低輝度ハロー」を呈し、静止期は「長い線状の成熟血管・稀な吻合(枯れ木様外観)」となる。活動期以外でも内部血流は高頻度で保たれる(活動期100%、瘢痕期約80%、萎縮期約90%)。ただしOCTAはMNVの活動性評価には向かない。6)
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”近視性MNVの発生には、Bruch膜の機械的断裂と脈絡膜循環障害の2つの機序が関与すると考えられている。
眼軸の進行性延長により脈絡網膜の伸展・菲薄化が生じる。
- Bruch膜の断裂(lacquer cracks):機械的断裂部位がMNVを伴う結合組織の足場となる
- 脈絡膜循環障害:脈絡毛細血管板の閉塞・消失に伴い、VEGFの産生が促進される
- patchy atrophyとlacquer cracksがMNV発症の予測因子である7)
- 局所的な脈絡網膜萎縮:特に中心窩周囲1乳頭径範囲の萎縮
- lacquer cracks:Bruch膜の線状亀裂。CNV発症OR 2.56
- ドーム状黄斑(dome-shaped macula; DSM):CNV発症のオッズ比が4.95と高い5)
- 後部ぶどう腫:高度近視の存在自体がリスク
- 長い眼軸長:近視性黄斑症の進行リスク因子
- 女性:近視性網脈絡膜萎縮病変の有病率がオッズ比3.29倍高い
強度近視眼のすべてに近視性MNVが生じるわけではない。発症率は5〜11%程度であり、lacquer cracksやpatchy atrophyが存在する眼で特にリスクが高い。7) 定期的な眼科検査で早期発見することが重要である。
4. 診断と検査方法
Section titled “4. 診断と検査方法”近視性MNVの診断には病的近視に伴う眼底変化とMNVの存在確認が必要である。6) 単純型黄斑部出血との鑑別が最重要であり、MNVの存在が確認できない症例への抗VEGF薬療法は推奨されない。6)
フルオレセイン蛍光眼底造影(FA)
Section titled “フルオレセイン蛍光眼底造影(FA)”ガイドラインで最も重視される検査。6)
- 近視性MNVはFA早期から明瞭な過蛍光を示し、活動性のあるMNVでは中期から後期にかけて蛍光漏出を認める
- 検眼鏡所見やOCTではっきりしない病変も検出可能
- 単純型黄斑部出血では蛍光ブロック(低蛍光)としてのみ観察され、過蛍光を伴わない → 鑑別に決定的
- 判断に迷う場合は積極的にFAを施行すべきである6)
光干渉断層計(OCT)
Section titled “光干渉断層計(OCT)”- 活動期:RPE上のドーム状高反射隆起病巣。周囲に網膜下液・フィブリン析出6)
- 瘢痕期:RPEによる囲い込み(encapsulation)の高反射ライン。囲い込みの明瞭性がMNV活動性評価に非常に有用6)
- 再燃時:ラインが不明瞭化(前回OCT画像との比較が重要)6)
- 単純型黄斑部出血との鑑別:OCTではHenle線維層に沿った高反射として観察される6)
- OCTのみでの鑑別が困難な場合はFAが必須6)
OCTアンギオグラフィー(OCTA)
Section titled “OCTアンギオグラフィー(OCTA)”- 非侵襲的に血流の有無を評価可能6)
- MNVの同定(単純型黄斑部出血との鑑別)に有用6)
- 感度90.48%、特異度93.75%との報告がある3)
- Angio-Bモードで構造OCTでは検出困難な早期MNVの検出が可能3)
- 活動性の評価には向かない(瘢痕期・萎縮期でも内部に血流シグナルを示すため)6), 14)
IA(インドシアニングリーン蛍光眼底造影)
Section titled “IA(インドシアニングリーン蛍光眼底造影)”FAF(眼底自発蛍光)
Section titled “FAF(眼底自発蛍光)”- 黄斑部萎縮は低蛍光として明瞭に描出されるため、診断および拡大の評価にFAFが有用6)
- MNV安定後の経過観察に推奨6)
近視性MNVと鑑別が必要な疾患を以下に示す。
| 鑑別疾患 | 鑑別のポイント |
|---|---|
| 単純型黄斑部出血 | FAで蛍光漏出なし(蛍光ブロックのみ)。OCTではHenle線維層に沿った高反射。出血は2〜3か月で自然吸収6), 15) |
| 加齢黄斑変性 | ドルーゼン・RPE剥離を伴う。MNVが大型で滲出性変化が強い |
| 点状脈絡膜内層症(PIC) | 近視眼の若年女性に好発。後極部に多発する小型(500μm以下)の境界明瞭な黄白色病巣。炎症に伴う脈絡膜肥厚6) |
| 多巣性脈絡膜炎(MFC) | PICの類縁疾患6) |
| Dome-shaped maculaに伴うMNV | OCTで黄斑部の内方への凸状突出。MNVを伴わなくても滲出性変化あり6) |
| 傾斜乳頭症候群(下方ぶどう腫) | 下方ぶどう腫エッジにMNVが発生しうる6) |
5. 標準的な治療法
Section titled “5. 標準的な治療法”抗VEGF薬硝子体内注射(第一選択)
Section titled “抗VEGF薬硝子体内注射(第一選択)”多施設前向き無作為化比較試験で有効性が唯一証明されている治療法である。6)
2024年8月現在の承認薬(日本):ラニビズマブ(ルセンティス®)およびそのバイオシミラー、アフリベルセプト(アイリーア®)。6)
Glachsら(2024)のネットワークメタ解析(34研究、2,098眼)では、抗VEGF薬は6か月以内に無治療群比+14.1文字(95% CI 10.8〜17.4)、PDT群比+12.1文字(95% CI 8.3〜15.8)の視力改善を示した(いずれもp<0.0001)。1)
投与レジメン:
- 導入期1回投与のみ+以後PRN法(1+PRN)が標準6), 11)
- 3+PRNとの間に視力改善の有意差なし。1+PRN群の方が注射回数が少ない(12か月で1.8回 vs 3.2回)1)
Cheung 2017 国際コンセンサスの治療原則:11)
- 近視性MNVに対して遅滞なく抗VEGF薬療法を行う
- 抗VEGF薬療法が不可能な場合はPDTを考慮(同程度の視力予後は期待できない)
- 導入期投与は1回のみで以後PRN法
- OCTで網膜下液・視力低下・FAでの蛍光漏出があれば再投与を考慮
- MNVが安定すれば最大3か月まで投与間隔を延長11)
主要臨床試験:
- MYRROR試験:アフリベルセプトの多施設RCT。有意な視力改善を証明。8)
- RADIANCE試験:ラニビズマブの多施設RCT。有効性を実証。9)
薬剤間比較:
ベバシズマブ・ラニビズマブ・アフリベルセプトの間で視力改善に有意差は認められていない。1) アフリベルセプトは中心網膜厚の減少がより大きいが、視力への影響に差はない。1)
その他の治療法
Section titled “その他の治療法”- 光線力学療法(PDT):抗VEGF薬に比べて視力改善効果は劣る。1) 長期的には黄斑萎縮増悪の可能性。保険適用なし。6)
- トリアムシノロンアセトニド硝子体内注射:抗VEGF薬に劣り、眼圧上昇や白内障進行のリスクあり。1)
- レーザー光凝固:ランオフ現象によりMNV再発を誘発する可能性。現在では推奨されない。
- 活動性MNVでは1〜3か月間隔でOCTと眼底検査を実施6)
- MNV安定後は数か月〜1年の間隔で経過観察6)
- 再発確認はOCT中心。MNV拡大・新規MNVが疑われればOCTA施行6)
- 活動性評価にFAは有用だが侵襲が高いため検査間隔・全身状態を考慮6)
- 黄斑部萎縮の評価にはFAFが有用6)
- 若年者・小型MNVでは瘢痕形成が小さく予後良好。発症後できるだけ早期の積極的介入が重要6)
1回投与+必要時再投与(1+PRN)が標準レジメンであり、12か月で平均1.8回との報告がある。1) 加齢黄斑変性に比べて必要注射回数は一般に少ない。ただし再発や萎縮の拡大に対する長期経過観察は不可欠であり、早期の再治療が推奨される。6)
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”Bruch膜断裂と創傷治癒反応
Section titled “Bruch膜断裂と創傷治癒反応”眼軸延長に伴う脈絡膜萎縮とBruch膜の弾性線維減少により、Bruch膜が機械的に断裂しlacquer cracksを生じる。この断裂部位を足場として創傷治癒反応としてのMNVを伴う結合組織が網膜下へ増殖する。patchy atrophyとlacquer cracksがMNV発症の予測因子である。7)
脈絡膜循環障害とVEGF
Section titled “脈絡膜循環障害とVEGF”病的近視眼では脈絡毛細血管板や血管層がほぼ消失し、脈絡膜大血管のみが残存する場合がある。EDI-OCTを用いた検討で、MNVを生じる強度近視眼では脈絡膜が有意に菲薄化していることが報告されている。菲薄化した脈絡膜組織の循環障害がVEGFの産生を促し、異常な血管網の形成につながる。
CNV由来血管(短後毛様動脈)
Section titled “CNV由来血管(短後毛様動脈)”swept source OCTとICGAを用いた検討で、短後毛様動脈が近視性MNV近傍で強膜を貫通しMNVに近接する所見が75.0%で確認されている。短後毛様動脈由来血管がMNVに還流していると考えられる症例は、活動期100%・瘢痕期87.9%・萎縮期73.8%と高頻度である。
近視性牽引黄斑症との合併
Section titled “近視性牽引黄斑症との合併”近視性MNVと近視性黄斑分離症(MF)の合併は稀だが重要な臨床的意義を持つ。
Sayanagiら(2023)は、近視性MNV周囲にMFを伴う3症例を報告した。2) 全例で経過観察中に黄斑部網膜剥離が増悪した。MNVによる網膜下液が向心性・遠心性の牽引バランスを破壊し、MFの進行を促進する可能性が示唆されている。
Pereiraら(2023)は、近視性黄斑分離症を伴う病的近視眼に発生したMNVが全層黄斑円孔の原因となった症例を報告した。4) MNVの滲出による機械的挙上が、脆弱化した中心窩のMüller細胞に応力を加え、裂孔形成に至ったと推察されている。
7. 最新の研究と今後の展望(研究段階の報告)
Section titled “7. 最新の研究と今後の展望(研究段階の報告)”近視性黄斑症の長期自然史
Section titled “近視性黄斑症の長期自然史”Carlàら(2025)は1,228眼の欧州コホートを対象とした長期研究で、近視性黄斑症の57%が10年以上の経過観察中に進行したことを報告した。5) 限局性萎縮を有する眼の47%が黄斑部萎縮に進行し(OR 4.21)、活動性のMNVは15%の眼に平均4.5年で発症した。MNVの発生は視力低下(p=0.001)および黄斑部萎縮への進展(OR 5.81)と有意に相関した。
抗VEGF薬の長期課題
Section titled “抗VEGF薬の長期課題”抗VEGF薬により短期的には良好な視力改善が得られるが、5年以上の長期成績は短期成績に劣る。無治療自然経過では5年で89%・10年で96%が小数視力0.1以下となる。12) 5年間のラニビズマブ投与では視力維持の有用性が報告されている。13) 萎縮の進展を抑制する治療法の開発が今後の課題である。
OCTAによる早期診断の可能性
Section titled “OCTAによる早期診断の可能性”OCT-A Angio-Bモードは、構造OCTや蛍光造影では検出困難な早期のMNVを検出できる可能性がある。3) 非侵襲的かつ高感度な検査法として、強度近視眼のスクリーニングへの応用が期待される。
8. 参考文献
Section titled “8. 参考文献”- Glachs L, Embacher S, Berghold A, et al. Treatment of myopic choroidal neovascularization: a network meta-analysis and review. Graefes Arch Clin Exp Ophthalmol. 2024;262:1693-1722.
- Sayanagi K, Hara C, Fukushima Y, et al. Three cases of macular retinal detachment exacerbated during follow-up with myopic foveoschisis around myopic choroidal neovascularization. Am J Ophthalmol Case Rep. 2023;32:101899.
- Rico S, Sher I, Lavinkfy F, et al. Optical coherence tomography Angio-B mode for early detection of myopic choroidal neovascularization and treatment with Bevacizumab. Am J Ophthalmol Case Rep. 2024;34:102041.
- Pereira A, Ballios BG, Sarraf D, Yan P. Full-thickness macular hole due to choroidal neovascularization in the setting of pathologic myopia. J VitreoRetinal Dis. 2023;7(1):65-69.
- Carlà MM, Boselli F, Giannuzzi F, et al. Longitudinal Progression of Myopic Maculopathy in a Long-Term Follow-Up of a European Cohort: Imaging Features and Visual Outcomes. Ophthalmol Retina. 2025;9(8):774-786. doi:10.1016/j.oret.2025.02.015. PMID:40010496.
- 大野京子, 三宅正裕, 柳靖雄, ほか. 近視性黄斑部新生血管の診療ガイドライン. 日眼会誌. 2024;128:719-729.
- Ohno-Matsui K, Yoshida T, Futagami S, et al. Patchy atrophy and lacquer cracks predispose to the development of choroidal neovascularisation in pathological myopia. Br J Ophthalmol. 2003;87:570-573.
- Ikuno Y, Ohno-Matsui K, Wong TY, et al; MYRROR Investigators. Intravitreal aflibercept injection in patients with myopic choroidal neovascularization: the MYRROR Study. Ophthalmology. 2015;122:1220-1227.
- Wolf S, Balciuniene VJ, Laganovska G, et al; RADIANCE Study Group. RADIANCE: a randomized controlled study of ranibizumab in patients with choroidal neovascularization secondary to pathologic myopia. Ophthalmology. 2014;121:682-692.
- Ohno-Matsui K, Kawasaki R, Jonas JB, et al; META-PM Study Group. International photographic classification and grading system for myopic maculopathy. Am J Ophthalmol. 2015;159:877-883.
- Cheung CMG, Arnold JJ, Holz FG, et al. Myopic choroidal neovascularization: review, guidance, and consensus statement on management. Ophthalmology. 2017;124:1690-1711.
- Yoshida T, Ohno-Matsui K, Yasuzumi K, et al. Myopic choroidal neovascularization: a 10-year follow-up. Ophthalmology. 2003;110:1297-1305.
- Onishi Y, Yokoi T, Kasahara K, et al. Five-year outcomes of intravitreal ranibizumab for choroidal neovascularization in patients with pathologic myopia. Retina. 2019;39:1289-1298.
- Miyata M, Ooto S, Hata M, et al. Detection of myopic choroidal neovascularization using optical coherence tomography angiography. Am J Ophthalmol. 2016;165:108-114.
- Goto S, Sayanagi K, Ikuno Y, et al. Comparison of visual prognosis between natural course of simple hemorrhage and choroidal neovascularization treated with intravitreal bevacizumab in highly myopic eyes: a 1-year follow-up. Retina. 2015;35:429-434.
