FA(フルオレセイン造影)
分子量:332
血漿蛋白結合率:約80%→血管外漏出が多い
励起/蛍光波長:465-490nm / 520-530nm(可視光域)
主な描出対象:網膜血管・RPE障害・内層CNV
RPE透過性:低い→脈絡膜の描出困難
代謝・排泄:腎排泄

インドシアニングリーン蛍光眼底造影(Indocyanine Green Angiography; ICGA)は、ICG色素を静脈注射して眼底を近赤外線で撮影する蛍光造影検査である。フルオレセイン蛍光造影(FA)では描出が困難な脈絡膜血管を詳細に観察できる。
ICG(インドシアニングリーン)は暗緑青色の水溶性色素で、分子量は約775(FAに使用するフルオレセインの約332と比べて約2.3倍)。以下の光学特性が脈絡膜造影に有利に働く。
FAが励起光465〜490nm・蛍光光520〜530nmの可視光域を使うのに対し、ICGAの近赤外線はRPEメラニンに吸収されにくい。この波長特性が、FAでは描出困難なRPE下・脈絡膜病変の可視化を可能にする。
ICGは投与後、血漿中濃度が指数関数的に減少する。半減期は約3〜4分と短く、肝実質細胞に取り込まれて代謝されることなく胆汁中へ排泄される(腸肝循環なし)。FAが腎排泄であるのとは代謝経路が異なる。腎機能低下患者でもある程度使用できる一方、肝機能低下では排泄遅延が生じるため慎重を要する。
FAとICGAの主な違いを以下に示す。
FA(フルオレセイン造影)
分子量:332
血漿蛋白結合率:約80%→血管外漏出が多い
励起/蛍光波長:465-490nm / 520-530nm(可視光域)
主な描出対象:網膜血管・RPE障害・内層CNV
RPE透過性:低い→脈絡膜の描出困難
代謝・排泄:腎排泄
ICGA(インドシアニングリーン造影)
分子量:775
血漿蛋白結合率:約98%→血管外漏出が少ない
励起/蛍光波長:785nm / 835nm(近赤外線域)
主な描出対象:脈絡膜血管・RPE下病変・BVN
RPE透過性:高い→脈絡膜を鮮明描出
代謝・排泄:肝取り込み→胆汁排泄(腸肝循環なし)
1960年代にFoxとWoodがICGを眼科領域に初めて応用した。1970年代に蛍光眼底造影への使用が報告され、1990年代にデジタル技術の普及により臨床応用が本格化した。
FAは網膜血管障害・RPE機能評価に優れ、ICGAは脈絡膜血管・RPE下病変の描出に優れる。PCVや脈絡膜血管過透性を伴う疾患(中心性漿液性脈絡網膜症など)ではICGAが必須となる。両者を同時施行することも多い。
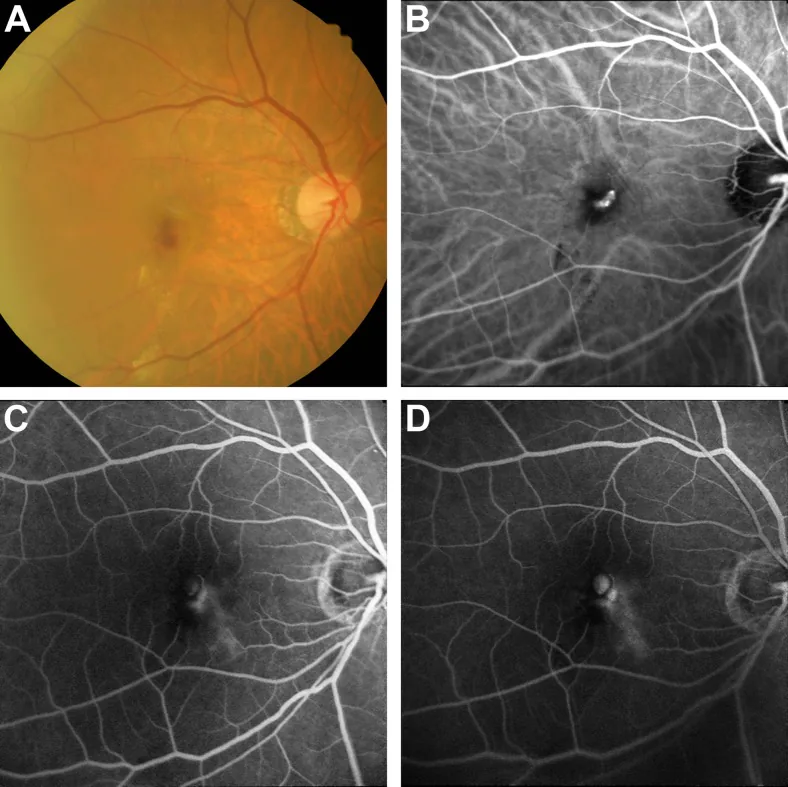
加齢黄斑変性の各サブタイプでICGAは異なる役割を担う。
ICGAはポリープ状脈絡膜血管症の確定診断のゴールドスタンダードである。2) 典型的なnAMDとポリープ状脈絡膜血管症/AT1(pachychoroid neovasculopathy type 1)の鑑別で最も検証された方法でもある。4)
脈絡膜血管過透性亢進の範囲と程度を描出し、光線力学的療法(PDT)の照射部位決定に有用。拡張した内層脈絡膜血管(pachyvessels)の描出にも優れる。
ICGAで特徴的な充盈パターン(早期強い過蛍光→後期洗い出し)を示す。
ラッカークラック周囲の脈絡膜新生血管をFAより鮮明に描出できる。
FAより脈絡膜循環を良好に評価。巨細胞性動脈炎(GCA)による眼虚血でも有用。5)
ICGAの撮影機器には主に以下の2種がある。
いずれの機器でも、FA(励起488nm)との同時撮影が可能なものが多い。
ICGAを安全に施行するため、以下の前準備を行う6)。
ICG製剤(日本ではオフサグリーン®など)を用いる。
散瞳はミドリンP®などで施行し、十分な散瞳(瞳孔径6mm以上が望ましい)を確保する。
ICGAでは撮影時相ごとに描出される血管構造が異なる。主な造影時相を下表に示す。
| 時相 | 経過時間 | 主な描出構造 |
|---|---|---|
| 早期相 | 〜2分 | 脈絡膜動脈・脈絡毛細血管板の充盈開始 |
| 中間相 | 2〜10分 | 脈絡膜新生血管・異常血管の描出 |
| 後期相 | 10〜30分 | 色素貯留・組織染の評価。病変部の残存蛍光で鑑別 |
早期相では短後毛様動脈から充盈が始まり、脈絡膜毛細血管板へ流入する。中間相では均一な脈絡膜背景蛍光が得られ、後期相では背景蛍光が減衰して大血管がシルエットとして浮かび上がる。残存蛍光(staining)は病変部の鑑別に有用である。
ICGは時間経過とともに指数関数的に蛍光強度が減弱するため、光量設定には注意を要する。撮影開始時は強めに設定し、蛍光が確認できたら弱め、後期相に向けて再度上げるのが一般的である。
FAとICGAを同時施行する際はFA→ICGの順次投与またはほぼ同時投与が行われる。SLO方式では1台の機器で両造影を同時撮影できる。
造影剤を静脈注射する際の軽い刺痛はあるが、検査自体は基本的に無痛で行える。散瞳薬の点眼が必要であり、散瞳後は数時間、まぶしさや手元のぼやけが生じる。車・バイクの運転は検査当日は控える必要がある。
正常眼では、早期相に脈絡膜動脈→静脈→毛細血管板の順に充盈し、中間相で均一な背景蛍光が得られる。後期相では背景蛍光が徐々に減弱し、大血管のシルエットが浮かび上がる。FAで観察される透過蛍光(window defect)はICGAでは生じない。ICGはRPEを透過して脈絡膜血管まで到達するためである。
低蛍光所見
過蛍光所見
色素貯留(staining):後期まで持続する高蛍光。瘢痕・Bruch膜変化。
組織染(tissue staining):血管外への緩徐な漏出と組織への蓄積。
血管透過性亢進:パキコロイドに伴う脈絡膜血管の過蛍光。中心性漿液性脈絡網膜症・ポリープ状脈絡膜血管症で典型的。
形態異常
ポリープ状拡張:ポリープ状脈絡膜血管症に特徴的な早期結節状高蛍光。後期に洗い出しを示す。
異常血管網(BVN):ポリープ状脈絡膜血管症に先行するbranching vascular networkの描出。
低蛍光・過蛍光の鑑別を体系的に整理する。
| 分類 | 機序 | 代表疾患 |
|---|---|---|
| 低蛍光:蛍光遮断 | 厚い出血・白斑・色素沈着がICGを遮断 | 黄斑出血・硬性白斑・脈絡膜母斑 |
| 低蛍光:充盈遅延 | 脈絡膜動脈の灌流低下 | GCA・三角症候群・高安動脈炎 |
| 低蛍光:choriocapillaris non-perfusion | 脈絡膜毛細血管板の非充盈 | APMPPE・MEWDS・VKH急性期 |
| 低蛍光:脈絡膜萎縮 | 脈絡膜実質の菲薄化 | 病的近視・光凝固後瘢痕・AMD晩期 |
| 過蛍光:血管透過性亢進 | 拡張した脈絡膜血管からの漏出 | CSC・PCV周囲のdilated choroidal vessels |
| 過蛍光:ポリープ状拡張 | BVNからの結節状拡張 | PCV(早期結節状高蛍光→後期洗い出し) |
| 過蛍光:脈絡膜新生血管 | MNVへのICG蓄積 | AMD Type 1・Type 2・Type 3 |
| 過蛍光:staining/tissue staining | 組織への色素蓄積 | 瘢痕・Bruch膜変化・ドルーゼン |
Bruch膜への脂質蓄積により、ICGが適切にRPEに到達できない部位が生じる。この部位はICGAの後期相で局所的な低蛍光スポット(ASHS-LIA: area of decreased late-phase hypofluorescence after ICG angiography)として観察される。4) 加齢黄斑変性・ポリープ状脈絡膜血管症の病態理解において重要な所見である。
ICGAは比較的安全な検査だが、静脈注射薬であるため副作用が生じることがある。Hope-Ross(1994)の報告によれば全副作用頻度は約0.15%、重篤なアナフィラキシーショックは約0.05%である。主な副作用の頻度を下表に示す。
| 重症度 | 症状 | 頻度(目安) |
|---|---|---|
| 軽微 | 悪心・嘔吐・熱感 | 約0.15% |
| 中等度 | 蕁麻疹・発熱・血圧変動 | 約0.2% |
| 重篤 | アナフィラキシーショック | 約0.05% |
参考として、FAでは死亡リスクが約20万人に1人と報告されており、5) ICGAも同程度のリスク管理が必要である。
検査終了後も血圧測定を行い、患者の状態を確認してから退室させる6)。副作用を経験した場合は、副作用報告を行うことが推奨される6)。
ICG製剤(オフサグリーン®など)にはヨウ化ナトリウムが安定剤として含まれている。ヨウ素アレルギーの既往がある場合はICGAの絶対禁忌であり、施行前には必ずアレルギー歴を確認する。ヨウ素を含まないインフラシアニングリーンへの変更を検討する場合もある。
ICGは分子量775の両親媒性シアニン色素である。以下に、ICGの薬理学的特性とFAとの比較を示す。
異常血管網(BVN)はOCTAで高血流として検出されるが、ポリープ病変の検出においてはICGAが優位である。2) ポリープ内での血流が比較的低速であること、ICGの血管内滞留性の高さにより時間をかけて充盈が鮮明化することが、後期相でのポリープ描出を可能にする。
TelCaps(Telangiectatic Capillary anomalies)は、ICGに対する高い親和性を持つ大型毛細血管異常(直径150μm以上)である。1) FAやOCTAでは検出が困難な病変で、抗VEGF治療抵抗性の黄斑浮腫の一因として注目されている。
PerrinとPorter(2024)は、TelCapsのICGAガイド下光凝固(TelCaps PDT)をケースシリーズとして報告した。1) 糖尿病黄斑浮腫13眼において、TelCaps標的の光凝固を施行したところ2年間にわたり有意な改善が得られた。現在、フランスで270名を対象とした前向きRCTが進行中である。
ICGAが施行できない施設でのポリープ状脈絡膜血管症診断を可能にする取り組みが進んでいる。
Cheungら(2025)は、OCTベースの非ICGA診断基準のAUCが0.90であることを報告した。4) この基準はOCTによるパキコロイド所見(脈絡膜肥厚・中心性漿液性脈絡網膜症様変化・BVN相当所見)を組み合わせたものである。
ただし、現時点でICGAの代替とはなっておらず、ポリープ状脈絡膜血管症の確定診断にはICGAが依然として必須である。
OCT画像の機械学習解析を用いたポリープ状脈絡膜血管症と加齢黄斑変性の自動鑑別が研究されており、2) 診断支援ツールとしての実用化が期待されている。
ポリープ状脈絡膜血管症の確定診断にはICGAが依然として必要である。OCTAはBVNの検出や血流評価に優れるが、ポリープ病変の検出感度ではICGAが優位であると報告されている。2) 非ICGA診断基準の開発は進んでいるが(AUC 0.90)、現時点では標準的なポリープ状脈絡膜血管症診断にICGAは不可欠である。