外網膜主体型

白点症候群
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 白点症候群とは
Section titled “1. 白点症候群とは”白点症候群(white dot syndromes)は、1977年にGassが命名した概念であり、眼底に白色または黄白色の斑点状病変を多発する一群の炎症性疾患を指す。対象疾患は研究者によって定義が異なるが、現在では外網膜・RPE・脈絡膜毛細血管板・脈絡膜を主座とする非感染性の特発性炎症性疾患群として広く用いられる1)。
ぶどう膜炎診療ガイドライン(日眼会誌 2019;123(6):635-696)では、後部ぶどう膜炎の病型分類として APMPPE・MEWDS・PIC・多発性脈絡膜炎・バードショット網脈絡膜症・蛇行状脈絡膜炎・AZOOR がそれぞれ独立した疾患として記載されており、「白点症候群」という包括的名称を用いる場合はこれらを総括する概念として扱われる2)。
分類の考え方
Section titled “分類の考え方”近年のマルチモーダルイメージング(OCT-A を含む)の進歩により、白点症候群は病変の主座となる層によって以下の3群に分類されるようになっている1)。
脈絡膜毛細血管板主体型
脈絡膜間質主体型
Birdshot 網脈絡膜症
- 脈絡膜ストロマへのリンパ球浸潤が一次病変
- OCT-A では Haller 層に flow void、初期は choriocapillaris 温存
- 慢性進行性で HLA-A29 との強い関連
さらに、AZOOR complex という概念も提唱されており、MEWDS・AZOOR・PIC・MFC・AMN・AIBSE・AAOR を遺伝的自己免疫/炎症機序の共通基盤を持つ連続体として統合的に理解する見方がある3)。
日本での疫学
Section titled “日本での疫学”日本眼炎症学会統計では、白点症候群各疾患のぶどう膜炎全体に占める割合は以下のとおりである2)。
| 疾患 | ぶどう膜炎全体に占める割合 |
|---|---|
| MEWDS | 約1〜2%(国内報告) |
| APMPPE | 稀(年間発症率は明確な統計なし) |
| PIC | 稀 |
| 蛇行状脈絡膜炎 | 約0.3% |
| バードショット網脈絡膜症 | 稀(白人に多く日本では極めてまれ) |
| AZOOR | まれ(近年報告数増加) |
2. 共通する臨床像
Section titled “2. 共通する臨床像”各疾患の症状は異なるが、以下の臨床的特徴が白点症候群群に共通する1, 2)。
自覚症状の共通パターン
Section titled “自覚症状の共通パターン”- 視力低下:程度は軽度(MEWDS・AZOOR)から高度(蛇行状脈絡膜炎・PIC の CNV 合併)まで幅広い
- 光視症(フォトプシア):外網膜・視細胞の障害を反映する最も一般的な症状
- 暗点・視野欠損:病変部位に対応した傍中心または中心暗点が多い
- 変視症:黄斑病変または CNV 合併時に生じる
前眼部炎症の有無
Section titled “前眼部炎症の有無”| 疾患群 | 前房・硝子体炎症 |
|---|---|
| MEWDS・APMPPE・PIC | 通常なし(APMPPE は軽度あり) |
| MFC(MFCwP) | 前房炎症+硝子体炎あり(PIC との鑑別点) |
| Birdshot | 前房炎症なし〜軽微、硝子体炎あり |
| 蛇行状脈絡膜炎 | 前房炎症・硝子体炎は通常軽微 |
| AZOOR | 通常なし |
3. 鑑別の考え方
Section titled “3. 鑑別の考え方”年齢・性別・片眼 vs 両眼・再発性による整理
Section titled “年齢・性別・片眼 vs 両眼・再発性による整理”若年女性・片眼・自然軽快
若年〜中年女性・両眼・CNV リスク
若年〜中年・両眼・急性発症
- 20〜30代(平均25歳)に好発、性差なし
- 両眼性・急性・自然軽快傾向
- 脳血管炎合併に注意(神経症状の出現時は緊急精査)
中高年・両眼・慢性進行
Birdshot・蛇行状脈絡膜炎
- Birdshot:40〜60代、やや女性多い
- 蛇行状:30〜50代、男性やや多い
- 両疾患とも慢性・再発性・長期免疫抑制が必要
- Birdshot の HLA-A29 陽性率(白人):80〜98%
鑑別フローチャート
Section titled “鑑別フローチャート”眼底に白点状病変 │ ├─ 片眼性? │ ├─ YES → MEWDS・AZOOR・AMN を考慮 │ │ ↳ FA で初期過蛍光 → MEWDS │ │ ↳ 眼底ほぼ正常・ERG 異常 → AZOOR │ └─ NO(両眼性) │ ├─ 急性発症・後極部大型白斑? │ └─ YES → APMPPE(FA 蛍光逆転現象を確認) │ ├─ 後極部小病変・近視女性・硝子体炎なし? │ └─ YES → PIC を考慮(CNV 検索:OCTA 必須) │ ├─ 小病変・硝子体炎あり・周辺部にも病変? │ └─ YES → MFC(MFCwP)を考慮 │ ├─ 乳頭周囲から蛇行状に進展・男性多め? │ └─ YES → 蛇行状脈絡膜炎(結核除外が最優先) │ └─ 後極部散弾状病変・中高年・HLA-A29? └─ YES → Birdshot 網脈絡膜症4. 主な疾患の比較
Section titled “4. 主な疾患の比較”メイン比較表:7疾患マトリクス
Section titled “メイン比較表:7疾患マトリクス”| 項目 | APMPPE | MEWDS | PIC | MFC(MFCwP) | Birdshot | 蛇行状脈絡膜炎 | AZOOR |
|---|---|---|---|---|---|---|---|
| 好発年齢 | 20〜30代(平均25歳) | 20〜50代 | 18〜40代(平均36歳) | 平均30歳 | 40〜60代 | 30〜50代 | 30代半ば中心 |
| 性別 | 性差なし | 女性優位(1:4) | 女性優位(約90%) | 女性優位(白人女性多) | やや女性多 | 男性やや多 | 女性優位(約75%) |
| 片眼/両眼 | 両眼性多 | 片眼性(95%以上) | 両眼性多(80%) | 両眼性 | 両眼性 | 両眼性 | 片眼→両眼進行(最終的に76%両眼) |
| 主な症状 | 視力低下・中心暗点・変視症 | 視力低下・光視症・霧視 | 暗点・視力低下・変視症 | 飛蚊症・視力低下・光視症 | 視力低下・夜盲・色覚異常 | 視力低下・傍中心暗点 | 光視症・視野欠損(眼底ほぼ正常) |
| 眼底白斑の特徴 | 後極部に大型クリーム色白斑(1/4〜1/2 乳頭径) | 後極部〜赤道部に淡い灰白色多発小斑(100〜200μm) | 後極部に黄白色小斑(100〜300μm)、12〜25個 | 後極部〜周辺に黄灰色斑(45〜350μm)、硝子体炎伴う | 後極部〜赤道部に散弾状クリーム色斑(1/4〜1/2 乳頭径) | 乳頭周囲から蛇行状に進展する地図状灰黄色病変 | 眼底ほぼ正常(急性期)、後期に外層萎縮 |
| OCT 所見 | ellipsoid zone 乱れ+外網膜高反射、回復後一部萎縮残存 | ellipsoid zone 著明乱れ・消失(急性期)→ 回復 | RPE 下高反射隆起+EZ 断裂(5段階進化) | RPE 下高反射+EZ 断裂(PIC に類似) | 脈絡膜病変・嚢胞様黄斑浮腫、EZ 消失が予後不良 | 活動期:外網膜高反射・網膜下液。瘢痕期:RPE 萎縮 | EZ(IS/OS)消失が最重要所見(視野欠損部位と一致) |
| FA 所見 | 早期低蛍光→後期過蛍光(蛍光逆転現象) | 初期から wreath-like(花冠状)過蛍光が持続 | 活動期:動脈期初期過蛍光→後期漏出 | 活動期:早期低蛍光→後期漏出 | 病変過蛍光(漏出なし)+血管漏出・乳頭過蛍光 | 活動期:早期低蛍光→後期過蛍光(漏出) | 通常正常または軽微な異常 |
| ICGA 所見 | 全相で低蛍光(脈絡膜毛細血管板虚血を直接反映) | 後期低蛍光(白点より広範囲) | 中期低蛍光、臨床下病変の検出に有用 | 早期〜全相低蛍光 | 早期・中期低蛍光→後期等蛍光(初期)→進行期:全相低蛍光 | 全相低蛍光(脈絡膜循環障害を反映) | 通常正常 |
| FAF 所見 | 急性期:低 or 過自発蛍光。寛解期:低自発蛍光 | 急性期:高自発蛍光(過蛍光多)。回復後:正常化 | 活動期:低自発蛍光(hypoAF)、辺縁高自発蛍光ハロー | 活動期:低自発蛍光 | 乳頭周囲の融合性低自発蛍光(73%に認められる) | 活動期:高自発蛍光辺縁+低自発蛍光ハロー。静止期:低自発蛍光 | 帯状の高〜低自発蛍光異常 |
| OCT-A 所見 | Choriocapillaris flow void(FA/ICGAと高い一致率) | Choriocapillaris 原則温存(一部に transient flow void) | Choriocapillaris flow void(炎症病変部位) | Choriocapillaris flow void | Haller 層 flow void(初期)→進行期:全層 flow void | Choriocapillaris flow void(高度) | Choriocapillaris 原則温存 |
| 再発性 | まれ(基本的に単回) | 約10%に再発 | 高い(慢性再発性) | 高い(反復性炎症エピソード) | 高い(慢性・再発寛解繰り返す) | 高い(3ヶ月〜4年間隔で反復) | 多くは6ヶ月以内に安定。一部で進行 |
| CNV 合併率 | まれ | まれ | 40〜76%(高リスク) | 最大60% | 網膜下 CNV:まれ | 最大35% | ほとんどなし |
| HLA 関連 | なし | HLA-B51(予備的報告) | HLA-DR2・HLA-DRB1*15 | IL-10 ハプロタイプ関連 | HLA-A29(白人で80〜98%) | HLA-B7・HLA-A2(関連報告) | なし(免疫学的素因) |
| 治療方針 | 経過観察(自然軽快)、重症:ステロイド | 経過観察、重症:ステロイド短期投与、CNV:抗VEGF | 経過観察(CNVなし)、CNV:抗VEGF+ステロイド、免疫抑制薬 | ステロイド+免疫調節療法、CNV:抗VEGF | ステロイド+ミコフェノール酸モフェチル/アダリムマブ(長期) | ステロイド+免疫抑制薬(アルキル化薬含む)、CNV:抗VEGF | 経過観察、重症:ステロイドパルス |
| 視力予後 | 良好(自然軽快多い) | 良好(再発・CNV で注意) | CNV 合併で不良リスク高 | CNV・黄斑浮腫で不良リスク | 治療なしで10年に16〜22%が視力0.1以下 | 中心窩に及べば不可逆、最大25%の眼で最終視力20/200未満 | 多くは安定。外層障害進行例で不良 |
各疾患の詳細な臨床像
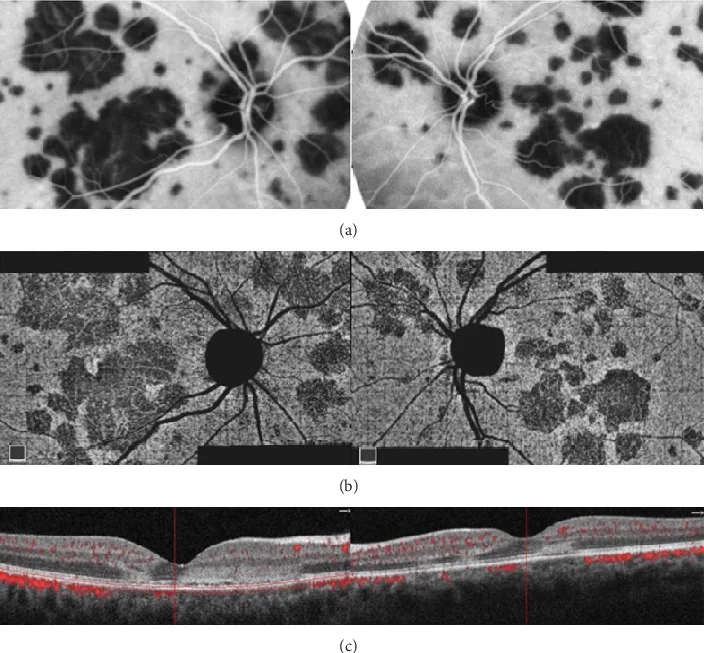
Section titled “各疾患の詳細な臨床像”APMPPE(急性後部多発性斑状色素上皮症)
Section titled “APMPPE(急性後部多発性斑状色素上皮症)”APMPPE は 20〜30 代(平均 25 歳)に好発し、性差はない。脈絡膜毛細血管板の輸入細動脈における閉塞性血管炎が本態と考えられており、ウイルス感染などが誘因として推測されている1, 2)。
前駆症状と経過
- 感冒様症状(インフルエンザ・EB ウイルス・水痘・連鎖球菌感染等)を約半数で認める
- 両眼後極部に 1/4〜1/2 乳頭径のクリーム色円板状白斑が多発する
- 白斑は数日のうちに中心部から消退し始め 7〜12 日で軽い脱色素を残して消失する
- 通常は単回のエピソードで自然軽快する(再発はまれ)
- 視力予後は通常良好だが、重症例や地図状脈絡膜炎に移行した症例では不良となることがある
特有の合併症:脳血管炎(MCAT)
APMPPE と中枢神経血管炎の合併(MCAT: multiple cerebral arterial thrombosis)は重篤な合併症であり、頭痛・発熱・神経症状が出現した場合は緊急で脳 MRI・MRA を施行する必要がある。脳血管炎合併例ではメチルプレドニゾロンパルス療法と神経内科連携が必要となる2)。
placoid chorioretinitis spectrum との関連
APMPPE は PPM(persistent placoid maculopathy)・RPC(relentless placoid chorioretinitis)とともに「placoid chorioretinitis spectrum」を形成し、脈絡膜毛細血管板虚血を共通病態基盤とする5)。
MEWDS(多発消失性白点症候群)
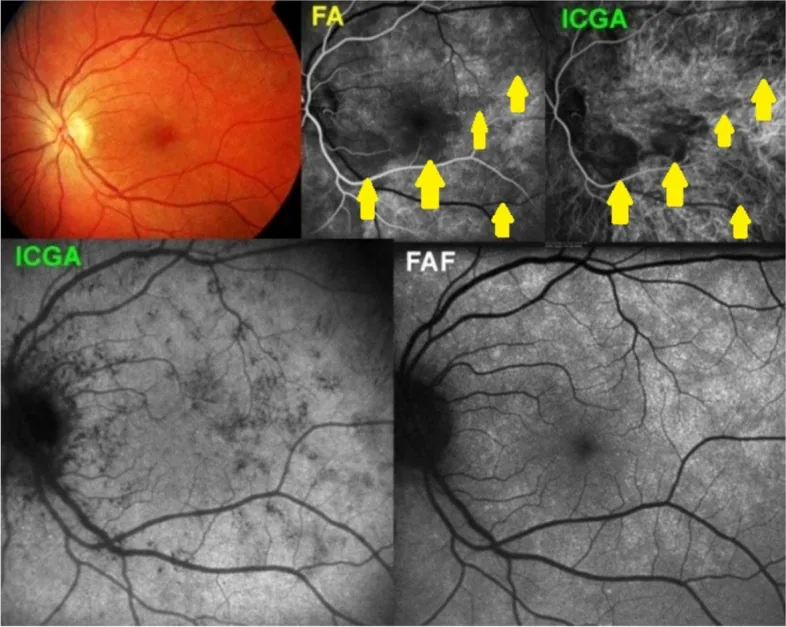
Section titled “MEWDS(多発消失性白点症候群)”MEWDS は 20〜50 代の女性(男女比 1:4)に好発し、片眼性・急性・自然軽快を特徴とする。
特有の臨床像
- 後極部〜赤道部の網膜深層〜RPE レベルに淡い灰白色多発小斑(100〜200 μm)
- foveal granularity(中心窩顆粒状変化):74〜96% の患者で認められ、白点消失後も唯一の残存所見となることがある。近赤外 FAF(NIR-FAF)で特徴的パターンを描出9)
- orange-dot appearance(橙色小点):眼底写真や近赤外線眼底撮影での特徴的所見
- ivory lesion(象牙色病変):眼底後極部の淡いぼかした白色変化
- 感冒様前駆症状が約 50% に先行する
- 年間発症率は 10 万人あたり約 0.22 例、10% に再発例を認める
FA での wreath-like(花冠状)過蛍光
FA 早期からの特徴的な wreath-like(花冠状)過蛍光が MEWDS 診断の要点である。白点病変部は FA 早期から過蛍光になり後期に拡大を認めない。この早期過蛍光は APMPPE の早期低蛍光(蛍光逆転現象)との重要な鑑別点である1, 9)。
AZOOR complex との連続性
MEWDS は視細胞の ellipsoid zone(IS/OS ライン)の一過性破壊が主座であり、AZOOR complex に属する疾患として理解されている。OCT で急性期に ellipsoid zone の乱れ・消失が確認でき、視力回復とともに改善する3)。
PIC(点状内層脈絡膜症)
Section titled “PIC(点状内層脈絡膜症)”PIC は近視(平均 -5D 前後)を有する 18〜40 代の若年女性(約 90%)に好発する。
特有の臨床像
- 後極部のみに限局した 100〜300 μm の黄白色小斑、通常 12〜25 個
- 前房炎症・硝子体炎なし(これが MFC との最重要鑑別点)
- 活動性病変は RPE 下の高反射隆起として OCT で確認できる
- 瘢痕化すると小さな萎縮病変を残す
CNV 合併(40〜76%)が最大の臨床問題
PIC で最も重要な合併症は CNV であり、その合併率は 40〜76% と報告されている7, 8)。CNV は以下の要因で生じやすい:
- 近視性脈絡膜変薄による Bruch 膜脆弱性
- RPE 下炎症による Bruch 膜破壊
- 炎症性サイトカイン(VEGF 等)の局所産生亢進
CNV スクリーニングとして OCT-A が FA より高感度であることが示されており、定期的な OCT-A モニタリングが推奨される。変視症の突然の悪化は CNV 発症のサインであり、速やかな精査が必要となる。
全身疾患との関連
PIC とサルコイドーシスの合併が報告されており、多発性肺病変を有する症例では胸部 CT・血清 ACE・リゾチームの検査を行う。HLA-DR2・HLA-DRB1*15 との関連も報告されている3)。
MFC(多巣性脈絡膜炎、MFCwP)
Section titled “MFC(多巣性脈絡膜炎、MFCwP)”MFC(multifocal choroiditis with panuveitis; MFCwP)は PIC と同一スペクトラム上の疾患であるが、硝子体炎・前房炎症を伴う点が最大の鑑別点である7)。
特有の臨床像
- 後極部だけでなく中間周辺部にも 45〜350 μm の黄灰色斑が多発
- 慢性再発性経過(反復性炎症エピソード)が特徴
- 網膜前膜(epiretinal membrane; ERM) の合併頻度が高く(最大 35%)、長期視力予後を左右する
- 一部の症例では免疫抑制療法なしに炎症をコントロールできない
治療における注意点
MFC は自然軽快しにくく、長期的な免疫調節療法が必要となる症例が多い。ステロイドのみでは不十分な場合にメトトレキサート(MTX)・アザチオプリン(AZA)・ミコフェノール酸モフェチル(MMF)を使用する。CNV 合併時は抗 VEGF 療法と免疫調節療法の二方向性アプローチが重要となる7, 8)。
Birdshot 網脈絡膜症(散弾状脈絡網膜症)
Section titled “Birdshot 網脈絡膜症(散弾状脈絡網膜症)”Birdshot(バードショット)は 40〜60 代の中高年(平均 50 歳代)、やや女性多め(1.5:1)に好発する。白人に多く、HLA-A29 との関連が既知の疾患の中で最も強力な遺伝的関連の一つ(白人で相対リスク 50〜224 倍)である4)。
特有の眼底所見
- 後極部〜赤道部に散弾痕様のクリーム色斑(1/4〜1/2 乳頭径)が左右対称性に多発
- 斑は色素沈着を伴わない瘢痕病巣へと移行する
- 網膜血管炎・乳頭腫脹を合併することがある
特有の機能変化
- 夜盲・色覚異常:早期から出現し、視力低下より先行することがある
- 全視野 ERG の negative type:初期に認められ、進行するにつれ a 波振幅が低下する
- 30Hz フリッカー ERG 遅延:活動性モニタリングの最感度指標であり、視力低下よりも早期に異常を検出できる17)
日本人での注意事項
日本人は HLA-A29 の保有頻度が低いため、HLA-A29 の診断感度が制限される。SUN 2021 分類基準における臨床所見(眼底散弾状病変・前眼部炎症の軽微さ・硝子体炎の存在)を重視した診断が必要となる10)。
長期合併症
蛇行状脈絡膜炎(Serpiginous choroidopathy)
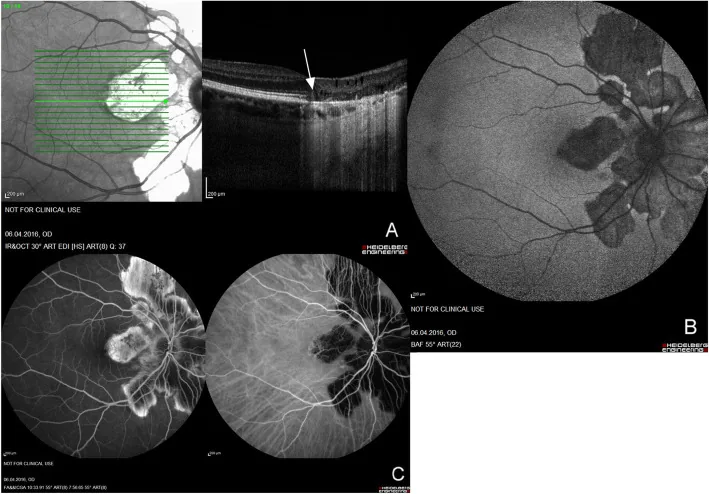
Section titled “蛇行状脈絡膜炎(Serpiginous choroidopathy)”蛇行状脈絡膜炎は 30〜50 代(男性やや多い)の両眼性慢性脈絡膜炎で、乳頭周囲から蛇行状に進展する地図状灰黄色病変が特徴である。
特有の進展パターン
- 視神経乳頭周囲(peripapillary)から求心性に始まり、病変辺縁部が徐々に蛇行状に拡大する
- 活動期:病変辺縁に灰白色の縁取りが出現する
- 瘢痕期:網脈絡膜萎縮病変として固定する
- 再発時は必ず既存瘢痕の辺縁部から新たな炎症が出現する(これが特徴的)
- 再発間隔は 3 か月〜4 年と個人差が大きい
最も重要:結核関連型(SLC)との鑑別
結核性蛇行様脈絡膜炎(serpiginous-like choroiditis; SLC)は蛇行状脈絡膜炎と画像所見が酷似するが、治療方針が根本的に異なる:
| 鑑別点 | 蛇行状脈絡膜炎 | 結核関連型(SLC) |
|---|---|---|
| 病変分布 | 乳頭周囲中心・求心性 | 後極部〜周辺部・多発性 |
| IGRA/TST | 陰性 | 陽性 |
| 病変の形 | 地図状・連続性 | 多発不連続な小病変が多い |
| 治療 | ステロイド+免疫抑制薬 | 抗結核薬が必須 |
SLC に免疫抑制薬を使用すると結核が著明に悪化するため、治療前の IGRA(クォンティフェロン)検査は絶対に省略できない2)。
CNV 合併(最大 35%)への対応
蛇行状脈絡膜炎では CNV が最大 35% に合併し、中心窩に及ぶと不可逆的な視力障害を来す。抗 VEGF 療法(ベバシズマブ・ラニビズマブ)の硝子体内注射が有効である18)。
AZOOR(急性帯状潜在性網膜外層症)
Section titled “AZOOR(急性帯状潜在性網膜外層症)”AZOOR は 1992 年に Gass が提唱した疾患概念であり、眼底がほぼ正常にもかかわらず急激に視力低下・視野欠損・光視症を来す外網膜症である3)。
AZOOR complex の概念
Jampol らが提唱した AZOOR complex は、MEWDS・AZOOR・PIC・MFC・AMN(acute macular neuroretinopathy)・AIBSE・AAOR を遺伝的自己免疫/炎症機序の共通基盤を持つ連続体として理解する概念である3)。
特有の臨床像
- 近視を有する 20〜50 代の若年女性に好発
- **photopsia(光視症)**が発症初期に出現することが多い(特に帯状・弧状に見える光)
- 片眼性で始まり、最終的に 76% が両眼性となる
- 眼底は急性期にはほぼ正常(視力低下と眼底所見の乖離が特徴)
- 視野欠損は不規則な帯状パターン(盲点に連続することが多い)
- 自己免疫疾患(橋本病・多発性硬化症)合併例もある
OCT と ERG が診断の鍵
- OCT での ellipsoid zone(IS/OS ライン)の消失・不明瞭化が最重要所見
- OCT で外層が消失した部位の機能回復は期待できない(予後予測にも有用)
- 多局所 ERG での振幅低下が眼底正常でも検出できる(全視野 ERG よりも多局所 ERG が感度高い)
- 赤外 FAF で病変部と正常部位の境界が描出されることがある
治療と予後
AZOOR に確立された治療法はない。軽症例は経過観察のみでよいが、重症例(視力低下または広範な視野欠損)にはメチルプレドニゾロンパルス療法(1,000 mg × 3 日)に続くプレドニゾロン内服を行う2)。多くの症例は 6 か月以内に安定するが、外層障害が残存した部位の視野は回復しない。
5. 画像検査の使い方
Section titled “5. 画像検査の使い方”モダリティ別の役割分担
Section titled “モダリティ別の役割分担”各画像検査の役割を明確に把握することが、白点症候群の正確な診断と活動性評価に不可欠である1, 5)。
| モダリティ | 最も強い適応・役割 |
|---|---|
| FA(フルオレセイン蛍光造影) | 網膜血管・RPE・choriocapillaris の漏出評価。APMPPE の蛍光逆転現象確認。MEWDS の wreath-like 過蛍光確認。血管炎(Birdshot)の評価 |
| ICGA(インドシアニングリーン蛍光造影) | 脈絡膜循環障害の直接評価。FA より早期に病変検出可能(特に Birdshot・APMPPE・蛇行状)。臨床所見より広範な病変の検出(MEWDS・PIC)。活動性病変の検出に最も鋭敏 |
| FAF(眼底自発蛍光) | RPE 障害の非侵襲的評価。活動性判定(APMPPE・蛇行状)。MEWDS の診断(早期白点部が高自発蛍光)。Birdshot の慢性化評価(乳頭周囲低自発蛍光73%) |
| OCT(光干渉断層計) | Ellipsoid zone 評価(MEWDS・AZOOR の診断的所見)。病変の5段階進化評価(PIC)。CNV・黄斑浮腫の評価。予後予測(EZ 消失 → 視力予後不良) |
| OCT-A | Choriocapillaris flow void の非侵襲的検出(APMPPE・蛇行状・PIC)。CNV の早期・鋭敏な検出(PIC・MFC で FA より高感度)。Birdshot の脈絡膜層別血流評価。治療効果モニタリング |
| 多局所 ERG / 全視野 ERG | AZOOR の診断(眼底ほぼ正常でも ERG 振幅低下)。Birdshot の活動性モニタリング(30Hz フリッカー遅延が最感度)。治療効果判定 |
疾患別「まずどの検査から」ガイド
Section titled “疾患別「まずどの検査から」ガイド”MEWDS が疑われるとき
APMPPE が疑われるとき
PIC/MFC が疑われるとき
蛇行状脈絡膜炎が疑われるとき
ICGA の低蛍光病変の意味
Section titled “ICGA の低蛍光病変の意味”ICGA で白点症候群病変が示す低蛍光は、**脈絡膜血流途絶(choriocapillaris 閉塞)**の直接的反映である1)。ICGA は脈絡膜循環を評価するモダリティとして FA より感度が高く、以下の特徴を持つ:
- 全相低蛍光:APMPPE・蛇行状脈絡膜炎・PIC・MFC で認められる。脈絡膜毛細血管板虚血の高度な閉塞を反映する。
- 後期低蛍光(FA では異常なし):MEWDS の ICGA 後期低蛍光は、choriocapillaris 主座ではなく RPE 異常による ICG 取り込み変化として説明されている(OCT-A で choriocapillaris は原則温存)1)。
- Haller 層 flow void → 進行期に全層 flow void:Birdshot に特有の脈絡膜間質(stroma)主座から choriocapillaris への二段階進展パターン14)。
ICGA は FA・OCT-A に比べて**臨床的に見えない隠れた病変(subclinical lesions)**を検出できる点でも優れており、特に MEWDS・PIC では白点よりも広範な脈絡膜病変を描出する1, 15)。
FAF の低・高蛍光パターン別疾患マップ
Section titled “FAF の低・高蛍光パターン別疾患マップ”FAF(眼底自発蛍光)のパターンは RPE の代謝状態を反映し、白点症候群の診断と活動性評価に有用である16)。
| FAF パターン | 疾患・病期 | 意味 |
|---|---|---|
| 高自発蛍光(過 AF) | MEWDS 急性期・Serpiginous 活動辺縁 | 視細胞変性産物(A2E 等)の RPE への蓄積 |
| 低自発蛍光(低 AF) | APMPPE 瘢痕期・PIC 活動病変・Birdshot 乳頭周囲 | RPE 消失・機能喪失 |
| 中心部低 AF+辺縁高 AF ハロー | Serpiginous 活動辺縁・PIC | 活動辺縁での RPE 障害パターン |
| 帯状異常 AF | AZOOR | 視細胞外層障害の分布に一致 |
| 中心窩顆粒状過 AF | MEWDS(NIR-FAF) | foveal granularity の非侵襲的描出 |
Birdshot では乳頭周囲の融合性低 AF が 73% に認められ、慢性化の指標として有用である17)。
OCT での ellipsoid zone(EZ)欠損パターン
Section titled “OCT での ellipsoid zone(EZ)欠損パターン”EZ(ellipsoid zone、旧 IS/OS ライン)の評価は白点症候群の活動性と予後予測において中心的役割を担う1)。
| EZ 所見 | 疾患・病期 | 予後 |
|---|---|---|
| EZ 著明乱れ→回復 | MEWDS 急性期→回復期 | 良好(EZ 回復と視力回復が連動) |
| EZ 消失(病変部一致) | AZOOR 活動期 | 消失部位の機能回復なし |
| EZ 乱れ+外網膜高反射 | APMPPE 急性期 | 回復後に一部萎縮残存あり |
| RPE 下高反射隆起+EZ 断裂 | PIC・MFC(5 段階進化) | CNV 合併で不良 |
| EZ 消失(嚢胞黄斑浮腫合併) | Birdshot 進行期 | 視力予後不良の危険因子 |
OCT-A での choriocapillaris flow void は FA・ICGA 所見と高い一致率を示す(APMPPE・蛇行状脈絡膜炎で特に有用)5, 13)。
FA の蛍光パターン:充満遅延 vs 過蛍光 vs 漏出
Section titled “FA の蛍光パターン:充満遅延 vs 過蛍光 vs 漏出”| FA パターン | 疾患 | 臨床的意味 |
|---|---|---|
| 早期低蛍光→後期過蛍光(蛍光逆転現象) | APMPPE | 脈絡膜毛細血管板虚血。早期流入障害→周囲組織からの遅延色素漏出 |
| 早期 wreath-like(花冠状)過蛍光 | MEWDS | RPE/視細胞障害を直接反映。後期に拡大しない点が鑑別 |
| 早期低蛍光→後期漏出 | Serpiginous・MFC 活動期 | 活動性脈絡膜炎の証拠 |
| 動脈期初期過蛍光→後期漏出 | PIC 活動期 | 炎症性 CNV の存在を疑わせる |
| 血管漏出+乳頭過蛍光(漏出なし) | Birdshot | 網膜血管炎の直接証拠 |
| 通常正常〜軽微 | AZOOR | FA 陰性でも視野欠損・ERG 異常が認められる乖離が特徴 |
6. 治療総論
Section titled “6. 治療総論”治療戦略の選択
Section titled “治療戦略の選択”白点症候群の治療は疾患の自然経過・重症度・CNV 合併の有無によって大きく異なる。
経過観察(治療不要)が原則の疾患
Section titled “経過観察(治療不要)が原則の疾患”ステロイド療法が主体となる疾患
Section titled “ステロイド療法が主体となる疾患”APMPPE(重症・乳頭炎合併)・PIC(中心窩近傍活動性病変)・AZOOR(重症例)
- プレドニゾロン 30〜60 mg/日より開始し漸減
- APMPPE で脳血管炎が合併した場合はメチルプレドニゾロンパルス+神経内科連携が必要
- AZOOR の重症基準:視力の良好な眼の矯正視力 < 0.3(日本眼科学会診断ガイドライン)
長期免疫抑制療法が必要な疾患
Section titled “長期免疫抑制療法が必要な疾患”バードショット網脈絡膜症・蛇行状脈絡膜炎・MFC
バードショット(長期管理)
- プレドニゾロン 0.5〜1 mg/kg/日で開始
- ミコフェノール酸モフェチル(MMF)2〜3 g/日(第一選択免疫抑制薬)
- メトトレキサート(MTX)10〜25 mg/週
- アザチオプリン(AZA)1〜3 mg/kg/日
- 難治例:アダリムマブ(93.2%が第一選択生物学的製剤として使用)
- 治療なしで10年に16〜22%が視力0.1以下
蛇行状脈絡膜炎(長期管理)
- プレドニゾロン 40〜80 mg/日で開始(漸減)
- アザチオプリン 1〜2.5 mg/kg/日(第一選択維持療法)
- ミコフェノール酸モフェチル・メトトレキサート(代替)
- 難治例:クロラムブシル(最も強力;0.2 mg/kg/日以下、毎週血液検査必須)
- 生物学的製剤:アダリムマブ(91.0%が推奨第一選択)
- 結核除外(IGRA 陽性なら抗結核薬先行)確認後に免疫抑制薬を導入
MFC の免疫調節療法
Section titled “MFC の免疫調節療法”MFC は慢性再発性経過をたどるため、ステロイド漸減後の維持療法として免疫調節薬が必要となる症例が多い。
| 薬剤 | 用量目安 | 特記事項 |
|---|---|---|
| メトトレキサート(MTX) | 10〜25 mg/週 | 葉酸 1 mg/日を併用。肝毒性モニタリング |
| アザチオプリン(AZA) | 1〜3 mg/kg/日 | TPMT 活性確認推奨。血球抑制に注意 |
| ミコフェノール酸モフェチル(MMF) | 1〜3 g/日 | 消化器症状が副作用として多い |
| シクロスポリン(CsA) | 3〜5 mg/kg/日 | 腎機能・血圧モニタリング必須 |
| アダリムマブ | 40 mg/2 週(皮下注) | 難治・ステロイド依存例。結核スクリーニング必須 |
CNV 合併への対応
Section titled “CNV 合併への対応”CNV は視力予後を左右する最重要合併症であり、PIC・MFC・蛇行状脈絡膜炎で特に高頻度に合併する。
| 疾患 | CNV 合併率 | 治療 |
|---|---|---|
| PIC | 40〜76% | 抗VEGF 硝子体内注射(ベバシズマブ・ラニビズマブ・アフリベルセプト)+ステロイド。OCTA PRN 戦略 |
| MFC | 最大60% | 抗VEGF 硝子体内注射+免疫調節療法 |
| 蛇行状脈絡膜炎 | 最大35% | 抗VEGF(ベバシズマブ・ラニビズマブ)硝子体内注射 |
| MEWDS・APMPPE | まれ | 抗VEGF(CNV 合併確認された場合) |
| Birdshot | まれ | 全身免疫抑制療法+CNV 合併時は抗VEGF |
治療における注意事項
Section titled “治療における注意事項”| 注意点 | 該当疾患 |
|---|---|
| 結核除外を最優先(免疫抑制前) | 蛇行状脈絡膜炎・MFC |
| HLA-A29 を考慮(診断) | バードショット(日本人では感度低い) |
| ステロイドインプラントの眼圧上昇リスク | バードショット(最大40%で線維柱帯切除が必要) |
| クロラムブシルの骨髄抑制・悪性腫瘍リスク | 蛇行状脈絡膜炎(毎週血液検査必須) |
| COVID-19 感染・ワクチン後の再燃 | PIC・MEWDS(再燃報告あり) |
| 脳血管炎合併時の緊急対応 | APMPPE(頭痛・神経症状→脳 MRI 緊急施行) |
6.5 全身疾患との関連
Section titled “6.5 全身疾患との関連”白点症候群の各疾患は特定の全身疾患・感染症との関連が知られており、治療前の系統的な除外検索が重要である。
| 疾患 | 関連する全身疾患・状態 | 臨床的意義 |
|---|---|---|
| APMPPE | 脳血管炎(MCAT)・連鎖球菌感染・EB ウイルス | 頭痛・神経症状→緊急脳 MRI |
| Birdshot | HLA-A29(白人 80〜98%)・サルコイドーシス類似 | HLA 検査が診断補助(日本人では感度低い) |
| 蛇行状脈絡膜炎 | 結核(SLC)・HLA-B7/A2 | IGRA 陽性→抗結核薬先行が原則 |
| PIC | サルコイドーシス・HLA-DRB1*15 | 胸部 CT・ACE 測定を考慮 |
| MFC | IL-10 ハプロタイプ・EBV・サルコイドーシス | 慢性再発例は全身精査を再評価 |
| MEWDS | COVID-19 感染・ワクチン接種後・HLA-B51 | SARS-CoV-2 感染が免疫トリガーとして機能 |
| AZOOR | 橋本病・多発性硬化症・自己免疫疾患 | 甲状腺機能・自己抗体検査を考慮 |
7. 各疾患の特記事項と最新知見
Section titled “7. 各疾患の特記事項と最新知見”APMPPE と placoid chorioretinitis spectrum
Section titled “APMPPE と placoid chorioretinitis spectrum”APMPPE は persistent placoid maculopathy(PPM)・relentless placoid chorioretinitis(RPC)と共に「placoid chorioretinitis spectrum」として統合的に理解されるようになっている。これら3疾患では OCT-A で choriocapillaris flow void が共通のパターンを示し、脈絡膜毛細血管板虚血が共通の病態基盤であることを示す5)。
Klufas ら(2017)は APMPPE・PPM・RPC の3疾患において OCT-A が FA・ICGA と高い一致率で choriocapillaris flow void を検出することを報告し、placoid chorioretinitis spectrum の概念を支持した5)。
MEWDS と foveal granularity
Section titled “MEWDS と foveal granularity”中心窩顆粒状変化(foveal granularity)は MEWDS の74〜96%に認められる診断的所見であり、白点消失後も唯一の所見として残ることがある。近赤外 FAF(NIR-FAF)で特徴的な中心窩顆粒状パターンが描出される9)。
PIC と MFC の疾患スペクトラム
Section titled “PIC と MFC の疾患スペクトラム”PIC と MFC(MFCwP)は共通の遺伝的背景(IL-10 ハプロタイプ・HLA-DRB1*15)を持ち、同一疾患スペクトラムの異なる表現型と考えられる。主な鑑別点は硝子体炎・前房炎症の有無と病変分布域である1, 3)。
| 鑑別点 | PIC | MFC(MFCwP) |
|---|---|---|
| 硝子体炎 | なし | あり(重要な鑑別点) |
| 前房炎症 | なし | 軽度あり |
| 病変分布 | 後極部に限局 | 後極部+中間周辺部 |
| 病変サイズ | 100〜300μm | 45〜350μm |
| CNV 合併率 | 40〜76% | 最大60% |
Birdshot と HLA-A29
Section titled “Birdshot と HLA-A29”Birdshot と HLA-A29 の関連は既知のあらゆる疾患の中で最も強い遺伝的関連の一つであり、白人患者では相対リスクが50〜224倍に上昇する4)。ただし日本人では HLA-A29 保有者が少ないため、診断における HLA-A29 陽性率の感度が限定的となる点に注意が必要である。SUN 2021 分類基準の臨床所見項目(眼底所見・前眼部炎症の軽微さ・硝子体炎)を重視した診断が重要となる10)。
AZOOR complex とウイルストリガー
Section titled “AZOOR complex とウイルストリガー”AZOOR は遺伝的素因(IL-10 ハプロタイプ等)にウイルス感染・ワクチン・薬剤などの環境トリガーが加わって発症すると考えられ、MEWDS・PIC・AMN・AIBSE と共に AZOOR complex として理解される3)。COVID-19 感染・ワクチン接種後の MEWDS 発症例が世界的に増加しており、SARS-CoV-2 が免疫トリガーとして機能する可能性が示唆されている11)。
8. 関連記事
Section titled “8. 関連記事”9. 参考文献
Section titled “9. 参考文献”- Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
- 日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(13〜18節:APMPPE・MEWDS・PIC・多発性脈絡膜炎・バードショット・蛇行状脈絡膜炎・AZOOR). 日本眼科学会雑誌. 2019;123(6):635-696.
- Jampol LM, Becker KG. White spot syndromes of the retina: a hypothesis based on the common genetic hypothesis of autoimmune/inflammatory disease. Am J Ophthalmol. 2003;135(3):376-379.
- Agrawal R, et al. The role of HLA-A29 in birdshot chorioretinopathy and immune checkpoint inhibitor-related uveitis. Am J Ophthalmol. 2025. doi:10.1016/j.ajo.2024.01.007
- Klufas MA, Phasukkijwatana N, Iafe NA, et al. Optical coherence tomography angiography reveals choriocapillaris flow reduction in placoid chorioretinitis. Ophthalmol Retina. 2017;1(1):77-91.
- Stattin M, Forster J, Ahmed D, Krepler K, Ansari-Shahrezaei S. Swept Source-Optical Coherence Tomography Angiography for Management of Secondary Choroidal Neovascularization in Punctate Inner Choroidopathy. Case Rep Ophthalmol. 2021;12:232-238.
- Spaide RF, Goldberg N, Freund KB. Redefining multifocal choroiditis and panuveitis and punctate inner choroidopathy through multimodal imaging. Retina. 2013;33(7):1315-1324.
- Leclaire MD, Clemens CR, Eter N, Mihailovic N. Choroidale Neovaskularisation infolge einer “punctate inner choroidopathy”, dargestellt mittels optischer Kohärenztomographie-Angiographie. Ophthalmologe. 2021;118:842-846.
- Mantovani A, Invernizzi A, Staurenghi G, Herbort CP Jr. Multiple evanescent white dot syndrome: a multimodal imaging study of foveal granularity. Ocul Immunol Inflamm. 2019;27(1):141-147.
- Standardization of Uveitis Nomenclature (SUN) Working Group. Classification criteria for birdshot chorioretinitis. Am J Ophthalmol. 2021;228:65-71.
- Chen N, Mandell M, Arjmand P. Multimodal imaging findings of multiple evanescent white dot syndrome in COVID-19 patients. IDCases. 2024;38:e02110.
- Seddigh S, Pinto A, Zaki AM, Gupta RR. Serpiginous choroiditis after COVID-19 infection. J Vitreoretinal Dis. 2025;9(2):246-252.
- Pakzad-Vaezi K, Khaksari K, Chu Z, Van Gelder RN, Wang RK, Pepple KL. Swept-source OCT angiography of serpiginous choroiditis. Ophthalmol Retina. 2018;2(7):712-719.
- Pepple KL, Chu Z, Weinstein J, Munk MR, Van Gelder RN, Wang RK. Use of en face swept-source optical coherence tomography angiography in identifying choroidal flow voids in 3 patients with birdshot chorioretinopathy. JAMA Ophthalmol. 2018;136(11):1288-1292. doi:10.1001/jamaophthalmol.2018.3474. PMID:30128478. PMCID:PMC6248174
- Khochtali S, Dridi T, Abroug N, et al. Swept-source optical coherence tomography angiography shows choriocapillaris flow reduction in multiple evanescent white dot syndrome. J Curr Ophthalmol. 2020;32(2):211-215.
- Yeh S, Forooghian F, Wong WT, et al. Fundus autofluorescence imaging of the white dot syndromes. Arch Ophthalmol. 2010;128(1):46-56.
- Minos E, Barry RJ, Southworth S, et al. Birdshot chorioretinopathy: current knowledge and new concepts in pathophysiology, diagnosis, monitoring and treatment. Orphanet J Rare Dis. 2016;11(1):61.
- Maleki A, Maldonado Cerda A, Garcia CM, et al. Chlorambucil combination therapy in refractory serpiginous choroiditis: a cure? Am J Ophthalmol Case Rep. 2021;21:101014.
- Niederer RL, Al-Janabi A, Engelbrecht C, et al. Immunomodulatory therapy prescribing practices for non-infectious uveitis: a survey of international experts. Br J Ophthalmol. 2024;108:482-489.
- Tomkins-Netzer O, et al. Treatment of non-infectious uveitis with biologics: a survey of the International Ocular Inflammation Society. Br J Ophthalmol. 2022;106:482-488.
