発症時

急性帯状潜在性網膜外層症(AZOOR)
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 急性帯状潜在性網膜外層症とは
Section titled “1. 急性帯状潜在性網膜外層症とは”急性帯状潜在性網膜外層症(acute zonal occult outer retinopathy; AZOOR)は、1990年代にGassが提唱・疾患概念を確立した急性炎症性疾患である3)。眼底所見がほぼ正常であるにもかかわらず、急性の視野欠損・光視症・視力低下をきたすことが特徴である。視細胞・網膜外層の障害が主座であり、その名称の通り「潜在性(occult)」の外網膜症である。
日本眼科学会により AZOOR の診断ガイドラインが作成されており、重症分類として「視力の良好な眼の矯正視力 < 0.3」が定義されている。ぶどう膜炎診療ガイドライン(日眼会誌 2019;123(6):635-696)における AZOOR complex の鑑別表(表3)にも AZOOR が収載されている1)。眼底所見では説明できない視野異常を認めたとき、鑑別診断に AZOOR の可能性を常に考える必要がある。
AZOORは AZOOR complex(MEWDS, AZOOR, AMN, PIC, MFC, AIBSE, AAOR)の一疾患として位置づけられており、これらの疾患群は外網膜・視細胞・RPEを主座とする炎症性疾患の連続体(スペクトラム)として理解されている1)2)。マルチモーダルイメージングの発展により、AZOOR complex の統合的病態理解が深まっている2)。
AZOORバリアントとして以下が報告されている1):
- AAOR(急性環状外層網膜症):片側性・環状灰白色境界線・求心性進行
- MORR(多帯状外層網膜色素上皮症):急性発症・進行性・RPE関与
- 末梢発症型:稀な変異体。乳頭周囲は非罹患で末梢から求心性に進行する11)
- 好発:若年女性の近視眼
- 患者の約3/4が女性で、30代半ばを中心とする若年層に多い
- 片眼発症が61%で始まり、中央値8年フォローアップで最終的に76%が両眼性に進行する
- 対側眼の発症は平均50ヶ月遅れる
- 自己免疫疾患との合併:橋本病(最多)・多発性硬化症1)
- 発症の約20%に感冒様前駆症状を認める
日本人患者における臨床的特徴については、日本人 AZOOR 症例のコホート研究(Saito S ら、2015)が報告されており、視機能の自然経過や予後因子が検討されている4)。
AZOORの主な障害部位は視細胞(外網膜・ellipsoid zone)である。眼底の外観が正常に見えても、OCTでは視野欠損部位に一致した ellipsoid zone(IS/OS ライン)の消失が確認できる。視細胞内節外節接合部の破綻が視機能低下を引き起こすため、眼底が正常に見えても視力・視野障害が生じる。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”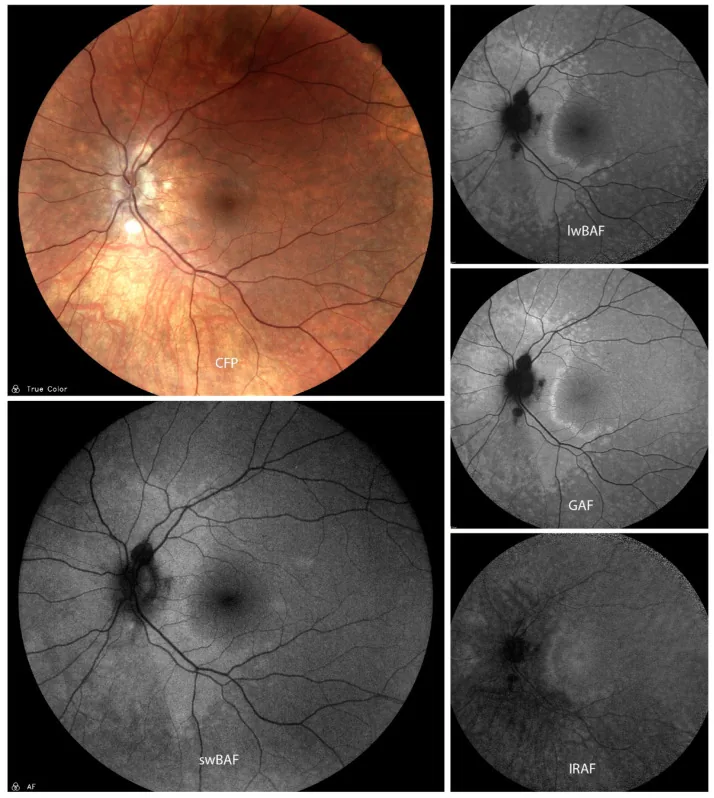
- 光視症:最も特徴的な症状の一つ。急性発症
- 急性視力低下・視野欠損(1〜数箇所)1)
- Mariotte盲点拡大・中心視野欠損・周辺視野欠損1)
- 前駆症状:感冒様症状(発症の約20%)
視野欠損は帯状・区域性に出現することが多く、眼底正常という外観から視神経炎などと誤診されることがある1)。Goldmann視野検査では Mariotte 盲点の著明な拡大や区域性暗点が確認される。
眼底は基本的に正常であり、視神経炎との鑑別が困難な場合がある1)。フルオレセイン蛍光眼底造影(FA)でも通常異常を認めないことが AZOOR の重要な特徴である。長期例ではびまん性・区域性の網脈絡膜萎縮が出現することがある。
慢性期
また、片眼性耳側半盲を呈する場合は鼻側網膜の障害によるものであり、垂直子午線を尊重した耳側半盲として出現することがあるため、視交叉病変を模倣しMRIが必要になる場合もある12)。RAPD(相対的瞳孔求心路障害)は一部の症例で経過中に出現することがある。
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”原因は不明であるが、ウイルス感染または自己免疫関与が主要な仮説として提唱されている。
- 発症の約20%に感冒様前駆症状 → ウイルス感染誘因仮説
- 橋本病・多発性硬化症との合併 → 自己免疫機序仮説1)
- 主な障害部位:視細胞(ellipsoid zone)・RPE・脈絡膜毛細血管板(諸説)
AZOOR の主たる病変部位については、視細胞・網膜色素上皮・脈絡膜毛細血管板などさまざまな説があり、まだ結論は出ていない。OCT での ellipsoid zone 消失は視細胞内節外節接合部(IS/OS ライン)の破綻を直接反映しており、その領域の機能回復は難しい場合が多い8)。
- 若年女性・近視眼
- 自己免疫疾患(橋本病・多発性硬化症)の合併1)
- AZOOR complex としての遺伝的素因+環境因子(ウイルス感染・自己免疫トリガー)2)
- てんかん:ラット研究でてんかん発作が網膜に炎症反応を誘発することが示されており、関連可能性がある13)
- 強膜バックル術後:術後5年以上を経てAZOOR様所見が出現した症例報告がある14)
Gassの51症例のうち約28%に自己免疫疾患の既往を認めた。橋本病・多発性硬化症のほか、バセドウ病・甲状腺機能低下症・アジソン病・重症筋無力症・クローン病・SLEなどが合併疾患として知られている。抗網膜抗体はAZOOR患者の約42%で検出される15)。
4. 診断と検査方法
Section titled “4. 診断と検査方法”AZOORの診断は20〜50歳の若年者で急激な片眼の視力低下・視野欠損・光視症を呈する場合に疑い、OCTと ERGを組み合わせて行う。眼底所見では説明できない視野異常を呈するときは、積極的にAZOORを鑑別に加えることが重要である。
推奨する検査の進め方
Section titled “推奨する検査の進め方”20〜50歳代の比較的若年者で急激な片眼の視力低下・視野欠損がみられ、さらに光視症を伴う場合、まず OCT を施行する。視野欠損部位に一致して OCT で網膜外層の異常がみられれば AZOOR が強く疑われる。続いて ERG・多局所ERGで確認する1)。
| 検査法 | 所見 |
|---|---|
| OCT | 視野欠損部位に一致した ellipsoid zone 消失・interdigitation zone 消失。予後予測に有用5) |
| 全視野ERG | 広範囲障害で振幅低下。錐体系異常 > 杆体系 |
| 多局所ERG | 視野欠損部位に一致した振幅低下。狭範囲病変の検出に感度高1) |
| 眼底自発蛍光(赤外光) | 病変部と正常部の境界確認 |
| FA | 基本的に正常所見 |
| Goldmann視野 | Mariotte盲点拡大・中心暗点・区域性暗点1) |
| 補償光学(AO) | 視細胞配列異常の可視化 |
| PERG(パターンERG) | P50低下・N95正常のパターンを呈することがある |
| EOG | 光反応(light rise)低下・Arden比低下を示すことがある |
OCT は予後予測にも有用である。外層(ellipsoid zone)が消失している部位では、その領域の機能回復は期待できないため、OCT での外層評価が治療方針決定と予後説明の根拠となる5)。障害されている範囲が狭い場合は全視野ERGよりも多局所ERGや局所ERGの方が診断に役立つ1)。
鑑別診断(ぶどう膜炎診療ガイドライン表3)1)
Section titled “鑑別診断(ぶどう膜炎診療ガイドライン表3)1)”| 疾患 | 鑑別ポイント |
|---|---|
| 視神経炎 | ERGで鑑別。視神経炎ではERG正常、眼球運動痛あり |
| MEWDS | 白点が可視(AZOORは眼底正常)。多局所ERGも低下 |
| AMN | 黄斑部赤褐色斑状病変・OCTでの外核層楔状病変 |
| AIBSE | 乳頭周囲輪状灰白色混濁・Mariotte盲点拡大が特徴的 |
| AAOR | 網膜深層の輪状灰白色混濁 |
| 多発性硬化症 | MRI所見・全身症状・視神経炎所見で鑑別 |
| np-AIR(非腫瘍随伴性自己免疫性網膜症) | 発症が亜急性〜慢性、FAFびまん性過蛍光、EOGは正常 |
| 梅毒性外層網膜症(SOR) | AZOORと酷似。梅毒血清検査が必須1) |
感染症除外として梅毒・CMV・VZV・HSVの検査を行う。耳側半盲を呈する場合はMRIにより視交叉病変を除外する12)。
5. 標準的な治療法
Section titled “5. 標準的な治療法”確立した治療法はなく、自然回復例と視力予後不良例が混在する。
- 軽症例:無治療で経過観察
- 重症例(視力の良好な眼の矯正視力 < 0.3):ステロイドパルス療法を考慮
病因として自己免疫や炎症の関与が推定されているため、特に重症例ではステロイドパルス療法が行われることがある。ただし、回復に関しては自然回復なのかステロイドの効果によるものかの区別が困難である。
ステロイドパルス療法プロトコル
Section titled “ステロイドパルス療法プロトコル”| 投与経路 | 薬剤名 | 用量・用法 |
|---|---|---|
| 点滴静注(パルス) | メチルプレドニゾロン(ソル・メドロール®) | 1,000 mg + ソリタ-T3注 500 mL を1時間かけて点滴静注、3日間 |
| 経口(後継療法) | プレドニゾロン(プレドニン®)錠 5 mg | 8〜6錠(40〜30 mg)分2 から漸減 |
ステロイドパルス療法の効果については自然回復との区別が困難な面があり、エビデンスは症例報告レベルにとどまる。無作為化比較試験(RCT)は現時点では存在しない。
硝子体内ステロイド注射
Section titled “硝子体内ステロイド注射”硝子体内ステロイド注射も報告されているが、白内障・眼圧上昇・中心性漿液性脈絡網膜症(CSR)などの副作用リスクに注意が必要である16)。
免疫抑制療法・その他
Section titled “免疫抑制療法・その他”難治例に対して以下が報告されている:
- MMF+シクロスポリン+IVIg:ミコフェノール酸モフェチル2g/日+シクロスポリン200mg/日+IVIg 2g/kg 月1回の併用でBCVA改善が報告されている17)
- シクロスポリン:4.5mg/kg/日の使用例がある
- アダリムマブ(Humira):有効例の報告がある
- 抗ウイルス療法:アシクロビル・バラシクロビルはGassらの報告では明確な効果が示されなかった3)
CNVM合併例
Section titled “CNVM合併例”脈絡膜新生血管膜(CNVM)を合併した場合は、抗VEGF硝子体内注射(ベバシズマブ、アフリベルセプト等)が適応となることがある1)。
難治例・再発例
Section titled “難治例・再発例”再発・慢性化した場合は免疫抑制薬(シクロスポリン等)の併用を検討する。AZOOR complex 関連疾患の治療に準拠した対応が参考とされる。
ステロイドパルス療法が有効との症例報告はあるが、無作為化比較試験は存在せず、自然回復との区別が困難である。重症例(視力の良好な眼の矯正視力 < 0.3)に限り施行を考慮するが、治療しても外層網膜の消失が持続する例では視力予後が不良となる。OCT で ellipsoid zone が消失している部位の機能回復は困難であることが多い8)。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”AZOORの病態は視細胞・ellipsoid zone(IS/OS 接合部)の急性障害である。
障害部位と OCT の関係
Section titled “障害部位と OCT の関係”OCT ellipsoid zone の消失は視細胞内節外節接合部(IS/OS ライン)の破綻を直接反映する。この領域が消失している部位では視細胞の回復が難しく、長期的な視機能障害の原因となる5)8)。軽症例や回復期では interdigitation zone のみが異常を示し、ellipsoid zone は保たれる場合がある。
- ウイルス感染(約20%に感冒様前駆症状)または自己免疫(橋本病・多発性硬化症合併)が関与
- 主障害部位:視細胞内節外節接合部(ellipsoid zone)。OCTでの消失が直接反映される
- 脈絡膜毛細血管板の関与についての諸説があるが、OCT-A では choriocapillaris の保存または軽微な変化にとどまる場合が多い2)
- AZOOR complex の一疾患として、遺伝的素因+環境因子(ウイルス感染・自己免疫)で発症2)
AZOOR complex としての理解
Section titled “AZOOR complex としての理解”AZOOR complex(MEWDS・AZOOR・AMN・PIC・MFC・AIBSE・AAOR)は同一疾患スペクトラム上にある類縁疾患として考えられており、外網膜・RPEを主座とする炎症性障害という共通基盤を持つ2)。Jampol・Becker(2003)はこれらの白点症候群が共通の遺伝的自己免疫/炎症機序に基づくという仮説を提唱した10)。
自己免疫疾患との合連関
Section titled “自己免疫疾患との合連関”橋本病が最も多く合併する自己免疫疾患であり、次いで多発性硬化症が多い。これらの合併は自己免疫機序による視細胞・外網膜への攻撃を示唆しており、AZOOR の病態理解における重要な手がかりとなっている。
ellipsoid zone の消失が持続する部位では視細胞の回復が困難であり、OCT での評価が長期予後予測に直結する。
一次病変部位:光受容体外節
Section titled “一次病変部位:光受容体外節”マルチモーダルイメージング解析により、AZOORの一次病変部位は光受容体外節であることが示されている18)。ICG蛍光造影でchoriocapillarisが保存されており、脈絡膜毛細血管は初期に障害されない。FAF過蛍光は光受容体外節消失によりRPEのリポフスチンが露出して生じる。脈絡膜は二次的に障害(collateral damage)を受け、進行例では脈絡網膜萎縮へと至る。
AO-TFI(適応光学眼底撮影)による定量解析では、光受容体(PR)密度が有意に低下する一方、RPE密度には有意差がないことが確認されており、PRが一次標的であることを細胞レベルで支持する19)。EZ回復後もONL菲薄化とPR密度低下が持続し、形態的回復と機能的障害の乖離が生じることがある。
Qianらのレビューでは「AZOORはAIRの特異的形態である」と主張されており、視神経乳頭縁からの抗体漏出を介して免疫産物が網膜下に拡散し、視神経に連続する大きな暗点を形成するとの機序が提唱されている17)。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”- AZOOR complex の統合理解:MEWDS・AMN・PIC・MFC・AIBSE・AAOR との共通基盤を持つ連続体概念の確立が進んでいる1)2)
- 補償光学(AO)による視細胞観察:病変部の視細胞配列異常の可視化が可能になり、病変範囲の詳細な評価が進んでいる
- AO-TFI(適応光学眼底撮影)の進歩:非侵襲的・in vivoでRPEおよび光受容体を細胞レベルで観察・定量化できる技術として注目されている19)。EZが形態的に回復した後もPR密度低下が持続することが初めて直接証明され、「構造・機能乖離」の解明に貢献した
- OCT-A choriocapillaris 評価:脈絡膜血流の関与解明に向けた研究が進行中である2)。OCT-A flow void が病態評価の指標となる可能性がある
- OCTAによる診断・治療モニタリング:En-face outer retinal slab での starry-sky 外観はAZOORの診断補助および治療反応モニタリングに活用できる可能性がある16)
- マルチモーダルイメージングによる病型分類:Mrejen ら(2014)は AZOOR のマルチモーダルイメージングに基づく分類体系を提唱した6)。これにより病型と予後の関連解明が進んでいる
- AZOORバリアントの認識と分類:末梢発症型バリアント(求心性進行・乳頭周囲非罹患)をはじめとする多様な病態の認識が進んでいる11)
- AZOORと二次性np-AIRの関連:AZOORが進行することで二次性np-AIR(非腫瘍随伴性自己免疫性網膜症)を引き起こす可能性が提唱されており、IVIgを含む免疫療法への応用が期待される17)
- ステロイド治療のエビデンス構築:RCTは現時点では存在せず、症例報告の集積が課題である4)
- 長期予後バイオマーカー:自然回復例と進行例の違いを予測する指標として、OCT での ellipsoid zone 保存・多局所ERGパターンの活用が検討されている4)7)
- 日本人症例コホートデータ:Saito らによる日本人 AZOOR 患者の長期追跡データが予後因子同定に貢献している4)9)
- 未解決課題:RCTによる治療法の確立・病因(ウイルス vs 自己免疫)の完全解明・早期介入の予後改善効果の検証・診断バイオマーカーの開発
8. 参考文献
Section titled “8. 参考文献”- 日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(AZOOR complex 鑑別表を含む). 日本眼科学会雑誌. 2019;123(6):635-696.
- Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
- Gass JD. Acute zonal occult outer retinopathy. Donders Lecture: The Netherlands Ophthalmological Society, Maastricht, Holland, June 19, 1992. J Clin Neuroophthalmol. 1993;13(2):79-97.
- Saito S, Saito W, Saito M, et al. Acute zonal occult outer retinopathy in Japanese patients: clinical features, visual function, and factors affecting visual function. PLoS One. 2015;10(4):e0125133.
- Saito W, Kase S, Fujiya A, et al. Multimodal imaging in acute zonal occult outer retinopathy. Br J Ophthalmol. 2019;103(7):908-913.
- Mrejen S, Khan S, Gallego-Pinazo R, et al. Acute zonal occult outer retinopathy: a classification based on multimodal imaging. JAMA Ophthalmol. 2014;132(9):1089-1098.
- Gass JD, Agarwal A, Scott IU. Acute zonal occult outer retinopathy: a long-term follow-up study. Am J Ophthalmol. 2002;134(3):329-339.
- Makino S, Tampo H. Optical coherence tomography and electroretinographic findings in patients with acute zonal occult outer retinopathy. Clin Ophthalmol. 2013;7:1.
- Jampol LM, Becker KG. White spot syndromes of the retina: a hypothesis based on the common genetic hypothesis of autoimmune/inflammatory disease. Am J Ophthalmol. 2003;135(3):376-379.
- Li D, Kishi S. Loss of photoreceptor outer segment in acute zonal occult outer retinopathy. Arch Ophthalmol. 2007;125(9):1194-1200.
- Ünlü BH, Karti O, Saatci AO. A case of an acute zonal occult outer retinopathy variant characterized with an insidious peripheral onset and centripetal progression. Cureus. 2024;16(5):e59600.
- Ahmed Y, Sayal A, Kaplan AJ, Micieli JA. Monocular temporal hemianopia due to acute zonal occult outer retinopathy. Case Rep Ophthalmol. 2022;13(1):44-9.
- Karska-Basta I, Romanowska-Dixon B, Pojda-Wilczek D, et al. Acute zonal occult outer retinopathy in a patient suffering from epilepsy: five-year follow-up. Medicina. 2021;57(11):1276.
- Fung AT, Lo-Cao E, Cornish EE. Acute zonal occult outer retinopathy-like presentation secondary to scleral buckle. Am J Ophthalmol Case Rep. 2022;28:101716.
- Roy R, Dutta Majumder P. Current understanding of acute zonal occult outer retinopathy (AZOOR). Indian J Ophthalmol. 2024;72(7):935-7.
- Özyol E, Özyol P. Acute zonal occult outer retinopathy: optical coherence tomography angiography findings and treatment response. GMS Ophthalmol Cases. 2022;12:Doc16.
- Khan S, Saigal K, Moxam J, Maleki A. A case of concomitant acute zonal occult outer retinopathy and secondary nonparaneoplastic autoimmune retinopathy. Case Rep Ophthalmol. 2025;16(1):124-32.
- Herbort CP Jr, Arapi I, Papasavvas I, Mantovani A, Jeannin B. Acute zonal occult outer retinopathy (AZOOR) results from a clinicopathological mechanism different from choriocapillaritis diseases: a multimodal imaging analysis. Diagnostics. 2021;11(7):1184.
- Iuliano M, Lombardo M, Falsini B, et al. Structural, functional, and cellular analysis of a case of acute zonal occult outer retinopathy (AZOOR). Biomedicines. 2025;13(7):1521.
