ラニビズマブ(ルセンティス®)

硝子体注射(抗VEGF療法)
1. 硝子体注射(抗VEGF療法)とは
Section titled “1. 硝子体注射(抗VEGF療法)とは”抗VEGF薬の硝子体内注射は、硝子体腔に薬液を直接注入することにより、VEGFの作用(血管新生・血管透過性亢進)を阻害する治療法である。加齢黄斑変性・糖尿病黄斑浮腫・網膜静脈閉塞症等の網膜血管疾患が主な適応となる。
抗VEGF療法は2000年代に急速に臨床応用が進んだ。
| 年 | 出来事 |
|---|---|
| 2004年 | ベバシズマブの眼内投与が探索的に開始 |
| 2006年 | ラニビズマブがFDA承認(MARINA/ANCHOR試験)12) |
| 2011年 | アフリベルセプトがFDA承認(VIEW試験)12) |
| 2019年 | ブロルシズマブがFDA承認(HAWK/HARRIER試験)10) |
| 2022年 | ファリシマブがFDA承認(TENAYA/LUCERNE/YOSEMITE/RHINE試験)8) |
主な適応疾患
Section titled “主な適応疾患”- 滲出型加齢黄斑変性(nAMD):脈絡膜新生血管(CNV)に対する第一選択治療1)
- 糖尿病黄斑浮腫(DME):糖尿病網膜症に伴う黄斑浮腫2)
- 網膜静脈閉塞症(RVO):網膜中心・分枝静脈閉塞症の黄斑浮腫6)
- 増殖糖尿病網膜症(PDR):PRP補助または代替(ラニビズマブ)5)
- 病的近視に伴う脈絡膜新生血管(mCNV):アフリベルセプト・ラニビズマブ4)
- ポリープ状脈絡膜血管症(PCV):ブロルシズマブのポリープ消退率が高い14)
- 未熟児網膜症(ROP):ラニビズマブ0.2 mg(2019年承認)・アフリベルセプト0.4 mg(2022年9月承認)3)
- 地図状萎縮(GA):補体阻害薬
- 眼内炎:抗菌薬・抗真菌薬・抗ウイルス薬の直接投与
加齢黄斑変性・糖尿病黄斑浮腫・網膜静脈閉塞症が三大適応疾患である。いずれもVEGFが過剰産生され、血管新生や血管透過性亢進が黄斑部の視力低下を引き起こす。抗VEGF薬を硝子体内に直接投与することで、これらの病的過程を阻害し視力改善・維持を図る。近年はPDR・mCNV・ROP・ポリープ状脈絡膜血管症などにも適応が広がっている。
2. 使用可能な抗VEGF薬(薬剤各論)
Section titled “2. 使用可能な抗VEGF薬(薬剤各論)”薬剤比較(一覧)
Section titled “薬剤比較(一覧)”| 薬剤名 | 商品名 | 分子量 | 作用機序 | 用量 | 承認(日本) |
|---|---|---|---|---|---|
| ラニビズマブ | ルセンティス® | 48 kDa | VEGF-A Fab断片 | 0.5 mg(AMD/RVO), 0.3 mg(DME) | 2009年 |
| アフリベルセプト | アイリーア® | 115 kDa | VEGF-A/B・PlGF阻害(デコイ受容体) | 2 mg / 8 mg(HD) | 2012年 |
| ペガプタニブ | マクジェン® | — | VEGF165アプタマー | 0.3 mg | 2008年 |
| ブロルシズマブ | ベオビュ® | 26 kDa | VEGF-A scFv | 6 mg | 2020年 |
| ファリシマブ | バビースモ® | 149 kDa | VEGF-A + Ang-2 二重特異性抗体 | 6 mg | 2023年 |
| ベバシズマブ | アバスチン® | 148 kDa | VEGF-A 完全長IgG | 1.25 mg | ー(適応外) |
アフリベルセプト(アイリーア®)
分子量:115 kDa(融合タンパク質)
作用機序:VEGF-A・VEGF-B・PlGFの3因子を同時阻害。VEGF-A親和性Kd=0.49 pMと最高。
主要試験:VIEW試験でラニビズマブに非劣性。高用量8 mg(HD)では最大16週間隔。12, 13)
特徴:幅広いVEGF阻害スペクトル。ROP適応では成人用量の20%(0.4 mg)を使用。13)
ブロルシズマブ(ベオビュ®)
分子量:26 kDa(scFv、既存薬中最小)
作用機序:scFv構造でアフリベルセプトの約12倍のモル濃度で投与可能。組織浸透性が高い。
主要試験:HAWK/HARRIER試験で非劣性達成。最大55%が12週間隔維持。10)
注意点:HAWK/HARRIERではIOI、網膜血管炎、網膜血管閉塞が報告されており、投与後の炎症所見に注意する10)。
ファリシマブ(バビースモ®)
ベバシズマブ(アバスチン®)
分子量:148 kDa(完全長IgG)
作用機序:VEGF-A阻害(眼科は適応外使用)
主要試験:CATT試験でラニビズマブと同等の有効性を確認。12)
使用状況:コストが大幅に低い。点滴静注用製剤を無菌的に分注して使用する。
ペガプタニブ(マクジェン®)
作用機序:VEGF165特異的アプタマー
現状:2008年承認の第一世代薬剤。現在は新世代薬剤が主流。初期の抗VEGF療法の概念確立に貢献。
眼科領域では適応外使用(オフラベル)であり、点滴静注用製剤を眼科用に無菌的に調製して使用する。CATT試験でラニビズマブと同等の視力改善効果が確認されており、コストが大幅に低いことから世界的に広く使用されている。ただし日本では保険適用がなく、使用は施設の判断による。
3. 適応疾患と投与レジメン
Section titled “3. 適応疾患と投与レジメン”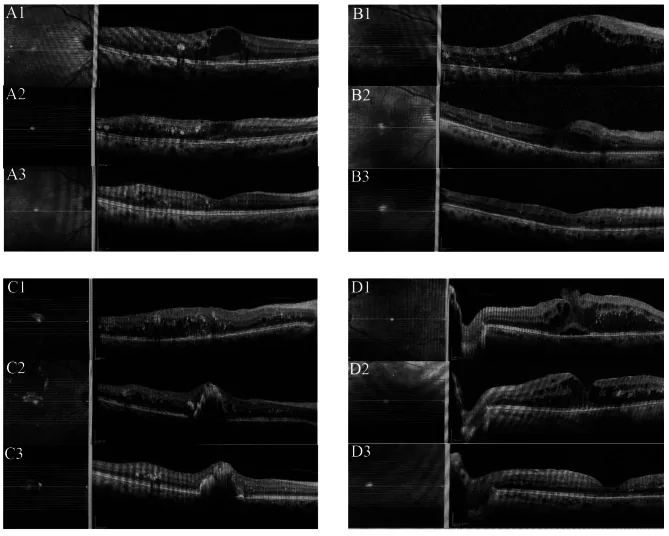
抗VEGF薬の投与は導入期と維持期の2段階で行う。
- 導入期:疾患活動性を強力に抑制するため、毎月固定で3〜6回投与する(疾患・薬剤により異なる)。
- 維持期の方式は以下の3種類がある。
- PRN(pro re nata):毎月受診し、再発所見がある場合のみ投与
- 固定投与:2か月ごと、3か月ごとなど一定間隔で定期投与
- Treat and Extend(T&E):活動性所見がなければ投与間隔を2週ずつ延長、再燃時は短縮
ラニビズマブは導入期3回(月1回)後に維持期PRN投与、アフリベルセプトは導入期3回(月1回)後に2か月ごと固定投与またはT&E法が基本的投与方法として勧められているが、近年はT&E法が多くの施設で導入されている。
疾患別の推奨レジメン
Section titled “疾患別の推奨レジメン”| 適応疾患 | 推奨薬剤 | 導入期 | 維持期 |
|---|---|---|---|
| nAMD(ラニビズマブ) | ルセンティス® 0.5 mg | 月1回×3回1) | PRN(月1回観察) |
| nAMD(アフリベルセプト) | アイリーア® 2 mg | 月1回×3回1) | 2か月ごと固定またはT&E(最長3か月) |
| nAMD(ブロルシズマブ) | ベオビュ® 6 mg | 月1回×3回 | 8〜12週間隔10) |
| nAMD(ファリシマブ) | バビースモ® 6 mg | Q4W×4回 | Q8W〜Q16W8) |
| DME(アフリベルセプト) | アイリーア® 2 mg | 月1回×5回2) | 2か月ごと |
| DME(ラニビズマブ) | ルセンティス® 0.5 mg | 月1回×3回2) | PRN |
| DME(ファリシマブ) | バビースモ® 6 mg | Q4W×4〜6回 | PTI(最大Q16W)8, 13) |
| RVO | アフリベルセプト/ファリシマブ | Q4W×6か月 | PTI(最大Q16W)8) |
| PDR | ラニビズマブ 0.3 mg | — | PRPに対し非劣性5) |
| mCNV | アフリベルセプト/ラニビズマブ | 初回1〜3回 | PRN(単回寛解もあり)4) |
| ROP(ラニビズマブ) | ルセンティス® 0.2 mg/0.02 mL | 初回 | 再燃時追加(1か月以上の間隔)3) |
| ROP(アフリベルセプト) | アイリーア® 0.4 mg/0.01 mL | 初回 | 再燃時追加(1か月以上の間隔)3) |
PCV(ポリープ状脈絡膜血管症)への対応:ブロルシズマブはポリープ消退率約79%と他剤を上回り、12週間隔維持76%(48週)が達成されている。14) ファリシマブはラニビズマブ抵抗性PCV例でも有効との報告がある。15)
網膜静脈閉塞症(RVO)へのファリシマブ
Section titled “網膜静脈閉塞症(RVO)へのファリシマブ”BALATON試験(BRVO、n=553) 8):ファリシマブ6.0 mg vs アフリベルセプト2.0 mg Q4W、24週BCVA変化はそれぞれ+16.9文字・+17.5文字(非劣性達成、95.03% CIの下限 > −4文字)。CST変化は−311.4 μm vs −304.4 μm。≥15文字改善はファリシマブ56.1% vs アフリベルセプト60.4%。FA漏出消失率はファリシマブ33.6% vs アフリベルセプト21.0%(名目p=0.0023)と有意にファリシマブが優れた。
COMINO試験(CRVO/HRVO、n=729) 8):同レジメンで24週BCVA変化はそれぞれ+16.9文字・+17.3文字(非劣性達成)。CST変化−461.6 μm vs −448.8 μm。≥15文字改善はファリシマブ56.6% vs アフリベルセプト58.1%。FA漏出消失率はファリシマブ44.4% vs アフリベルセプト30.0%(名目p=0.0002)と有意に優れ、Ang-2阻害による血管安定化効果が示された。
RVOにおけるIOI安全性(24週) 8):COMINO試験ではIOIがファリシマブ2.2% vs アフリベルセプト1.1%。重篤ぶどう膜炎2件(ファリシマブ群)。BALATON/COMINO両試験で網膜血管炎の報告なし。APTC事象はBALATON ファリシマブ1.1% vs アフリベルセプト1.5%、COMINO 1.1% vs 1.4%と同等であった。
補助治療(RVO):BRVO黄斑浮腫では、ラニビズマブにサブスレッショルド・マイクロパルスレーザーを併用する治療が、単独療法との比較で検討されている11)。
未熟児網膜症(ROP)への抗VEGF療法
Section titled “未熟児網膜症(ROP)への抗VEGF療法”ROP治療における抗VEGF薬の承認薬剤(2022年12月時点)は以下の2剤である。3)
- ラニビズマブ(ルセンティス®)0.2 mg/0.02 mL:成人用量の40%。2019年承認。バイアル製剤のみROP認可。
- アフリベルセプト(アイリーア®)0.4 mg/0.01 mL:成人用量の20%。2022年9月承認。バイアル製剤のみROP認可。
- 再投与は1か月以上の間隔をあけること(添付文書規定)。
治療適応(ETROP study基準に準拠) 3):
- plus diseaseを伴うZone I すべてのROP
- plus diseaseを伴わないZone I Stage 3 ROP
- plus diseaseを伴うZone II Stage 3 ROP
- Aggressive ROP(A-ROP):可及的速やかに施行
主要臨床試験データ 26, 28, 30):
| 試験 | 薬剤・用量 | n | 治療成功率 | レーザー成功率 | 備考 |
|---|---|---|---|---|---|
| BEAT-ROP30) | ベバシズマブ 0.625 mg | 150 | Zone I 再発4% | Zone I 再発22% | Zone I RVでベバシズマブ優越 |
| RAINBOW26) | ラニビズマブ 0.2 mg | 225 | 80.0% | 66.2% | 5歳時高度近視8% vs レーザー24% |
| FIREFLEYE28) | アフリベルセプト 0.4 mg | 118 | 85.5% | 82.1% | 非劣性基準未達だが閾値66%超 |
RAINBOW試験の長期成績 26, 29):5歳時の高度近視はラニビズマブ0.2 mg群8% vs レーザー群24%(有意差あり)。構造異常率はラニビズマブ0.2 mg群1.5% vs レーザー群10%。再投与率31%、再治療時期は投与後4〜16週(中央値8週)。
FIREFLEYE試験の追跡成績 28):再燃率21.9%、再投与率17.8%、再投与までの期間は平均11週(4〜17週)。FIREFLEYE Next(2歳まで追跡)では全身発育・神経発達への治療関連有害事象なし。
再燃率の薬剤間比較 3):
- アフリベルセプト:13.9〜28%(再燃時期平均11〜14.2週)
- ラニビズマブ:20.8〜83.0%(再燃時期5.9〜9.3週と早期 → より早期からの慎重な観察が必要)
A-ROPの注意点 3):A-ROPでは抗VEGF単独では75.0〜87.5%に追加治療が必要である。投与後1〜3週以内の早期再燃があり、1か月未満の再燃にはレーザー光凝固を併用する。線維増殖が広範な場合は抗VEGF単独治療の適応外(収縮による牽引性網膜剥離リスク)。
ROPへの注射手技(成人と異なる点) 3):
- 刺入位置:角膜輪部から1.0〜1.5 mm後方(成人の3.5〜4 mmと大きく異なる。成人と同じ位置では網膜貫通リスク)。
- 針の方向:下方(後方)に向けて刺入(水晶体が相対的に大きいため、中央向きは水晶体貫通リスク)。
- 30ゲージ以下の注射針を使用する。
- 投与量の確認:ラニビズマブ0.02 mL、アフリベルセプト0.01 mL(過量投与防止のため慎重に確認)。
- 麻酔:点眼麻酔・経静脈麻酔・全身麻酔のいずれかを施設の状況に応じて選択。
経過観察 3):網膜血管がZone IIIまで伸展していない場合は、投与後17週までは週1回の眼底検査が推奨される。投与後1年間は定期的眼底検査を継続(牽引性網膜剥離は投与後4〜335日で発生の報告あり)。
Protocol T試験では1年時点でアフリベルセプトの視力改善が最大であった。ただし軽度群(BCVA≧20/40)では3剤間に統計的有意差はなかった。13) ファリシマブはYOSEMITE/RHINE試験でアフリベルセプトと同等の視力改善を示しながら、維持期の注射間隔をより延長できる(2年目にQ16W達成60〜64%)。8) 患者背景や通院頻度の希望により薬剤を選択する。
4. 硝子体注射の手技
Section titled “4. 硝子体注射の手技”注射前の準備
Section titled “注射前の準備”- 患者・投与眼・薬剤の取り違え防止:注射を決定したら首に患者識別タグをかけて確認する。
- ヨードアレルギーの確認:事前に必ず確認する。
- 必要物品の準備:
- 皮膚消毒用10%ポビドンヨード
- 麻酔点眼薬、希釈し室温に戻したPAヨード点眼液、抗菌薬点眼(必要に応じて)
- ガーゼ・綿棒(洗眼時用と注射時用に3本)・テープ付き穴あきドレープ
- 開瞼器・キャリパー・マイクロ有鈎鑷子
- 注射針・注射液(バイアル使用時は1 mLシリンジとフィルター付き採液針)
消毒・麻酔手順
Section titled “消毒・麻酔手順”麻酔:消毒薬が飛散して僚眼に入る可能性を考慮し、ベノキシール®点眼液を両眼に投与後、4%キシロカイン®点眼液を投与眼に2回行う。
PAヨード消毒の注意点:
- 冷蔵庫から出した直後のPAヨードは抗菌・抗真菌の不活化効果が低下しているため、必ず室温に戻す。
- 非密閉容器25°Cで保存した場合、有効成分残存率は5時間で60%まで低下する。長時間経過したPAヨードは使用しない。
- 細菌・真菌の不活化には1分程度の接触時間が必要なため、洗眼後も閉瞼させて結膜との接触時間を十分確保する。
口腔内細菌対策:穴あきドレープと術者・介助者・患者全員のマスク着用で飛沫を防止する。細菌性眼内炎の起炎菌に口腔内細菌が含まれるため、呼気が眼表面へ広がらないようドレープとマスクで眼の間をシールすることが望ましい。
刺入位置と針の方向
Section titled “刺入位置と針の方向”外科的輪部からの刺入距離は以下の通りである。刺入位置を守ることで毛様体扁平部(毛様体皺襞部の後方)での刺入が可能となり、水晶体損傷や硝子体出血を防ぐ。
| 眼の状態 | 輪部からの距離 |
|---|---|
| 有水晶体眼 | 4 mm(毛様体扁平部) |
| 無水晶体眼・眼内レンズ挿入眼 | 3.5 mm |
| 未熟児(ROP) | 1.0〜1.5 mm |
針は硝子体腔の中心へ向かって刺入する。輪部に近い位置で刺入すると毛様体皺襞部を損傷し硝子体出血が生じやすく、水晶体との距離が近くなるため水晶体損傷のリスクが高まる。
注射手技と術後管理
Section titled “注射手技と術後管理”- 穴あきドレープを貼付し、開瞼器で眼瞼を開大する。
- キャリパーで輪部からの刺入距離を計測する。
- 注射部位は耳上側または耳下側とする(水平直筋損傷防止)。
- 鑷子で眼球を固定し、注射前に結膜をやや前方へずらすと抜針後の針孔がずれて液漏れを防ぐ。
- 30G短針を強膜に対してほぼ垂直に刺入し、薬液を緩徐に注入する(急速注入は持続的眼圧上昇の原因となる)。
- 抜針後、綿棒で刺入部位を圧迫する。
- 術直後に視力(指数弁)を確認する。指数弁が認識できない場合は前房穿刺を行う。
- 術後3日間は広域抗菌薬点眼を継続する。
点眼麻酔(ベノキシール®・4%キシロカイン®)を行った上で施行するため、注射中の痛みは軽微である。消毒薬(PAヨード)による刺激感を感じることはあるが、術後早期の不快感にはヒアルロン酸Na点眼が有効である。
5. 合併症と対策
Section titled “5. 合併症と対策”感染性眼内炎(最重要合併症)
Section titled “感染性眼内炎(最重要合併症)”感染性眼内炎は最も重篤な合併症で、発生率は約0.027〜0.065%である。発症した場合、バンコマイシン1.0 mg+セフタジジム2.0 mgの硝子体内注射による緊急治療を要する。
予防の最重要策:
- PAヨードの適切な消毒(室温に戻す、1分以上の接触時間)
- 穴あきドレープの使用(口腔内細菌飛沫防止)
術後の予防的抗菌薬点眼については、複数の研究で眼内炎発生率を低下させないことが示されており、有効性のエビデンスは一致していない。
無菌性眼内炎(Sterile Endophthalmitis)
Section titled “無菌性眼内炎(Sterile Endophthalmitis)”細菌感染を伴わない眼内炎症反応で、抗VEGF薬投与後のまれな合併症として報告されている7)。薬剤、製剤調製、ロットなどで頻度に差があるため、感染性眼内炎との鑑別を優先する。
- 発症時期:注射後早期に発症することが多いが、感染性眼内炎との鑑別が必要である7)
- 主要所見:硝子体混濁、前房炎症、視力低下などを来しうる7)
- 確定診断:培養陰性(PCRによる病原体否定も有用)
- 薬剤差:ベバシズマブ、ラニビズマブ、アフリベルセプトのいずれでも報告があるが、報告頻度は研究・調製条件で異なる7)
- 治療:軽症では保存的治療を行うことが多いが、感染性眼内炎が否定できない場合は培養採取・抗菌薬硝子体内投与・硝子体手術を含めて迅速に判断する。7)
IRIS Registryの1,044例解析では、硝子体注射後眼内炎に対する早期硝子体手術の転帰が大規模データで検討されている24)。
眼内炎症(IOI)・網膜血管炎(ブロルシズマブ特異的)
Section titled “眼内炎症(IOI)・網膜血管炎(ブロルシズマブ特異的)”ブロルシズマブは他の抗VEGF薬より高頻度のIOIを引き起こすことが知られている。
| 試験・集団 | IOI発生率 | 備考 |
|---|---|---|
| HAWK/HARRIER(IOI関連) | 報告あり | 網膜血管炎・血管閉塞を含む炎症性有害事象に注意10) |
| KESTREL(6mg) | 3.7%(対照0.5%) | DME試験10) |
| MERLIN(4週間隔) | 9.3% | 試験中断10) |
| 日本人症例 | 症例報告・市販後情報で報告 | 頻度推定には注意 |
| 市販後(血管炎+閉塞複合) | 3.73/10,000注射 |
IOIの大多数は初回投与後6か月以内・4回以内の注射後に発症する。10)
機序:抗薬物抗体や免疫複合体を介した炎症機序が関与する可能性が議論されている10, 25)。
強膜炎(世界初報告):ブロルシズマブ投与後の後部強膜炎が日本人3例で報告されており、眼圧24〜49 mmHgへの上昇を伴い、うち1例は網膜動脈閉塞と血管炎に進展した。9)
治療:トリアムシノロンアセトニド(STTA)5〜20 mgの結膜下またはTenon嚢下注射が有効。STTA予防投与との組み合わせも報告されている。20, 21)
ファリシマブ関連IOI
Section titled “ファリシマブ関連IOI”IOI発生率はnAMD 2.0%・DME 1.3%・RVO 1.4%であり、両眼投与例では8.5%に認められた。8) 市販後調査での網膜血管炎は0.17/10,000注射と低頻度だが、出血性閉塞性網膜血管炎(HORV)は重篤な転帰をとりうる。8) ファリシマブ関連の網膜血管炎・IOIは症例報告として集積されており、重篤例では出血性閉塞性網膜血管炎(HORV)が問題となる16-18)。
RPE裂孔はファリシマブ群でTENAYA 2.7%・LUCERNE 3.0%に生じており、PED高さ550 μm超がリスク因子である。19)
Crunch syndrome(ROP治療後の牽引性網膜剥離)
Section titled “Crunch syndrome(ROP治療後の牽引性網膜剥離)”ROP患者において抗VEGF療法後に線維血管膜が急速に収縮し、牽引性網膜剥離(TRD)を来す合併症をCrunch syndromeという。27)
- 機序:VEGF抑制によりTGF-βの活性が相対的に亢進。TGF-βは線維化・細胞外マトリックスリモデリングを促進する。未熟児は生理的にTGF-β上昇期にあり、抗VEGF投与で不均衡が増幅される。27)
- 予防:治療前に線維性変化を慎重に評価する。広範な充血した線維増殖がある場合は抗VEGF単独治療の適応外。3)
- 晩期合併症:牽引性網膜剥離は投与後4〜335日で発生が報告されており、投与後1年間の定期的眼底検査が不可欠。3)
持続無血管網膜(PAR)
Section titled “持続無血管網膜(PAR)”抗VEGF治療後も完全な網膜血管化が達成されないことがあり、血管-無血管境界にシャント血管や異常分岐パターンが形成される。27) 長期フォローが必要(再燃リスクおよび晩期合併症の評価)。蛍光眼底造影が網膜血管の正常発達評価に有用である。
針による機械的合併症
Section titled “針による機械的合併症”注射直後の一過性眼圧上昇は注射を受けた全患者に生じる。0.05 mLの注入で眼圧は即座に50 mmHgへ上昇するが、通常は可逆的である。緑内障の既往がある場合は持続的眼圧上昇に注意が必要で、必要に応じて前房穿刺で減圧する。
動脈血栓塞栓事象(ATE)
Section titled “動脈血栓塞栓事象(ATE)”脳卒中・心筋梗塞のリスクが理論上存在する。ブロルシズマブのHAWK試験ではATE 1.1〜1.4%が認められた。10) 既往のある患者では慎重投与が必要である。
6. 病態生理(VEGFの役割と薬剤の作用機序)
Section titled “6. 病態生理(VEGFの役割と薬剤の作用機序)”VEGFの病的役割
Section titled “VEGFの病的役割”VEGFは血管内皮細胞のVEGFR-1・VEGFR-2に結合し、内皮細胞増殖・血管透過性亢進・新生血管形成を促進する。
硝子体内注射によりVEGFレベルが低下すると、血管透過性が低下し黄斑浮腫が改善する。抗VEGF薬の効果は一時的であるため、定期的な再投与が必要となる。
未熟児網膜症(ROP)の病態生理
Section titled “未熟児網膜症(ROP)の病態生理”ROP発症は2段階で進行する。27)
Phase I(血管化停止期):早産後の高酸素環境下でVEGF・IGF-1が抑制される。これにより正常な網膜血管化が阻害され、無血管網膜が形成される。
Phase II(病的血管新生期):酸素離脱後、発育に伴い増大する虚血網膜から過剰なVEGFが放出される。血管-無血管境界で病的血管新生が生じ、Stage 1〜2の分界線・隆起からStage 3の網膜外血管新生へ進行する。重症例ではStage 4〜5の牽引性網膜剥離に至る。
抗VEGF薬はPhase IIの過剰VEGF産生を抑制することで病的血管新生を阻止する。しかし生理的VEGF依存性の血管化も阻害するため、正常血管発達への影響を慎重にモニタリングする必要がある。
各薬剤の分子的特徴
Section titled “各薬剤の分子的特徴”| 薬剤 | 分子量 | VEGF-A親和性(Kd) | 標的 |
|---|---|---|---|
| ブロルシズマブ | 26 kDa | 28.4 pM | VEGF-A(全アイソフォーム) |
| ラニビズマブ | 48 kDa | 20.6 pM | VEGF-A(全アイソフォーム) |
| アフリベルセプト | 115 kDa | 0.49 pM(最高) | VEGF-A/B・PlGF |
| ベバシズマブ | 148 kDa | 35.1 pM | VEGF-A |
| ファリシマブ | 149 kDa | — | VEGF-A + Ang-2 |
Ang-2とファリシマブの作用
Section titled “Ang-2とファリシマブの作用”Ang-2はTie-2受容体のアンタゴニストとして血管不安定化に関与する。ファリシマブがAng-2を阻害することでTie-2経路が正常化し、血管安定性が向上するとともにVEGF感受性が低下する。この二重阻害効果が投与間隔延長を可能にする薬理学的基盤である。
導入期集中投与の意義
Section titled “導入期集中投与の意義”導入期に毎月固定で3〜5回投与を行う理由は、疾患活動性を早期に強力に抑制するためである。T&E法では硝子体内の薬剤濃度が治療域を維持できる範囲で再燃を許容しない枠組みを提供する。
7. 最新の研究と今後の展望(研究段階の報告)
Section titled “7. 最新の研究と今後の展望(研究段階の報告)”ポートデリバリーシステム(Susvimo)
Section titled “ポートデリバリーシステム(Susvimo)”ラニビズマブのPDS(ポートデリバリーシステム)では6か月ごとの補充投与で98%が月1回注射不要となった。12) 2025年にはDMEへの適応追加が検討されている。13) 注射負担の大幅な軽減が見込まれる。
高用量アフリベルセプト8 mg(アイリーア® HD)
Section titled “高用量アフリベルセプト8 mg(アイリーア® HD)”PULSAR試験(AMD)では48週時点で79%が12週間隔、77%が16週間隔を維持した。12) PHOTON試験(DME)でも93%が12週間隔以上を達成した。13)
ブロルシズマブの適応拡大試験
Section titled “ブロルシズマブの適応拡大試験”PCV・黄斑部毛細血管拡張症1型(AT1)を対象としたPROUD試験(韓国)が進行中であり、アジア特有疾患へのエビデンス蓄積が期待される14, 23)。
ファリシマブのPCV対象試験(SALWEEN試験)
Section titled “ファリシマブのPCV対象試験(SALWEEN試験)”PCV患者へのファリシマブの効果を検討するSALWEEN試験が進行中である。22) PCV患者の房水中でAng-2高値が確認されており、Ang-2阻害の上乗せ効果が期待されている。
STTA併用によるIOI予防
Section titled “STTA併用によるIOI予防”結膜下・Tenon嚢下トリアムシノロンアセトニド(STTA)とブロルシズマブの併用投与がIOI予防と滲出制御の両面で有効な可能性がある。20, 21) 至適用量・投与タイミングの標準化に向けた研究が進んでいる。
バイオマーカーによる早期鑑別
Section titled “バイオマーカーによる早期鑑別”無菌性眼内炎と感染性眼内炎の早期鑑別のため、硝子体液中サイトカインプロファイル(IL-6・IL-8・IL-10)の測定が補助ツールになる可能性が期待されている。7)
バイオシミラー
Section titled “バイオシミラー”ラニビズマブ・ベバシズマブのバイオシミラーが登場しつつある。コストの大幅な低下により、治療継続率の向上と医療アクセスの改善が期待される。12)
ROP治療の新規候補薬 27)
Section titled “ROP治療の新規候補薬 27)”- β遮断薬(プロプラノロール):経口投与でStage 2 ROPの重症化予防。0.2%点眼が安全かつ有効(Stage 1で増殖期に開始した場合)とされるが長期データは不足。
- アラキドン酸(AA)・DHAサプリメント:Mega Donna Mega Trialで重症ROP発症を50%低減(15.8% vs 33.3%)。
- カフェイン:未熟児無呼吸治療薬だがVEGF・MMPsの下方制御によりROP進行抑制の可能性。
- ビタミンA:メタ解析でROP発症・進行を低減。
SAFER-ROPプロトコル 27)
Section titled “SAFER-ROPプロトコル 27)”新生児特有の課題(NICU環境での感染予防・注射後モニタリング)に対応した標準化プロトコルとして、SAFER-ROPが提唱されている。Short Needle, Antiseptic/Antibiotic, Follow-Up, Extra Attention to Detail, Recheckの頭字語に基づき、各施設での手技の標準化に活用されている。
8. 参考文献
Section titled “8. 参考文献”-
日本眼科学会. 新生血管型加齢黄斑変性の診療ガイドライン. 日眼会誌. 2024.
-
Lim JI, Kim SJ, Bailey ST, Kovach JL, Vemulakonda GA, Ying GS, Flaxel CJ; American Academy of Ophthalmology Preferred Practice Pattern Retina/Vitreous Committee. Diabetic Retinopathy Preferred Practice Pattern®. Ophthalmology. 2025. doi:10.1016/j.ophtha.2024.12.020. PMID:39918521.
-
Ikuno Y, Ohno-Matsui K, Wong TY, et al. Intravitreal aflibercept injection for myopic choroidal neovascularization: the MYRROR study. Ophthalmology. 2015;122(6):1220-1227. doi:10.1016/j.ophtha.2015.07.013. PMID:26300374.
-
American Academy of Ophthalmology. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024. [Protocol S data]
-
American Academy of Ophthalmology. Retinal Vein Occlusion Preferred Practice Pattern. Ophthalmology. 2024. [BRAVO data]
-
Baudin F, et al. Sterile endophthalmitis after anti-vascular endothelial growth factor agents: a literature review. J Fr Ophtalmol. 2015;38(9):865-871. PMID:26501239.
-
Tadayoni R, Paris LP, Danzig CJ, et al. Efficacy and safety of faricimab for macular edema due to retinal vein occlusion: 24-week results from the BALATON and COMINO trials. Ophthalmology. 2024;131(8):950-960.
-
Takayama T, et al. Scleritis following intravitreal brolucizumab injection: a case series. J Med Case Rep. 2024;18:80.
-
Sharma A, et al. Understanding retinal vasculitis associated with brolucizumab. Ocul Immunol Inflamm. 2022;30(6):1508-1510. PMID:34014141.
-
Nawar AE. Subthreshold micropulse laser combined with ranibizumab versus ranibizumab monotherapy in branch retinal vein occlusion with macular edema. Clin Ophthalmol. 2022;16:1139-1151.
-
Flaxel CJ, Adelman RA, Bailey ST, et al. Age-related macular degeneration preferred practice pattern. Ophthalmology. 2024;131(1):P1-P68.
-
Flaxel CJ, Adelman RA, Bailey ST, et al. Diabetic retinopathy preferred practice pattern. Ophthalmology. 2024;131(1):P99-P168.
-
Sen P, et al. Polypoidal choroidal vasculopathy: update on diagnosis and treatment. Clin Ophthalmol. 2023;17:53-70.
-
Bloom J, Madani R, Haidar AJ, Alasil T. Faricimab treatment of polypoidal choroidal vasculopathy resistant to intravitreal ranibizumab injections and ranibizumab port delivery (Susvimo). J VitreoRetin Dis. 2024;8(6):731-734. PMID:39554622.
-
Siddiqui MZ, Durrani A, Smith BT. Faricimab-associated retinal vasculitis. J VitreoRetin Dis. 2024;8(5):627-630.
-
Dhillon N, Macleod S. Intraocular inflammation following intravitreal faricimab: insights from five bilateral cases. J VitreoRetin Dis. 2025.
-
Yavari N, Gupta AS, Mitsios A, et al. Bilateral hemorrhagic occlusive retinal vasculitis and panuveitis following intravitreal faricimab injection. Am J Ophthalmol Case Rep. 2026;41:102532.
-
Clemens CR, Alten F, Zimmermann JA, Eter N. Old problem in a new guise: retinal pigment epithelium tear after intravitreal faricimab injection. Case Rep Ophthalmol. 2023;14:241-244.
-
Shigemoto Y, et al. Combination therapy of STTA and IVbr for brolucizumab-related IOI. Medicine. 2021;100(42):e27580.
-
Saito M, et al. IOI after IVbr monitored by laser flare-cell photometer. Am J Ophthalmol Case Rep. 2022;28:101727.
-
Cheung CMG, Lai TYY, Teo K, et al. Polypoidal choroidal vasculopathy: consensus nomenclature and non-indocyanine green angiograph diagnostic criteria. Eye. 2024;39:819-834.
-
Carta V, et al. Effect of intravitreal brolucizumab in PCV with foveal lipid exudation. Cureus. 2023;15(10):e47942.
-
Breazzano MP, Bond JB 3rd, Beardsley RM, et al. Endophthalmitis after intravitreal injection: early pars plana vitrectomy outcomes from the IRIS Registry (Intelligent Research in Sight). Ophthalmology. 2024. PMID:38432901.
-
Teo KYC, et al. Brolucizumab-associated intraocular inflammation: type IV hypersensitivity and cytokine activation. Am J Ophthalmol. 2024.
-
Stahl A, Lepore D, Fielder A, et al. Ranibizumab versus laser therapy for the treatment of very preterm infants with retinopathy of prematurity (RAINBOW): an open-label randomised controlled trial. Lancet. 2019;394(10208):1551-1559. doi:10.1016/S0140-6736(19)30690-5. PMID:31126750.
-
Marra KV, Chen JS, Nudleman E, Robbins SL. Review of retinopathy of prematurity management in the anti-VEGF era: evolving global paradigms, persistent challenges and our AI-assisted future. Ophthalmic Res. 2025.
-
Stahl A, Lepore D, Fielder AR, et al. Aflibercept vs laser for retinopathy of prematurity: the FIREFLEYE randomized clinical trial. JAMA. 2022;328(4):348-359. doi:10.1001/jama.2022.10727. PMID:35862896.
-
Marlow N, Reynolds JD, Lepore D, et al. Ranibizumab versus laser therapy for the treatment of very low birthweight infants with retinopathy of prematurity (RAINBOW): five-year outcomes. eClinicalMedicine. 2024;71:102567.
-
Mintz-Hittner HA, Kennedy KA, Chuang AZ. Efficacy of intravitreal bevacizumab for stage 3+ retinopathy of prematurity. N Engl J Med. 2011;364(7):603-615.
