라니비주맙 (루센티스®)

유리체 주사 (항VEGF 요법)
1. 유리체 주사(항VEGF 요법)란?
섹션 제목: “1. 유리체 주사(항VEGF 요법)란?”항VEGF 약물의 유리체내 주사는 약액을 유리체강에 직접 주입하여 VEGF의 작용(혈관신생 및 혈관투과성 항진)을 억제하는 치료법입니다. 주요 적응증은 연령관련 황반변성, 당뇨병성 황반부종, 망막정맥폐쇄 등의 망막혈관질환입니다.
항VEGF 요법은 2000년대에 급속히 임상 응용이 진행되었습니다.
| 연도 | 사건 |
|---|---|
| 2004년 | 베바시주맙의 안내 투여가 탐색적으로 시작됨 |
| 2006년 | 라니비주맙이 FDA 승인을 받음 (MARINA/ANCHOR 시험) 12) |
| 2011년 | 아플리버셉트가 FDA 승인을 받음 (VIEW 시험) 12) |
| 2019년 | 브롤루시주맙이 FDA 승인을 받음 (HAWK/HARRIER 시험) 10) |
| 2022년 | 파리시맙이 FDA 승인을 받음 (TENAYA/LUCERNE/YOSEMITE/RHINE 시험) 8) |
주요 적응증
섹션 제목: “주요 적응증”- 삼출성 연령관련 황반변성(nAMD): 맥락막 신생혈관(CNV)의 일차 치료1)
- 당뇨병성 황반부종(DME): 당뇨망막병증에 동반된 황반부종2)
- 망막정맥폐쇄(RVO): 망막 중심 또는 분지정맥폐쇄로 인한 황반부종6)
- 증식성 당뇨망막병증(PDR): PRP 보조 또는 대체(라니비주맙)5)
- 병적 근시에 동반된 맥락막 신생혈관(mCNV): 애플리버셉트, 라니비주맙4)
- 폴립양 맥락막혈관병증(PCV): 브롤루시주맙의 폴립 소실률이 높음14)
- 미숙아 망막병증(ROP): 라니비주맙 0.2 mg(2019년 승인), 애플리버셉트 0.4 mg(2022년 9월 승인)3)
- 지도형 위축(GA): 보체 억제제
- 안내염: 항생제, 항진균제, 항바이러스제 직접 투여
2. 사용 가능한 항VEGF 약물(약제 각론)
섹션 제목: “2. 사용 가능한 항VEGF 약물(약제 각론)”약제 비교(일람)
섹션 제목: “약제 비교(일람)”| 약제명 | 상품명 | 분자량 | 작용 기전 | 용량 | 일본 승인 |
|---|---|---|---|---|---|
| 라니비주맙 | 루센티스® | 48 kDa | VEGF-A Fab 단편 | 0.5 mg (AMD/RVO), 0.3 mg (DME) | 2009년 |
| 아플리베르셉트 | 아일리아® | 115 kDa | VEGF-A/B 및 PlGF 억제제(미끼 수용체) | 2 mg / 8 mg (HD) | 2012년 |
| 페갑타닙 | 마쿠젠® | — | VEGF165 앱타머 | 0.3 mg | 2008년 |
| 브롤루시주맙 | 베오뷰® | 26 kDa | VEGF-A scFv | 6 mg | 2020년 |
| 파리시맙 | 바비스모® | 149 kDa | VEGF-A + Ang-2 이중특이항체 | 6 mg | 2023년 |
| 베바시주맙 | 아바스틴® | 148 kDa | VEGF-A 전장 IgG | 1.25 mg | — (적응증 외 사용) |
아플리베르셉트 (아일리아®)
분자량: 115 kDa (융합 단백질)
작용 기전: VEGF-A, VEGF-B, PlGF 세 가지 인자를 동시 억제. VEGF-A 친화도 Kd=0.49 pM로 최고.
주요 임상시험: VIEW 시험에서 라니비주맙에 비열등. 고용량 8 mg(HD)은 최대 16주 간격. 12, 13)
특징: 광범위한 VEGF 억제 스펙트럼. ROP 적응증에서는 성인 용량의 20%(0.4 mg) 사용. 13)
브롤루시주맙 (베오뷰®)
파리시맙 (바비스모®)
베바시주맙 (아바스틴®)
분자량: 148 kDa (전장 IgG)
작용 기전: VEGF-A 억제 (안과 적응증 외 사용)
주요 임상시험: CATT 연구에서 라니비주맙과 동등한 유효성 확인. 12)
사용 현황: 비용이 현저히 낮음. 정맥 주사용 제제를 무균적으로 분주하여 사용.
페갑타닙 (마쿠젠®)
작용 기전: VEGF165 특이적 앱타머
현황: 2008년 승인된 1세대 약물. 현재는 신세대 약물이 주류. 초기 항VEGF 치료 개념 확립에 기여.
안과 영역에서는 적응증 외 사용(오프라벨)이며, 정맥주사용 제제를 안과용으로 무균 조제하여 사용합니다. CATT 연구에서 라니비주맙과 동등한 시력 개선 효과가 확인되었고, 비용이 훨씬 낮아 전 세계적으로 널리 사용됩니다. 그러나 일본에서는 보험 적용이 없으며, 사용은 기관의 판단에 따릅니다.
3. 적응 질환과 투여 요법
섹션 제목: “3. 적응 질환과 투여 요법”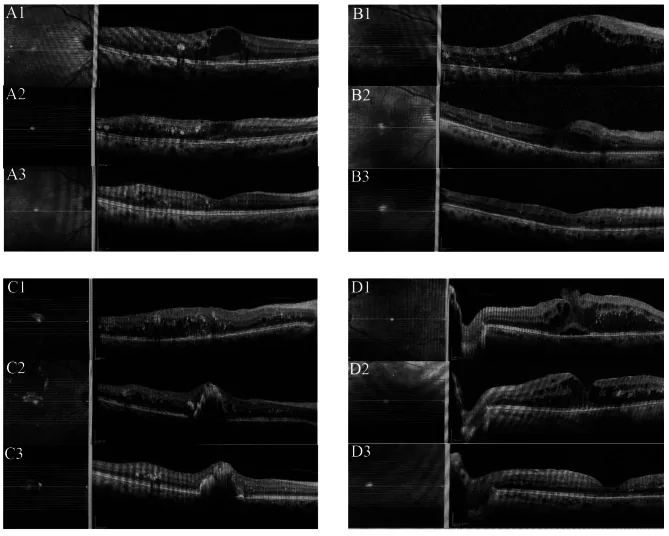
항VEGF 약물 투여는 도입기와 유지기의 두 단계로 이루어집니다.
- 도입기: 질환 활동성을 강력히 억제하기 위해 매월 고정으로 3~6회 투여합니다(질환 및 약물에 따라 다름).
- 유지기의 방식은 다음과 같은 세 가지가 있습니다.
- PRN (pro re nata): 매월 내원하여 재발 소견이 있는 경우에만 투여
- 고정 투여: 2개월마다, 3개월마다 등 일정 간격으로 정기 투여
- Treat and Extend (T&E): 활동성 소견이 없으면 투여 간격을 2주씩 연장, 재발 시 단축
라니비주맙은 도입기 3회(월 1회) 후 유지기 PRN 투여, 아플리버셉트는 도입기 3회(월 1회) 후 2개월마다 고정 투여 또는 T&E법이 기본 투여 방법으로 권장되지만, 최근에는 T&E법이 많은 기관에서 도입되고 있습니다.
질환별 권장 요법
섹션 제목: “질환별 권장 요법”| 적응 질환 | 권장 약물 | 도입기 | 유지기 |
|---|---|---|---|
| nAMD (라니비주맙) | 루센티스® 0.5 mg | 월 1회 × 3회1) | PRN (월 1회 관찰) |
| nAMD (아플리베르셉트) | 아일리아® 2 mg | 월 1회 × 3회1) | 2개월 고정 또는 T&E (최대 3개월) |
| nAMD (브롤루시주맙) | 베오뷰® 6 mg | 월 1회 × 3회 | 8~12주 간격10) |
| nAMD (파리시맙) | 바비스모® 6 mg | Q4W × 4회 | Q8W~Q16W8) |
| DME (아플리베르셉트) | 아일리아® 2 mg | 월 1회×5회2) | 2개월마다 |
| DME (라니비주맙) | 루센티스® 0.5 mg | 월 1회×3회2) | PRN |
| DME (파리시맙) | 바비스모® 6 mg | Q4W×4~6회 | PTI (최대 Q16W)8, 13) |
| RVO | 아플리베르셉트/파리시맙 | Q4W×6개월 | PTI (최대 Q16W)8) |
| PDR | 라니비주맙 0.3 mg | — | PRP에 비해 비열등5) |
| mCNV | 아플리버셉트/라니비주맙 | 초기 1~3회 | PRN (단회 관해 가능)4) |
| ROP (라니비주맙) | 루센티스® 0.2 mg/0.02 mL | 초회 | 재발 시 추가 (1개월 이상 간격)3) |
| ROP (아플리버셉트) | 아일리아® 0.4 mg/0.01 mL | 초회 | 재발 시 추가 (1개월 이상 간격)3) |
PCV(폴립양 맥락막혈관병증)의 대응: 브롤루시주맙은 폴립 소실률 약 79%로 다른 약물을 능가하며, 48주에 76%가 12주 간격을 유지했습니다. 14) 파리시맙은 라니비주맙 저항성 PCV 사례에서도 효과적이라는 보고가 있습니다. 15)
망막정맥폐쇄(RVO)에 대한 파리시맙
섹션 제목: “망막정맥폐쇄(RVO)에 대한 파리시맙”BALATON 시험(BRVO, n=553) 8): 파리시맙 6.0 mg 대 아플리베르셉트 2.0 mg Q4W, 24주 BCVA 변화는 각각 +16.9글자, +17.5글자(비열등성 달성, 95.03% CI 하한 > −4글자). CST 변화는 −311.4 μm 대 −304.4 μm. ≥15글자 개선: 파리시맙 56.1% 대 아플리베르셉트 60.4%. FA 누출 소실률은 파리시맙 33.6% 대 아플리베르셉트 21.0%(명목 p=0.0023)로 파리시맙이 유의하게 우수했습니다.
COMINO 시험(CRVO/HRVO, n=729) 8): 동일 요법으로 24주 BCVA 변화는 각각 +16.9글자, +17.3글자(비열등성 달성). CST 변화 −461.6 μm 대 −448.8 μm. ≥15글자 개선: 파리시맙 56.6% 대 아플리베르셉트 58.1%. FA 누출 소실률은 파리시맙 44.4% 대 아플리베르셉트 30.0%(명목 p=0.0002)로 유의하게 우수하여, Ang-2 억제를 통한 혈관 안정화 효과가 입증되었습니다.
RVO에서의 IOI 안전성(24주) 8): COMINO 시험에서 IOI는 파리시맙 2.2% 대 아플리베르셉트 1.1%. 중증 포도막염 2건(파리시맙군). BALATON/COMINO 두 시험 모두에서 망막혈관염 보고 없음. APTC 사건은 BALATON 파리시맙 1.1% 대 아플리베르셉트 1.5%, COMINO 1.1% 대 1.4%로 유사했습니다.
보조 치료(RVO): BRVO 황반부종에서 라니비주맙에 역치하 마이크로펄스 레이저를 병용하는 치료가 단독 요법과 비교 연구되고 있습니다. 11)
미숙아 망막병증(ROP)에 대한 항VEGF 요법
섹션 제목: “미숙아 망막병증(ROP)에 대한 항VEGF 요법”2022년 12월 기준, ROP 치료에 승인된 항VEGF 약물은 다음 두 가지입니다. 3)
- 라니비주맙(루센티스®) 0.2 mg/0.02 mL: 성인 용량의 40%. 2019년 승인. 바이알 제제만 ROP 승인.
- 아플리베르셉트(아일리아®) 0.4 mg/0.01 mL: 성인 용량의 20%. 2022년 9월 승인. 바이알 제제만 ROP 승인.
- 재투여는 1개월 이상 간격을 두어야 합니다(첨부문서 규정).
치료 적응증(ETROP 연구 기준에 따름) 3):
- plus disease를 동반한 Zone I 모든 ROP
- plus disease를 동반하지 않은 Zone I Stage 3 ROP
- plus disease를 동반한 Zone II Stage 3 ROP
- 공격형 ROP (A-ROP): 가능한 신속히 시행
주요 임상시험 데이터 26, 28, 30):
| 시험 | 약물/용량 | n | 치료 성공률 | 레이저 성공률 | 비고 |
|---|---|---|---|---|---|
| BEAT-ROP30) | 베바시주맙 0.625 mg | 150 | Zone I 재발 4% | Zone I 재발 22% | Zone I ROP에서 베바시주맙 우월 |
| RAINBOW26) | 라니비주맙 0.2 mg | 225 | 80.0% | 66.2% | 5세 고도근시 8% vs 레이저 24% |
| FIREFLEYE28) | 아플리버셉트 0.4 mg | 118 | 85.5% | 82.1% | 비열등성 기준 미달이나 역치 66% 초과 |
RAINBOW 시험의 장기 결과 26, 29): 5세 시점 고도근시는 라니비주맙 0.2 mg군 8% 대 레이저군 24% (유의한 차이). 구조 이상률은 라니비주맙 0.2 mg군 1.5% 대 레이저군 10%. 재치료율 31%, 재치료 시기는 주사 후 4~16주 (중앙값 8주).
FIREFLEYE 시험의 추적 결과 28): 재발률 21.9%, 재치료율 17.8%, 재치료까지 평균 기간 11주 (4~17주). FIREFLEYE Next (2세까지 추적)에서는 전신 발달 및 신경 발달에 대한 치료 관련 이상 반응 없음.
약물 간 재발률 비교 3):
- 아플리버셉트: 13.9
28% (재발 시기 평균 1114.2주) - 라니비주맙: 20.8
83.0% (재발 시기 5.99.3주로 조기 → 더 이른 시기부터 주의 깊은 관찰 필요)
A-ROP 주의사항 3): A-ROP에서 항VEGF 단독 요법은 75.087.5%에서 추가 치료가 필요합니다. 투여 후 13주 이내에 조기 재발이 있을 수 있으며, 1개월 미만의 재발에는 레이저 광응고술을 병용합니다. 섬유증식이 광범위한 경우 항VEGF 단독 치료는 적응증 외입니다(수축으로 인한 견인망막박리 위험).
- 주사 위치: 각막 윤부에서 1.0
1.5 mm 후방(성인의 3.54 mm와 크게 다름. 성인과 같은 위치에서는 망막 천공 위험). - 바늘 방향: 아래쪽(후방)으로 주사(수정체가 상대적으로 크므로 중앙 방향은 수정체 천공 위험).
- 30게이지 이하의 주사바늘을 사용합니다.
- 투여량 확인: 라니비주맙 0.02 mL, 아플리버셉트 0.01 mL(과량 투여 방지를 위해 신중히 확인).
- 마취: 점안마취, 정맥마취, 전신마취 중 시설 상황에 따라 선택.
경과 관찰 3): 망막 혈관이 Zone III까지 확장되지 않은 경우, 투여 후 17주까지는 주 1회 안저 검사가 권장됩니다. 투여 후 1년간 정기적인 안저 검사를 지속합니다(견인망막박리는 투여 후 4~335일에 발생한 보고 있음).
Protocol T 연구에서 1년 시점에 아플리버셉트의 시력 개선이 가장 컸습니다. 그러나 경증군(BCVA ≥20/40)에서는 세 약제 간 통계적 유의차가 없었습니다. 13) 파리시맙은 YOSEMITE/RHINE 연구에서 아플리버셉트와 동등한 시력 개선을 보이면서 유지기 주사 간격을 더 연장할 수 있습니다(2년차에 Q16W 달성 60~64%). 8) 환자 배경이나 통원 빈도 희망에 따라 약제를 선택합니다.
4. 유리체 주사 기술
섹션 제목: “4. 유리체 주사 기술”주사 전 준비
섹션 제목: “주사 전 준비”- 환자/주사안/약물 혼동 방지: 주사 결정 후 환자 목에 식별 태그를 걸어 확인합니다.
- 요오드 알레르기 확인: 사전에 반드시 확인합니다.
- 필요 물품 준비:
소독 및 마취 절차
섹션 제목: “소독 및 마취 절차”마취: 소독약이 반대쪽 눈에 튈 가능성을 고려하여, 베녹실® 점안액을 양안에 투여한 후 4% 자일로카인® 점안액을 주사안에 2회 점안합니다.
PA 요오드 소독 주의사항:
- 냉장고에서 꺼낸 직후의 PA 요오드는 항균 및 항진균 효과가 감소하므로 반드시 실온으로 되돌립니다.
- 비밀봉 용기에서 25°C로 보관할 경우 유효 성분 잔존율이 5시간에 60%까지 감소합니다. 오래 경과된 PA 요오드는 사용하지 마십시오.
- 세균 및 진균 불활성화에는 약 1분의 접촉 시간이 필요하므로, 세안 후에도 눈을 감아 결막과의 접촉 시간을 충분히 확보합니다.
구강 내 세균 대책: 구멍 뚫린 드레이프와 술자·보조자·환자 모두의 마스크 착용으로 비말을 방지합니다. 세균성 안내염의 원인균에 구강 내 세균이 포함되므로, 호흡기가 눈 표면으로 퍼지지 않도록 드레이프와 마스크로 눈 사이를 밀봉하는 것이 바람직합니다.
주입 위치와 바늘 방향
섹션 제목: “주입 위치와 바늘 방향”외과적 윤부로부터의 주입 거리는 다음과 같습니다. 주입 위치를 지키면 섬모체 평면부(섬모체 주름부 후방)에서의 주입이 가능해져 수정체 손상이나 유리체 출혈을 방지할 수 있습니다.
| 눈 상태 | 윤부로부터의 거리 |
|---|---|
| 수정체안 | 4 mm (섬모체 평면부) |
| 무수정체안 또는 안내렌즈 삽입안 | 3.5 mm |
| 미숙아 (ROP) | 1.0~1.5 mm |
바늘은 유리체강의 중심을 향해 주입합니다. 윤부에 가까운 위치에서 주입하면 섬모체 주름부를 손상시켜 유리체 출혈이 발생하기 쉽고, 수정체와의 거리가 가까워져 수정체 손상 위험이 높아집니다.
주입 술기와 수술 후 관리
섹션 제목: “주입 술기와 수술 후 관리”- 구멍 뚫린 드레이프를 부착하고, 개검기로 눈꺼풀을 벌립니다.
- 캘리퍼스로 윤부로부터의 주입 거리를 측정합니다.
- 주사 부위는 귀 위쪽 또는 귀 아래쪽 사분면으로 한다 (수평직근 손상 방지).
- 겸자로 안구를 고정하고, 주사 전에 결막을 약간 앞쪽으로 밀어 바늘 제거 후 바늘 구멍이 어긋나게 하여 액체 누출을 방지한다.
- 30G 짧은 바늘을 공막에 거의 수직으로 삽입하고 약액을 천천히 주입한다 (급속 주입은 지속적인 안압 상승의 원인이 됨).
- 바늘 제거 후 면봉으로 주사 부위를 압박한다.
- 수술 직후 시력 (손가락 헤아리기)을 확인한다. 손가락 헤아리기가 인식되지 않으면 전방천자를 시행한다.
- 수술 후 3일간 광범위 항생제 점안액을 계속 사용한다.
5. 합병증과 대책
섹션 제목: “5. 합병증과 대책”감염성 안내염 (가장 중요한 합병증)
섹션 제목: “감염성 안내염 (가장 중요한 합병증)”감염성 안내염은 가장 심각한 합병증으로, 발생률은 약 0.027~0.065%입니다. 발생 시 반코마이신 1.0mg과 세프타지딤 2.0mg의 유리체내 주사에 의한 응급 치료가 필요합니다.
가장 중요한 예방 조치:
- 포비돈 요오드의 적절한 소독 (실온으로 되돌리고, 1분 이상 접촉 시간)
- 구멍이 뚫린 드레이프 사용 (구강 내 세균 비말 방지)
수술 후 예방적 항생제 점안에 대해서는 여러 연구에서 안내염 발생률을 낮추지 않는 것으로 나타났으며, 유효성에 대한 증거는 일치하지 않습니다.
무균성 안내염
섹션 제목: “무균성 안내염”세균 감염을 동반하지 않은 안내 염증 반응으로, 항VEGF 약물 투여 후 드문 합병증으로 보고됩니다7). 약제, 제제 조제, 로트 등에 따라 빈도에 차이가 있으므로 감염성 안내염과의 감별을 우선시합니다.
- 발병 시기: 주사 후 조기에 발생하는 경우가 많지만, 감염성 안내염과의 감별이 필요합니다7)
- 주요 소견: 유리체 혼탁, 전방 염증, 시력 저하 등이 나타날 수 있습니다7)
- 확진: 배양 음성 (PCR에 의한 병원체 배제도 유용)
- 약제 차이: 베바시주맙, 라니비주맙, 아플리버셉트 모두에서 보고가 있지만, 보고 빈도는 연구 및 조제 조건에 따라 다릅니다7)
- 치료: 경증에서는 보존적 치료를 하는 경우가 많지만, 감염성 안내염을 배제할 수 없는 경우 배양 채취, 항생제 유리체내 투여, 유리체 절제술을 포함하여 신속히 판단합니다. 7)
IRIS Registry의 1,044례 분석에서는 유리체 주사 후 안내염에 대한 조기 유리체 절제술의 결과가 대규모 데이터로 검토되었습니다24).
안내 염증(IOI) 및 망막 혈관염 (브롤루시주맙 특이적)
섹션 제목: “안내 염증(IOI) 및 망막 혈관염 (브롤루시주맙 특이적)”브롤루시주맙은 다른 항VEGF 약물보다 더 높은 빈도로 IOI를 유발하는 것으로 알려져 있습니다.
| 시험/집단 | IOI 발생률 | 비고 |
|---|---|---|
| HAWK/HARRIER (IOI 관련) | 보고됨 | 망막혈관염 및 혈관폐쇄를 포함한 염증성 이상반응 주의10) |
| KESTREL (6mg) | 3.7% (대조군 0.5%) | DME 시험10) |
| MERLIN (4주 간격) | 9.3% | 시험 중단10) |
| 일본인 증례 | 증례 보고 및 시판 후 자료에서 보고됨 | 빈도 추정 시 주의 |
| 시판 후 (혈관염 + 폐쇄 복합) | 3.73/10,000회 주사 |
대부분의 IOI는 첫 투여 후 6개월 이내, 4회 이내 주사 후에 발생합니다. 10)
기전: 항약물 항체나 면역 복합체를 매개한 염증 기전이 관여할 가능성이 논의되고 있습니다. 10, 25)
공막염 (세계 최초 보고): 브롤루시주맙 투여 후 후부 공막염이 일본인 3명에서 보고되었으며, 안압이 24~49 mmHg로 상승하고, 그중 1예는 망막동맥 폐쇄 및 혈관염으로 진행되었습니다. 9)
치료: 트리암시놀론 아세토니드 (STTA) 5~20 mg의 결막하 또는 테논낭하 주사가 효과적입니다. 예방적 STTA 투여와의 병용도 보고되었습니다. 20, 21)
파리시맙 관련 IOI
섹션 제목: “파리시맙 관련 IOI”IOI 발생률은 nAMD 2.0%, DME 1.3%, RVO 1.4%이며, 양안 투여 예에서는 8.5%에서 관찰되었습니다. 8) 시판 후 조사에서 망막혈관염은 0.17/10,000회 주사로 낮은 빈도이지만, 출혈성 폐쇄성 망막혈관염(HORV)은 중증 결과를 초래할 수 있습니다. 8) 파리시맙 관련 망막혈관염 및 IOI는 증례 보고로 축적되고 있으며, 중증 예에서는 출혈성 폐쇄성 망막혈관염(HORV)이 문제가 됩니다. 16-18)
RPE 열공은 파리시맙군에서 TENAYA 2.7%, LUCERNE 3.0%에서 발생했으며, PED 높이 550 μm 초과가 위험 인자입니다. 19)
Crunch 증후군 (ROP 치료 후 견인성 망막박리)
섹션 제목: “Crunch 증후군 (ROP 치료 후 견인성 망막박리)”ROP 환자에서 항VEGF 요법 후 섬유혈관막이 급속히 수축하여 견인성 망막박리(TRD)를 초래하는 합병증을 Crunch 증후군이라고 합니다. 27)
- 기전: VEGF 억제로 TGF-β 활성이 상대적으로 항진됩니다. TGF-β는 섬유화 및 세포외 기질 리모델링을 촉진합니다. 미숙아는 생리적으로 TGF-β 상승기에 있으며, 항VEGF 투여로 불균형이 증폭됩니다. 27)
- 예방: 치료 전에 섬유성 변화를 신중히 평가합니다. 광범위한 충혈된 섬유증식이 있는 경우 항VEGF 단독 치료는 적응증이 아닙니다. 3)
- 후기 합병증: 견인성 망막박리는 투여 후 4~335일에 발생이 보고되었으며, 투여 후 1년간 정기적인 안저 검사가 필수적입니다. 3)
지속성 무혈관 망막 (PAR)
섹션 제목: “지속성 무혈관 망막 (PAR)”항VEGF 치료 후에도 완전한 망막 혈관화가 달성되지 않을 수 있으며, 혈관-무혈관 경계에 션트 혈관이나 비정상 분지 패턴이 형성될 수 있습니다. 27) 장기 추적 관찰이 필요합니다(재발 위험 및 후기 합병증 평가). 형광 안저 혈관조영술은 망막 혈관의 정상 발달 평가에 유용합니다.
바늘 관련 기계적 합병증
섹션 제목: “바늘 관련 기계적 합병증”- 수정체 손상: 백내장 진행. 삽입 거리(유수정체안 4mm) 준수로 예방합니다.
- 망막 손상: 열공성 망막박리. 30G 짧은 바늘의 적절한 삽입으로 예방합니다.
- 섬모체 손상: 유리체 출혈. 삽입 위치 및 방향 준수로 예방합니다.
안압 상승
섹션 제목: “안압 상승”주사 직후의 일시적 안압 상승은 주사를 받은 모든 환자에서 발생합니다. 0.05mL 주입 시 안압이 즉시 50mmHg로 상승하지만, 일반적으로 가역적입니다. 녹내장 병력이 있는 경우 지속적인 안압 상승에 주의해야 하며, 필요 시 전방천자로 감압합니다.
동맥 혈전색전증(ATE)
섹션 제목: “동맥 혈전색전증(ATE)”뇌졸중 및 심근경색의 위험이 이론적으로 존재합니다. 브롤루시주맙의 HAWK 시험에서 ATE는 1.1~1.4%로 보고되었습니다. 10) 병력이 있는 환자에서는 신중히 투여해야 합니다.
6. 병태생리(VEGF의 역할과 약물의 작용 기전)
섹션 제목: “6. 병태생리(VEGF의 역할과 약물의 작용 기전)”VEGF의 병적 역할
섹션 제목: “VEGF의 병적 역할”VEGF는 혈관 내피 세포의 VEGFR-1 및 VEGFR-2에 결합하여 내피 세포 증식, 혈관 투과성 항진, 신생 혈관 형성을 촉진합니다.
- AMD : 맥락막 신생혈관(CNV)의 증식 및 혈관 투과성 항진
- DME : 혈액-망막 장벽(BRB)의 파괴 → 황반 부종 형성
- RVO : 허혈 → VEGF 과잉 → 황반 부종 및 신생혈관
유리체강 내 주사를 통해 VEGF 수치가 감소하면 혈관 투과성이 낮아지고 황반 부종이 개선됩니다. 항VEGF 약물의 효과는 일시적이므로 정기적인 재투여가 필요합니다.
미숙아 망막병증(ROP)의 병태생리
섹션 제목: “미숙아 망막병증(ROP)의 병태생리”ROP 발병은 2단계로 진행됩니다. 27)
1단계(혈관화 정지기) : 조산 후 고산소 환경에서 VEGF와 IGF-1이 억제됩니다. 이로 인해 정상적인 망막 혈관화가 저해되어 무혈관 망막이 형성됩니다.
2단계(병적 신생혈관기) : 산소 제거 후, 발달에 따라 커지는 허혈 망막에서 과잉 VEGF가 방출됩니다. 혈관-무혈관 경계에서 병적 신생혈관이 발생하여 12기의 경계선, 융기에서 3기의 망막 외 신생혈관으로 진행됩니다. 중증 사례에서는 45기의 견인 망막 박리에 이릅니다.
항VEGF 약물은 2단계의 과잉 VEGF 생성을 억제하여 병적 신생혈관을 차단합니다. 그러나 생리적 VEGF 의존성 혈관화도 억제하므로 정상 혈관 발달에 미치는 영향을 신중히 모니터링해야 합니다.
각 약물의 분자적 특징
섹션 제목: “각 약물의 분자적 특징”| 약물 | 분자량 | VEGF-A 친화도(Kd) | 표적 |
|---|---|---|---|
| 브롤루시주맙 | 26 kDa | 28.4 pM | VEGF-A (모든 이소형) |
| 라니비주맙 | 48 kDa | 20.6 pM | VEGF-A (모든 이소형) |
| 아플리베르셉트 | 115 kDa | 0.49 pM (최고) | VEGF-A/B, PlGF |
| 베바시주맙 | 148 kDa | 35.1 pM | VEGF-A |
| 파리시맙 | 149 kDa | — | VEGF-A + Ang-2 |
Ang-2와 파리시맙의 작용
섹션 제목: “Ang-2와 파리시맙의 작용”Ang-2는 Tie-2 수용체의 길항제로 작용하여 혈관 불안정화에 관여합니다. 파리시맙이 Ang-2를 억제함으로써 Tie-2 경로가 정상화되고 혈관 안정성이 향상되며 VEGF 민감도가 감소합니다. 이중 억제 효과가 투여 간격 연장을 가능하게 하는 약리학적 기반입니다.
도입기 집중 투여의 의의
섹션 제목: “도입기 집중 투여의 의의”도입기에 매월 고정으로 3~5회 투여하는 이유는 질환 활동성을 조기에 강력하게 억제하기 위함입니다. T&E법은 유리체 내 약물 농도가 치료 범위를 유지할 수 있는 범위에서 재발을 허용하지 않는 틀을 제공합니다.
7. 최신 연구와 향후 전망 (연구 단계 보고)
섹션 제목: “7. 최신 연구와 향후 전망 (연구 단계 보고)”포트 전달 시스템 (Susvimo)
섹션 제목: “포트 전달 시스템 (Susvimo)”라니비주맙의 PDS(포트 전달 시스템)에서는 6개월마다 보충 투여로 98%가 월 1회 주사가 필요 없게 되었습니다. 12) 2025년에는 DME에 대한 적응증 추가가 검토되고 있습니다. 13) 주사 부담의 대폭적인 경감이 기대됩니다.
고용량 아플리버셉트 8 mg (Eylea® HD)
섹션 제목: “고용량 아플리버셉트 8 mg (Eylea® HD)”PULSAR 시험(AMD)에서 48주 시점에 79%가 12주 간격, 77%가 16주 간격을 유지했습니다. 12) PHOTON 시험(DME)에서도 93%가 12주 이상의 간격을 달성했습니다. 13)
브롤루시주맙의 적응증 확대 시험
섹션 제목: “브롤루시주맙의 적응증 확대 시험”PCV 및 황반 모세혈관확장증 1형(AT1)을 대상으로 한 PROUD 시험(한국)이 진행 중이며, 아시아 특이 질환에 대한 근거 축적이 기대됩니다. 14, 23)
파리시맙의 PCV 대상 시험(SALWEEN 시험)
섹션 제목: “파리시맙의 PCV 대상 시험(SALWEEN 시험)”PCV 환자에 대한 파리시맙의 효과를 평가하는 SALWEEN 시험이 진행 중입니다. 22) PCV 환자의 방수에서 Ang-2 수치가 높게 확인되었으며, Ang-2 억제의 추가 효과가 기대됩니다.
STTA 병용을 통한 IOI 예방
섹션 제목: “STTA 병용을 통한 IOI 예방”결막하/테논낭하 트리암시놀론 아세토나이드(STTA)와 브롤루시주맙의 병용 투여가 IOI 예방과 삼출 조절 모두에 효과적일 가능성이 있습니다. 20, 21) 최적 용량 및 투여 시점 표준화를 위한 연구가 진행 중입니다.
바이오마커를 통한 조기 감별
섹션 제목: “바이오마커를 통한 조기 감별”무균성 안내염과 감염성 안내염의 조기 감별을 위해 유리체액 내 사이토카인 프로파일(IL-6, IL-8, IL-10) 측정이 보조 도구로 유용할 것으로 기대됩니다. 7)
바이오시밀러
섹션 제목: “바이오시밀러”라니비주맙 및 베바시주맙의 바이오시밀러가 등장하고 있습니다. 비용이 크게 절감되어 치료 지속률 향상과 의료 접근성 개선이 기대됩니다. 12)
ROP 치료의 새로운 후보 약물 27)
섹션 제목: “ROP 치료의 새로운 후보 약물 27)”- 베타 차단제(프로프라놀롤) : 경구 투여로 2기 ROP의 중증화를 예방합니다. 0.2% 점안액은 안전하고 효과적(1기 증식기에 시작한 경우)으로 간주되지만 장기 데이터는 부족합니다.
- 아라키돈산(AA) 및 DHA 보충제 : Mega Donna Mega 시험에서 중증 ROP 발생을 50% 감소시켰습니다(15.8% 대 33.3%).
- 카페인 : 미숙아 무호흡증 치료제이지만 VEGF 및 MMPs 하향 조절을 통해 ROP 진행을 억제할 가능성이 있습니다.
- 비타민 A: 메타분석에서 ROP 발생 및 진행 감소 효과 확인.
SAFER-ROP 프로토콜 27)
섹션 제목: “SAFER-ROP 프로토콜 27)”SAFER-ROP는 신생아 특유의 과제(NICU 환경에서의 감염 예방, 주사 후 모니터링)에 대응한 표준화 프로토콜로 제안되었다. Short Needle, Antiseptic/Antibiotic, Follow-Up, Extra Attention to Detail, Recheck의 두문자어에 기반하여 각 시설에서의 시술 표준화에 활용된다.
8. 참고문헌
섹션 제목: “8. 참고문헌”-
日本眼科学会. 新生血管型加齢黄斑変性の診療ガイドライン. 日眼会誌. 2024.
-
Lim JI, Kim SJ, Bailey ST, Kovach JL, Vemulakonda GA, Ying GS, Flaxel CJ; American Academy of Ophthalmology Preferred Practice Pattern Retina/Vitreous Committee. Diabetic Retinopathy Preferred Practice Pattern®. Ophthalmology. 2025. doi:10.1016/j.ophtha.2024.12.020. PMID:39918521.
-
日本未熟児網膜症研究会. 未熟児網膜症に対する抗VEGF療法の手引き(第2版). 2024.
-
Ikuno Y, Ohno-Matsui K, Wong TY, et al. Intravitreal aflibercept injection for myopic choroidal neovascularization: the MYRROR study. Ophthalmology. 2015;122(6):1220-1227. doi:10.1016/j.ophtha.2015.07.013. PMID:26300374.
-
American Academy of Ophthalmology. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024. [Protocol S data]
-
American Academy of Ophthalmology. Retinal Vein Occlusion Preferred Practice Pattern. Ophthalmology. 2024. [BRAVO data]
-
Baudin F, et al. Sterile endophthalmitis after anti-vascular endothelial growth factor agents: a literature review. J Fr Ophtalmol. 2015;38(9):865-871. PMID:26501239.
-
Tadayoni R, Paris LP, Danzig CJ, et al. Efficacy and safety of faricimab for macular edema due to retinal vein occlusion: 24-week results from the BALATON and COMINO trials. Ophthalmology. 2024;131(8):950-960.
-
Takayama T, et al. Scleritis following intravitreal brolucizumab injection: a case series. J Med Case Rep. 2024;18:80.
-
Sharma A, et al. Understanding retinal vasculitis associated with brolucizumab. Ocul Immunol Inflamm. 2022;30(6):1508-1510. PMID:34014141.
-
Nawar AE. Subthreshold micropulse laser combined with ranibizumab versus ranibizumab monotherapy in branch retinal vein occlusion with macular edema. Clin Ophthalmol. 2022;16:1139-1151.
-
Flaxel CJ, Adelman RA, Bailey ST, et al. Age-related macular degeneration preferred practice pattern. Ophthalmology. 2024;131(1):P1-P68.
-
Flaxel CJ, Adelman RA, Bailey ST, et al. Diabetic retinopathy preferred practice pattern. Ophthalmology. 2024;131(1):P99-P168.
-
Sen P, et al. Polypoidal choroidal vasculopathy: update on diagnosis and treatment. Clin Ophthalmol. 2023;17:53-70.
-
Bloom J, Madani R, Haidar AJ, Alasil T. Faricimab treatment of polypoidal choroidal vasculopathy resistant to intravitreal ranibizumab injections and ranibizumab port delivery (Susvimo). J VitreoRetin Dis. 2024;8(6):731-734. PMID:39554622.
-
Siddiqui MZ, Durrani A, Smith BT. Faricimab-associated retinal vasculitis. J VitreoRetin Dis. 2024;8(5):627-630.
-
Dhillon N, Macleod S. Intraocular inflammation following intravitreal faricimab: insights from five bilateral cases. J VitreoRetin Dis. 2025.
-
Yavari N, Gupta AS, Mitsios A, et al. Bilateral hemorrhagic occlusive retinal vasculitis and panuveitis following intravitreal faricimab injection. Am J Ophthalmol Case Rep. 2026;41:102532.
-
Clemens CR, Alten F, Zimmermann JA, Eter N. Old problem in a new guise: retinal pigment epithelium tear after intravitreal faricimab injection. Case Rep Ophthalmol. 2023;14:241-244.
-
Shigemoto Y, et al. Combination therapy of STTA and IVbr for brolucizumab-related IOI. Medicine. 2021;100(42):e27580.
-
Saito M, et al. IOI after IVbr monitored by laser flare-cell photometer. Am J Ophthalmol Case Rep. 2022;28:101727.
-
Cheung CMG, Lai TYY, Teo K, et al. Polypoidal choroidal vasculopathy: consensus nomenclature and non-indocyanine green angiograph diagnostic criteria. Eye. 2024;39:819-834.
-
Carta V, et al. Effect of intravitreal brolucizumab in PCV with foveal lipid exudation. Cureus. 2023;15(10):e47942.
-
Breazzano MP, Bond JB 3rd, Beardsley RM, et al. Endophthalmitis after intravitreal injection: early pars plana vitrectomy outcomes from the IRIS Registry (Intelligent Research in Sight). Ophthalmology. 2024. PMID:38432901.
-
Teo KYC, et al. Brolucizumab-associated intraocular inflammation: type IV hypersensitivity and cytokine activation. Am J Ophthalmol. 2024.
-
Stahl A, Lepore D, Fielder A, et al. Ranibizumab versus laser therapy for the treatment of very preterm infants with retinopathy of prematurity (RAINBOW): an open-label randomised controlled trial. Lancet. 2019;394(10208):1551-1559. doi:10.1016/S0140-6736(19)30690-5. PMID:31126750.
-
Marra KV, Chen JS, Nudleman E, Robbins SL. Review of retinopathy of prematurity management in the anti-VEGF era: evolving global paradigms, persistent challenges and our AI-assisted future. Ophthalmic Res. 2025.
-
Stahl A, Lepore D, Fielder AR, et al. Aflibercept vs laser for retinopathy of prematurity: the FIREFLEYE randomized clinical trial. JAMA. 2022;328(4):348-359. doi:10.1001/jama.2022.10727. PMID:35862896.
-
Marlow N, Reynolds JD, Lepore D, et al. Ranibizumab versus laser therapy for the treatment of very low birthweight infants with retinopathy of prematurity (RAINBOW): five-year outcomes. eClinicalMedicine. 2024;71:102567.
-
Mintz-Hittner HA, Kennedy KA, Chuang AZ. Efficacy of intravitreal bevacizumab for stage 3+ retinopathy of prematurity. N Engl J Med. 2011;364(7):603-615.
