라니비주맙 (루센티스®)

유리체 주사 (항VEGF 요법)
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 유리체 주사(항VEGF 요법)란?
섹션 제목: “1. 유리체 주사(항VEGF 요법)란?”항VEGF 약물의 유리체내 주사는 약액을 유리체강에 직접 주입하여 VEGF의 작용(혈관신생 및 혈관투과성 항진)을 억제하는 치료법입니다. 주요 적응증은 연령관련 황반변성, 당뇨병성 황반부종, 망막정맥폐쇄 등의 망막혈관 질환입니다.
항VEGF 요법은 2000년대에 급속히 임상 응용이 진행되었습니다.
| 연도 | 사건 |
|---|---|
| 2004년 | 베바시주맙의 안내 투여가 탐색적으로 시작됨 |
| 2006년 | 라니비주맙이 FDA 승인을 받음 (MARINA/ANCHOR 임상시험) 12) |
| 2011년 | 아플리버셉트가 FDA 승인을 받음 (VIEW 임상시험) 12) |
| 2019년 | 브롤루시주맙이 FDA 승인을 받음 (HAWK/HARRIER 임상시험) 10) |
| 2022년 | 파리시맙이 FDA 승인을 받음 (TENAYA/LUCERNE/YOSEMITE/RHINE 임상시험) 8) |
주요 적응증
섹션 제목: “주요 적응증”- 삼출성 연령 관련 황반변성(nAMD): 맥락막 신생혈관(CNV)의 1차 치료
- 당뇨병성 황반부종(DME): 당뇨망막병증에 동반된 황반부종
- 망막정맥폐쇄(RVO): 망막 중심 또는 분지 정맥 폐쇄로 인한 황반부종6)
- 증식당뇨망막병증(PDR): PRP 보조 또는 대체(라니비주맙)5)
- 병적 근시에 동반된 맥락막 신생혈관(mCNV): 애플리버셉트, 라니비주맙4)
- 폴립양 맥락막혈관병증(PCV): 브롤루시주맙의 폴립 소실률이 높음14)
- 미숙아 망막병증(ROP): 라니비주맙 0.2mg(2019년 승인), 애플리버셉트 0.4mg(2022년 9월 승인). 둘 다 성인 용량의 20~40%에 해당하는 저용량 제제가 사용됩니다.3)
- 지도모양 위축(GA): 보체 억제제
- 안내염: 항생제, 항진균제, 항바이러스제 직접 투여
- 안내 악성 림프종: 메토트렉세이트
2. 사용 가능한 항VEGF 약물(약물 각론)
섹션 제목: “2. 사용 가능한 항VEGF 약물(약물 각론)”약물 비교(일람)
섹션 제목: “약물 비교(일람)”| 약물명 | 상품명 | 분자량 | 작용 기전 | 용량 | 승인 (일본) |
|---|---|---|---|---|---|
| 라니비주맙 | 루센티스® | 48 kDa | VEGF-A Fab 단편 | 0.5 mg (AMD/RVO), 0.3 mg (DME) | 2009년 |
| 아플리버셉트 | 아일리아® | 115 kDa | VEGF-A/B 및 PlGF 억제 (미끼 수용체) | 2 mg / 8 mg (HD) | 2012년 |
| 페갑타닙 | Macugen® | — | VEGF165 앱타머 | 0.3 mg | 2008년 |
| 브롤루시주맙 | Beovu® | 26 kDa | VEGF-A scFv | 6 mg | 2020년 |
| 파리시맙 | Vabysmo® | 149 kDa | VEGF-A + Ang-2 이중특이항체 | 6 mg | 2023년 |
| 베바시주맙 | 아바스틴® | 148 kDa | VEGF-A 전장 IgG | 1.25 mg | — (적응증 외 사용) |
아플리버셉트 (아일리아®)
분자량: 115 kDa (융합 단백질)
작용 기전: VEGF-A, VEGF-B, PlGF 세 가지 인자를 동시 억제. VEGF-A 친화도 Kd=0.49 pM로 최고.
주요 임상시험: VIEW 시험에서 라니비주맙에 비열등. 고용량 8 mg (HD)은 최대 16주 간격 가능. 12, 13)
특징: 광범위한 VEGF 억제 스펙트럼. DME에서 Protocol T 시험에서 1년 시력 개선이 최대였습니다. 13)
브롤루시주맙 (Beovu®)
분자량: 26 kDa (scFv, 기존 약물 중 최소)
작용 기전: scFv 구조로 아플리베르셉트의 약 12배 몰 농도로 투여 가능. 조직 침투성이 높습니다.
주요 시험: HAWK/HARRIER 시험에서 비열등성 달성. 최대 55%가 12주 간격 유지. 10)
주의점: IOI 발생률 4.4% (HAWK/HARRIER), 일본인 15~20%. 망막 혈관염 및 혈관 폐쇄 위험. 10)
파리시맙 (Vabysmo®)
베바시주맙 (Avastin®)
분자량: 148 kDa (전장 IgG)
작용 기전: VEGF-A 억제 (안과 적응증 외 사용)
주요 시험: CATT 시험에서 라니비주맙과 동등한 유효성 확인. 12)
사용 상황: 비용이 크게 낮습니다. 정맥 주사용 제제를 무균적으로 분주하여 사용합니다.
페갑타닙 (Macugen®)
작용 기전: VEGF165 특이적 앱타머
현황: 2008년 승인된 1세대 약물. 현재는 신세대 약물이 주류입니다. 초기 항VEGF 치료 개념 확립에 기여했습니다.
안과 영역에서는 적응증 외 사용(오프라벨)이며, 정맥 주사용 제제를 안과용으로 무균적으로 조제하여 사용합니다. CATT 시험에서 라니비주맙과 동등한 시력 개선 효과가 확인되었으며, 비용이 크게 낮아 전 세계적으로 널리 사용됩니다. 그러나 일본에서는 보험 적용이 없으며, 사용은 기관의 판단에 따릅니다.
3. 적응 질환과 투여 요법
섹션 제목: “3. 적응 질환과 투여 요법”항VEGF 약물 투여는 도입기와 유지기의 두 단계로 진행합니다.
- 도입기: 질환 활동성을 강력히 억제하기 위해 매월 고정으로 3~6회 투여합니다 (질환 및 약물에 따라 다름).
- 유지기의 방식은 다음 세 가지가 있습니다.
- PRN (pro re nata): 매월 내원하여 재발 소견이 있을 때만 투여
- 고정 투여: 2개월마다, 3개월마다 등 일정 간격으로 정기 투여
- Treat and Extend (T&E): 활동성 소견이 없으면 투여 간격을 2주씩 연장, 재발 시 단축
라니비주맙은 도입기 3회(월 1회) 후 유지기 PRN 투여, 아플리베르셉트는 도입기 3회(월 1회) 후 2개월마다 고정 투여 또는 T&E법이 기본 투여 방법으로 권장되지만, 최근에는 많은 기관에서 T&E법이 도입되고 있습니다.
질환별 권장 요법
섹션 제목: “질환별 권장 요법”| 적응 질환 | 권장 약제 | 도입기 | 유지기 |
|---|---|---|---|
| nAMD (라니비주맙) | 루센티스® 0.5 mg | 월 1회 × 3회1) | PRN (월 1회 관찰) |
| nAMD (아플리베르셉트) | 아일리아® 2 mg | 월 1회 × 3회1) | 2개월마다 고정 또는 T&E (최대 3개월) |
| nAMD (브롤루시주맙) | 베오뷰® 6 mg | 월 1회 × 3회 | 8~12주 간격10) |
| nAMD (파리시맙) | 바비스모® 6 mg | Q4W×4회 | Q8W~Q16W8) |
| DME (애플리버셉트) | 아일리아® 2 mg | 월 1회×5회2) | 2개월마다 |
| DME (라니비주맙) | 루센티스® 0.5 mg | 월 1회×3회2) | PRN |
| DME (파리시맙) | 바비스모® 6 mg | Q4W×4~6회 | PTI (최대 Q16W)8, 13) |
| RVO | 아플리베르셉트/파리시맙 | Q4W×6개월 | PTI (최대 Q16W) 8) |
| PDR | 라니비주맙 0.3 mg | — | PRP에 비해 비열등 5) |
| mCNV | 아플리베르셉트/라니비주맙 | 초기 1~3회 | PRN (단회 관해 가능) 4) |
| ROP (라니비주맙) | 루센티스® 0.2 mg | 초회 | 재발 시 추가 (1개월 이상 간격) 3) |
| ROP (아플리베르셉트) | 아일리아® 0.4 mg | 초회 | 재발 시 추가 (1개월 이상 간격) 3) |
PCV (폴립양 맥락막혈관병증) 대응: 브롤루시주맙은 폴립 소실률 약 79%로 다른 약제보다 우수하며, 12주 간격 유지율 76% (48주)를 달성했습니다. 14) 파리시맙은 라니비주맙 저항성 PCV 사례에서도 효과적이라는 보고가 있습니다. 15)
BALATON 시험 (BRVO, n=553): 파리시맙 6.0 mg 대 아플리베르셉트 2.0 mg Q4W, 24주 BCVA 변화는 각각 +16.9글자, +17.5글자 (비열등성 달성). FA 누출 소실률은 파리시맙 33.6% 대 아플리베르셉트 21.0% (명목 p=0.0023)로 파리시맙이 유의하게 우수했습니다. 8)
COMINO 시험 (CRVO/HRVO, n=729): 동일 요법으로 24주 BCVA 변화는 각각 +16.9글자, +17.3글자 (비열등성 달성). CST 변화 −461.6 μm 대 −448.8 μm. FA 누출 소실률은 파리시맙 44.4% 대 아플리베르셉트 30.0% (명목 p=0.0002)로 유의하게 우수하여, Ang-2 억제에 의한 혈관 안정화 효과가 입증되었습니다. 8)
STTA 병용 (RVO): 라니비주맙 + 상맥락막강 트리암시놀론 4 mg 병용은 라니비주맙 단독과 비교하여 주사 횟수를 유의하게 감소시킵니다 (4.4회 → 2.47회, p<0.001). 11)
3-8. 미숙아 망막병증 (ROP)에 대한 항VEGF 요법
섹션 제목: “3-8. 미숙아 망막병증 (ROP)에 대한 항VEGF 요법”ROP 치료에서 승인된 항VEGF 약제 (2022년 12월 기준)는 다음과 같은 2가지입니다. 3)
- 라니비주맙 (루센티스®) 0.2 mg/0.02 mL: 성인 용량의 40%. 2019년 승인.
- 아플리베르셉트 (아일리아®) 0.4 mg/0.01 mL: 성인 용량의 20%. 2022년 9월 승인.
- 재투여는 1개월 이상 간격을 두어야 합니다 (첨부문서 규정).
치료 적응증 (ETROP 연구 기준에 따름) 3):
- plus disease를 동반한 Zone I 모든 ROP
- plus disease가 없는 Zone I Stage 3 ROP
- plus disease를 동반한 Zone II Stage 3 ROP
- 공격형 ROP (A-ROP): 가능한 한 신속히 시행
재발률과 경과 관찰 3):
아플리버셉트의 재발률은 13.928%(재발 시기 평균 1114.2주), 라니비주맙은 20.883.0%(재발 시기 5.99.3주로 조기)입니다. 라니비주맙 사용 시 투여 후 조기부터 주의 깊은 관찰이 필요합니다. 망막 혈관이 Zone III까지 확장되지 않은 경우, 투여 후 17주까지 주 1회 안저 검사가 권장됩니다.
A-ROP에서 항VEGF 단독 요법은 75.087.5%에서 추가 치료가 필요합니다. 투여 후 13주 이내 조기 재발이 있을 수 있으며, 섬유 증식이 광범위한 경우 항VEGF 단독 치료는 적응증 외입니다(수축으로 인한 견인 망막박리 위험).
- 주입 위치: 각막 윤부에서 1.0
1.5 mm 후방 (성인의 3.54 mm와 크게 다름). - 바늘 방향: 아래쪽을 향해 주입 (수정체가 상대적으로 크므로 중앙을 향하면 수정체 관통 위험).
- 30게이지 이하의 주사 바늘 사용.
- 투여량 확인: 라니비주맙 0.02 mL, 아플리버셉트 0.01 mL (과량 투여 방지를 위해 신중히 확인).
Protocol T 시험에서 1년 시점에 아플리버셉트의 시력 개선이 가장 컸습니다. 단, 경증군(BCVA ≥20/40)에서는 세 약제 간 통계적 유의차가 없었습니다. 13) 파리시맙은 YOSEMITE/RHINE 시험에서 아플리버셉트와 동등한 시력 개선을 보이면서 유지기 주사 간격을 더 연장할 수 있습니다(2년째 Q16W 달성 60~64%). 8) 환자 배경이나 통원 빈도 희망에 따라 약제를 선택합니다.
4. 유리체강내 주사 술기
섹션 제목: “4. 유리체강내 주사 술기”주사 전 준비
섹션 제목: “주사 전 준비”- 환자/안구/약물 혼동 방지: 주사 결정 후 환자 식별 태그를 확인합니다.
- 요오드 알레르기 확인: 사전에 반드시 확인합니다.
- 필요 물품 준비:
소독 및 마취 절차
섹션 제목: “소독 및 마취 절차”마취: 소독약이 반대쪽 눈에 튈 가능성을 고려하여, 베녹실® 점안액을 양안에 점안한 후, 4% 자일로카인® 점안액을 치료안에 2회 점안합니다.
PA 요오드 소독 주의점:
- 냉장고에서 꺼낸 직후의 PA 요오드는 항균 및 항진균 불활성화 효과가 감소하므로 반드시 실온으로 되돌립니다.
- 비밀봉 용기에서 25°C로 보관할 경우, 유효 성분 잔존율이 5시간에 60%까지 감소합니다. 장시간 경과된 PA 요오드는 사용하지 마십시오.
- 세균 및 진균 불활성화에는 약 1분의 접촉 시간이 필요하므로, 세안 후에도 눈을 감고 결막과의 접촉 시간을 충분히 확보하십시오.
구강 내 세균 관리: 구멍이 뚫린 드레이프를 사용하고, 시술자, 보조자, 환자 모두 마스크를 착용하여 비말을 방지합니다.
주입 위치와 바늘 방향
섹션 제목: “주입 위치와 바늘 방향”외과적 윤부로부터의 주입 거리는 다음과 같습니다. 올바른 주입 위치를 지키면 모양체 편평부(모양체 주름부 후방)에서 주입이 가능해져 수정체 손상이나 유리체 출혈을 예방할 수 있습니다.
| 눈의 상태 | 윤부로부터의 거리 |
|---|---|
| 수정체가 있는 눈 | 4 mm (모양체 편평부) |
| 무수정체안 또는 인공수정체 삽입안 | 3.5 mm |
| 미숙아 | 1.0~1.5 mm |
바늘은 유리체강의 중심을 향해 주입합니다. 윤부에 가까운 위치에서 주입하면 모양체 주름부를 손상시켜 유리체 출혈이 발생하기 쉽고, 수정체와의 거리가 가까워져 수정체 손상 위험이 높아집니다.
주입 기술과 수술 후 관리
섹션 제목: “주입 기술과 수술 후 관리”- 구멍이 뚫린 드레이프를 부착하고, 개검기로 눈꺼풀을 벌립니다.
- 캘리퍼로 윤부로부터의 주입 거리를 측정합니다.
- 주사 부위는 귀 위쪽 또는 귀 아래쪽 사분면으로 한다 (수평직근 손상 방지).
- 겸자로 안구를 고정하고, 주사 전에 결막을 약간 앞쪽으로 밀어 바늘 제거 후 바늘 구멍이 어긋나게 하여 액체 누출을 방지한다.
- 30G 짧은 바늘을 공막에 거의 수직으로 찔러 넣고 약액을 천천히 주입한다 (급속 주입은 지속적인 안압 상승의 원인이 됨).
- 바늘 제거 후 면봉으로 주사 부위를 압박한다.
- 수술 직후 시력 (지수변)을 확인한다. 지수변이 인식되지 않으면 전방천자를 시행한다.
- 수술 후 3일간 광범위 항생제 점안을 지속한다.
5. 합병증과 대책
섹션 제목: “5. 합병증과 대책”감염성 안내염 (가장 중요한 합병증)
섹션 제목: “감염성 안내염 (가장 중요한 합병증)”감염성 안내염은 가장 심각한 합병증으로, 발생률은 약 0.027~0.065%입니다. 발생 시 반코마이신 1.0mg + 세프타지딤 2.0mg의 유리체내 주사에 의한 응급 치료가 필요합니다.
가장 중요한 예방 조치:
- 포비돈 요오드의 적절한 소독 (실온으로 되돌리기, 1분 이상 접촉 시간)
- 구멍이 뚫린 드레이프 사용 (구강 내 세균 비말 방지)
수술 후 예방적 항생제 점안에 대해서는 여러 연구에서 안내염 발생률을 낮추지 않는 것으로 나타났으며, 유효성에 대한 증거는 일치하지 않습니다.
무균성 안내염
섹션 제목: “무균성 안내염”세균 감염을 동반하지 않은 안내 염증 반응으로, 발생률은 약제에 따라 0.005~4.4%로 다릅니다. 7)
- 발병 시기: 주사 후 24
48시간 이내가 많음 (감염성은 27일 후) 7) - 주요 소견: 유리체 혼탁 (약 80%), 전방 축농 (약 5%) 7)
- 확진: 배양 음성 (PCR에 의한 병원체 배제도 유용)
- 약제별 발생률 (‰): 베바시주맙 3.64 / 라니비주맙 1.39 / 아플리베르셉트 0.76 7)
- 치료: 경증은 보존적 (스테로이드 점안, 결막하 주사). CEVE 프로토콜 (즉시 완전 유리체 절제술)에서는 평균 17.8일 시력 회복이 보고되었습니다. 7)
IRIS 레지스트리의 매칭 코호트 분석에서는 주사 관리만 시행한 군과 조기 유리체 절제술 군 간에 시력 결과에 유의한 차이가 없었습니다. 21)
안내 염증 (IOI) / 망막 혈관염 (브롤루시주맙 특이적)
섹션 제목: “안내 염증 (IOI) / 망막 혈관염 (브롤루시주맙 특이적)”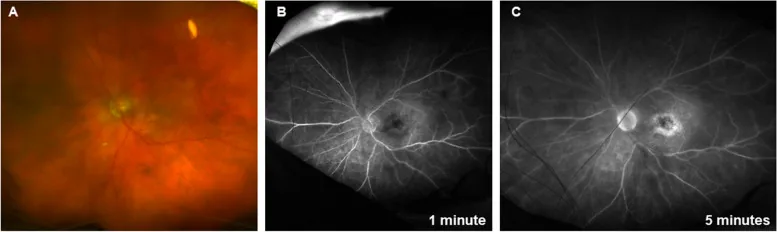
브롤루시주맙은 다른 항VEGF 약물보다 더 높은 빈도로 안내염증(IOI)을 유발하는 것으로 알려져 있습니다.
| 시험/집단 | IOI 발생률 | 비고 |
|---|---|---|
| HAWK/HARRIER (전체 IOI) | 4.4% | 망막혈관염 3.6%, 혈관폐쇄 2.1%10) |
| KESTREL (6mg) | 3.7% (대조군 0.5%) | DME 시험10) |
| MERLIN (4주 간격) | 9.3% | 시험 중단10) |
| 일본인 증례 | 15~20% | 10) |
| 시판 후 (혈관염 + 폐쇄 복합) | 3.73/10,000회 주사 |
IOI의 대부분은 첫 투여 후 6개월 이내, 4회 이내 주사 후에 발생합니다. 10)
기전: 브롤루시주맙에서 ADA(항약물항체) 양성률이 35~52%로 높고(라니비주맙, 아플리버셉트의 5% 미만과 대조적), 면역복합체 침착에 의한 III형 과민반응으로 생각됩니다. 10)
공막염(세계 최초 보고): 브롤루시주맙 투여 후 후부 공막염이 일본인 3예에서 보고되었으며, 안압 24~49 mmHg 상승을 동반하고, 그중 1예는 망막동맥폐쇄 및 혈관염으로 진행되었습니다. 9)
치료: 결막하 또는 테논낭하 트리암시놀론아세토나이드(STTA) 5~20 mg 주사가 효과적입니다. 예방적 STTA 투여와의 병용도 보고되었습니다. 18, 19)
파리시맙 관련 IOI
섹션 제목: “파리시맙 관련 IOI”IOI 발생률은 nAMD 2.0%, DME 1.3%, RVO 1.4%이며, 양안 투여 예에서는 8.5%에서 관찰되었습니다. 8) 시판 후 조사에서 망막혈관염은 0.17/10,000회 주사로 드물지만, 출혈성 폐쇄성 망막혈관염(HORV)은 중증 결과를 초래할 수 있습니다. 8) HORV는 IV형(지연형) 과민반응과의 연관성이 병리학적으로 시사됩니다. 16)
RPE 열공은 파리시맙군에서 TENAYA 2.7%, LUCERNE 3.0%에서 발생했으며, PED 높이 550 μm 초과가 위험인자입니다. 17)
Crunch 증후군(견인성 망막박리)
섹션 제목: “Crunch 증후군(견인성 망막박리)”ROP 환자에서 항VEGF 치료 후 섬유혈관막이 급속히 수축하여 견인성 망막박리(TRD)를 초래하는 합병증을 crunch 증후군이라고 합니다. 3) 섬유증식이 광범위하게 존재하는 경우 항VEGF 단독 치료는 적응증 외이며, 유리체절제술이 필요합니다. 투여 후 조기 안저검사에서 증식 조직의 변화를 확인하는 것이 중요합니다.
바늘에 의한 기계적 합병증
섹션 제목: “바늘에 의한 기계적 합병증”- 수정체 손상: 백내장 진행. 삽입 거리(유수정체안 4 mm) 준수로 예방합니다.
- 망막 손상: 열공성 망막박리. 30G 짧은 바늘의 적절한 삽입으로 예방합니다.
- 섬모체 손상: 유리체출혈. 삽입 위치 및 방향 준수로 예방합니다.
안압 상승
섹션 제목: “안압 상승”주사 직후 일시적인 안압 상승은 주사를 맞은 모든 환자에게 발생합니다. 0.05mL 주입 시 안압이 즉시 50mmHg까지 상승하지만, 일반적으로 가역적입니다. 녹내장 병력이 있는 경우 지속적인 안압 상승에 주의해야 하며, 필요 시 전방천자를 통해 감압합니다.
동맥 혈전색전증 사건 (ATE)
섹션 제목: “동맥 혈전색전증 사건 (ATE)”뇌졸중, 심근경색의 위험이 이론적으로 존재합니다. 브롤루시주맙의 HAWK 시험에서 ATE는 1.1~1.4%로 관찰되었습니다. 10) 병력이 있는 환자에서는 신중히 투여해야 합니다.
6. 병태생리 (VEGF의 역할과 약제의 작용 기전)
섹션 제목: “6. 병태생리 (VEGF의 역할과 약제의 작용 기전)”VEGF의 병적 역할
섹션 제목: “VEGF의 병적 역할”VEGF는 혈관 내피 세포의 VEGFR-1 및 VEGFR-2에 결합하여 내피 세포 증식, 혈관 투과성 항진, 신생 혈관 형성을 촉진합니다.
- AMD: 맥락막 신생혈관(CNV)의 증식 및 혈관 투과성 항진
- DME: 혈액-망막 장벽(BRB)의 파괴 → 황반 부종 형성
- RVO: 허혈 → VEGF 과잉 → 황반 부종 및 신생혈관
유리체강 내 주사로 VEGF 수치가 감소하면 혈관 투과성이 저하되고 황반 부종이 개선됩니다. 항VEGF 약제의 효과는 일시적이므로 정기적인 재투여가 필요합니다.
각 약물의 분자적 특징
섹션 제목: “각 약물의 분자적 특징”| 약물 | 분자량 | VEGF-A 친화도 (Kd) | 표적 |
|---|---|---|---|
| 브롤루시주맙 | 26 kDa | 28.4 pM | VEGF-A (모든 이소형) |
| 라니비주맙 | 48 kDa | 20.6 pM | VEGF-A (모든 이소형) |
| 아플리베르셉트 | 115 kDa | 0.49 pM (최고) | VEGF-A/B, PlGF |
| 베바시주맙 | 148 kDa | 35.1 pM | VEGF-A |
| 파리시맙 | 149 kDa | — | VEGF-A + Ang-2 |
Ang-2와 파리시맙의 작용
섹션 제목: “Ang-2와 파리시맙의 작용”Ang-2는 Tie-2 수용체의 길항제로서 혈관 불안정화에 관여합니다. 파리시맙이 Ang-2를 억제함으로써 Tie-2 경로가 정상화되고 혈관 안정성이 향상되며 VEGF 민감도가 감소합니다. 이 이중 억제 효과가 투여 간격 연장을 가능하게 하는 약리학적 기반입니다.
도입기 집중 투여의 의의
섹션 제목: “도입기 집중 투여의 의의”도입기에 매월 고정으로 3~5회 투여하는 이유는 질환 활동성을 조기에 강력하게 억제하기 위해서입니다. 치료-연장(T&E)법은 유리체 내 약물 농도가 치료 범위를 유지할 수 있는 범위에서 재발을 허용하지 않는 틀을 제공합니다.
7. 최신 연구와 향후 전망 (연구 단계 보고)
섹션 제목: “7. 최신 연구와 향후 전망 (연구 단계 보고)”포트 전달 시스템 (Susvimo)
섹션 제목: “포트 전달 시스템 (Susvimo)”라니비주맙의 PDS(포트 전달 시스템)는 6개월마다 보충 투여로 98%가 월 1회 주사가 필요 없게 되었습니다. 12) 2025년에는 DME에 대한 적응증 추가가 검토되고 있습니다. 13) 주사 부담의 대폭적인 감소가 기대됩니다.
고용량 아플리베르셉트 8 mg (아일리아® HD)
섹션 제목: “고용량 아플리베르셉트 8 mg (아일리아® HD)”PULSAR 시험(AMD)에서 48주 시점에 79%가 12주 간격, 77%가 16주 간격을 유지했습니다. 12) PHOTON 시험(DME)에서도 93%가 12주 이상 간격을 달성했습니다. 13)
브롤루시주맙 적응증 확대 시험
섹션 제목: “브롤루시주맙 적응증 확대 시험”PCV 및 황반부 모세혈관 확장증 1형(AT1)을 대상으로 한 PROUD 시험(한국)이 진행 중이며, 아시아 특유 질환에 대한 근거 축적이 기대됩니다. 14)
파리시맙 PCV 대상 시험 (SALWEEN 시험)
섹션 제목: “파리시맙 PCV 대상 시험 (SALWEEN 시험)”PCV 환자에 대한 파리시맙의 효과를 검토하는 SALWEEN 시험이 진행 중입니다. 20) PCV 환자의 방수에서 Ang-2 고값이 확인되었으며, Ang-2 억제의 추가 효과가 기대됩니다.
STTA 병용에 의한 IOI 예방
섹션 제목: “STTA 병용에 의한 IOI 예방”결막하/테논낭하 트리암시놀론 아세토나이드(STTA)와 브롤루시주맙의 병용 투여가 IOI 예방과 삼출 조절 양면에서 유효할 가능성이 있습니다. 18, 19) 최적 용량·투여 시기의 표준화를 위한 연구가 진행 중입니다.
바이오마커에 의한 조기 감별
섹션 제목: “바이오마커에 의한 조기 감별”무균성 안내염과 감염성 안내염의 조기 감별을 위해 유리체액 내 사이토카인 프로파일(IL-6, IL-8, IL-10) 측정이 보조 도구가 될 가능성이 기대됩니다. 7)
바이오시밀러
섹션 제목: “바이오시밀러”라니비주맙·베바시주맙의 바이오시밀러가 등장하고 있습니다. 비용의 대폭적인 감소로 치료 지속률 향상과 의료 접근성 개선이 기대됩니다. 12)
8. 참고문헌
섹션 제목: “8. 참고문헌”- 日本眼科学会. 新生血管型加齢黄斑変性の診療ガイドライン. 日眼会誌. 2024.
- 日本眼科学会. 糖尿病網膜症診療ガイドライン(第1版). 日眼会誌. 2023.
- 日本未熟児網膜症研究会. 未熟児網膜症に対する抗VEGF療法の手引き(第2版). 2024.
- 日本眼科学会. 近視性黄斑部新生血管の診療ガイドライン. 日眼会誌. 2023.
- American Academy of Ophthalmology. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024. [Protocol S data]
- American Academy of Ophthalmology. Retinal Vein Occlusion Preferred Practice Pattern. Ophthalmology. 2024. [BRAVO data]
- Kudasiewicz-Kardaszewska A, Ozimek MA, Kardaszewska A, et al. Complete and Early Vitrectomy for Sterile Endophthalmitis After Bevacizumab: A Case Series. Cureus. 2025;17(10):e93996. doi:10.7759/cureus.93996.
- Tadayoni R, Paris LP, Danzig CJ, et al. Efficacy and safety of faricimab for macular edema due to retinal vein occlusion: 24-week results from the BALATON and COMINO trials. Ophthalmology. 2024;131(8):950-960.
- Takayama T, et al. Scleritis following intravitreal brolucizumab injection: a case series. J Med Case Rep. 2024;18:80.
- Sharma A, et al. Understanding retinal vasculitis associated with brolucizumab. Ocul Immunol Inflamm. 2022;30(6):1508-1510.
- Nawar AE, Abdelrahman AM, Ebeid OM, Ahmed SM, El-Abhar AE. Subthreshold micropulse laser combined with ranibizumab versus ranibizumab monotherapy in branch retinal vein occlusion with macular edema. Clin Ophthalmol. 2022;16:1139-1151. doi:10.2147/OPTH.S355315. PMID:35386091. PMCID:PMC8968960
- Flaxel CJ, Adelman RA, Bailey ST, et al. Age-related macular degeneration preferred practice pattern. Ophthalmology. 2024;131(1):P1-P68.
- Flaxel CJ, Adelman RA, Bailey ST, et al. Diabetic retinopathy preferred practice pattern. Ophthalmology. 2024;131(1):P99-P168.
- Sen P, et al. Polypoidal choroidal vasculopathy: update on diagnosis and treatment. Clin Ophthalmol. 2023;17:53-70.
- Bloom J, Madani R, Haidar AJ, Alasil T. Faricimab treatment of polypoidal choroidal vasculopathy resistant to intravitreal ranibizumab. J VitreoRetin Dis. 2024;8(6):731-734.
- Yavari N, Gupta AS, Mitsios A, et al. Bilateral hemorrhagic occlusive retinal vasculitis and panuveitis following intravitreal faricimab injection. Am J Ophthalmol Case Rep. 2026;41:102532.
- Clemens CR, Alten F, Zimmermann JA, Eter N. Old problem in a new guise: retinal pigment epithelium tear after intravitreal faricimab injection. Case Rep Ophthalmol. 2023;14:241-244.
- Shigemoto Y, et al. Combination therapy of STTA and IVbr for brolucizumab-related IOI. Medicine. 2021;100(42):e27580.
- Saito M, et al. IOI after IVbr monitored by laser flare-cell photometer. Am J Ophthalmol Case Rep. 2022;28:101727.
- Cheung CMG, Lai TYY, Teo K, et al. Polypoidal choroidal vasculopathy: consensus nomenclature and non-indocyanine green angiograph diagnostic criteria. Eye. 2024;39:819-834.
- American Academy of Ophthalmology. Similar visual outcomes are seen with two post-injection endophthalmitis treatments. AAO Editors’ Choice. 2024 Oct 8. Available from: https://www.aao.org/education/editors-choice/similar-visual-outcomes-are-seen-with-two-post-inj
