การฉีดยาต้าน VEGF เข้าน้ำวุ้นตา เป็นการรักษาที่ยับยั้งการทำงานของ VEGF (การสร้างเส้นเลือดใหม่และการเพิ่มการซึมผ่านของหลอดเลือด) โดยการฉีดยาเข้าไปในช่องวุ้นตา โดยตรงจอประสาทตา เสื่อมตามอายุ (AMD ), จอประสาทตา บวมจากเบาหวาน (DME) และหลอดเลือดดำจอประสาทตาอุดตัน (RVO ) เป็นข้อบ่งชี้หลัก และเป็นหนึ่งในหัตถการผู้ป่วยนอกทางจักษุวิทยาที่พบบ่อยที่สุดในปัจจุบันยาต้าน VEGF ที่มีให้ใช้ ได้แก่ รานิบิซูแมบ , แอฟลิเบอร์เซป, โบรลูซิซูแมบ , ฟาริซิแมบ และเบวาซิซูแมบ (นอกข้อบ่งใช้) และการเลือกยาขึ้นอยู่กับโรค ภาวะ และความต้องการช่วงห่างการให้ยาการให้ยาทำเป็นสองระยะ: ระยะเริ่มต้น (คงที่ทุกเดือน) และระยะบำรุงรักษา (PRN, คงที่ หรือ T&E) ด้วยฟาริซิแมบ หรือแอฟลิเบอร์เซปขนาดสูง สามารถขยายช่วงห่างได้ถึง 16 สัปดาห์
ภาวะแทรกซ้อนที่สำคัญที่สุดคือเยื่อบุตาอักเสบ ติดเชื้อ (อุบัติการณ์ 0.027-0.065%) และมาตรการป้องกันที่ดีที่สุดคือการฆ่าเชื้ออย่างเหมาะสมด้วยโพวิโดน-ไอโอดีน
โบรลูซิซูแมบ มีอุบัติการณ์การอักเสบในลูกตา (IOI) และหลอดเลือดจอประสาทตาอักเสบ สูงกว่ายาอื่น (4.4-20%) จึงจำเป็นต้องติดตามผลอย่างใกล้ชิดหลังฉีด การฉีดยาต้าน VEGF เข้าในน้ำวุ้นตา เป็นการรักษาโดยการฉีดยาโดยตรงเข้าไปในโพรงน้ำวุ้นตา เพื่อยับยั้งการทำงานของ VEGF (การสร้างเส้นเลือดใหม่และการเพิ่มการซึมผ่านของหลอดเลือด) ข้อบ่งชี้หลักคือโรคหลอดเลือดจอประสาทตา เช่น จอประสาทตา เสื่อมตามอายุ ภาวะบวมน้ำที่จอประสาทตา จากเบาหวาน และการอุดตันของหลอดเลือดดำจอประสาทตา
การรักษาด้วยยาต้าน VEGF ได้รับการนำมาใช้ทางคลินิกอย่างรวดเร็วในช่วงปี 2000
ปี เหตุการณ์ 2004 เริ่มการใช้ยาเบวาซิซูแมบ ในลูกตาแบบสำรวจ 2006 FDA อนุมัติรานิบิซูแมบ (การทดลอง MARINA/ANCHOR) 12) 2011 FDA อนุมัติอะฟลิเบอร์เซปต์ (การทดลอง VIEW) 12) 2019 FDA อนุมัติโบรลูซิซูแมบ (การทดลอง HAWK/HARRIER) 10) 2022 FDA อนุมัติฟาริซิแมบ (การทดลอง TENAYA/LUCERNE/YOSEMITE/RHINE) 8)
จอประสาทตา เสื่อมชนิดเปียกที่สัมพันธ์กับอายุ (nAMD )จอประสาทตา (CNV )จอประสาทตา บวมจากเบาหวาน (DME)จอประสาทตา บวมที่เกิดร่วมกับจอประสาทตาเสื่อมจากเบาหวาน หลอดเลือดดำจอประสาทตาอุดตัน (RVO )จอประสาทตา บวมจากหลอดเลือดดำจอประสาทตา ส่วนกลางหรือแขนงอุดตัน 6) จอประสาทตาเสื่อมจากเบาหวาน ชนิดงอกเส้นเลือด (PDR)PRP (ranibizumab) 5) เส้นเลือดใหม่ใต้จอประสาทตา จากสายตาสั้น ผิดปกติ (mCNV ) : Aflibercept, ranibizumab 4) โรคหลอดเลือดคอรอยด์ แบบโพลิป (PCV ) : Brolucizumab มีอัตราการยุบตัวของโพลิปสูง 14) จอประสาทตา ในทารกคลอดก่อนกำหนด (ROP )3) จอประสาทตา ฝ่อแบบแผนที่ (GA)คอมพลีเมนต์ เยื่อบุตาอักเสบ ภายในลูกตามะเร็งต่อมน้ำเหลืองภายในลูกตา : Methotrexate
Q
การรักษาด้วยยาต้าน VEGF ใช้กับโรคอะไรบ้าง?
A
จอประสาทตา เสื่อมตามอายุ จอประสาทตา บวมจากเบาหวาน และหลอดเลือดดำจอประสาทตาอุดตัน เป็นสามโรคหลักที่บ่งชี้ ในโรคเหล่านี้ทั้งหมด มีการผลิต VEGF มากเกินไป ทำให้เกิดเส้นเลือดใหม่และการซึมผ่านของหลอดเลือดเพิ่มขึ้น ส่งผลให้การมองเห็น ในจอประสาทตา ลดลง โดยการฉีดยาต้าน VEGF เข้าไปในวุ้นตา โดยตรง จะยับยั้งกระบวนการทางพยาธิวิทยาเหล่านี้เพื่อปรับปรุงหรือรักษาการมองเห็น ในช่วงไม่กี่ปีที่ผ่านมา ข้อบ่งชี้ได้ขยายไปถึง PDR, mCNV , ROP , โรคหลอดเลือดคอรอยด์ แบบโพลิป และอื่นๆ
ชื่อยา ชื่อการค้า น้ำหนักโมเลกุล กลไกการออกฤทธิ์ ขนาดยา การอนุมัติ (ญี่ปุ่น) รานิบิซูแมบ ลูเซนทิส® 48 kDa ชิ้นส่วน Fab ที่ต้าน VEGF-A 0.5 มก. (AMD /RVO ), 0.3 มก. (DME) 2009 อะฟลิเบอร์เซปต์ อายลีอา® 115 kDa ยับยั้ง VEGF-A/B และ PlGF (ตัวรับล่อ) 2 มก. / 8 มก. (ขนาดสูง) 2012 เพกาพทานิบ แมคยูเจน® — VEGF165 อะพทาเมอร์ 0.3 มก. พ.ศ. 2551 โบรลูซิซูแมบ เบโอวู® 26 กิโลดาลตัน VEGF-A scFv 6 มก. พ.ศ. 2563 ฟาริซิแมบ วาบิสโม® 149 กิโลดาลตัน แอนติบอดีแบบคู่จำเพาะต่อ VEGF-A + Ang-2 6 มก. พ.ศ. 2566 เบวาซิซูแมบ อาวาสติน® 148 กิโลดาลตัน VEGF-A IgG แบบเต็มความยาว 1.25 มก. — (นอกข้อบ่งใช้)
รานิบิซูแมบ (ลูเซนทิส®)
น้ำหนักโมเลกุล : 48 กิโลดาลตัน (ชิ้นส่วน Fab)
กลไกการออกฤทธิ์ : ยับยั้งไอโซฟอร์มทั้งหมดของ VEGF-A
การศึกษาหลัก : การศึกษา MARINA/ANCHOR แสดงประสิทธิภาพใน AMD การศึกษา CATT แสดงความเท่าเทียมกับเบวาซิซูแมบ 12)
คุณสมบัติ : สามารถให้ยาเสริมทุก 6 เดือนผ่าน PDS 98% ไม่ต้องฉีดรายเดือนหลังจาก 2 ปี 12)
อะฟลิเบอร์เซปต์ (อายเลีย®)
น้ำหนักโมเลกุล : 115 กิโลดาลตัน (โปรตีนฟิวชัน)
กลไกการออกฤทธิ์ : ยับยั้งสามปัจจัยพร้อมกัน: VEGF-A, VEGF-B และ PlGF มีความสัมพันธ์สูงสุดกับ VEGF-A Kd=0.49 pM
การศึกษาหลัก : การศึกษา VIEW แสดงความไม่ด้อยกว่ารานิบิซูแมบ ขนาดสูง 8 มก. (HD) ให้ระยะห่างได้ถึง 16 สัปดาห์ 12, 13)
ลักษณะเด่น : สเปกตรัมการยับยั้ง VEGF ที่กว้าง ใน DME การทดลอง Protocol T แสดงการมองเห็น ดีขึ้นมากที่สุดใน 1 ปี 13)
โบรลูซิซูแมบ (เบโอวู®)
น้ำหนักโมเลกุล : 26 kDa (scFv, เล็กที่สุดในบรรดายาที่มีอยู่)
กลไกการออกฤทธิ์ : โครงสร้าง scFv ทำให้สามารถให้ยาในความเข้มข้นโมลาร์สูงกว่าอัฟลิเบอร์เซปต์ประมาณ 12 เท่า มีการซึมผ่านเนื้อเยื่อสูง
การทดลองหลัก : การทดลอง HAWK/HARRIER แสดงให้เห็นว่าไม่ด้อยกว่า ผู้ป่วยสูงสุด 55% รักษาช่วงห่าง 12 สัปดาห์ได้ 10)
ข้อควรระวัง : อุบัติการณ์ IOI 4.4% (HAWK/HARRIER), 15-20% ในคนญี่ปุ่น ความเสี่ยงต่อจอประสาทตา อักเสบและหลอดเลือดอุดตัน 10)
ฟาริซิแมบ (วาบิซโม®)
น้ำหนักโมเลกุล : 149 kDa (แอนติบอดี IgG แบบสองตำแหน่ง)
กลไกการออกฤทธิ์ : ยับยั้ง VEGF-A และ Ang-2 (แองจิโอพอยอิติน-2) พร้อมกัน เป็นยาที่มีเป้าหมายคู่แรกของโลก
การทดลองหลัก : TENAYA/LUCERNE (nAMD ) สูงสุด Q16W ผู้ป่วย nAMD 63% บรรลุ Q16W ในปีที่สอง 8)
ลักษณะเด่น : ใน RVO (BALATON/COMINO ) อัตราการหายไปของการรั่วซึม FA เหนือกว่าอัฟลิเบอร์เซปต์ 8)
เบวาซิซูแมบ (อาวาสติน®)
น้ำหนักโมเลกุล : 148 kDa (IgG ความยาวเต็ม)
กลไกการออกฤทธิ์ : ยับยั้ง VEGF-A (การใช้แบบนอกข้อบ่งชี้ในจักษุวิทยา)
การทดลองหลัก : การทดลอง CATT ยืนยันประสิทธิภาพเทียบเท่ารานิบิซูแมบ 12)
สถานะการใช้ : ต้นทุนต่ำกว่าอย่างมีนัยสำคัญ ใช้ผลิตภัณฑ์สำหรับฉีดเข้าหลอดเลือดดำโดยแบ่งบรรจุภายใต้สภาวะปลอดเชื้อ
เพกาพทาไนบ์ (Macugen®)
กลไกการออกฤทธิ์ : อะพทาเมอร์ที่จำเพาะต่อ VEGF165
สถานะปัจจุบัน : ยารุ่นแรกที่ได้รับการอนุมัติในปี 2008 ปัจจุบันยารุ่นใหม่เป็นหลัก มีส่วนช่วยในการสร้างแนวคิดเริ่มต้นของการรักษาด้วย anti-VEGF
Q
ควรเลือกยาใด?
A
พิจารณาจากโรคที่บ่งชี้ ความต้องการช่วงห่างการให้ยา และความเสี่ยงของภาวะแทรกซ้อน โดยทั่วไปใน nAMD ยา aflibercept, faricimab และ brolucizumab เหนือกว่าในแง่การยืดช่วงห่างการให้ยา ใน DME ยา aflibercept และ faricimab เป็นมาตรฐาน Brolucizumab มีข้อดีคืออัตราการหายของติ่งเนื้อสูงในผู้ป่วย PCV โดยคำนึงถึงความเสี่ยง IOI Faricimab สามารถให้ยาได้สูงสุดทุก 16 สัปดาห์ (Q16W) ลดภาระการมาโรงพยาบาล ท้ายที่สุด แพทย์ผู้รักษาจะตัดสินใจอย่างครอบคลุม
Q
สามารถใช้ bevacizumab (Avastin) ได้หรือไม่?
A
ในสาขาจักษุวิทยา เป็นการใช้แบบนอกข้อบ่งชี้ (off-label) โดยเตรียมผลิตภัณฑ์สำหรับฉีดเข้าหลอดเลือดดำภายใต้สภาวะปลอดเชื้อเพื่อใช้ทางตา การทดลอง CATT ยืนยันประสิทธิภาพในการปรับปรุงการมองเห็น ที่เทียบเท่ากับ ranibizumab และใช้กันอย่างแพร่หลายทั่วโลกเนื่องจากต้นทุนต่ำกว่าอย่างมีนัยสำคัญ อย่างไรก็ตาม ในญี่ปุ่นไม่มีการครอบคลุมของประกัน และการใช้ขึ้นอยู่กับดุลยพินิจของสถานพยาบาล
การให้ยา anti-VEGF แบ่งเป็น 2 ระยะ: ระยะเริ่มต้นและระยะบำรุงรักษา
ระยะเริ่มต้น : เพื่อระงับกิจกรรมของโรคอย่างรุนแรง ให้ยาคงที่เดือนละครั้ง 3-6 ครั้ง (แตกต่างกันตามโรคและยา)ระยะบำรุงรักษา มี 3 รูปแบบ:
PRN (pro re nata) : มาตรวจทุกเดือน ให้ยาเฉพาะเมื่อมีอาการกลับเป็นซ้ำการให้ยาคงที่ : ให้ยาสม่ำเสมอในช่วงเวลาคงที่ เช่น ทุก 2 เดือนหรือ 3 เดือนTreat and Extend (T&E) : หากไม่มีสัญญาณของกิจกรรม ให้ยืดช่วงห่างออกไปครั้งละ 2 สัปดาห์ หากกลับเป็นซ้ำให้缩短
สำหรับรานิบิซูแมบ แนะนำให้ให้ยา 3 ครั้งในระยะนำ (เดือนละครั้ง) ตามด้วยการให้แบบ PRN ในระยะบำรุงรักษา ส่วนอะฟลิเบอร์เซปต์ แนะนำให้ให้ยา 3 ครั้งในระยะนำ (เดือนละครั้ง) ตามด้วยการให้แบบคงที่ทุก 2 เดือน หรือวิธี T&E เป็นวิธีการให้พื้นฐาน แต่ในช่วงไม่กี่ปีที่ผ่านมา วิธี T&E ถูกนำมาใช้ในหลายสถานพยาบาล
โรคที่บ่งชี้ ยาที่แนะนำ ระยะนำ ระยะบำรุงรักษา nAMD (รานิบิซูแมบ ) ลูเซนทิส® 0.5 มก. เดือนละครั้ง × 3 ครั้ง1) PRN (ติดตามเดือนละครั้ง) nAMD (อะฟลิเบอร์เซปต์) อายเลีย® 2 มก. เดือนละครั้ง × 3 ครั้ง1) คงที่ทุก 2 เดือน หรือ T&E (สูงสุด 3 เดือน) nAMD (โบรลูซิซูแมบ ) เบโอวู® 6 มก. เดือนละครั้ง × 3 ครั้ง ช่วงห่าง 8–12 สัปดาห์10) nAMD (ฟาริซิแมบ ) Vabysmo® 6 มก. Q4W × 4 ครั้ง Q8W ถึง Q16W8) DME (แอฟลิเบอร์เซปต์ ) Eylea® 2 มก. เดือนละ 1 ครั้ง × 5 ครั้ง2) ทุก 2 เดือน DME (รานิบิซูแมบ ) Lucentis® 0.5 มก. เดือนละ 1 ครั้ง × 3 ครั้ง2) PRN DME (ฟาริซิแมบ ) Vabysmo® 6 มก. Q4W × 4 ถึง 6 ครั้ง PTI (สูงสุด Q16W)8, 13) RVO อะฟลิเบอร์เซปต์/ฟาริซิแมบ Q4W × 6 เดือน PTI (สูงสุด Q16W) 8) PDR รานิบิซูแมบ 0.3 มก.— ไม่ด้อยกว่า PRP 5) mCNV อะฟลิเบอร์เซปต์/รานิบิซูแมบ 1-3 ครั้งแรก PRN (อาจหายได้ด้วยครั้งเดียว) 4) ROP (รานิบิซูแมบ )ลูเซนทิส® 0.2 มก. ครั้งแรก เพิ่มเมื่อกลับเป็นซ้ำ (ห่างกัน ≥1 เดือน) 3) ROP (อะฟลิเบอร์เซปต์)Eylea® 0.4 มก. ครั้งแรก ให้ซ้ำเมื่อกลับมาเป็นอีก (ห่างกันอย่างน้อย 1 เดือน) 3)
การจัดการ PCV (Polypoidal Choroidal Vasculopathy) : โบรลูซิซูแมบ มีอัตราการหายของพอลิพประมาณ 79% สูงกว่ายาอื่น และรักษาระยะห่าง 12 สัปดาห์ได้ 76% (48 สัปดาห์) 14) มีรายงานว่าฟาริซิแมบ มีประสิทธิภาพแม้ในกรณี PCV ที่ดื้อต่อรานิบิซูแมบ 15)
การศึกษา BALATON (BRVO , n=553) : ฟาริซิแมบ 6.0 มก. เทียบกับอะฟลิเบอร์เซปต์ 2.0 มก. ทุก 4 สัปดาห์ การเปลี่ยนแปลง BCVA ที่ 24 สัปดาห์คือ +16.9 ตัวอักษร และ +17.5 ตัวอักษรตามลำดับ (บรรลุ non-inferiority) อัตราการหายของการรั่วซึม FA คือ 33.6% สำหรับฟาริซิแมบ เทียบกับ 21.0% สำหรับอะฟลิเบอร์เซปต์ (p nominal=0.0023) ซึ่งดีกว่าอย่างมีนัยสำคัญ 8)
การศึกษา COMINO (CRVO /HRVO , n=729) : ด้วยสูตรเดียวกัน การเปลี่ยนแปลง BCVA ที่ 24 สัปดาห์คือ +16.9 ตัวอักษร และ +17.3 ตัวอักษร (บรรลุ non-inferiority) การเปลี่ยนแปลง CST -461.6 μm เทียบกับ -448.8 μm อัตราการหายของการรั่วซึม FA คือ 44.4% สำหรับฟาริซิแมบ เทียบกับ 30.0% สำหรับอะฟลิเบอร์เซปต์ (p nominal=0.0002) ซึ่งดีกว่าอย่างมีนัยสำคัญ แสดงให้เห็นผลการรักษาเสถียรภาพของหลอดเลือดผ่านการยับยั้ง Ang-2 8)
การใช้ STTA ร่วม (RVO ) : การใช้รานิบิซูแมบ ร่วมกับไตรแอมซิโนโลน เหนือคอรอยด์ 4 มก. ช่วยลดจำนวนครั้งการฉีดอย่างมีนัยสำคัญเมื่อเทียบกับรานิบิซูแมบ เพียงอย่างเดียว (4.4 ครั้ง → 2.47 ครั้ง, p<0.001) 11)
ยาต้าน VEGF ที่ได้รับการอนุมัติสำหรับการรักษา ROP (ณ ธันวาคม 2022) มีสองชนิดดังนี้ 3)
รานิบิซูแมบ (Lucentis®) 0.2 มก./0.02 มล.อะฟลิเบอร์เซปต์ (Eylea®) 0.4 มก./0.01 มล. : 20% ของขนาดผู้ใหญ่ อนุมัติในเดือนกันยายน 2022การให้ซ้ำต้องห่างกันอย่างน้อย 1 เดือน (ตามข้อกำหนดในเอกสารกำกับยา)
ข้อบ่งชี้การรักษา (ตามเกณฑ์การศึกษา ETROP ) 3) :
ROP ทุกรายใน Zone I ที่มีโรค plusROP ระยะที่ 3 โซน I ที่ไม่มี plus diseaseROP ระยะที่ 3 โซน II ที่มี plus diseaseROP ชนิดรุนแรง (A-ROP ): ดำเนินการโดยเร็วที่สุด
อัตราการกลับเป็นซ้ำและการติดตามผล 3) :
อัตราการกลับเป็นซ้ำของ aflibercept คือ 13.9–28% (เวลาเฉลี่ยที่กลับเป็นซ้ำ 11–14.2 สัปดาห์) ส่วน ranibizumab คือ 20.8–83.0% (เวลาที่กลับเป็นซ้ำเร็วกว่า 5.9–9.3 สัปดาห์) เมื่อใช้ ranibizumab จำเป็นต้องสังเกตอย่างใกล้ชิดตั้งแต่ระยะแรกหลังฉีด หากหลอดเลือดจอประสาทตา ยังไม่ขยายไปถึงโซน III แนะนำให้ตรวจอวัยวะภายในดวงตาทุกสัปดาห์จนถึง 17 สัปดาห์หลังฉีด
ข้อควรระวังเกี่ยวกับ A-ROP 3) :
ใน A-ROP 75.0–87.5% ของกรณีจำเป็นต้องได้รับการรักษาเพิ่มเติมด้วย anti-VEGF เพียงอย่างเดียว มีการกลับเป็นซ้ำเร็วภายใน 1–3 สัปดาห์หลังฉีด และหากมีพังผืดกว้างขวาง การรักษาด้วย anti-VEGF เพียงอย่างเดียวไม่เหมาะสม (เสี่ยงต่อจอประสาทตาลอก แบบดึงรั้งเนื่องจากการหดตัว)
เทคนิคการฉีดสำหรับ ROP (ความแตกต่างจากผู้ใหญ่) 3) :
ตำแหน่งแทงเข็ม: 1.0–1.5 มม. ด้านหลังลิมบัส ของกระจกตา (แตกต่างอย่างมากจาก 3.5–4 มม. ในผู้ใหญ่)
ทิศทางของเข็ม: แทงลงด้านล่าง (เนื่องจากเลนส์มีขนาดค่อนข้างใหญ่ การแทงเข้าสู่ศูนย์กลางเสี่ยงต่อการทะลุเลนส์)
ใช้เข็มเบอร์ 30 หรือเล็กกว่า
ยืนยันขนาดยา: ranibizumab 0.02 มล., aflibercept 0.01 มล. (ตรวจสอบอย่างระมัดระวังเพื่อป้องกันการใช้ยาเกินขนาด)
Q
ยาใดมีประสิทธิภาพมากที่สุดสำหรับจอประสาทตาบวมจากเบาหวาน?
A
ในการทดลอง Protocol T การมองเห็น ดีขึ้นด้วย aflibercept มากที่สุดที่ 1 ปี อย่างไรก็ตาม ในกลุ่มที่มีความรุนแรงน้อย (BCVA ≥ 20/40) ไม่มีความแตกต่างอย่างมีนัยสำคัญทางสถิติระหว่างยาทั้งสามชนิด 13) Faricimab ในการทดลอง YOSEMITE/RHINE แสดงการมองเห็น ดีขึ้นเทียบเท่า aflibercept ในขณะที่สามารถยืดระยะห่างการฉีดในระยะบำรุงรักษาได้ (บรรลุ Q16W 60–64% ในปีที่ 2) 8) เลือกยาตามประวัติผู้ป่วยและความถี่ในการมาพบแพทย์ที่ต้องการ
การป้องกันการสับสนระหว่างผู้ป่วย ตา และยา : หลังจากตัดสินใจฉีด ให้ตรวจสอบป้ายระบุตัวผู้ป่วยการยืนยันการแพ้ไอโอดีน : ตรวจสอบล่วงหน้าทุกครั้งการเตรียมวัสดุที่จำเป็น :
โพวิโดนไอโอดีน 10% สำหรับฆ่าเชื้อผิวหนัง
ยาหยอดตาชา, สารละลาย PA ไอโอดีนที่เจือจางและปรับอุณหภูมิห้อง, ยาหยอดตาปฏิชีวนะ (ถ้าจำเป็น)
ผ้าก๊อซ, สำลีพันก้าน, ผ้าปิดแผลมีรูพร้อมเทป
เครื่องเปิดเปลือกตา, คาลิปเปอร์, คีมจับเนื้อเยื่อขนาดเล็ก
เข็มฉีดยา, สารละลายสำหรับฉีด (เมื่อใช้ขวด ให้ใช้กระบอกฉีดยา 1 มล. และเข็มดูดพร้อมตัวกรอง)
การชา : พิจารณาถึงความเป็นไปได้ที่น้ำยาฆ่าเชื้อจะกระเด็นเข้าตาอีกข้าง ให้หยอด Benoxil® ทั้งสองตา จากนั้นหยอด Xylocaine® 4% ในตาที่จะรักษาสองครั้ง
ข้อควรระวังเกี่ยวกับการฆ่าเชื้อด้วย PA ไอโอดีน :
PA ไอโอดีนที่เพิ่งนำออกจากตู้เย็นมีฤทธิ์ต้านเชื้อแบคทีเรียและเชื้อราลดลง ดังนั้นต้องแน่ใจว่าได้ปรับอุณหภูมิให้เป็นอุณหภูมิห้อง
เมื่อเก็บในภาชนะที่ไม่ปิดสนิทที่อุณหภูมิ 25°C อัตราคงเหลือของส่วนประกอบที่ออกฤทธิ์จะลดลงเหลือ 60% ภายใน 5 ชั่วโมง ห้ามใช้ PA ไอโอดีนที่ผ่านไปนาน
เพื่อยับยั้งแบคทีเรียและเชื้อรา ต้องใช้เวลาสัมผัสประมาณ 1 นาที ดังนั้นหลังจากล้างตา ให้ปิดเปลือกตาเพื่อให้แน่ใจว่ามีเวลาสัมผัสกับเยื่อบุตา อย่างเพียงพอ
มาตรการป้องกันแบคทีเรียในช่องปาก : ใช้ผ้าปิดแผลที่มีรูและสวมหน้ากากอนามัยสำหรับศัลยแพทย์ ผู้ช่วย และผู้ป่วยทุกคนเพื่อป้องกันละอองฝอย
ระยะการแทงเข็มจากลิมบัส ผ่าตัดมีดังนี้ การปฏิบัติตามตำแหน่งแทงเข็มจะช่วยให้สามารถแทงเข้าสู่พาร์สพลานา (ด้านหลังรอยพับซิลิอารี) ได้ ซึ่งป้องกันความเสียหายต่อเลนส์แก้วตา หรือเลือดออกในวุ้นตา
สภาพตา ระยะห่างจากลิมบัส ตาที่มีเลนส์แก้วตา ธรรมชาติ 4 มม. (พาร์สพลานา) ตาที่ไม่มีเลนส์แก้วตา หรือมีเลนส์แก้วตาเทียม 3.5 มม. ทารกคลอดก่อนกำหนด 1.0–1.5 มม.
เข็มถูกแทงเข้าสู่ศูนย์กลางของช่องวุ้นตา หากแทงใกล้ลิมบัส เกินไป อาจทำให้รอยพับซิลิอารีเสียหาย เกิดเลือดออกในวุ้นตา ได้ง่าย และเพิ่มความเสี่ยงต่อความเสียหายของเลนส์แก้วตา เนื่องจากระยะห่างที่ใกล้ขึ้น
ติดผ้าปิดแผลที่มีรูและเปิดเปลือกตาด้วยเครื่องเปิดเปลือกตา
วัดระยะการแทงจากลิมบัส ด้วยคาลิปเปอร์
ตำแหน่งฉีดคือด้านบนหรือด้านล่างของหู (เพื่อป้องกันการบาดเจ็บของกล้ามเนื้อเรกตัสแนวนอน)
ยึดลูกตาด้วยคีม และเลื่อนเยื่อบุตา ไปข้างหน้าเล็กน้อยก่อนฉีดเพื่อป้องกันการรั่วของของเหลวหลังจากถอนเข็ม
สอดเข็มสั้น 30G เกือบตั้งฉากกับตาขาว และฉีดยาช้าๆ (การฉีดเร็วอาจทำให้ความดันลูกตา สูงขึ้นอย่างต่อเนื่อง)
หลังจากถอนเข็ม ให้กดบริเวณที่ฉีดด้วยสำลี
ทันทีหลังทำหัตถการ ให้ตรวจสอบการมองเห็น (นับนิ้ว) หากไม่สามารถจำนิ้วได้ ให้ทำการเจาะช่องหน้าม่านตา
ใช้ยาหยอดตาปฏิชีวนะชนิดออกฤทธิ์กว้างต่อไปอีก 3 วันหลังทำหัตถการ
Q
การฉีดเจ็บหรือไม่?
A
เนื่องจากทำหลังจากการหยอดยาชาเฉพาะที่ (Benoxil® / Xylocaine 4%) ความเจ็บปวดระหว่างฉีดจึงน้อยมาก อาจรู้สึกระคายเคืองจากน้ำยาฆ่าเชื้อ (PA iodine) แต่ยาหยอดตาโซเดียมไฮยาลูโรเนตมีประสิทธิภาพในการลดความรู้สึกไม่สบายหลังทำหัตถการในระยะแรก
เยื่อบุตาอักเสบ ติดเชื้อเป็นภาวะแทรกซ้อนที่ร้ายแรงที่สุด โดยมีอุบัติการณ์ประมาณ 0.027–0.065% เมื่อเกิดขึ้น จำเป็นต้องได้รับการรักษาฉุกเฉินด้วยการฉีดยาเข้าแก้วตา vancomycin 1.0 มก. + ceftazidime 2.0 มก.
มาตรการป้องกันที่สำคัญที่สุด:
การฆ่าเชื้ออย่างเหมาะสมด้วยโพวิโดนไอโอดีน (ทำให้กลับสู่อุณหภูมิห้อง ระยะเวลาสัมผัสอย่างน้อย 1 นาที)
การใช้ผ้าปิดที่มีรู (ป้องกันละอองแบคทีเรียในช่องปาก)
สำหรับการใช้ยาหยอดตาปฏิชีวนะป้องกันหลังผ่าตัด การศึกษาหลายชิ้นแสดงว่าไม่ลดอุบัติการณ์ของเยื่อบุตาอักเสบ และหลักฐานเกี่ยวกับประสิทธิภาพไม่สอดคล้องกัน
ปฏิกิริยาการอักเสบภายในตาโดยไม่มีการติดเชื้อแบคทีเรีย อุบัติการณ์แตกต่างกัน 0.005–4.4% ขึ้นอยู่กับยา 7)
ระยะเวลาเกิด: มักภายใน 24–48 ชั่วโมงหลังฉีด (ชนิดติดเชื้อ 2–7 วัน) 7) อาการสำคัญ: ความขุ่นของแก้วตา (ประมาณ 80%) หนองในช่องหน้าตา (ประมาณ 5%) 7) การวินิจฉัยแน่นอน: เพาะเชื้อให้ผลลบ (การไม่พบเชื้อก่อโรคด้วย PCR ก็มีประโยชน์)อุบัติการณ์แยกตามยา (‰): Bevacizumab 3.64 / Ranibizumab 1.39 / Aflibercept 0.76 7) การรักษา: รายที่ไม่รุนแรงรักษาแบบประคับประคอง (ยาหยอดสเตียรอยด์ ฉีดใต้เยื่อบุตา ) โปรโตคอล CEVE (การตัดแก้วตาทั้งหมดทันที) รายงานการฟื้นฟูการมองเห็น เฉลี่ย 17.8 วัน 7)
การวิเคราะห์กลุ่มที่จับคู่จาก IRIS Registry ไม่พบความแตกต่างอย่างมีนัยสำคัญในผลลัพธ์การมองเห็น ระหว่างการจัดการด้วยการฉีดยาเพียงอย่างเดียวและการตัดแก้วตาตั้งแต่เนิ่นๆ 21)
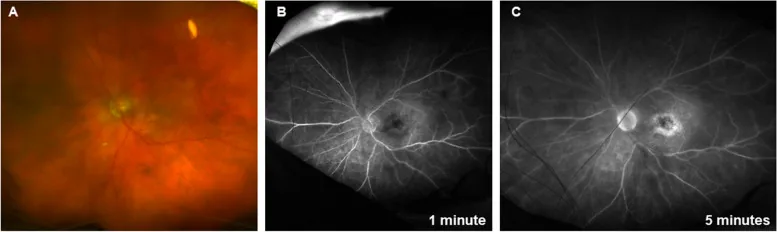
ภาพ IOI จาก Brolucizumab Bahram Bodaghi; Arshad M Khanani; Ramin Khoramnia; Carlos Pavesio; Quan Dong Nguyen. Gains in the current understanding of managing neovascular
AMD with brolucizumab. J Ophthalmic Inflamm Infect. 2023 Nov 23; 13:51 Figure 2. PM
CI D: PMC10667168. License: CC BY.
Panuveitis ร่วมกับ nonocclusive vasculitis ในตาซ้ายหลังฉีด brolucizumab การตรวจ fundus พบ vitreous haze, hyperemia ของ optic nerve และ sheathing รอบหลอดเลือดจอประสาทตา บางส่วน การตรวจ fluorescein angiography พบการรั่วของ optic nerve และ perivascular leakage ใน posterior pole และ peripheral retina
เป็นที่ทราบกันว่า brolucizumab ทำให้เกิด IOI บ่อยกว่ายาต้าน VEGF อื่นๆ
การศึกษา/ประชากร อุบัติการณ์ IOI หมายเหตุ HAWK/HARRIER (IOI โดยรวม) 4.4% จอประสาทตา อักเสบ 3.6%, หลอดเลือดอุดตัน 2.1%10) KESTREL (6 มก.) 3.7% (กลุ่มควบคุม 0.5%) การศึกษา DME10) MERLIN (ช่วง 4 สัปดาห์) 9.3% ยุติการศึกษา10) ผู้ป่วยชาวญี่ปุ่น 15-20% 10) หลังวางตลาด (หลอดเลือดอักเสบ + การอุดตันเชิงซ้อน) 3.73/10,000 การฉีด
IOI ส่วนใหญ่เกิดขึ้นภายใน 6 เดือนหลังการให้ยาครั้งแรก หรือหลังการฉีด 4 ครั้ง 10)
กลไก : อัตราการตรวจพบ ADA (แอนติบอดีต่อยา) สูงใน brolucizumab (35–52%) เมื่อเทียบกับ ranibizumab และ aflibercept (น้อยกว่า 5%) และเชื่อว่าเป็นปฏิกิริยาภูมิไวเกินชนิดที่ 3 จากการสะสมของอิมมูนคอมเพล็กซ์ 10)
เยื่อบุตาอักเสบ (รายงานแรกของโลก)เยื่อบุตาอักเสบ ส่วนหลังหลังฉีด brolucizumab ในผู้ป่วยญี่ปุ่น 3 ราย ร่วมกับความดันลูกตา สูงขึ้นถึง 24–49 มม.ปรอท และหนึ่งรายลุกลามเป็นหลอดเลือดแดงจอประสาทตา อุดตันและหลอดเลือดอักเสบ 9)
การรักษา : การฉีด triamcinolone acetonide (STTA) ขนาด 5–20 มก. ใต้เยื่อบุตา หรือใต้ Tenon ได้ผลดี มีรายงานการใช้ร่วมกับการป้องกันด้วย STTA 18, 19)
อุบัติการณ์ของ IOI คือ 2.0% ใน nAMD , 1.3% ใน DME, 1.4% ใน RVO และ 8.5% ในกรณีฉีดสองตา 8) ในการสำรวจหลังวางตลาด หลอดเลือดจอประสาทตาอักเสบ พบน้อย (0.17/10,000 การฉีด) แต่หลอดเลือดจอประสาทตาอักเสบ ชนิดอุดตันร่วมกับเลือดออก (HORV ) อาจทำให้เกิดผลลัพธ์รุนแรง 8) HOLV สงสัยว่าเกี่ยวข้องกับปฏิกิริยาภูมิไวเกินชนิดที่ 4 (แบบช้า) จากการตรวจทางพยาธิวิทยา 16)
การฉีกขาดของ RPE เกิดขึ้นในกลุ่ม faricimab 2.7% ใน TENAYA และ 3.0% ใน LUCERNE โดยความสูงของ PED >550 ไมครอนเป็นปัจจัยเสี่ยง 17)
ในผู้ป่วย ROP หลังการรักษาด้วย anti-VEGF เยื่อหุ้มเส้นใยหลอดเลือดอาจหดตัวอย่างรวดเร็วทำให้เกิดจอประสาทตาลอก แบบดึงรั้ง (TRD) ภาวะแทรกซ้อนนี้เรียกว่า crunch syndrome 3) หากมีการเจริญของเนื้อเยื่อเส้นใยอย่างกว้างขวาง การรักษาด้วย anti-VEGF เพียงอย่างเดียวไม่เหมาะสม จำเป็นต้องผ่าตัดน้ำวุ้นตา การตรวจอวัยวะภายในตาหลังฉีดเร็วเป็นสิ่งสำคัญเพื่อติดตามการเปลี่ยนแปลงของเนื้อเยื่อที่เจริญ
การบาดเจ็บเลนส์ : ต้อกระจก ดำเนินไป ป้องกันโดยปฏิบัติตามระยะการแทงเข็ม (4 มม. ในตาที่มีเลนส์)การบาดเจ็บจอประสาทตา : จอประสาทตาลอก แบบมีรอยฉีกขาด ป้องกันโดยใช้เข็มสั้น 30G อย่างเหมาะสมการบาดเจ็บซิลิอารีบอดี : เลือดออกในน้ำวุ้นตา ป้องกันโดยปฏิบัติตามตำแหน่งและทิศทางการแทงเข็ม
ความดันลูกตา ที่เพิ่มขึ้นชั่วคราวทันทีหลังการฉีดเกิดขึ้นในผู้ป่วยทุกรายที่ได้รับการฉีด การฉีด 0.05 มล. ทำให้ความดันลูกตา เพิ่มขึ้นทันทีเป็น 50 มม.ปรอท แต่โดยปกติแล้วสามารถกลับคืนได้ ในผู้ป่วยที่มีประวัติโรคต้อหิน ต้องระวังความดันลูกตา ที่สูงอย่างต่อเนื่อง และหากจำเป็น ให้เจาะช่องหน้าม่านตา เพื่อลดความดัน
มีความเสี่ยงทางทฤษฎีของโรคหลอดเลือดสมองและกล้ามเนื้อหัวใจตาย ในการทดลอง HAWK ของโบรลูซิซูแมบ พบ ATE 1.1-1.4% 10) ในผู้ป่วยที่มีประวัติ ต้องใช้ยาด้วยความระมัดระวัง
Q
หลังฉีด ควรไปพบแพทย์เมื่อมีอาการใด?
A
หากมีอาการต่อไปนี้ ให้ไปพบจักษุแพทย์ทันที: ① การมองเห็น ลดลงอย่างรวดเร็ว ② อาการปวดตา หรือตาแดง แย่ลง ③ จำนวนจุดลอยตัวเพิ่มขึ้นอย่างชัดเจน ④ มีสารคัดหลั่ง อาการเหล่านี้อาจบ่งบอกถึงเยื่อบุตาอักเสบ ติดเชื้อหรือการอักเสบภายในลูกตา (IOI) โดยเฉพาะอย่างยิ่งต้องระวังในช่วง 24-72 ชั่วโมงหลังฉีด
Q
หากเกิด IOI จากโบรลูซิซูแมบ ควรทำอย่างไร?
A
หากเกิดการมองเห็น ลดลงอย่างรวดเร็ว จุดลอยตัวแย่ลง ตาแดง หรือปวดตา ให้ไปพบจักษุแพทย์ทันที หลังการวินิจฉัย การฉีดไตรแอมซิโนโลน อะซีโทไนด์ (STTA) ใต้เยื่อบุตา หรือใต้แคปซูลเทนอนได้ผล และการอักเสบจะดีขึ้นในกรณีส่วนใหญ่ 18, 19) การฉีดซ้ำควรพิจารณาอย่างรอบคอบหลังจากยืนยันว่าการอักเสบหายไปด้วย LFP (Laser Flare Cell Photometer) และอื่นๆ หากมีภาวะหลอดเลือดอุดตันรุนแรง การฉีดซ้ำอาจมีข้อห้าม ดังนั้นควรพิจารณาเปลี่ยนไปใช้ยาทางเลือกอื่น
VEGF จับกับ VEGFR-1 และ VEGFR-2 บนเซลล์บุผนังหลอดเลือด ส่งเสริมการเพิ่มจำนวนเซลล์บุผนังหลอดเลือด การเพิ่มการซึมผ่านของหลอดเลือด และการสร้างเส้นเลือดใหม่
AMD คอรอยด์ (CNV ) และการเพิ่มการซึมผ่านของหลอดเลือดDME : การทำลาย Blood-Retinal Barrier (BRB) → การเกิดจอประสาทตา บวมน้ำRVO จอประสาทตา บวมน้ำและเส้นเลือดใหม่
เมื่อระดับ VEGF ลดลงหลังการฉีดเข้าแก้วตา การซึมผ่านของหลอดเลือดลดลงและจอประสาทตา บวมน้ำดีขึ้น ผลของยาต้าน VEGF เป็นเพียงชั่วคราว ดังนั้นจึงจำเป็นต้องฉีดซ้ำเป็นระยะ
ยา น้ำหนักโมเลกุล ความสัมพันธ์กับ VEGF-A (Kd) เป้าหมาย โบรลูซิซูแมบ 26 กิโลดาลตัน 28.4 พิโคโมลาร์ VEGF-A (ไอโซฟอร์มทั้งหมด) รานิบิซูแมบ 48 กิโลดาลตัน 20.6 พิโคโมลาร์ VEGF-A (ไอโซฟอร์มทั้งหมด) อะฟลิเบอร์เซปต์ 115 กิโลดาลตัน 0.49 พิโคโมลาร์ (สูงสุด) VEGF-A/B และ PlGF เบวาซิซูแมบ 148 กิโลดาลตัน 35.1 พิโคโมลาร์ VEGF-A ฟาริซิแมบ 149 กิโลดาลตัน — VEGF-A + Ang-2
Ang-2 มีส่วนเกี่ยวข้องกับการทำให้หลอดเลือดไม่เสถียรในฐานะตัวต้านรีเซพเตอร์ Tie-2 การยับยั้ง Ang-2 โดยฟาริซิแมบ จะทำให้วิถี Tie-2 กลับสู่ปกติ เพิ่มความเสถียรของหลอดเลือด และลดความไวต่อ VEGF ผลการยับยั้งแบบคู่นี้เป็นพื้นฐานทางเภสัชวิทยาที่ทำให้สามารถยืดระยะห่างระหว่างการให้ยาได้
เหตุผลที่ให้ยา 3-5 ครั้งคงที่ทุกเดือนในระยะเริ่มต้นคือเพื่อระงับกิจกรรมของโรคอย่างรุนแรงตั้งแต่เนิ่นๆ วิธี T&E ให้กรอบที่ไม่ยอมให้เกิดการกลับเป็นซ้ำตราบใดที่ความเข้มข้นของยาในวุ้นตา ยังคงอยู่ในช่วงการรักษา
ใน PDS (ระบบนำส่งผ่านพอร์ต) ของ ranibizumab ผู้ป่วย 98% ไม่จำเป็นต้องฉีดทุกเดือนด้วยการให้ยาเสริมทุก 6 เดือน 12) ในปี 2025 กำลังพิจารณาการขยายข้อบ่งชี้สำหรับ DME 13) คาดว่าจะลดภาระการฉีดลงอย่างมาก
ในการทดลอง PULSAR (AMD ) ผู้ป่วย 79% รักษาช่วงห่าง 12 สัปดาห์ และ 77% รักษาช่วงห่าง 16 สัปดาห์ที่สัปดาห์ที่ 48 12) ในการทดลอง PHOTON (DME) ผู้ป่วย 93% บรรลุช่วงห่าง 12 สัปดาห์ขึ้นไป 13)
การทดลอง PROUD (เกาหลี) กำลังดำเนินการสำหรับ PCV และ AT1 และคาดว่าจะสะสมหลักฐานสำหรับโรคเฉพาะในเอเชีย 14)
การทดลอง SALWE EN กำลังดำเนินการเพื่อศึกษาผลของ faricimab ในผู้ป่วย PCV 20) พบระดับ Ang-2 สูงใน aqueous humor ของผู้ป่วย PCV และคาดว่าจะมีผลเพิ่มเติมจากการยับยั้ง Ang-2
การใช้ STTA ร่วมกับ brolucizumab อาจมีประสิทธิภาพในการป้องกัน IOI และควบคุมการรั่วซึม 18, 19) กำลังมีการวิจัยเพื่อกำหนดขนาดยาและช่วงเวลาที่เหมาะสม
เพื่อการวินิจฉัยแยกโรค早期ระหว่าง endophthalmitis ที่ไม่ติดเชื้อและติดเชื้อ การวัดโปรไฟล์ไซโตไคน์ในน้ำวุ้นตา (IL-6, IL-8, IL-10) คาดว่าจะเป็นเครื่องมือช่วย 7)
ยาชีววัตถุ คล้ายคลึงของ ranibizumab และ bevacizumab กำลังเกิดขึ้น การลดต้นทุนอย่างมีนัยสำคัญคาดว่าจะช่วยเพิ่มอัตราการรักษาต่อเนื่องและการเข้าถึงการรักษาพยาบาล 12)
日本眼科学会. 新生血管型加齢黄斑変性の診療ガイドライン. 日眼会誌. 2024.
日本眼科学会. 糖尿病網膜症診療ガイドライン(第1版). 日眼会誌. 2023.
日本未熟児網膜症研究会. 未熟児網膜症に対する抗VEGF療法の手引き(第2版). 2024.
日本眼科学会. 近視性黄斑部新生血管の診療ガイドライン. 日眼会誌. 2023.
American Academy of Ophthalmology. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024. [Protocol S data]
American Academy of Ophthalmology. Retinal Vein Occlusion Preferred Practice Pattern. Ophthalmology. 2024. [BRAVO data]
Kudasiewicz-Kardaszewska A, Ozimek MA, Kardaszewska A, et al. Complete and Early Vitrectomy for Sterile Endophthalmitis After Bevacizumab: A Case Series. Cureus. 2025;17(10):e93996. doi:10.7759/cureus.93996.
Tadayoni R, Paris LP, Danzig CJ, et al. Efficacy and safety of faricimab for macular edema due to retinal vein occlusion: 24-week results from the BALATON and COMINO trials. Ophthalmology. 2024;131(8):950-960.
Takayama T, et al. Scleritis following intravitreal brolucizumab injection: a case series. J Med Case Rep. 2024;18:80.
Sharma A, et al. Understanding retinal vasculitis associated with brolucizumab. Ocul Immunol Inflamm. 2022;30(6):1508-1510.
Nawar AE, Abdelrahman AM, Ebeid OM, Ahmed SM, El-Abhar AE. Subthreshold micropulse laser combined with ranibizumab versus ranibizumab monotherapy in branch retinal vein occlusion with macular edema. Clin Ophthalmol. 2022;16:1139-1151. doi:10.2147/OPTH.S355315. PMID:35386091. PMCI D:PMC8968960
Flaxel CJ, Adelman RA, Bailey ST, et al. Age-related macular degeneration preferred practice pattern. Ophthalmology. 2024;131(1):P1-P68.
Flaxel CJ, Adelman RA, Bailey ST, et al. Diabetic retinopathy preferred practice pattern. Ophthalmology. 2024;131(1):P99-P168.
Sen P, et al. Polypoidal choroidal vasculopathy: update on diagnosis and treatment. Clin Ophthalmol. 2023;17:53-70.
Bloom J, Madani R, Haidar AJ, Alasil T. Faricimab treatment of polypoidal choroidal vasculopathy resistant to intravitreal ranibizumab. J VitreoRetin Dis. 2024;8(6):731-734.
Yavari N, Gupta AS, Mitsios A, et al. Bilateral hemorrhagic occlusive retinal vasculitis and panuveitis following intravitreal faricimab injection. Am J Ophthalmol Case Rep. 2026;41:102532.
Clemens CR, Alten F, Zimmermann JA, Eter N. Old problem in a new guise: retinal pigment epithelium tear after intravitreal faricimab injection. Case Rep Ophthalmol. 2023;14:241-244.
Shigemoto Y, et al. Combination therapy of STTA and IVbr for brolucizumab-related IOI. Medicine. 2021;100(42):e27580.
Saito M, et al. IOI after IVbr monitored by laser flare-cell photometer. Am J Ophthalmol Case Rep. 2022;28:101727.
Cheung CMG, Lai TYY, Teo K, et al. Polypoidal choroidal vasculopathy: consensus nomenclature and non-indocyanine green angiograph diagnostic criteria. Eye. 2024;39:819-834.
American Academy of Ophthalmology. Similar visual outcomes are seen with two post-injection endophthalmitis treatments. AAO Editors’ Choice. 2024 Oct 8. Available from: https://www.aao.org/education/editors-choice/similar-visual-outcomes-are-seen-with-two-post-inj