雷珠单抗(诺适得®)

玻璃体注射(抗VEGF疗法)
一目了然的要点
Section titled “一目了然的要点”1. 什么是玻璃体注射(抗VEGF疗法)?
Section titled “1. 什么是玻璃体注射(抗VEGF疗法)?”抗VEGF药物的玻璃体内注射是通过将药液直接注入玻璃体腔,抑制VEGF的作用(新生血管形成和血管通透性增加)的治疗方法。主要适应症包括年龄相关性黄斑变性、糖尿病性黄斑水肿和视网膜静脉阻塞等视网膜血管疾病。
抗VEGF疗法在2000年代迅速进入临床应用。
| 年份 | 事件 |
|---|---|
| 2004年 | 贝伐珠单抗的眼内给药开始探索性应用 |
| 2006年 | 雷珠单抗获得FDA批准(MARINA/ANCHOR试验)12) |
| 2011年 | 阿柏西普获得FDA批准(VIEW试验)12) |
| 2019年 | 布罗鲁珠单抗获得FDA批准(HAWK/HARRIER试验)10) |
| 2022年 | 法瑞西单抗获得FDA批准(TENAYA/LUCERNE/YOSEMITE/RHINE试验)8) |
- 渗出型年龄相关性黄斑变性(nAMD):脉络膜新生血管(CNV)的一线治疗
- 糖尿病黄斑水肿(DME):糖尿病视网膜病变伴发的黄斑水肿
- 视网膜静脉阻塞(RVO):视网膜中央或分支静脉阻塞引起的黄斑水肿6)
- 增殖性糖尿病视网膜病变(PDR):PRP的辅助或替代治疗(雷珠单抗)5)
- 病理性近视继发脉络膜新生血管(mCNV):阿柏西普、雷珠单抗4)
- 息肉状脉络膜血管病变(PCV):布罗鲁珠单抗的息肉消退率较高14)
- 早产儿视网膜病变(ROP):雷珠单抗0.2 mg(2019年获批)、阿柏西普0.4 mg(2022年9月获批)。两者均为成人剂量的20%~40%的低剂量制剂。3)
- 地图样萎缩(GA):补体抑制剂
- 眼内炎:直接给予抗生素、抗真菌药或抗病毒药
- 眼内恶性淋巴瘤:甲氨蝶呤
年龄相关性黄斑变性、糖尿病黄斑水肿和视网膜静脉阻塞是三大主要适应症。这些疾病中,VEGF过度产生,导致新生血管形成和血管通透性增加,进而引起黄斑部视力下降。通过向玻璃体内直接注射抗VEGF药物,可以抑制这些病理过程,从而改善或维持视力。近年来,适应症已扩展到PDR、mCNV、ROP和息肉状脉络膜血管病变等。
2. 可用的抗VEGF药物(各论)
Section titled “2. 可用的抗VEGF药物(各论)”药物比较(一览)
Section titled “药物比较(一览)”| 药物名称 | 商品名 | 分子量 | 作用机制 | 剂量 | 批准(日本) |
|---|---|---|---|---|---|
| 雷珠单抗 | 诺适得® | 48 kDa | VEGF-A Fab片段 | 0.5 mg(AMD/RVO),0.3 mg(DME) | 2009年 |
| 阿柏西普 | 艾力雅® | 115 kDa | VEGF-A/B和PlGF抑制(诱饵受体) | 2 mg / 8 mg(HD) | 2012年 |
| 培加他尼 | Macugen® | — | VEGF165适配体 | 0.3 mg | 2008年 |
| 布罗鲁珠单抗 | Beovu® | 26 kDa | VEGF-A scFv | 6 mg | 2020年 |
| 法瑞西单抗 | Vabysmo® | 149 kDa | VEGF-A + Ang-2双特异性抗体 | 6 mg | 2023年 |
| 贝伐珠单抗 | 安维汀® | 148 kDa | VEGF-A 全长IgG | 1.25 mg | —(超说明书使用) |
阿柏西普(艾力雅®)
分子量:115 kDa(融合蛋白)
作用机制:同时抑制VEGF-A、VEGF-B和PlGF。VEGF-A亲和力Kd=0.49 pM,最高。
主要试验:VIEW试验显示非劣效于雷珠单抗。高剂量8 mg(HD)可延长至16周间隔。12, 13)
特点:广泛的VEGF抑制谱。在DME中,Protocol T试验显示1年视力改善最大。13)
布罗鲁珠单抗(Beovu®)
分子量:26 kDa(scFv,现有药物中最小)
作用机制:scFv结构,给药摩尔浓度约为阿柏西普的12倍。组织渗透性高。
主要试验:HAWK/HARRIER试验达到非劣效性。高达55%的患者维持12周间隔。10)
注意事项:IOI发生率4.4%(HAWK/HARRIER),日本人15-20%。视网膜血管炎和血管闭塞风险。10)
法瑞西单抗(Vabysmo®)
贝伐珠单抗(Avastin®)
分子量:148 kDa(全长IgG)
作用机制:抑制VEGF-A(眼科超说明书使用)
主要试验:CATT试验证实与雷珠单抗疗效相当。12)
使用情况:成本大幅降低。无菌分装静脉滴注制剂后使用。
培加他尼(Macugen®)
作用机制:VEGF165特异性适配体
现状:2008年获批的第一代药物。目前新一代药物为主流。为早期抗VEGF治疗概念的建立做出了贡献。
在眼科领域属于超说明书使用,无菌制备静脉滴注制剂用于眼科。CATT试验证实其与雷珠单抗具有同等的视力改善效果,且成本大幅降低,因此在全球广泛使用。但在日本没有保险覆盖,使用取决于医疗机构。
3. 适应症和给药方案
Section titled “3. 适应症和给药方案”抗VEGF药物的给药分为诱导期和维持期两个阶段。
- 诱导期:为强力抑制疾病活动性,每月固定给药3至6次(因疾病和药物而异)。
- 维持期有以下三种方式:
- PRN(按需治疗):每月就诊,仅在出现复发迹象时给药
- 固定给药:每2个月或每3个月等固定间隔定期给药
- 治疗并延长(T&E):若无活动性迹象,则每2周延长一次间隔;复发时缩短间隔。
雷珠单抗推荐的基本给药方案为:导入期每月1次共3次,之后维持期按需治疗(PRN);阿柏西普推荐导入期每月1次共3次,之后每2个月固定给药或采用治疗并延长(T&E)方案。近年来,许多机构已采用T&E方案。
按疾病推荐的方案
Section titled “按疾病推荐的方案”| 适应症 | 推荐药物 | 导入期 | 维持期 |
|---|---|---|---|
| nAMD(雷珠单抗) | Lucentis® 0.5 mg | 每月1次×3次1) | PRN(每月监测) |
| nAMD(阿柏西普) | Eylea® 2 mg | 每月1次×3次1) | 每2个月固定或T&E(最长3个月) |
| nAMD(布罗鲁珠单抗) | Beovu® 6 mg | 每月1次×3次 | 每8~12周10) |
| nAMD(法瑞西单抗) | Vabysmo® 6 mg | 每4周1次×4次 | 每8周至每16周8) |
| DME(阿柏西普) | Eylea® 2 mg | 每月1次×5次2) | 每2个月 |
| DME(雷珠单抗) | Lucentis® 0.5 mg | 每月1次×3次2) | PRN |
| DME(法瑞西单抗) | Vabysmo® 6 mg | 每4周1次×4至6次 | PTI(最长每16周)8, 13) |
| RVO | 阿柏西普/法瑞西单抗 | Q4W×6个月 | PTI(最长Q16W)8) |
| PDR | 雷珠单抗 0.3 mg | — | 非劣效于PRP 5) |
| mCNV | 阿柏西普/雷珠单抗 | 初始1~3次 | PRN(可能单次缓解)4) |
| ROP(雷珠单抗) | 诺适得® 0.2 mg | 初始剂量 | 复发时追加(间隔≥1个月)3) |
| ROP(阿柏西普) | 艾力雅® 0.4 mg | 首次 | 复发时追加(间隔1个月以上)3) |
PCV(息肉状脉络膜血管病变)的处理:布罗珠单抗的息肉消退率约79%,优于其他药物,76%的患者维持12周间隔(48周)。14) 法瑞西单抗在雷珠单抗抵抗性PCV病例中也有效。15)
BALATON试验(BRVO,n=553):法瑞西单抗6.0 mg vs 阿柏西普2.0 mg Q4W,24周BCVA变化分别为+16.9个字母和+17.5个字母(达到非劣效性)。FA渗漏消失率法瑞西单抗33.6% vs 阿柏西普21.0%(名义p=0.0023),法瑞西单抗显著更优。8)
COMINO试验(CRVO/HRVO,n=729):相同方案,24周BCVA变化分别为+16.9个字母和+17.3个字母(达到非劣效性)。CST变化−461.6 μm vs −448.8 μm。FA渗漏消失率法瑞西单抗44.4% vs 阿柏西普30.0%(名义p=0.0002),显著更优,显示了Ang-2抑制的血管稳定作用。8)
STTA联合治疗(RVO):雷珠单抗联合脉络膜上腔曲安奈德4 mg与雷珠单抗单药相比,显著减少注射次数(4.4次→2.47次,p<0.001)。11)
3-8. 早产儿视网膜病变(ROP)的抗VEGF治疗
Section titled “3-8. 早产儿视网膜病变(ROP)的抗VEGF治疗”截至2022年12月,ROP治疗中获批的抗VEGF药物有以下两种:3)
- 雷珠单抗(诺适得®)0.2 mg/0.02 mL:成人剂量的40%。2019年获批。
- 阿柏西普(艾力雅®)0.4 mg/0.01 mL:成人剂量的20%。2022年9月获批。
- 再次给药应间隔1个月以上(药品说明书规定)。
治疗适应症(基于ETROP研究标准) 3):
复发率与随访 3):
阿柏西普的复发率为13.9%~28%(平均复发时间11~14.2周),雷珠单抗为20.8%~83.0%(复发时间5.9~9.3周,更早)。使用雷珠单抗时,需从注射后早期开始密切观察。如果视网膜血管未延伸至III区,建议注射后17周内每周进行一次眼底检查。
A-ROP的注意事项 3):
在A-ROP中,抗VEGF单药治疗需要额外治疗的比例为75.0%~87.5%。注射后1~3周内可能出现早期复发,若纤维增殖广泛,则抗VEGF单药治疗不适用(收缩导致牵拉性视网膜脱离的风险)。
ROP的注射技术(与成人的不同点) 3):
- 进针位置:角膜缘后1.0~1.5 mm(与成人的3.5~4 mm有很大不同)。
- 针头方向:向下进针(因为晶状体相对较大,朝向中央有穿透晶状体的风险)。
- 使用30G或更细的针头。
- 确认剂量:雷珠单抗0.02 mL,阿柏西普0.01 mL(仔细确认以防止过量给药)。
Protocol T试验显示,1年时阿柏西普的视力改善最大。但在轻度组(BCVA ≥20/40)中,三种药物之间无统计学显著差异。13) 法瑞西单抗在YOSEMITE/RHINE试验中显示出与阿柏西普相当的视力改善,同时维持期注射间隔可进一步延长(第2年Q16W达成率60%~64%)。8) 应根据患者背景和就诊频率意愿选择药物。
4. 玻璃体注射技术
Section titled “4. 玻璃体注射技术”- 防止患者、眼别、药物混淆:决定注射后,确认患者识别标签。
- 确认碘过敏:务必提前确认。
- 准备必要物品:
- 皮肤消毒用10%聚维酮碘
- 麻醉眼药水、稀释并恢复至室温的PA碘眼药水、抗菌眼药水(必要时)
- 纱布、棉签、带胶带的有孔手术巾
- 开睑器、卡尺、显微有齿镊
- 注射针、注射液(使用药瓶时:1 mL注射器和带过滤器的抽液针)
消毒和麻醉步骤
Section titled “消毒和麻醉步骤”麻醉:考虑到消毒液可能飞溅到对侧眼,先双眼滴用贝诺克西尔®眼药水,然后对治疗眼滴用4%赛洛卡因®眼药水两次。
PA碘消毒注意事项:
- 刚从冰箱取出的PA碘抗菌和抗真菌灭活效果降低,务必恢复至室温。
- 在非密闭容器中于25°C保存时,有效成分残留率在5小时内降至60%。不要使用放置时间过长的PA碘。
- 灭活细菌和真菌需要约1分钟的接触时间,因此冲洗后应保持闭眼,确保与结膜有足够的接触时间。
口腔细菌控制:使用带孔手术巾,术者、助手及患者均佩戴口罩以防止飞沫传播。
穿刺位置与针头方向
Section titled “穿刺位置与针头方向”从外科角膜缘开始的穿刺距离如下。保持正确的穿刺位置可确保在睫状体平坦部(睫状体皱褶部后方)穿刺,从而避免晶状体损伤和玻璃体出血。
| 眼部状态 | 距角膜缘的距离 |
|---|---|
| 有晶状体眼 | 4 mm(睫状体平坦部) |
| 无晶状体眼或人工晶状体植入眼 | 3.5 mm |
| 早产儿 | 1.0~1.5 mm |
针头朝向玻璃体腔中心穿刺。在靠近角膜缘的位置穿刺可能损伤睫状体皱褶部,易导致玻璃体出血,且因与晶状体距离较近,晶状体损伤风险增加。
注射技术与术后管理
Section titled “注射技术与术后管理”- 粘贴带孔手术巾,用开睑器撑开眼睑。
- 用卡尺测量距角膜缘的穿刺距离。
- 注射部位应选择颞上或颞下象限(以防止损伤水平直肌)。
- 用镊子固定眼球,注射前将结膜稍向前推移,使拔针后的针孔错位,防止液体渗漏。
- 将30G短针几乎垂直刺入巩膜,缓慢注入药液(快速注射可能导致持续性眼压升高)。
- 拔针后,用棉签压迫注射部位。
- 术后立即检查视力(数指)。如果无法识别数指,则进行前房穿刺。
- 术后继续使用广谱抗生素眼药水3天。
由于在滴眼麻醉(贝诺西尔®、4%利多卡因®)后进行,注射中的疼痛很轻微。您可能会感到消毒剂(PA碘)的刺激感,但术后早期的不适可使用透明质酸钠滴眼液缓解。
5. 并发症与对策
Section titled “5. 并发症与对策”感染性眼内炎(最重要的并发症)
Section titled “感染性眼内炎(最重要的并发症)”感染性眼内炎是最严重的并发症,发生率约为0.027%~0.065%。一旦发生,需要紧急进行玻璃体内注射万古霉素1.0 mg + 头孢他啶2.0 mg治疗。
最重要的预防措施:
- 聚维酮碘的适当消毒(恢复至室温,接触时间至少1分钟)
- 使用带孔手术巾(防止口腔细菌飞沫污染)
关于术后预防性抗生素滴眼液,多项研究表明其不能降低眼内炎的发生率,有效性的证据不一致。
无菌性眼内炎
Section titled “无菌性眼内炎”这是一种无细菌感染的眼内炎症反应,发生率因药物而异,为0.005%~4.4%。7)
- 发病时间:通常在注射后24~48小时内(感染性眼内炎发生在2~7天后)7)
- 主要表现:玻璃体混浊(约80%)、前房积脓(约5%)7)
- 确诊:培养阴性(PCR排除病原体也有用)
- 不同药物的发生率(‰):贝伐珠单抗3.64 / 雷珠单抗1.39 / 阿柏西普0.76 7)
- 治疗:轻症保守治疗(类固醇滴眼液、结膜下注射)。CEVE方案(即刻完全玻璃体切除术)报告平均17.8天视力恢复。7)
在IRIS注册研究的匹配队列分析中,仅注射管理与早期玻璃体切除术的视力结果无显著差异。21)
眼内炎症(IOI)/ 视网膜血管炎(布罗鲁珠单抗特异性)
Section titled “眼内炎症(IOI)/ 视网膜血管炎(布罗鲁珠单抗特异性)”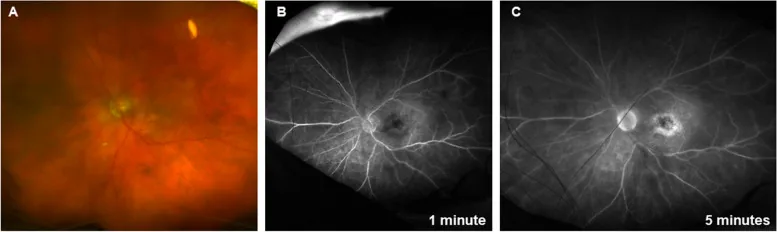
布罗鲁珠单抗比其他抗VEGF药物更容易引起眼内炎症(IOI)。
| 试验/人群 | IOI发生率 | 备注 |
|---|---|---|
| HAWK/HARRIER(总体IOI) | 4.4% | 视网膜血管炎3.6%,血管闭塞2.1%10) |
| KESTREL(6mg) | 3.7%(对照组0.5%) | DME试验10) |
| MERLIN(4周间隔) | 9.3% | 试验中断10) |
| 日本病例 | 15~20% | 10) |
| 上市后(血管炎+闭塞复合) | 3.73/10,000次注射 |
大多数IOI发生在首次给药后6个月内、4次注射以内。10)
机制:brolucizumab的ADA(抗药物抗体)阳性率高达35-52%(与雷珠单抗和阿柏西普的<5%形成对比),被认为是免疫复合物沉积引起的III型超敏反应。10)
巩膜炎(全球首报):日本有3例患者在brolucizumab注射后出现后巩膜炎,伴有眼压升高至24-49 mmHg,其中1例进展为视网膜动脉闭塞和血管炎。9)
治疗:结膜下或Tenon囊下注射曲安奈德(STTA)5-20 mg有效。也有与预防性STTA联合使用的报道。18, 19)
Faricimab相关IOI
Section titled “Faricimab相关IOI”IOI发生率在nAMD为2.0%,DME为1.3%,RVO为1.4%,双眼注射病例中为8.5%。8) 上市后监测中视网膜血管炎发生率为0.17/10,000次注射,但出血性闭塞性视网膜血管炎(HORV)可能导致严重后果。8) 病理学提示HORV与IV型(迟发型)超敏反应相关。16)
Faricimab组中RPE裂孔发生率在TENAYA试验为2.7%,LUCERNE试验为3.0%,PED高度>550 μm是危险因素。17)
Crunch综合征(牵拉性视网膜脱离)
Section titled “Crunch综合征(牵拉性视网膜脱离)”在ROP患者中,抗VEGF治疗后纤维血管膜迅速收缩,导致牵拉性视网膜脱离(TRD),这种并发症称为crunch综合征。3) 当存在广泛纤维增殖时,抗VEGF单药治疗为禁忌,需要玻璃体切除术。给药后早期眼底检查观察增殖组织的变化非常重要。
针头相关机械并发症
Section titled “针头相关机械并发症”- 晶状体损伤:白内障进展。遵守插入距离(有晶状体眼4 mm)可预防。
- 视网膜损伤:孔源性视网膜脱离。正确使用30G短针可预防。
- 睫状体损伤:玻璃体积血。遵守插入位置和方向可预防。
注射后立即出现的一过性眼压升高在所有接受注射的患者中都会发生。注入0.05 mL后眼压会立即升至50 mmHg,但通常是可逆的。有青光眼病史的患者需注意持续性眼压升高,必要时可通过前房穿刺减压。
动脉血栓栓塞事件(ATE)
Section titled “动脉血栓栓塞事件(ATE)”理论上存在脑卒中和心肌梗死的风险。在brolucizumab的HAWK试验中,ATE发生率为1.1-1.4%。10) 有既往史的患者需谨慎用药。
6. 病理生理(VEGF的作用与药物作用机制)
Section titled “6. 病理生理(VEGF的作用与药物作用机制)”VEGF的病理作用
Section titled “VEGF的病理作用”VEGF与血管内皮细胞上的VEGFR-1和VEGFR-2结合,促进内皮细胞增殖、血管通透性增加和新生血管形成。
玻璃体内注射后VEGF水平降低,血管通透性降低,黄斑水肿改善。抗VEGF药物的效果是暂时的,因此需要定期重复给药。
各药物的分子特征
Section titled “各药物的分子特征”| 药物 | 分子量 | VEGF-A亲和力(Kd) | 靶点 |
|---|---|---|---|
| 布罗珠单抗 | 26 kDa | 28.4 pM | VEGF-A(所有亚型) |
| 雷珠单抗 | 48 kDa | 20.6 pM | VEGF-A(所有亚型) |
| 阿柏西普 | 115 kDa | 0.49 pM(最高) | VEGF-A/B、PlGF |
| 贝伐珠单抗 | 148 kDa | 35.1 pM | VEGF-A |
| 法瑞西单抗 | 149 kDa | — | VEGF-A + Ang-2 |
Ang-2与法瑞西单抗的作用
Section titled “Ang-2与法瑞西单抗的作用”Ang-2作为Tie-2受体的拮抗剂参与血管不稳定化。法瑞西单抗通过抑制Ang-2使Tie-2通路正常化,提高血管稳定性并降低VEGF敏感性。这种双重抑制效应是延长给药间隔的药理学基础。
导入期集中给药的意义
Section titled “导入期集中给药的意义”导入期每月固定给药3至5次的原因是为了早期强力抑制疾病活动性。治疗-延长(T&E)法提供了一个框架,在维持玻璃体内药物浓度在治疗范围内的情况下不允许复发。
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”端口递送系统(Susvimo)
Section titled “端口递送系统(Susvimo)”雷珠单抗的PDS(端口递送系统)每6个月补充给药一次,98%的患者无需每月注射。12) 2025年正在考虑扩展适应症至DME。13) 预计可大幅减轻注射负担。
高剂量阿柏西普8 mg(艾力雅® HD)
Section titled “高剂量阿柏西普8 mg(艾力雅® HD)”PULSAR试验(AMD)中,48周时79%维持12周间隔,77%维持16周间隔。12) PHOTON试验(DME)中,93%达到12周或更长间隔。13)
布罗鲁珠单抗适应症扩展试验
Section titled “布罗鲁珠单抗适应症扩展试验”针对PCV和黄斑毛细血管扩张症1型(AT1)的PROUD试验(韩国)正在进行中,预计将为亚洲特有疾病积累证据。14)
法瑞西单抗PCV试验(SALWEEN试验)
Section titled “法瑞西单抗PCV试验(SALWEEN试验)”评估法瑞西单抗对PCV患者效果的SALWEEN试验正在进行中。20) PCV患者房水中Ang-2水平升高已被确认,预计Ang-2抑制具有附加获益。
联合STTA预防IOI
Section titled “联合STTA预防IOI”结膜下/筋膜囊下曲安奈德(STTA)与布罗鲁珠单抗联合给药可能在预防IOI和控制渗出方面均有效。18, 19) 关于最佳剂量和给药时机标准化的研究正在进行中。
利用生物标志物进行早期鉴别
Section titled “利用生物标志物进行早期鉴别”测量玻璃体液中细胞因子谱(IL-6、IL-8、IL-10)有望成为早期鉴别无菌性和感染性眼内炎的辅助工具。7)
雷珠单抗和贝伐珠单抗的生物类似药正在出现。预计大幅降低成本将提高治疗持续率和改善医疗可及性。12)
8. 参考文献
Section titled “8. 参考文献”- 日本眼科学会. 新生血管型加齢黄斑変性の診療ガイドライン. 日眼会誌. 2024.
- 日本眼科学会. 糖尿病網膜症診療ガイドライン(第1版). 日眼会誌. 2023.
- 日本未熟児網膜症研究会. 未熟児網膜症に対する抗VEGF療法の手引き(第2版). 2024.
- 日本眼科学会. 近視性黄斑部新生血管の診療ガイドライン. 日眼会誌. 2023.
- American Academy of Ophthalmology. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024. [Protocol S data]
- American Academy of Ophthalmology. Retinal Vein Occlusion Preferred Practice Pattern. Ophthalmology. 2024. [BRAVO data]
- Kudasiewicz-Kardaszewska A, Ozimek MA, Kardaszewska A, et al. Complete and Early Vitrectomy for Sterile Endophthalmitis After Bevacizumab: A Case Series. Cureus. 2025;17(10):e93996. doi:10.7759/cureus.93996.
- Tadayoni R, Paris LP, Danzig CJ, et al. Efficacy and safety of faricimab for macular edema due to retinal vein occlusion: 24-week results from the BALATON and COMINO trials. Ophthalmology. 2024;131(8):950-960.
- Takayama T, et al. Scleritis following intravitreal brolucizumab injection: a case series. J Med Case Rep. 2024;18:80.
- Sharma A, et al. Understanding retinal vasculitis associated with brolucizumab. Ocul Immunol Inflamm. 2022;30(6):1508-1510.
- Nawar AE, Abdelrahman AM, Ebeid OM, Ahmed SM, El-Abhar AE. Subthreshold micropulse laser combined with ranibizumab versus ranibizumab monotherapy in branch retinal vein occlusion with macular edema. Clin Ophthalmol. 2022;16:1139-1151. doi:10.2147/OPTH.S355315. PMID:35386091. PMCID:PMC8968960
- Flaxel CJ, Adelman RA, Bailey ST, et al. Age-related macular degeneration preferred practice pattern. Ophthalmology. 2024;131(1):P1-P68.
- Flaxel CJ, Adelman RA, Bailey ST, et al. Diabetic retinopathy preferred practice pattern. Ophthalmology. 2024;131(1):P99-P168.
- Sen P, et al. Polypoidal choroidal vasculopathy: update on diagnosis and treatment. Clin Ophthalmol. 2023;17:53-70.
- Bloom J, Madani R, Haidar AJ, Alasil T. Faricimab treatment of polypoidal choroidal vasculopathy resistant to intravitreal ranibizumab. J VitreoRetin Dis. 2024;8(6):731-734.
- Yavari N, Gupta AS, Mitsios A, et al. Bilateral hemorrhagic occlusive retinal vasculitis and panuveitis following intravitreal faricimab injection. Am J Ophthalmol Case Rep. 2026;41:102532.
- Clemens CR, Alten F, Zimmermann JA, Eter N. Old problem in a new guise: retinal pigment epithelium tear after intravitreal faricimab injection. Case Rep Ophthalmol. 2023;14:241-244.
- Shigemoto Y, et al. Combination therapy of STTA and IVbr for brolucizumab-related IOI. Medicine. 2021;100(42):e27580.
- Saito M, et al. IOI after IVbr monitored by laser flare-cell photometer. Am J Ophthalmol Case Rep. 2022;28:101727.
- Cheung CMG, Lai TYY, Teo K, et al. Polypoidal choroidal vasculopathy: consensus nomenclature and non-indocyanine green angiograph diagnostic criteria. Eye. 2024;39:819-834.
- American Academy of Ophthalmology. Similar visual outcomes are seen with two post-injection endophthalmitis treatments. AAO Editors’ Choice. 2024 Oct 8. Available from: https://www.aao.org/education/editors-choice/similar-visual-outcomes-are-seen-with-two-post-inj
