رانیبیزوماب (لوسنتیس®)

تزریق داخل زجاجیه (درمان ضد VEGF)
نکات کلیدی در یک نگاه
Section titled “نکات کلیدی در یک نگاه”1. تزریق داخل زجاجیه (درمان ضد VEGF) چیست؟
Section titled “1. تزریق داخل زجاجیه (درمان ضد VEGF) چیست؟”تزریق داخل زجاجیه داروی ضد VEGF، با تزریق مستقیم دارو به حفره زجاجیه، اثر VEGF (رگزایی و افزایش نفوذپذیری عروق) را مهار میکند. بیماریهای عروقی شبکیه مانند دژنراسیون ماکولا وابسته به سن، ادم ماکولا دیابتی و انسداد ورید شبکیه از موارد اصلی کاربرد آن هستند.
تاریخچه
Section titled “تاریخچه”درمان ضد VEGF در دهه ۲۰۰۰ به سرعت وارد کاربرد بالینی شد.
| سال | رویداد |
|---|---|
| ۲۰۰۴ | شروع آزمایشی تجویز داخل چشمی بواسیزوماب |
| ۲۰۰۶ | تأیید رانیبیزوماب توسط FDA (آزمایشهای MARINA/ANCHOR) 12) |
| ۲۰۱۱ | تأیید آفلیبرسپت توسط FDA (آزمایشهای VIEW) 12) |
| ۲۰۱۹ | تأیید برولوسیزوماب توسط FDA (آزمایشهای HAWK/HARRIER) 10) |
| ۲۰۲۲ | تأیید فاریسیماب توسط FDA (آزمایشهای TENAYA/LUCERNE/YOSEMITE/RHINE) 8) |
بیماریهای اصلی قابل درمان
Section titled “بیماریهای اصلی قابل درمان”- دژنراسیون ماکولای وابسته به سن از نوع مرطوب (nAMD): درمان خط اول برای نئوواسکولاریزاسیون مشیمیه (CNV)
- ادم ماکولای دیابتی (DME): ادم ماکولا همراه با رتینوپاتی دیابتی
- انسداد ورید شبکیه (RVO): ادم ماکولا در انسداد ورید مرکزی یا شاخهای شبکیه6)
- رتینوپاتی دیابتی پرولیفراتیو (PDR): به عنوان کمککننده یا جایگزین PRP (رانیبیزوماب)5)
- نئوواسکولاریزاسیون مشیمیه همراه با نزدیکبینی پاتولوژیک (mCNV): آفلیبرسپت، رانیبیزوماب4)
- واسکولوپاتی پولیپوئیدال مشیمیه (PCV): برولوسیزوماب با نرخ بالای پسرفت پولیپ14)
- رتینوپاتی نارسی (ROP): رانیبیزوماب 0.2 میلیگرم (تأیید شده در 2019) و آفلیبرسپت 0.4 میلیگرم (تأیید شده در سپتامبر 2022). هر دو با دوز پایینتر معادل 20-40٪ دوز بزرگسالان استفاده میشوند3)
- آتروفی جغرافیایی (GA): مهارکنندههای کمپلمان
- اندوفتالمیت: تجویز مستقیم آنتیبیوتیکها، ضدقارچها و ضدویروسها
- لنفوم داخل چشمی بدخیم: متوترکسات
دژنراسیون ماکولای وابسته به سن، ادم ماکولای دیابتی و انسداد ورید شبکیه سه بیماری اصلی قابل درمان هستند. در همه این موارد، VEGF بیش از حد تولید میشود و نئوواسکولاریزاسیون یا افزایش نفوذپذیری عروقی باعث کاهش بینایی در ماکولا میشود. با تزریق مستقیم داروی ضد VEGF به داخل زجاجیه، این فرآیندهای پاتولوژیک مهار شده و بینایی بهبود یا حفظ میشود. در سالهای اخیر، این درمان به PDR، mCNV، ROP و واسکولوپاتی پولیپوئیدال مشیمیه نیز گسترش یافته است.
2. داروهای ضد VEGF موجود (بررسی هر دارو)
Section titled “2. داروهای ضد VEGF موجود (بررسی هر دارو)”مقایسه داروها (فهرست)
Section titled “مقایسه داروها (فهرست)”| نام دارو | نام تجاری | وزن مولکولی | مکانیسم اثر | دوز | تأیید شده (ژاپن) |
|---|---|---|---|---|---|
| رانیبیزوماب | لوسنتیس® | 48 کیلودالتون | قطعه Fab ضد VEGF-A | 0.5 میلیگرم (AMD/RVO)، 0.3 میلیگرم (DME) | 2009 |
| آفلیبرسپت | آیلیا® | 115 کیلودالتون | مهار VEGF-A/B و PlGF (گیرنده فریبنده) | 2 میلیگرم / 8 میلیگرم (HD) | 2012 |
| پگاپتانیب | ماکوجن® | — | آپتامر VEGF165 | 0.3 میلیگرم | 2008 |
| برولوسیزوماب | بیوویو® | 26 کیلودالتون | scFv VEGF-A | 6 میلیگرم | 2020 |
| فاریسیماب | وابیسمو® | 149 کیلودالتون | آنتیبادی دوویژه VEGF-A + Ang-2 | 6 میلیگرم | 2023 |
| بواسیزوماب | آواستین® | 148 کیلودالتون | VEGF-A IgG کامل | 1.25 میلیگرم | — (خارج از برچسب) |
آفلیبرسپت (آیلیا®)
وزن مولکولی: 115 کیلودالتون (پروتئین همجوش)
مکانیسم اثر: مهار همزمان سه عامل VEGF-A، VEGF-B و PlGF. بالاترین میل ترکیبی VEGF-A با Kd=0.49 pM.
مطالعات اصلی: در مطالعه VIEW غیرپایینتر از رانیبیزوماب بود. دوز بالای ۸ میلیگرم (HD) تا فواصل ۱۶ هفته. 12, 13)
ویژگیها: طیف گسترده مهار VEGF. در DME، مطالعه Protocol T بهبود بینایی در یک سال را به حداکثر رساند. 13)
برولوسیزوماب (بیوویو®)
وزن مولکولی: 26 کیلودالتون (scFv، کوچکترین در میان داروهای موجود)
مکانیسم اثر: با ساختار scFv میتوان آن را با غلظت مولی حدود 12 برابر آفلیبرسپت تجویز کرد. نفوذپذیری بافتی بالایی دارد.
مطالعات اصلی: در مطالعات HAWK/HARRIER به غیرپایینتری دست یافت. حداکثر 55% فاصله 12 هفته را حفظ کردند. 10)
نکات احتیاطی: بروز IOI 4.4% (HAWK/HARRIER)، در ژاپنیها 15-20%. خطر واسکولیت شبکیه و انسداد عروق. 10)
فاریسیماب (وابیسمو®)
وزن مولکولی: 149 کیلودالتون (آنتیبادی IgG دوویژه)
مکانیسم اثر: مهار همزمان VEGF-A و Ang-2 (آنژیوپویتین-2). اولین داروی دو هدفه در جهان.
مطالعات اصلی: در TENAYA/LUCERNE (nAMD) تا Q16W. 63% از بیماران nAMD در سال دوم به Q16W دست یافتند. 8)
ویژگیها: در RVO (BALATON/COMINO) نرخ ناپدید شدن نشت FA نسبت به آفلیبرسپت برتری داشت. 8)
بواسیزوماب (آواستین®)
وزن مولکولی: 148 کیلودالتون (IgG کامل)
مکانیسم اثر: مهار VEGF-A (استفاده خارج از برچسب در چشم)
مطالعات اصلی: مطالعه CATT اثربخشی مشابه با رانیبیزوماب را تأیید کرد. 12)
وضعیت مصرف: هزینه به طور قابل توجهی پایینتر است. از فرآورده تزریقی وریدی به صورت استریل تقسیمبندی شده و استفاده میشود.
پگاپتانیب (ماکوجن®)
مکانیسم اثر: آپتامر اختصاصی VEGF165
وضعیت فعلی: داروی نسل اول تأیید شده در سال ۲۰۰۸. در حال حاضر داروهای نسل جدید غالب هستند. در ایجاد مفهوم اولیه درمان ضد VEGF نقش داشته است.
با توجه به بیماری قابل درمان، تمایل به فاصله تزریق و خطر عوارض تعیین میشود. به طور کلی در nAMD، آفلیبرسپت، فاریسیماب و برولوسیزوماب از نظر افزایش فاصله تزریق برتر هستند. در DME، آفلیبرسپت و فاریسیماب استاندارد هستند. برولوسیزوماب با در نظر گرفتن خطر IOI، در بیماران PCV مزیت نرخ بالاتر پسرفت پولیپ را دارد. فاریسیماب امکان تزریق تا هر ۱۶ هفته (Q16W) را دارد که کمترین بار مراجعه را دارد. در نهایت پزشک معالج به طور جامع تصمیم میگیرد.
در حوزه چشم پزشکی استفاده خارج از برچسب (آف-لیبل) است و فرآورده تزریقی وریدی به صورت استریل برای استفاده چشمی آماده میشود. در مطالعه CATT اثربخشی بهبود بینایی مشابه رانیبیزوماب تأیید شده است و به دلیل هزینه بسیار پایینتر، در سراسر جهان به طور گسترده استفاده میشود. با این حال در ژاپن تحت پوشش بیمه نیست و استفاده آن به تشخیص مرکز درمانی بستگی دارد.
۳. بیماریهای قابل درمان و رژیم دوز
Section titled “۳. بیماریهای قابل درمان و رژیم دوز”تجویز داروهای ضد VEGF در دو مرحله فاز القا و فاز نگهدارنده انجام میشود.
- فاز القا: برای سرکوب قوی فعالیت بیماری، به مدت ۳ تا ۶ ماه به صورت ماهانه ثابت تزریق میشود (بسته به بیماری و دارو متفاوت است).
- روشهای فاز نگهدارنده به سه نوع زیر است:
- PRN (pro re nata): مراجعه ماهانه و تزریق تنها در صورت وجود علائم عود
- تزریق ثابت: تزریق منظم در فواصل معین مانند هر ۲ ماه یا هر ۳ ماه
- Treat and Extend (T&E): در صورت عدم وجود علائم فعالیت، فاصله تزریق هر بار ۲ هفته افزایش مییابد و در صورت عود کاهش مییابد.
برای رانی بیزوماب، روش پایهای توصیه شده شامل ۳ دوز ماهانه در فاز القا و سپس دوزهای PRN در فاز نگهدارنده است. برای آفلیبرسپت، روش پایهای شامل ۳ دوز ماهانه در فاز القا و سپس دوزهای ثابت هر دو ماه یکبار یا روش T&E است. در سالهای اخیر، روش T&E در بسیاری از مراکز معرفی شده است.
رژیمهای توصیه شده بر اساس بیماری
Section titled “رژیمهای توصیه شده بر اساس بیماری”| بیماری تحت درمان | داروی توصیه شده | فاز القا | فاز نگهدارنده |
|---|---|---|---|
| nAMD (رانی بیزوماب) | Lucentis® 0.5 mg | ماهی یک بار × ۳ بار1) | PRN (مشاهده ماهانه) |
| nAMD (آفلیبرسپت) | Eylea® 2 mg | ماهی یک بار × ۳ بار1) | ثابت هر دو ماه یک بار یا T&E (حداکثر ۳ ماه) |
| nAMD (برولوسیزوماب) | Beovu® 6 mg | ماهی یک بار × ۳ بار | فواصل ۸ تا ۱۲ هفته10) |
| nAMD (فاریسیما) | Vabysmo® 6 mg | Q4W × 4 دوز | Q8W تا Q16W8) |
| DME (آفلیبرسپت) | Eylea® 2 mg | ماهی یک بار × 5 دوز2) | هر 2 ماه یک بار |
| DME (رانیبیزوماب) | Lucentis® 0.5 mg | ماهی یک بار × 3 دوز2) | PRN |
| DME (فاریسیما) | Vabysmo® 6 mg | Q4W × 4 تا 6 دوز | PTI (حداکثر Q16W)8, 13) |
| RVO | آفلیبرسپت/فاریسیماب | Q4W × 6 ماه | PTI (حداکثر Q16W) 8) |
| PDR | رانیبیزوماب 0.3 میلیگرم | — | غیرپایینتر از PRP 5) |
| mCNV | آفلیبرسپت/رانیبیزوماب | 1 تا 3 بار اولیه | PRN (احتمال بهبودی یکباره) 4) |
| ROP (رانیبیزوماب) | لوسنتیس® 0.2 میلیگرم | اولیه | اضافه در عود (فاصله ≥1 ماه) 3) |
| ROP (آفلیبرسپت) | آیلیا® 0.4 میلیگرم | اولین دوز | دوز اضافی در هنگام عود (با فاصله حداقل یک ماه) 3) |
مدیریت PCV (پلیپوئیدال کوروئیدواسکولوپاتی): برولوسیزوماب با نرخ محو شدن پولیپ حدود 79% از سایر داروها بهتر است و فاصله 12 هفتهای در 76% موارد (هفته 48) حفظ میشود. 14) فاریسیسیماب حتی در موارد PCV مقاوم به رانیبیزوماب نیز مؤثر گزارش شده است. 15)
مطالعه BALATON (BRVO، n=553): فاریسیسیماب 6.0 میلیگرم در مقابل آفلیبرسپت 2.0 میلیگرم هر 4 هفته، تغییر BCVA در هفته 24 به ترتیب +16.9 و +17.5 حرف (غیرپایینتر). نرخ محو شدن نشت FA: فاریسیسیماب 33.6% در مقابل آفلیبرسپت 21.0% (p اسمی=0.0023) که به طور معنیداری فاریسیسیماب برتر بود. 8)
مطالعه COMINO (CRVO/HRVO، n=729): با همان رژیم، تغییر BCVA در هفته 24 به ترتیب +16.9 و +17.3 حرف (غیرپایینتر). تغییر CST: 461.6- میکرومتر در مقابل 448.8- میکرومتر. نرخ محو شدن نشت FA: فاریسیسیماب 44.4% در مقابل آفلیبرسپت 30.0% (p اسمی=0.0002) که به طور معنیداری برتر بود و اثر تثبیت عروقی ناشی از مهار Ang-2 را نشان داد. 8)
ترکیب STTA (RVO): ترکیب رانیبیزوماب با تریامسینولون 4 میلیگرم در فضای فوقکوروئید، تعداد تزریقات را در مقایسه با رانیبیزوماب به تنهایی به طور معنیداری کاهش میدهد (4.4 به 2.47 بار، p<0.001). 11)
3-8. درمان ضد VEGF برای رتینوپاتی نوزادان نارس (ROP)
Section titled “3-8. درمان ضد VEGF برای رتینوپاتی نوزادان نارس (ROP)”داروهای ضد VEGF تأیید شده برای درمان ROP (تا دسامبر 2022) دو داروی زیر هستند. 3)
- رانیبیزوماب (لوسنتیس®) 0.2 میلیگرم/0.02 میلیلیتر: 40% دوز بزرگسالان. تأیید شده در سال 2019.
- آفلیبرسپت (آیلیا®) 0.4 میلیگرم/0.01 میلیلیتر: 20% دوز بزرگسالان. تأیید شده در سپتامبر 2022.
- تجویز مجدد باید با فاصله حداقل یک ماه انجام شود (طبق برچسب دارو).
اندیکاسیون درمان (بر اساس معیارهای مطالعه ETROP) 3):
- همه ROP های Zone I همراه با plus disease
- ROP مرحله 3 ناحیه I بدون plus disease
- ROP مرحله 3 ناحیه II همراه با plus disease
- ROP تهاجمی (A-ROP): انجام در اسرع وقت
نرخ عود و پیگیری 3):
نرخ عود آفلیبرسپت 13.9 تا 28% (میانگین زمان عود 11 تا 14.2 هفته) و رانیبیزوماب 20.8 تا 83.0% (زمان عود زودتر، 5.9 تا 9.3 هفته) است. هنگام استفاده از رانیبیزوماب، پیگیری دقیق از اوایل پس از تزریق ضروری است. اگر عروق شبکیه تا ناحیه III گسترش نیافته باشند، معاینه هفتگی فوندوس تا 17 هفته پس از تزریق توصیه میشود.
نکات مهم در A-ROP 3):
در A-ROP، درمان با anti-VEGF به تنهایی در 75.0 تا 87.5% موارد نیاز به درمان اضافی دارد. عود زودرس در 1 تا 3 هفته پس از تزریق رخ میدهد و در صورت فیبروز گسترده، درمان تکدارویی anti-VEGF منع مصرف دارد (خطر جداشدگی کششی شبکیه به دلیل انقباض).
تکنیک تزریق در ROP (تفاوت با بزرگسالان) 3):
- محل ورود: 1.0 تا 1.5 میلیمتر پشت لیمبوس (تفاوت قابل توجه با 3.5 تا 4 میلیمتر در بزرگسالان).
- جهت سوزن: به سمت پایین (به دلیل بزرگتر بودن نسبی عدسی، جهت مرکزی خطر سوراخ شدن عدسی را دارد).
- استفاده از سوزن 30 گیج یا کوچکتر.
- تأیید دوز: رانیبیزوماب 0.02 میلیلیتر، آفلیبرسپت 0.01 میلیلیتر (برای جلوگیری از مصرف بیش از حد با دقت بررسی شود).
در مطالعه Protocol T، آفلیبرسپت در یک سال بهترین بهبود بینایی را داشت. با این حال، در گروه خفیف (BCVA ≥ 20/40) تفاوت آماری معنیداری بین سه دارو وجود نداشت. 13) فاریسیماب در مطالعات YOSEMITE/RHINE بهبود بینایی مشابه آفلیبرسپت را نشان داد در حالی که فاصله تزریق در مرحله نگهدارنده را بیشتر افزایش میدهد (60 تا 64% در سال دوم به Q16W رسیدند). 8) انتخاب دارو بر اساس شرایط بیمار و ترجیح دفعات مراجعه انجام میشود.
4. تکنیک تزریق داخل زجاجیه
Section titled “4. تکنیک تزریق داخل زجاجیه”آمادهسازی قبل از تزریق
Section titled “آمادهسازی قبل از تزریق”- جلوگیری از اشتباه در شناسایی بیمار، چشم تحت درمان و دارو: پس از تصمیم به تزریق، برچسب شناسایی بیمار را بررسی کنید.
- بررسی آلرژی به ید: حتماً از قبل بررسی شود.
- آمادهسازی وسایل مورد نیاز:
- پوویدون ید ۱۰٪ برای ضدعفونی پوست
- قطره بیحسی چشمی، قطره چشمی PA ید رقیق شده و به دمای اتاق رسیده، قطره آنتیبیوتیک (در صورت نیاز)
- گاز، سواب پنبهای، درپوش سوراخدار با چسب
- پلکبازکن، کالیپر، فورسپس میکرو با قلاب
- سوزن تزریق، محلول تزریقی (در صورت استفاده از ویال، سرنگ ۱ میلیلیتری و سوزن نمونهبرداری با فیلتر)
مراحل ضدعفونی و بیحسی
Section titled “مراحل ضدعفونی و بیحسی”بیحسی: با توجه به احتمال پاشیده شدن ماده ضدعفونی به چشم مقابل، ابتدا قطره بنوکسیل® در هر دو چشم و سپس قطره زایلوکائین ۴٪ دو بار در چشم تحت درمان ریخته شود.
نکات مهم در ضدعفونی با PA ید:
- PA ید بلافاصله پس از خارج شدن از یخچال اثر ضدباکتریایی و ضدقارچی کاهش یافته دارد، بنابراین حتماً به دمای اتاق برسد.
- در صورت نگهداری در ظرف غیردربسته در دمای ۲۵ درجه سانتیگراد، میزان ماده مؤثر پس از ۵ ساعت به ۶۰٪ کاهش مییابد. از PA ید که مدت طولانی مانده استفاده نکنید.
- برای غیرفعال کردن باکتریها و قارچها حدود ۱ دقیقه زمان تماس لازم است، بنابراین پس از شستشوی چشم، پلکها را بسته نگه دارید تا زمان تماس کافی با ملتحمه فراهم شود.
اقدامات ضد باکتریهای دهانی: با استفاده از درپوش سوراخدار و ماسک زدن جراح، دستیار و همه بیماران از پخش قطرات جلوگیری کنید.
موقعیت ورود و جهت سوزن
Section titled “موقعیت ورود و جهت سوزن”فاصله ورود از لیمبوس جراحی به شرح زیر است. با رعایت موقعیت ورود، امکان ورود از ناحیه پارس پلانا (پشت چینهای مژگانی) فراهم شده و از آسیب عدسی و خونریزی زجاجیه جلوگیری میشود.
| وضعیت چشم | فاصله از لیمبوس |
|---|---|
| چشم با عدسی طبیعی | ۴ میلیمتر (پارس پلانا) |
| چشم بدون عدسی یا با لنز داخل چشمی | ۳.۵ میلیمتر |
| نوزاد نارس | ۱.۰ تا ۱.۵ میلیمتر |
سوزن به سمت مرکز حفره زجاجیه وارد میشود. ورود در نزدیکی لیمبوس باعث آسیب به چینهای مژگانی و خونریزی زجاجیه میشود و به دلیل نزدیکی به عدسی، خطر آسیب عدسی افزایش مییابد.
تکنیک تزریق و مراقبتهای پس از عمل
Section titled “تکنیک تزریق و مراقبتهای پس از عمل”- درپوش سوراخدار را بچسبانید و با استفاده از پلکبازکن، پلکها را باز کنید.
- با کولیس، فاصله ورود از لیمبوس را اندازهگیری کنید.
- محل تزریق باید در قسمت فوقانی یا تحتانی گیجگاهی باشد (برای جلوگیری از آسیب به عضلات راست افقی).
- با پنس کره چشم را ثابت کرده و قبل از تزریق، ملتحمه را کمی به سمت جلو جابجا کنید تا پس از خروج سوزن، سوراخ سوزن جابجا شده و از نشت مایع جلوگیری شود.
- سوزن کوتاه 30G را تقریباً عمود بر صلبیه وارد کرده و دارو را به آرامی تزریق کنید (تزریق سریع باعث افزایش پایدار فشار داخل چشم میشود).
- پس از خروج سوزن، محل ورود را با یک سواب پنبهای فشار دهید.
- بلافاصله پس از عمل، دید (شمارش انگشتان) را بررسی کنید. اگر شمارش انگشتان قابل تشخیص نبود، پاراسنتز اتاق قدامی انجام دهید.
- به مدت 3 روز پس از عمل، قطره چشمی آنتیبیوتیک وسیعالطیف را ادامه دهید.
از آنجایی که تزریق پس از بیحسی موضعی با قطره (بنوکسیل®، زایلواکائین 4%) انجام میشود، درد حین تزریق خفیف است. ممکن است احساس سوزش ناشی از ضدعفونیکننده (ید P.A) وجود داشته باشد، اما برای ناراحتی اولیه پس از عمل، قطره چشمی هیالورونات سدیم مؤثر است.
5. عوارض و اقدامات
Section titled “5. عوارض و اقدامات”اندوفتالمیت عفونی (مهمترین عارضه)
Section titled “اندوفتالمیت عفونی (مهمترین عارضه)”اندوفتالمیت عفونی جدیترین عارضه است و میزان بروز آن حدود 0.027 تا 0.065٪ میباشد. در صورت بروز، نیاز به درمان فوری با تزریق داخل زجاجیهای 1.0 میلیگرم وانکومایسین + 2.0 میلیگرم سفتازیدیم است.
مهمترین اقدام پیشگیرانه:
- ضدعفونی مناسب با پوویدون-ید (بازگرداندن به دمای اتاق، زمان تماس حداقل 1 دقیقه)
- استفاده از درپوش سوراخدار (جلوگیری از پاشیدن باکتریهای دهانی)
در مورد استفاده پیشگیرانه از قطرههای آنتیبیوتیک پس از عمل، چندین مطالعه نشان داده است که میزان بروز اندوفتالمیت را کاهش نمیدهد و شواهد مربوط به اثربخشی آن متناقض است.
اندوفتالمیت استریل (Sterile Endophthalmitis)
Section titled “اندوفتالمیت استریل (Sterile Endophthalmitis)”یک واکنش التهابی داخل چشمی بدون عفونت باکتریایی است که میزان بروز آن بسته به دارو از 0.005 تا 4.4٪ متغیر است. 7)
- زمان بروز: اغلب 24 تا 48 ساعت پس از تزریق (نوع عفونی 2 تا 7 روز بعد) 7)
- یافتههای اصلی: کدورت زجاجیه (حدود 80٪) و هیپوپیون (حدود 5٪) 7)
- تشخیص قطعی: کشت منفی (رد پاتوژن با PCR نیز مفید است)
- میزان بروز بر اساس دارو (‰): بواسیزوماب 3.64 / رانیبیزوماب 1.39 / آفلیبرسپت 0.76 7)
- درمان: موارد خفیف به صورت محافظهکارانه (قطرههای استروئیدی، تزریق زیر ملتحمه). در پروتکل CEVE (ویترکتومی کامل فوری) بهبود بینایی به طور متوسط پس از 17.8 روز گزارش شده است. 7)
در تحلیل کوهورت همسانسازی شده از IRIS Registry، تفاوت معنیداری در پیامد بینایی بین مدیریت فقط با تزریق و ویترکتومی زودهنگام مشاهده نشد. 21)
التهاب داخل چشمی (IOI) و واسکولیت شبکیه (ویژه برولوسیزوماب)
Section titled “التهاب داخل چشمی (IOI) و واسکولیت شبکیه (ویژه برولوسیزوماب)”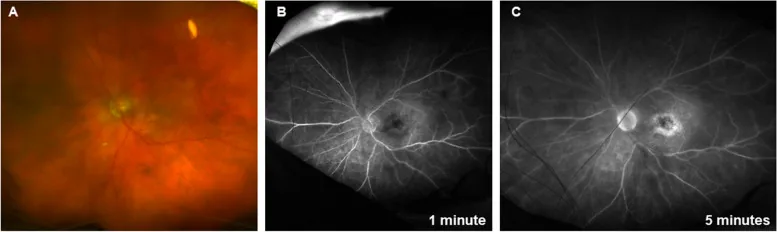
برولوسیزوماب شناخته شده است که با فراوانی بیشتری نسبت به سایر داروهای ضد VEGF باعث IOI میشود.
| مطالعه/جمعیت | بروز IOI | یادداشتها |
|---|---|---|
| HAWK/HARRIER (کل IOI) | 4.4% | واسکولیت شبکیه 3.6%، انسداد عروق 2.1%10) |
| KESTREL (6 میلیگرم) | 3.7% (شاهد 0.5%) | مطالعه DME10) |
| MERLIN (فاصله 4 هفته) | 9.3% | قطع مطالعه10) |
| بیماران ژاپنی | 15 تا 20% | 10) |
| پس از عرضه به بازار (واسکولیت + انسداد ترکیبی) | 3.73/10,000 تزریق |
اکثر موارد IOI در ۶ ماه اول و پس از ۴ تزریق اول رخ میدهد. 10)
مکانیسم: میزان مثبت بودن ADA (آنتیداروی آنتیبادی) در برولوسیزوماب ۳۵-۵۲٪ است (در مقابل کمتر از ۵٪ در رانیبیزوماب و آفلیبرسپت) و تصور میشود که به دلیل واکنش حساسیت نوع III ناشی از رسوب کمپلکسهای ایمنی باشد. 10)
اسکلریت (اولین گزارش جهانی): اسکلریت خلفی پس از تزریق برولوسیزوماب در ۳ بیمار ژاپنی گزارش شده است که با افزایش فشار داخل چشم به ۲۴-۴۹ میلیمتر جیوه همراه بود و در یک مورد به انسداد شریان شبکیه و واسکولیت پیشرفت کرد. 9)
درمان: تزریق زیر ملتحمه یا زیر تونک تریامسینولون استونید (STTA) ۵-۲۰ میلیگرم مؤثر است. ترکیب با تجویز پیشگیرانه STTA نیز گزارش شده است. 18, 19)
IOI مرتبط با فاریسیماب
Section titled “IOI مرتبط با فاریسیماب”میزان بروز IOI در nAMD ۲.۰٪، DME ۱.۳٪ و RVO ۱.۴٪ است و در موارد تزریق دوطرفه ۸.۵٪ مشاهده شده است. 8) در مطالعات پس از عرضه، واسکولیت شبکیه با فراوانی ۰.۱۷/۱۰,۰۰۰ تزریق نادر است، اما واسکولیت انسدادی هموراژیک شبکیه (HORV) میتواند پیامد شدیدی داشته باشد. 8) از نظر پاتولوژیک، ارتباط HOLV با واکنش حساسیت نوع IV (تأخیری) مطرح شده است. 16)
پارگی RPE در گروه فاریسیماب در TENAYA ۲.۷٪ و LUCERNE ۳.۰٪ رخ داده است و ارتفاع PED بیش از ۵۵۰ میکرومتر یک عامل خطر است. 17)
سندرم کرانچ (جداشدگی تراکشنال شبکیه)
Section titled “سندرم کرانچ (جداشدگی تراکشنال شبکیه)”در بیماران ROP، پس از درمان ضد VEGF، غشای فیبروواسکولار به سرعت منقبض شده و باعث جداشدگی تراکشنال شبکیه (TRD) میشود که به آن سندرم کرانچ میگویند. 3) در صورت وجود تکثیر فیبروزی گسترده، درمان با ضد VEGF به تنهایی منع مصرف دارد و ویترکتومی لازم است. معاینه زودهنگام فوندوس پس از تزریق برای بررسی تغییرات بافت پرولیفراتیو مهم است.
عوارض مکانیکی ناشی از سوزن
Section titled “عوارض مکانیکی ناشی از سوزن”- آسیب عدسی: پیشرفت آب مروارید. با رعایت فاصله نفوذ (۴ میلیمتر در چشمهای دارای عدسی) قابل پیشگیری است.
- آسیب شبکیه: جداشدگی رگماتوژن شبکیه. با استفاده صحیح از سوزن کوتاه ۳۰G قابل پیشگیری است.
- آسیب جسم مژگانی: خونریزی زجاجیه. با رعایت موقعیت و جهت تزریق قابل پیشگیری است.
افزایش فشار داخل چشم
Section titled “افزایش فشار داخل چشم”افزایش گذرای فشار داخل چشم بلافاصله پس از تزریق در تمام بیماران رخ میدهد. با تزریق 0.05 میلیلیتر، فشار داخل چشم بلافاصله به 50 میلیمتر جیوه افزایش مییابد، اما معمولاً برگشتپذیر است. در صورت سابقه گلوکوم، باید به افزایش پایدار فشار داخل چشم توجه کرد و در صورت لزوم با پاراسنتز اتاق قدامی فشار را کاهش داد.
رویدادهای ترومبوآمبولیک شریانی (ATE)
Section titled “رویدادهای ترومبوآمبولیک شریانی (ATE)”از نظر تئوری خطر سکته مغزی و انفارکتوس میوکارد وجود دارد. در مطالعه HAWK بر روی برولوسیزوماب، ATE در 1.1 تا 1.4٪ موارد مشاهده شد. 10) در بیماران با سابقه قبلی، تجویز با احتیاط ضروری است.
در صورت بروز علائم زیر، سریعاً به چشمپزشک مراجعه کنید: ① کاهش ناگهانی بینایی، ② تشدید درد و قرمزی چشم، ③ افزایش قابل توجه مگسپران، ④ ظهور ترشحات. این موارد ممکن است نشانه اندوفتالمیت عفونی یا التهاب داخل چشمی (IOI) باشند. به ویژه 24 تا 72 ساعت پس از تزریق نیاز به احتیاط است.
در صورت کاهش ناگهانی بینایی، بدتر شدن مگسپران، قرمزی و درد چشم، سریعاً به چشمپزشک مراجعه کنید. پس از تشخیص، تزریق زیر ملتحمه یا زیر تونک تریامسینولون استونید (STTA) مؤثر است و در بسیاری از موارد التهاب بهبود مییابد. 18, 19) تجویز مجدد باید پس از تأیید فروکش التهاب با LFP (لیزر فلر سل فوتومتر) و با احتیاط تصمیمگیری شود. در صورت همراهی با انسداد عروقی شدید، تجویز مجدد ممکن است منع شود، بنابراین تغییر به داروی جایگزین را در نظر بگیرید.
6. پاتوفیزیولوژی (نقش VEGF و مکانیسم اثر دارو)
Section titled “6. پاتوفیزیولوژی (نقش VEGF و مکانیسم اثر دارو)”نقش پاتولوژیک VEGF
Section titled “نقش پاتولوژیک VEGF”VEGF به VEGFR-1 و VEGFR-2 روی سلولهای اندوتلیال عروقی متصل شده و تکثیر سلولهای اندوتلیال، افزایش نفوذپذیری عروق و تشکیل عروق جدید را تحریک میکند.
- AMD: تکثیر عروق جدید مشیمیه (CNV) و افزایش نفوذپذیری عروق
- DME: تخریب سد خونی-شبکیه (BRB) → تشکیل ادم ماکولا
- RVO: ایسکمی → VEGF اضافی → ادم ماکولا و عروق جدید
با تزریق داخل زجاجیه، سطح VEGF کاهش یافته، نفوذپذیری عروق کم شده و ادم ماکولا بهبود مییابد. اثر داروهای ضد VEGF موقتی است، بنابراین نیاز به تزریق مجدد منظم وجود دارد.
ویژگیهای مولکولی هر دارو
Section titled “ویژگیهای مولکولی هر دارو”| دارو | وزن مولکولی | تمایل به VEGF-A (Kd) | هدف |
|---|---|---|---|
| برولوسیزوماب | 26 کیلودالتون | 28.4 پیکومولار | VEGF-A (همه ایزوفرمها) |
| رانیبیزوماب | 48 کیلودالتون | 20.6 پیکومولار | VEGF-A (همه ایزوفرمها) |
| آفلیبرسپت | 115 کیلودالتون | 0.49 پیکومولار (بالاترین) | VEGF-A/B و PlGF |
| بوسیزماب | 148 کیلودالتون | 35.1 پیکومولار | VEGF-A |
| فاریسیماب | 149 کیلودالتون | — | VEGF-A + Ang-2 |
عمل Ang-2 و فاریسیماب
Section titled “عمل Ang-2 و فاریسیماب”Ang-2 به عنوان آنتاگونیست گیرنده Tie-2 در بیثباتی عروقی نقش دارد. فاریسیماب با مهار Ang-2 مسیر Tie-2 را نرمال میکند، پایداری عروق را بهبود میبخشد و حساسیت به VEGF را کاهش میدهد. این اثر مهار دوگانه، مبنای فارماکولوژیکی برای افزایش فاصله تزریق است.
اهمیت تزریق متمرکز در فاز القایی
Section titled “اهمیت تزریق متمرکز در فاز القایی”دلیل تجویز 3 تا 5 تزریق ماهانه ثابت در فاز القایی، سرکوب قوی و زودهنگام فعالیت بیماری است. در روش T&E، چارچوبی فراهم میشود که تا زمانی که غلظت دارو در زجاجیه در محدوده درمانی باقی میماند، از عود جلوگیری کند.
7. تحقیقات جدید و چشمانداز آینده (گزارشهای مرحله تحقیقاتی)
Section titled “7. تحقیقات جدید و چشمانداز آینده (گزارشهای مرحله تحقیقاتی)”سیستم تحویل پورت (Susvimo)
Section titled “سیستم تحویل پورت (Susvimo)”در سیستم تحویل پورت (PDS) رانیبیزوماب، با تزریق تقویتی هر ۶ ماه، ۹۸٪ از بیماران نیازی به تزریق ماهانه نداشتند. 12) در سال ۲۰۲۵، افزودن اندیکاسیون برای DME بررسی میشود. 13) انتظار میرود بار تزریق به طور قابل توجهی کاهش یابد.
آفلیبرسپت با دوز بالا ۸ میلیگرم (Eylea® HD)
Section titled “آفلیبرسپت با دوز بالا ۸ میلیگرم (Eylea® HD)”در مطالعه PULSAR (AMD)، در هفته ۴۸، ۷۹٪ فاصله ۱۲ هفته و ۷۷٪ فاصله ۱۶ هفته را حفظ کردند. 12) در مطالعه PHOTON (DME)، ۹۳٪ به فاصله ۱۲ هفته یا بیشتر دست یافتند. 13)
مطالعه گسترش اندیکاسیون برولوسیزوماب
Section titled “مطالعه گسترش اندیکاسیون برولوسیزوماب”مطالعه PROUD (کره) که بر روی PCV و نوع ۱ تلانژکتازی ماکولار (AT1) متمرکز است، در حال انجام است و انتظار میرود شواهدی برای بیماریهای خاص آسیا جمعآوری شود. 14)
مطالعه فاریسیماب در PCV (مطالعه SALWEEN)
Section titled “مطالعه فاریسیماب در PCV (مطالعه SALWEEN)”مطالعه SALWEEN که اثر فاریسیماب را در بیماران PCV بررسی میکند، در حال انجام است. 20) سطوح بالای Ang-2 در زلالیه بیماران PCV تأیید شده است و انتظار میرود مهار Ang-2 اثر افزایشی داشته باشد.
پیشگیری از IOI با ترکیب STTA
Section titled “پیشگیری از IOI با ترکیب STTA”تجویز همزمان تریامسینولون استونید زیر ملتحمه و زیر تونون (STTA) با برولوسیزوماب ممکن است هم در پیشگیری از IOI و هم در کنترل تراوش مؤثر باشد. 18, 19) تحقیقات برای استانداردسازی دوز و زمانبندی بهینه در حال انجام است.
تشخیص زودهنگام با نشانگرهای زیستی
Section titled “تشخیص زودهنگام با نشانگرهای زیستی”برای تشخیص زودهنگام اندوفتالمیت غیرعفونی از عفونی، اندازهگیری پروفایل سیتوکینها (IL-6، IL-8، IL-10) در زجاجیه به عنوان یک ابزار کمکی امیدوارکننده است. 7)
زیستمشابهها
Section titled “زیستمشابهها”زیستمشابههای رانیبیزوماب و بواسیزوماب در حال ظهور هستند. انتظار میرود کاهش قابل توجه هزینه منجر به بهبود نرخ ادامه درمان و دسترسی به مراقبت شود. 12)
8. منابع
Section titled “8. منابع”- 日本眼科学会. 新生血管型加齢黄斑変性の診療ガイドライン. 日眼会誌. 2024.
- 日本眼科学会. 糖尿病網膜症診療ガイドライン(第1版). 日眼会誌. 2023.
- 日本未熟児網膜症研究会. 未熟児網膜症に対する抗VEGF療法の手引き(第2版). 2024.
- 日本眼科学会. 近視性黄斑部新生血管の診療ガイドライン. 日眼会誌. 2023.
- American Academy of Ophthalmology. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024. [Protocol S data]
- American Academy of Ophthalmology. Retinal Vein Occlusion Preferred Practice Pattern. Ophthalmology. 2024. [BRAVO data]
- Kudasiewicz-Kardaszewska A, Ozimek MA, Kardaszewska A, et al. Complete and Early Vitrectomy for Sterile Endophthalmitis After Bevacizumab: A Case Series. Cureus. 2025;17(10):e93996. doi:10.7759/cureus.93996.
- Tadayoni R, Paris LP, Danzig CJ, et al. Efficacy and safety of faricimab for macular edema due to retinal vein occlusion: 24-week results from the BALATON and COMINO trials. Ophthalmology. 2024;131(8):950-960.
- Takayama T, et al. Scleritis following intravitreal brolucizumab injection: a case series. J Med Case Rep. 2024;18:80.
- Sharma A, et al. Understanding retinal vasculitis associated with brolucizumab. Ocul Immunol Inflamm. 2022;30(6):1508-1510.
- Nawar AE, Abdelrahman AM, Ebeid OM, Ahmed SM, El-Abhar AE. Subthreshold micropulse laser combined with ranibizumab versus ranibizumab monotherapy in branch retinal vein occlusion with macular edema. Clin Ophthalmol. 2022;16:1139-1151. doi:10.2147/OPTH.S355315. PMID:35386091. PMCID:PMC8968960
- Flaxel CJ, Adelman RA, Bailey ST, et al. Age-related macular degeneration preferred practice pattern. Ophthalmology. 2024;131(1):P1-P68.
- Flaxel CJ, Adelman RA, Bailey ST, et al. Diabetic retinopathy preferred practice pattern. Ophthalmology. 2024;131(1):P99-P168.
- Sen P, et al. Polypoidal choroidal vasculopathy: update on diagnosis and treatment. Clin Ophthalmol. 2023;17:53-70.
- Bloom J, Madani R, Haidar AJ, Alasil T. Faricimab treatment of polypoidal choroidal vasculopathy resistant to intravitreal ranibizumab. J VitreoRetin Dis. 2024;8(6):731-734.
- Yavari N, Gupta AS, Mitsios A, et al. Bilateral hemorrhagic occlusive retinal vasculitis and panuveitis following intravitreal faricimab injection. Am J Ophthalmol Case Rep. 2026;41:102532.
- Clemens CR, Alten F, Zimmermann JA, Eter N. Old problem in a new guise: retinal pigment epithelium tear after intravitreal faricimab injection. Case Rep Ophthalmol. 2023;14:241-244.
- Shigemoto Y, et al. Combination therapy of STTA and IVbr for brolucizumab-related IOI. Medicine. 2021;100(42):e27580.
- Saito M, et al. IOI after IVbr monitored by laser flare-cell photometer. Am J Ophthalmol Case Rep. 2022;28:101727.
- Cheung CMG, Lai TYY, Teo K, et al. Polypoidal choroidal vasculopathy: consensus nomenclature and non-indocyanine green angiograph diagnostic criteria. Eye. 2024;39:819-834.
- American Academy of Ophthalmology. Similar visual outcomes are seen with two post-injection endophthalmitis treatments. AAO Editors’ Choice. 2024 Oct 8. Available from: https://www.aao.org/education/editors-choice/similar-visual-outcomes-are-seen-with-two-post-inj
