雷珠單抗(樂舒晴®)

玻璃體注射(抗VEGF療法)
一目瞭然的要點
Section titled “一目瞭然的要點”1. 什麼是玻璃體注射(抗VEGF療法)?
Section titled “1. 什麼是玻璃體注射(抗VEGF療法)?”抗VEGF藥物的玻璃體內注射是通過將藥液直接注入玻璃體腔,抑制VEGF的作用(新生血管形成和血管通透性增加)的治療方法。主要適應症包括年齡相關性黃斑部病變、糖尿病性黃斑水腫和視網膜靜脈阻塞等視網膜血管疾病。
抗VEGF療法在2000年代迅速進入臨床應用。
| 年份 | 事件 |
|---|---|
| 2004年 | 貝伐珠單抗的眼內給藥開始探索性應用 |
| 2006年 | 雷珠單抗獲得FDA批准(MARINA/ANCHOR試驗)12) |
| 2011年 | 阿柏西普獲得FDA批准(VIEW試驗)12) |
| 2019年 | 布羅魯珠單抗獲得FDA批准(HAWK/HARRIER試驗)10) |
| 2022年 | 法瑞西單抗獲得FDA批准(TENAYA/LUCERNE/YOSEMITE/RHINE試驗)8) |
- 滲出型老年性黃斑部病變(nAMD):脈絡膜新生血管(CNV)的第一線治療
- 糖尿病黃斑部水腫(DME):糖尿病視網膜病變伴隨的黃斑部水腫
- 視網膜靜脈阻塞(RVO):視網膜中央或分枝靜脈阻塞引起的黃斑部水腫6)
- 增殖性糖尿病視網膜病變(PDR):PRP的輔助或替代治療(ranibizumab)5)
- 病理性近視併發脈絡膜新生血管(mCNV):aflibercept、ranibizumab4)
- 息肉狀脈絡膜血管病變(PCV):brolucizumab的息肉消退率較高14)
- 早產兒視網膜病變(ROP):ranibizumab 0.2 mg(2019年核准)、aflibercept 0.4 mg(2022年9月核准)。兩者均為成人劑量的20%~40%的低劑量製劑。3)
- 地圖狀萎縮(GA):補體抑制劑
- 眼內炎:直接給予抗生素、抗真菌藥或抗病毒藥
- 眼內惡性淋巴瘤:methotrexate
老年性黃斑部病變、糖尿病黃斑部水腫和視網膜靜脈阻塞是三大主要適應症。這些疾病中,VEGF過度產生,導致新生血管形成和血管通透性增加,進而引起黃斑部視力下降。透過直接注射抗VEGF藥物至玻璃體內,可以抑制這些病理過程,從而改善或維持視力。近年來,適應症已擴展到PDR、mCNV、ROP和息肉狀脈絡膜血管病變等。
2. 可用的抗VEGF藥物(各論)
Section titled “2. 可用的抗VEGF藥物(各論)”藥物比較(一覽)
Section titled “藥物比較(一覽)”| 藥物名稱 | 商品名 | 分子量 | 作用機轉 | 劑量 | 核准(日本) |
|---|---|---|---|---|---|
| 雷珠單抗 | 樂舒晴® | 48 kDa | VEGF-A Fab片段 | 0.5 mg(AMD/RVO),0.3 mg(DME) | 2009年 |
| 阿柏西普 | 采視明® | 115 kDa | VEGF-A/B和PlGF抑制(誘餌受體) | 2 mg / 8 mg(HD) | 2012年 |
| 培加他尼 | Macugen® | — | VEGF165適體 | 0.3 mg | 2008年 |
| 布羅魯珠單抗 | Beovu® | 26 kDa | VEGF-A scFv | 6 mg | 2020年 |
| 法瑞西單抗 | Vabysmo® | 149 kDa | VEGF-A + Ang-2雙特異性抗體 | 6 mg | 2023年 |
| 貝伐珠單抗 | 癌思停® | 148 kDa | VEGF-A 全長IgG | 1.25 mg | —(仿單標示外使用) |
阿柏西普(采視明®)
分子量:115 kDa(融合蛋白)
作用機轉:同時抑制VEGF-A、VEGF-B和PlGF。VEGF-A親和力Kd=0.49 pM,最高。
主要試驗:VIEW試驗顯示非劣效於雷珠單抗。高劑量8 mg(HD)可延長至16週間隔。12, 13)
特點:廣泛的VEGF抑制譜。在DME中,Protocol T試驗顯示1年視力改善最大。13)
布羅魯珠單抗(Beovu®)
分子量:26 kDa(scFv,現有藥物中最小)
作用機轉:scFv結構,給藥莫耳濃度約為阿柏西普的12倍。組織滲透性高。
主要試驗:HAWK/HARRIER試驗達到非劣效性。高達55%的患者維持12週間隔。10)
注意事項:IOI發生率4.4%(HAWK/HARRIER),日本人15-20%。視網膜血管炎和血管阻塞風險。10)
法瑞西單抗(Vabysmo®)
貝伐珠單抗(Avastin®)
分子量:148 kDa(全長IgG)
作用機轉:抑制VEGF-A(眼科適應症外使用)
主要試驗:CATT試驗證實與雷珠單抗療效相當。12)
使用情況:成本大幅降低。無菌分裝靜脈滴注製劑後使用。
培加他尼(Macugen®)
作用機制:VEGF165特異性適體
現狀:2008年核准的第一代藥物。目前新一代藥物為主流。為早期抗VEGF治療概念的建立做出了貢獻。
在眼科領域屬於仿單標示外使用,無菌製備靜脈滴注製劑用於眼科。CATT試驗證實其與雷珠單抗具有同等的視力改善效果,且成本大幅降低,因此在全球廣泛使用。但在日本沒有保險給付,使用取決於醫療機構。
3. 適應症和給藥方案
Section titled “3. 適應症和給藥方案”抗VEGF藥物的給藥分為誘導期和維持期兩個階段。
- 誘導期:為強力抑制疾病活動性,每月固定給藥3至6次(因疾病和藥物而異)。
- 維持期有以下三種方式:
- PRN(按需治療):每月就診,僅在出現復發跡象時給藥
- 固定給藥:每2個月或每3個月等固定間隔定期給藥
- 治療並延長(T&E):若無活動性跡象,則每2週延長一次間隔;復發時縮短間隔。
Ranibizumab 建議的基本給藥方式為導入期每月1次共3次,之後維持期採 PRN 給藥;Aflibercept 建議導入期每月1次共3次,之後每2個月固定給藥或採治療並延長(T&E)方案。近年來,許多機構已導入 T&E 方案。
依疾病建議之方案
Section titled “依疾病建議之方案”| 適應症 | 建議藥物 | 導入期 | 維持期 |
|---|---|---|---|
| nAMD(ranibizumab) | Lucentis® 0.5 mg | 每月1次×3次1) | PRN(每月監測) |
| nAMD(aflibercept) | Eylea® 2 mg | 每月1次×3次1) | 每2個月固定或T&E(最長3個月) |
| nAMD(brolucizumab) | Beovu® 6 mg | 每月1次×3次 | 每8~12週10) |
| nAMD(法瑞西單抗) | Vabysmo® 6 mg | 每4週1次×4次 | 每8週至每16週8) |
| DME(阿柏西普) | Eylea® 2 mg | 每月1次×5次2) | 每2個月 |
| DME(雷珠單抗) | Lucentis® 0.5 mg | 每月1次×3次2) | PRN |
| DME(法瑞西單抗) | Vabysmo® 6 mg | 每4週1次×4至6次 | PTI(最長每16週)8, 13) |
| RVO | 阿柏西普/法瑞西單抗 | Q4W×6個月 | PTI(最長Q16W)8) |
| PDR | 雷珠單抗 0.3 mg | — | 非劣效於PRP 5) |
| mCNV | 阿柏西普/雷珠單抗 | 初始1~3次 | PRN(可能單次緩解)4) |
| ROP(雷珠單抗) | 諾適得® 0.2 mg | 初始劑量 | 復發時追加(間隔≥1個月)3) |
| ROP(阿柏西普) | 艾力雅® 0.4 mg | 初次 | 復發時追加(間隔1個月以上)3) |
PCV(息肉狀脈絡膜血管病變)的處理:布羅珠單抗的息肉消退率約79%,優於其他藥物,76%的患者維持12週間隔(48週)。14) 法瑞西單抗在雷珠單抗抗藥性PCV病例中也有效。15)
BALATON試驗(BRVO,n=553):法瑞西單抗6.0 mg vs 阿柏西普2.0 mg Q4W,24週BCVA變化分別為+16.9個字母和+17.5個字母(達到非劣效性)。FA滲漏消失率法瑞西單抗33.6% vs 阿柏西普21.0%(名義p=0.0023),法瑞西單抗顯著較優。8)
COMINO試驗(CRVO/HRVO,n=729):相同方案,24週BCVA變化分別為+16.9個字母和+17.3個字母(達到非劣效性)。CST變化−461.6 μm vs −448.8 μm。FA滲漏消失率法瑞西單抗44.4% vs 阿柏西普30.0%(名義p=0.0002),顯著較優,顯示了Ang-2抑制的血管穩定作用。8)
STTA聯合治療(RVO):雷珠單抗聯合脈絡膜上腔曲安奈德4 mg與雷珠單抗單藥相比,顯著減少注射次數(4.4次→2.47次,p<0.001)。11)
3-8. 早產兒視網膜病變(ROP)的抗VEGF治療
Section titled “3-8. 早產兒視網膜病變(ROP)的抗VEGF治療”截至2022年12月,ROP治療中獲批的抗VEGF藥物有以下兩種:3)
- 雷珠單抗(諾適得®)0.2 mg/0.02 mL:成人劑量的40%。2019年獲批。
- 阿柏西普(艾力雅®)0.4 mg/0.01 mL:成人劑量的20%。2022年9月獲批。
- 再次給藥應間隔1個月以上(藥品說明書規定)。
治療適應症(基於ETROP研究標準) 3):
復發率與追蹤觀察 3):
阿柏西普的復發率為13.9%~28%(平均復發時間11~14.2週),雷珠單抗為20.8%~83.0%(復發時間5.9~9.3週,較早)。使用雷珠單抗時,需從注射後早期開始仔細觀察。若視網膜血管未延伸至Zone III,建議注射後17週內每週進行一次眼底檢查。
A-ROP的注意事項 3):
在A-ROP中,抗VEGF單一治療需要額外治療的比例為75.0%~87.5%。注射後1~3週內可能出現早期復發,若纖維增殖廣泛,則抗VEGF單一治療不適用(收縮導致牽引性視網膜剝離的風險)。
ROP的注射技術(與成人的不同點) 3):
- 進針位置:角膜緣後1.0~1.5 mm(與成人的3.5~4 mm有很大不同)。
- 針頭方向:向下進針(因為水晶體相對較大,朝向中央有穿透水晶體的風險)。
- 使用30G或更細的針頭。
- 確認劑量:雷珠單抗0.02 mL,阿柏西普0.01 mL(仔細確認以防止過量給藥)。
Protocol T試驗顯示,1年時阿柏西普的視力改善最大。但在輕度組(BCVA ≥20/40)中,三種藥物之間無統計學顯著差異。13) 法瑞西單抗在YOSEMITE/RHINE試驗中顯示出與阿柏西普相當的視力改善,同時維持期注射間隔可進一步延長(第2年Q16W達成率60%~64%)。8) 應根據患者背景和就診頻率意願選擇藥物。
4. 玻璃體內注射技術
Section titled “4. 玻璃體內注射技術”- 防止病人、患眼、藥物混淆:決定注射後,確認病人識別標籤。
- 確認碘過敏:務必事先確認。
- 準備必要物品:
- 皮膚消毒用10%聚維酮碘
- 麻醉眼藥水、稀釋並回溫至室溫的PA碘眼藥水、抗菌眼藥水(必要時)
- 紗布、棉棒、附膠帶的有孔手術巾
- 開瞼器、卡尺、顯微有齒鑷
- 注射針、注射液(使用藥瓶時:1 mL注射器與附過濾器的抽液針)
消毒與麻醉步驟
Section titled “消毒與麻醉步驟”麻醉:考量消毒藥可能飛濺至對側眼,先雙眼滴用貝諾克西爾®眼藥水,再對治療眼滴用4%賽洛卡因®眼藥水兩次。
PA碘消毒注意事項:
- 剛從冰箱取出的PA碘抗菌及抗真菌滅活效果降低,務必回溫至室溫。
- 在非密閉容器中於25°C保存時,有效成分殘留率在5小時內降至60%。請勿使用放置過久的PA碘。
- 滅活細菌和真菌需要約1分鐘的接觸時間,因此沖洗後應保持閉眼,確保與結膜有足夠的接觸時間。
口腔細菌控制:使用有孔手術巾,術者、助手及患者均配戴口罩以防止飛沫傳播。
穿刺位置與針頭方向
Section titled “穿刺位置與針頭方向”從外科角膜緣開始的穿刺距離如下。保持正確的穿刺位置可確保在睫狀體平坦部(睫狀體皺褶部後方)穿刺,從而避免水晶體損傷和玻璃體出血。
| 眼部狀態 | 距角膜緣的距離 |
|---|---|
| 有水晶體眼 | 4 mm(睫狀體平坦部) |
| 無水晶體眼或人工水晶體植入眼 | 3.5 mm |
| 早產兒 | 1.0~1.5 mm |
針頭朝向玻璃體腔中心穿刺。在靠近角膜緣的位置穿刺可能損傷睫狀體皺褶部,易導致玻璃體出血,且因與水晶體距離較近,水晶體損傷風險增加。
注射技術與術後管理
Section titled “注射技術與術後管理”- 貼上有孔手術巾,用開瞼器撐開眼瞼。
- 用卡尺測量距角膜緣的穿刺距離。
- 注射部位應選擇顳上或顳下象限(以防止損傷水平直肌)。
- 用鑷子固定眼球,注射前將結膜稍向前推移,使拔針後的針孔錯位,防止液體滲漏。
- 將30G短針幾乎垂直刺入鞏膜,緩慢注入藥液(快速注射可能導致持續性眼壓升高)。
- 拔針後,用棉籤壓迫注射部位。
- 術後立即檢查視力(數指)。如果無法識別數指,則進行前房穿刺。
- 術後繼續使用廣譜抗生素眼藥水3天。
由於在點眼麻醉(貝諾西爾®、4%利多卡因®)後進行,注射中的疼痛很輕微。您可能會感到消毒劑(PA碘)的刺激感,但術後早期的不適可使用玻尿酸鈉眼藥水緩解。
5. 併發症與對策
Section titled “5. 併發症與對策”感染性眼內炎(最重要的併發症)
Section titled “感染性眼內炎(最重要的併發症)”感染性眼內炎是最嚴重的併發症,發生率約為0.027%~0.065%。一旦發生,需要緊急進行玻璃體內注射萬古黴素1.0 mg + 頭孢他啶2.0 mg治療。
最重要的預防措施:
- 聚維酮碘的適當消毒(恢復至室溫,接觸時間至少1分鐘)
- 使用有孔手術巾(防止口腔細菌飛沫污染)
關於術後預防性抗生素眼藥水,多項研究表明其不能降低眼內炎的發生率,有效性的證據不一致。
無菌性眼內炎
Section titled “無菌性眼內炎”這是一種無細菌感染的眼內炎症反應,發生率因藥物而異,為0.005%~4.4%。7)
- 發病時間:通常在注射後24~48小時內(感染性眼內炎發生在2~7天後)7)
- 主要表現:玻璃體混濁(約80%)、前房蓄膿(約5%)7)
- 確診:培養陰性(PCR排除病原體也有用)
- 不同藥物的發生率(‰):貝伐珠單抗3.64 / 雷珠單抗1.39 / 阿柏西普0.76 7)
- 治療:輕症保守治療(類固醇眼藥水、結膜下注射)。CEVE方案(立即完全玻璃體切除術)報告平均17.8天視力恢復。7)
在IRIS註冊研究的匹配隊列分析中,僅注射管理與早期玻璃體切除術的視力結果無顯著差異。21)
眼內炎症(IOI)/ 視網膜血管炎(布羅魯珠單抗特異性)
Section titled “眼內炎症(IOI)/ 視網膜血管炎(布羅魯珠單抗特異性)”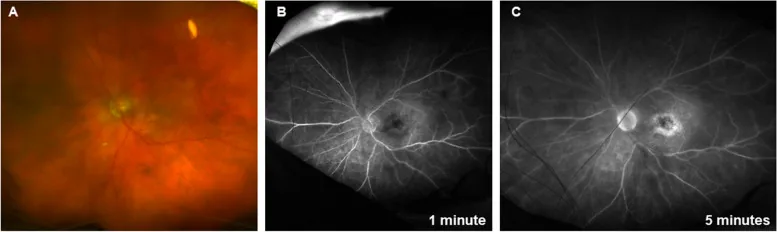
布羅魯珠單抗比其他抗VEGF藥物更容易引起眼內炎症(IOI)。
| 試驗/族群 | IOI發生率 | 備註 |
|---|---|---|
| HAWK/HARRIER(整體IOI) | 4.4% | 視網膜血管炎3.6%,血管閉塞2.1%10) |
| KESTREL(6mg) | 3.7%(對照組0.5%) | DME試驗10) |
| MERLIN(4週間隔) | 9.3% | 試驗中斷10) |
| 日本病例 | 15~20% | 10) |
| 上市後(血管炎+閉塞複合) | 3.73/10,000次注射 |
大多數IOI發生在首次給藥後6個月內、4次注射以內。10)
機轉:brolucizumab的ADA(抗藥物抗體)陽性率高達35-52%(與ranibizumab和aflibercept的<5%形成對比),被認為是免疫複合物沉積引起的III型過敏反應。10)
鞏膜炎(全球首報):日本有3例患者在brolucizumab注射後出現後鞏膜炎,伴隨眼壓升高至24-49 mmHg,其中1例進展為視網膜動脈阻塞和血管炎。9)
治療:結膜下或Tenon囊下注射triamcinolone acetonide(STTA)5-20 mg有效。也有與預防性STTA合併使用的報告。18, 19)
Faricimab相關IOI
Section titled “Faricimab相關IOI”IOI發生率在nAMD為2.0%,DME為1.3%,RVO為1.4%,雙眼注射病例中為8.5%。8) 上市後監測中視網膜血管炎發生率為0.17/10,000次注射,但出血性阻塞性視網膜血管炎(HORV)可能導致嚴重後果。8) 病理學提示HORV與IV型(遲發型)過敏反應相關。16)
Faricimab組中RPE裂孔發生率在TENAYA試驗為2.7%,LUCERNE試驗為3.0%,PED高度>550 μm是危險因子。17)
Crunch症候群(牽引性視網膜剝離)
Section titled “Crunch症候群(牽引性視網膜剝離)”在ROP患者中,抗VEGF治療後纖維血管膜迅速收縮,導致牽引性視網膜剝離(TRD),這種併發症稱為crunch症候群。3) 當存在廣泛纖維增殖時,抗VEGF單一治療為禁忌,需要玻璃體切除術。給藥後早期眼底檢查觀察增殖組織的變化非常重要。
針頭相關機械性併發症
Section titled “針頭相關機械性併發症”注射後立即出現的一過性眼壓升高在所有接受注射的患者中都會發生。注入0.05 mL後眼壓會立即升至50 mmHg,但通常是可逆的。有青光眼病史的患者需注意持續性眼壓升高,必要時可透過前房穿刺減壓。
動脈血栓栓塞事件(ATE)
Section titled “動脈血栓栓塞事件(ATE)”理論上存在腦中風和心肌梗塞的風險。在brolucizumab的HAWK試驗中,ATE發生率為1.1-1.4%。10) 有既往史的患者需謹慎用藥。
6. 病理生理(VEGF的作用與藥物作用機制)
Section titled “6. 病理生理(VEGF的作用與藥物作用機制)”VEGF的病理作用
Section titled “VEGF的病理作用”VEGF與血管內皮細胞上的VEGFR-1和VEGFR-2結合,促進內皮細胞增殖、血管通透性增加和新生血管形成。
玻璃體內注射後VEGF水平降低,血管通透性降低,黃斑水腫改善。抗VEGF藥物的效果是暫時的,因此需要定期重複給藥。
各藥物的分子特徵
Section titled “各藥物的分子特徵”| 藥物 | 分子量 | VEGF-A親和力(Kd) | 標靶 |
|---|---|---|---|
| 布羅珠單抗 | 26 kDa | 28.4 pM | VEGF-A(所有亞型) |
| 雷珠單抗 | 48 kDa | 20.6 pM | VEGF-A(所有亞型) |
| 阿柏西普 | 115 kDa | 0.49 pM(最高) | VEGF-A/B、PlGF |
| 貝伐珠單抗 | 148 kDa | 35.1 pM | VEGF-A |
| 法瑞西單抗 | 149 kDa | — | VEGF-A + Ang-2 |
Ang-2與法瑞西單抗的作用
Section titled “Ang-2與法瑞西單抗的作用”Ang-2作為Tie-2受體的拮抗劑參與血管不穩定化。法瑞西單抗通過抑制Ang-2使Tie-2路徑正常化,提高血管穩定性並降低VEGF敏感性。這種雙重抑制效應是延長給藥間隔的藥理學基礎。
導入期集中給藥的意義
Section titled “導入期集中給藥的意義”導入期每月固定給藥3至5次的原因是為了早期強力抑制疾病活動性。治療-延長(T&E)法提供了一個框架,在維持玻璃體內藥物濃度在治療範圍內的情況下不允許復發。
7. 最新研究與未來展望(研究階段報告)
Section titled “7. 最新研究與未來展望(研究階段報告)”端口遞送系統(Susvimo)
Section titled “端口遞送系統(Susvimo)”Ranibizumab的PDS(端口遞送系統)每6個月補充給藥一次,98%的患者無需每月注射。12) 2025年正在考慮擴展適應症至DME。13) 預計可大幅減輕注射負擔。
高劑量Aflibercept 8 mg(Eylea® HD)
Section titled “高劑量Aflibercept 8 mg(Eylea® HD)”PULSAR試驗(AMD)中,48週時79%維持12週間隔,77%維持16週間隔。12) PHOTON試驗(DME)中,93%達到12週或更長間隔。13)
Brolucizumab適應症擴展試驗
Section titled “Brolucizumab適應症擴展試驗”針對PCV和黃斑部毛細血管擴張症1型(AT1)的PROUD試驗(韓國)正在進行中,預計將為亞洲特有疾病累積證據。14)
Faricimab PCV試驗(SALWEEN試驗)
Section titled “Faricimab PCV試驗(SALWEEN試驗)”評估Faricimab對PCV患者效果的SALWEEN試驗正在進行中。20) PCV患者房水中Ang-2水平升高已被確認,預計Ang-2抑制具有附加益處。
聯合STTA預防IOI
Section titled “聯合STTA預防IOI”結膜下/Tenon囊下Triamcinolone Acetonide(STTA)與Brolucizumab聯合給藥可能在預防IOI和控制滲出方面均有效。18, 19) 關於最佳劑量和給藥時機標準化的研究正在進行中。
利用生物標誌物進行早期鑑別
Section titled “利用生物標誌物進行早期鑑別”測量玻璃體液中細胞因子譜(IL-6、IL-8、IL-10)有望成為早期鑑別無菌性和感染性眼內炎的輔助工具。7)
Ranibizumab和Bevacizumab的生物相似藥正在出現。預計大幅降低成本將提高治療持續率和改善醫療可及性。12)
8. 參考文獻
Section titled “8. 參考文獻”- 日本眼科学会. 新生血管型加齢黄斑変性の診療ガイドライン. 日眼会誌. 2024.
- 日本眼科学会. 糖尿病網膜症診療ガイドライン(第1版). 日眼会誌. 2023.
- 日本未熟児網膜症研究会. 未熟児網膜症に対する抗VEGF療法の手引き(第2版). 2024.
- 日本眼科学会. 近視性黄斑部新生血管の診療ガイドライン. 日眼会誌. 2023.
- American Academy of Ophthalmology. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024. [Protocol S data]
- American Academy of Ophthalmology. Retinal Vein Occlusion Preferred Practice Pattern. Ophthalmology. 2024. [BRAVO data]
- Kudasiewicz-Kardaszewska A, Ozimek MA, Kardaszewska A, et al. Complete and Early Vitrectomy for Sterile Endophthalmitis After Bevacizumab: A Case Series. Cureus. 2025;17(10):e93996. doi:10.7759/cureus.93996.
- Tadayoni R, Paris LP, Danzig CJ, et al. Efficacy and safety of faricimab for macular edema due to retinal vein occlusion: 24-week results from the BALATON and COMINO trials. Ophthalmology. 2024;131(8):950-960.
- Takayama T, et al. Scleritis following intravitreal brolucizumab injection: a case series. J Med Case Rep. 2024;18:80.
- Sharma A, et al. Understanding retinal vasculitis associated with brolucizumab. Ocul Immunol Inflamm. 2022;30(6):1508-1510.
- Nawar AE, Abdelrahman AM, Ebeid OM, Ahmed SM, El-Abhar AE. Subthreshold micropulse laser combined with ranibizumab versus ranibizumab monotherapy in branch retinal vein occlusion with macular edema. Clin Ophthalmol. 2022;16:1139-1151. doi:10.2147/OPTH.S355315. PMID:35386091. PMCID:PMC8968960
- Flaxel CJ, Adelman RA, Bailey ST, et al. Age-related macular degeneration preferred practice pattern. Ophthalmology. 2024;131(1):P1-P68.
- Flaxel CJ, Adelman RA, Bailey ST, et al. Diabetic retinopathy preferred practice pattern. Ophthalmology. 2024;131(1):P99-P168.
- Sen P, et al. Polypoidal choroidal vasculopathy: update on diagnosis and treatment. Clin Ophthalmol. 2023;17:53-70.
- Bloom J, Madani R, Haidar AJ, Alasil T. Faricimab treatment of polypoidal choroidal vasculopathy resistant to intravitreal ranibizumab. J VitreoRetin Dis. 2024;8(6):731-734.
- Yavari N, Gupta AS, Mitsios A, et al. Bilateral hemorrhagic occlusive retinal vasculitis and panuveitis following intravitreal faricimab injection. Am J Ophthalmol Case Rep. 2026;41:102532.
- Clemens CR, Alten F, Zimmermann JA, Eter N. Old problem in a new guise: retinal pigment epithelium tear after intravitreal faricimab injection. Case Rep Ophthalmol. 2023;14:241-244.
- Shigemoto Y, et al. Combination therapy of STTA and IVbr for brolucizumab-related IOI. Medicine. 2021;100(42):e27580.
- Saito M, et al. IOI after IVbr monitored by laser flare-cell photometer. Am J Ophthalmol Case Rep. 2022;28:101727.
- Cheung CMG, Lai TYY, Teo K, et al. Polypoidal choroidal vasculopathy: consensus nomenclature and non-indocyanine green angiograph diagnostic criteria. Eye. 2024;39:819-834.
- American Academy of Ophthalmology. Similar visual outcomes are seen with two post-injection endophthalmitis treatments. AAO Editors’ Choice. 2024 Oct 8. Available from: https://www.aao.org/education/editors-choice/similar-visual-outcomes-are-seen-with-two-post-inj
