玻璃體混濁的特徵
帶狀和索狀模式:從後極向周邊呈放射狀擴散的獨特模式。
極光樣混濁:細胞密度高,動態觀察可見被形容為「極光樣」的玻璃體混濁。
大小不一的細胞:高密度淋巴瘤細胞大小不一地存在。
與視力保留的乖離:混濁程度與良好視力不匹配是懷疑本病的關鍵。

全身無淋巴瘤而眼內首發惡性淋巴瘤的情況稱為原發性眼內淋巴瘤(primary intraocular lymphoma; PIOL)。由於多數在視網膜和玻璃體形成病灶,最近也常稱為玻璃體視網膜淋巴瘤(vitreo-retinal lymphoma; VRL)。腫瘤性淋巴細胞浸潤眼內,呈現葡萄膜炎樣眼部表現,因此被認為是典型的偽裝症候群之一。許多病例合併中樞神經系統淋巴瘤(PCNSL),常導致致命性病程。
眼內原發淋巴瘤的組織學類型幾乎均為瀰漫性大B細胞淋巴瘤(diffuse large B-cell lymphoma; DLBCL)。其惡性程度極高,與眼附屬器常見的低度惡性MALT淋巴瘤在病理和預後上均有顯著差異。此外,眼科領域的惡性淋巴瘤多為非何杰金氏淋巴瘤,PIOL也屬於這一範疇。
當葡萄膜炎對類固醇治療(點眼或口服)反應不佳時,必須將眼內惡性淋巴瘤(PIOL)作為重要的鑑別診斷加以考慮。PIOL也被稱為「偽裝症候群」,其表現與炎性葡萄膜炎極為相似。此外,類固醇可能暫時溶解淋巴瘤細胞並改善症狀,導致後續活檢出現偽陰性結果。當玻璃體混濁嚴重但視力良好時,尤其要懷疑。必須檢測IL-10/IL-6比值並進行玻璃體活檢以確診。
眼內淋巴瘤根據發生部位分為4型。
| 類型 | 特徵 |
|---|---|
| 眼+中樞神經系統型 | 最常見(約佔全部病例的60%)。與PCNSL密切相關。 |
| 僅限眼內(狹義眼內淋巴瘤) | 局限型。孤立性PVRL。 |
| 眼+其他器官型 | 播散至CNS以外的器官。 |
| 眼+其他器官+CNS型 | 最廣泛的病變。 |
眼和中樞神經系統同時受累的類型最常見,約佔全部病例的60%。
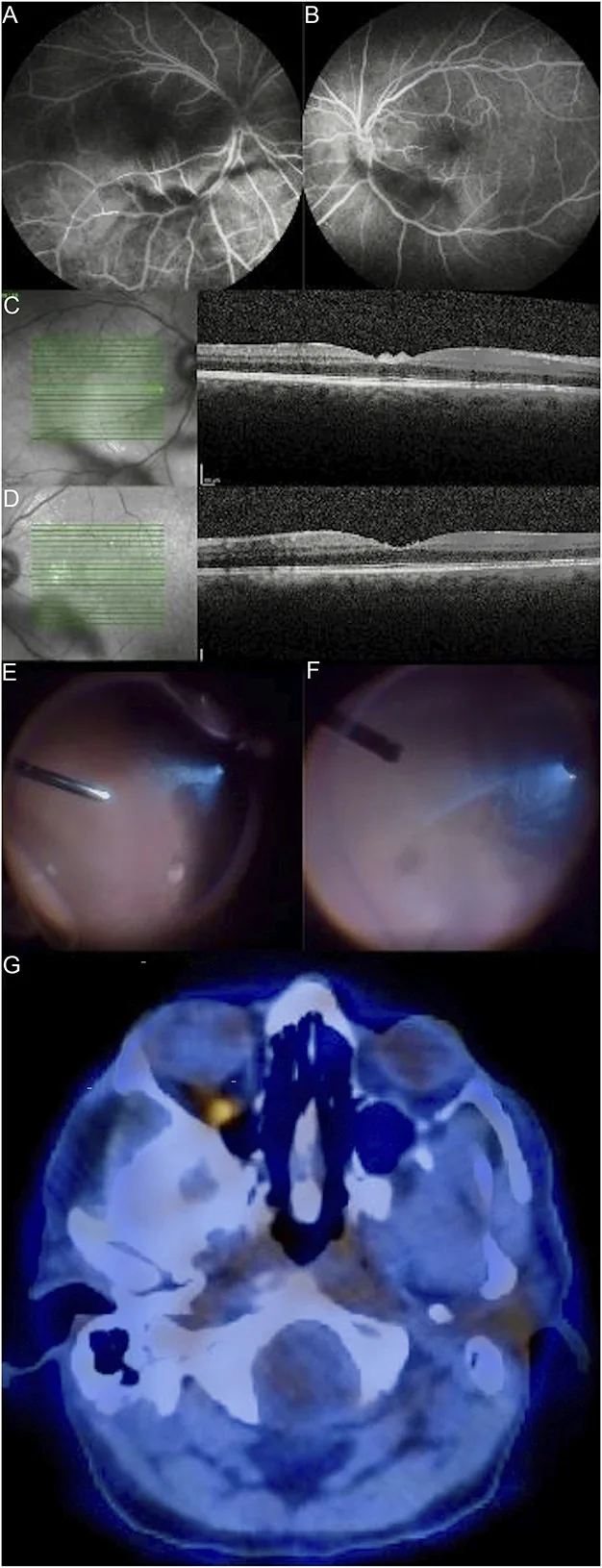
典型的自覺症狀如下所示。
視物模糊是最常見的自覺症狀。與玻璃體混濁程度不相稱的良好視力是懷疑本病的重要線索。
玻璃體混濁的特徵
帶狀和索狀模式:從後極向周邊呈放射狀擴散的獨特模式。
極光樣混濁:細胞密度高,動態觀察可見被形容為「極光樣」的玻璃體混濁。
大小不一的細胞:高密度淋巴瘤細胞大小不一地存在。
與視力保留的乖離:混濁程度與良好視力不匹配是懷疑本病的關鍵。
視網膜和RPE表現
黃白色斑狀病變:淋巴瘤細胞浸潤視網膜色素上皮(RPE)下和Bruch膜下,形成黃白色點狀至斑狀病變。
病灶融合擴大:小的點狀病灶融合並擴大為大型病灶。
視乳頭炎樣表現:腫瘤細胞浸潤視乳頭周圍的視網膜下間隙,可能引起視乳頭炎樣表現(罕見)。
白鞘形成:也可能出現類似視網膜血管炎的血管白鞘形成。
眼內復發時,角膜後沉著物(KP)的頻率有比初發時增加的趨勢,已有報導2)。
PIOL的確診需要進行類似玻璃體切除術的玻璃體切片檢查。利用採集的玻璃體液,結合細胞學檢查、IL-10/IL-6比值測定、PCR檢測IgH基因重排和流式細胞術進行診斷。單獨細胞學檢查陽性率僅約50%,但IL-10/IL-6比值>1(敏感性89.4%)、流式細胞術(敏感性88.0%)和PCR(敏感性85.1%)的組合是有用的1)。如果診斷前使用過類固醇,存在偽陰性風險,因此應盡可能停用類固醇後再進行切片檢查。
確診時的平均年齡為63歲,女性略多。在大學醫院的葡萄膜炎病例中,發生率約為1-2%。中樞神經系統淋巴瘤患者中15-20%出現眼部症狀。
在香港的10例患者(17隻眼)的病例系列中,中位年齡59歲,女性佔70%,雙側受累佔70%1)。上海一項51例的回顧性研究報告雙側受累佔78.4%2)。這表明該病多為雙側性,即使單眼發病,對側眼的檢查和追蹤也很重要。
從發病到確診常有延遲(由於偽裝症候群,平均12-18個月3))。免疫缺陷(如HIV感染)和免疫抑制狀態(如器官移植後、使用免疫抑制劑)被認為是危險因子。
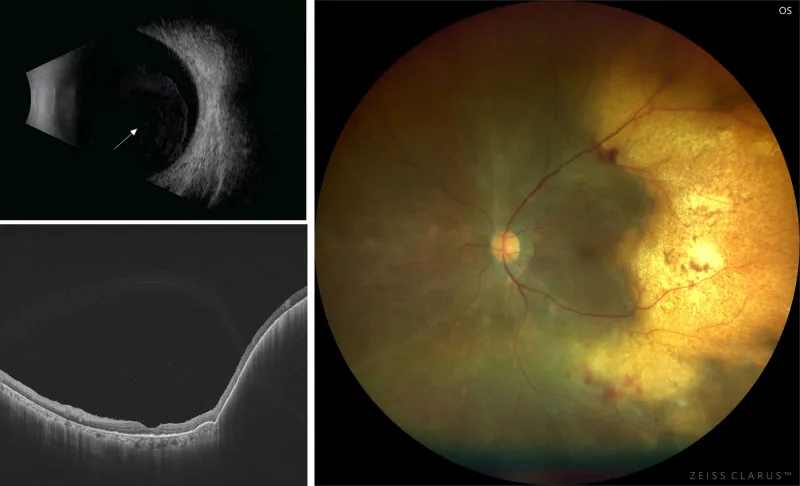
確診需要進行類似玻璃體切除術的玻璃體活檢。僅靠細胞學檢查不一定能確診,必須結合PCR檢測免疫球蛋白基因重排和細胞因子測定。
| 檢查方法 | 特點/靈敏度 | 臨床意義 |
|---|---|---|
| 細胞學檢查 | 陽性率50%(香港系列)1) | 基本檢查。注意假陰性。 |
| IL-10/IL-6比值 | >1時靈敏度89.4%1) | 最重要的生物標誌物 |
| IL-10絕對值 | ≥50 pg/mL有幫助 | 復發時比比值>1更可靠2) |
| 流式細胞術 | CD20+ B細胞。敏感度88.0%5) | 單株增殖評估 |
| PCR(IgH基因重組) | 敏感度85.1%5) | B細胞克隆增殖證據 |
| MYD88突變分析 | 敏感度70%6) | 也有助於分子病理診斷 |
| 透過游離DNA檢測MYD88 | 檢出率比細胞DNA提高約30%1) | 微創診斷。房水也可行9, 10) |
| 6項診斷框架 | 敏感度97.5%,特異度100%8) | 複合指標的高精度診斷 |
眼內液中IL-10升高,而發炎性疾病中升高的IL-6低於IL-10,IL-10/IL-6比值>1具有診斷價值。但復發時該比值可能下降(僅43.8%>1),IL-10絕對值≥50 pg/mL是更可靠的指標2)。
確診眼內淋巴瘤後,應定期進行以下檢查以早期發現中樞神經系統淋巴瘤。
PIOL的治療以眼局部治療和全身化療相結合為基礎。由於血-視網膜屏障(BRB)限制全身化療藥物進入眼內,局部治療對於控制眼內病變至關重要。
甲氨蝶呤(甲氨蝶呤注射液200 mg)以400 μg/0.1 mL的劑量進行玻璃體內注射。標準方案如下。
香港系列報告顯示,中位注射5次後完全緩解率為77.8%1)。也可使用400 μg/0.05 mL的低劑量。一項累積20年經驗的大規模研究報告完全緩解率為97%6)。
主要副作用:角膜病變(33~100%)。透過無防腐劑眼藥水、繃帶式隱形眼鏡(BCL)和口服葉酸進行管理1)。
總劑量約30 Gy的眼局部照射有效。適用於雙側病變、老年、MTX不耐受或就醫困難的患者。但存在放射性視網膜病變、視神經病變和白內障等副作用風險,如果可能,優先考慮MTX注射4)。
部分患者在診斷性玻璃體切除術後獲得完全緩解(香港系列:75%1),另一報告:19.7%7))。其機制被認為是去除了淋巴瘤細胞增殖的支架並減少了腫瘤負荷。對於MTX不耐受或拒絕的患者,這是一個選擇。
大劑量MTX全身給藥是基礎治療。
必要時可加用全腦放療(WBRT),但由於存在白質腦病等副作用風險,尤其對於老年患者,應謹慎決定適應症。
| 病況 | 推薦治療 |
|---|---|
| 僅眼內病變 | MTX玻璃體內注射 ± 眼部局部放射線(30 Gy) |
| 合併CNS | 大劑量MTX全身給藥 ± 全腦照射 + 眼部局部治療 |
| 眼內復發時 | MTX玻璃體內注射(完全緩解55.6%,部分緩解33.3%)2) |
全身化療與玻璃體內化療聯合使用可能降低眼內復發風險。無玻璃體內化療史被報導為眼內復發的獨立危險因子2),顯示積極進行眼部局部治療的重要性。
眼內原發性淋巴瘤中絕大多數(95%以上)為瀰漫性大B細胞淋巴瘤(DLBCL)。它是由淋巴細胞單株增殖引起的惡性腫瘤,與眼附屬器常見的低惡性度MALT淋巴瘤相比,惡性度極高。
MYD88 L265P突變在PVRL/PCNSL中高頻檢出。此突變導致Toll樣受體訊息持續活化,持續活化NF-κB路徑,維持腫瘤細胞的增殖與存活6)。BTK(布魯頓酪氨酸激酶)也位於該路徑下游,作為治療靶點備受關注。
VEGF和IL-10的高表現有助於腫瘤細胞的免疫逃逸。IL-10是腫瘤細胞自身產生的細胞激素,參與免疫抑制環境的形成。
腫瘤細胞的轉變發生在中樞神經系統之外,隨後遷移到具有免疫特權的眼內3)。由於血-視網膜屏障(BRB)限制了全身化療藥物進入眼內,控制眼內病變必須採用玻璃體內注射或眼部局部放療等局部治療。
主要浸潤部位:
玻璃體混濁呈帶狀或索狀,呈現從後極向周邊放射狀擴散的獨特模式。浸潤視網膜的淋巴瘤細胞逐漸形成黃白色斑塊狀病灶,有時會融合擴大。
PIOL和PCNSL在基因表現譜上有許多共同點,兩者被認為屬於同一疾病譜系3)。這是PIOL患者頻繁發生中樞神經系統病變的背景。
利用玻璃體液和房水中的游離DNA檢測MYD88突變正受到關注。其檢出率比細胞DNA高約30%1),即使在高度稀釋的樣本中也有效。已有報導在房水中檢測(使用超靈敏ddPCR檢測MYD88 L265P突變)9, 10),有望應用於玻璃體活檢困難的病例。
一項針對51例病例的回顧性研究表明,全身化療聯合玻璃體內化療可能降低眼內復發風險2)。最佳給藥方案需要進一步的前瞻性研究。
在PIOL中,相當數量的病例最終會發展為CNS病變。孤立性PVRL(僅眼部)的55.6%發生了新的CNSL(中樞神經系統淋巴瘤),中位時間為35.1個月2)。在香港系列中,10例中有7例(70%)出現CNS病變,其中57.1%的眼部病變先於CNS病變1)。因此,即使在確認眼內病變後,也必須定期進行釓增強頭部MRI的CNS檢查。儘管有報導稱眼內復發不會直接影響CNS復發率或總生存期2),但CNS病變發生後的預後通常仍然嚴峻。