急性期:發病後數小時至數天

內源性細菌性眼內炎
1. 什麼是內源性細菌性眼內炎?
Section titled “1. 什麼是內源性細菌性眼內炎?”細菌性眼內炎是細菌侵入眼內引起的眼內炎症性疾病,根據感染途徑分為外源性和內源性。外源性眼內炎發生於眼科手術、玻璃體內注射或穿孔性眼外傷後,主要致病菌為革蘭陽性菌(如凝固酶陰性葡萄球菌、腸球菌)。相比之下,內源性細菌性眼內炎是其他器官的感染灶中的細菌經血行播散至視網膜和脈絡膜而發病。常繼發於敗血症(菌血症),主要致病菌為革蘭陰性桿菌。
一般來說,細菌性眼內炎比真菌性眼內炎進展更快,而由革蘭陰性桿菌引起的內源性眼內炎進展尤其迅速,預後不良。葡萄膜炎診療指南將其歸類為感染性眼內炎的一種,根據致病微生物(細菌性 vs 真菌性)和感染途徑(外源性 vs 內源性)兩方面進行整理1)。
流行病學與發生情況
Section titled “流行病學與發生情況”內源性細菌性眼內炎不會發生於健康人。患者總是存在某種基礎疾病或危險因素,好發於老年人、糖尿病、器官膿瘍(肺、肝、腎)或接受免疫抑制治療等易感宿主。
其中,肝膿瘍作為眼內炎發病風險最高的基礎疾病尤為重要。過去肝膿瘍的主要致病菌為大腸桿菌,但自1990年代以來,在東南亞、歐美和日本,肺炎克雷伯菌已占肝膿瘍致病菌的80%以上。肺炎克雷伯菌肝膿瘍中**3%~8%**會併發眼內炎,需特別注意該菌引起的內源性眼內炎。此外,80%以上的病例為單眼發病。
一項針對342例病例的系統性回顧顯示,內源性細菌性眼內炎的致病菌分布因地區而異,亞洲以革蘭氏陰性桿菌(尤其是肺炎克雷伯菌)為主2)。
| 主要基礎疾病/危險因子 | 備註 |
|---|---|
| 肝膿瘍(最常見) | 肺炎克雷伯菌占80%以上,眼內炎發生率3%~8% |
| 尿路感染 | 經由革蘭氏陰性桿菌菌血症介導 |
| 肺膿瘍 | 從膿瘍直接血行播散 |
| 感染性心內膜炎 | 由金黃色葡萄球菌等引起的革蘭氏陽性菌眼內炎 |
| 腦膜炎 | 繼發於嚴重全身感染 |
| 惡性腫瘤 | 免疫功能低下/化療背景 |
| 糖尿病 | 高血糖導致的中性球功能障礙 |
| 類固醇/免疫抑制治療 | 宿主防禦功能全面下降 |
| 膠原病 | 疾病本身及治療藥物導致的易感染性 |
最大的差異在於感染途徑與致病菌。外源性眼內炎由手術、外傷、玻璃體內注射等直接侵入眼睛引發,主要致病菌為革蘭氏陽性菌(凝固酶陰性葡萄球菌、腸球菌等)。而內源性眼內炎由肝膿瘍、泌尿道感染等其他器官的感染灶經由血流到達視網膜脈絡膜引發,主要致病菌為革蘭氏陰性桿菌(如克雷伯氏肺炎桿菌)。外源性有明確的手術或外傷史,而內源性則以發燒等全身感染症狀為前驅為特徵。
2. 主要症狀與臨床所見
Section titled “2. 主要症狀與臨床所見”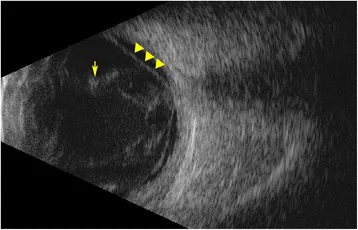
全身症狀(前驅症狀)
Section titled “全身症狀(前驅症狀)”內源性眼內炎中,眼部症狀之前或同時出現全身感染徵象。可見降鈣素原(PCT)升高(重症細菌感染的血清標記)、白血球數增加、CRP升高。若基礎疾病為糖尿病,則可見高血糖與HbA1c升高。全身狀態極差時,患者可能無法識別或主訴眼部症狀。
- 發燒、全身倦怠(作為感染徵象必發)
- PCT升高(重症細菌感染的血清標記)
- 白血球數增加及CRP升高(急性發炎標記)
- 高血糖及HbA1c升高(見於合併糖尿病的患者)
眼部自覺症狀
Section titled “眼部自覺症狀”早期自覺症狀包括飛蚊症、視力模糊及視力下降。急性期除視力下降和畏光外,還會感到眼痛。視力迅速惡化,有時可降至手動或光感程度。
進展期:發炎波及全眼球
玻璃體膿瘍形成:一旦形成,常導致全眼球炎,預後極差。
視網膜及視神經損傷:視網膜血管阻塞、視網膜壞死及視神經萎縮導致不可逆的視力喪失1)。
波及眼周組織:發炎可蔓延至眼眶組織,引起眼球突出及眼球運動受限。
緊急手術的必要性:進展為全眼球炎的病例需要緊急手術介入。
3. 原因與風險因素
Section titled “3. 原因與風險因素”內因性細菌性眼內炎的主要致病菌是革蘭氏陰性桿菌。
- 克雷伯氏肺炎桿菌:在肝膿瘍引起的內因性眼內炎中最為重要。自1990年代以來在亞洲(包括東南亞和日本)的發生率顯著增加,佔肝膿瘍致病菌的80%以上。由該菌引起的肝膿瘍中,3%~8%併發眼內炎。
- 大腸桿菌:以前是肝膿瘍和泌尿道感染的主要致病菌,仍然很重要。
- 綠膿桿菌:在免疫功能低下宿主中引起嚴重感染。
也有報告由金黃色葡萄球菌引起的轉移性眼內炎,繼發於革蘭氏陽性菌引起的全身感染,如感染性心內膜炎 1)。
在亞洲地區,克雷伯氏肺炎桿菌肝膿瘍相關眼內炎的發生率高於歐美國家 3)。在東亞的臨床實務中,需要考慮到該菌引起的內因性眼內炎。
增加風險的基礎疾病
Section titled “增加風險的基礎疾病”內因性眼內炎的發生,除了原發感染灶(如肝膿瘍、泌尿道感染)外,幾乎總是伴隨宿主方面的易感因素。
- 糖尿病:高血糖導致嗜中性球功能障礙和免疫功能下降,促進感染。
- 惡性腫瘤:腫瘤本身引起的免疫抑制,以及化療或放療後的骨髓抑制。
- 膠原病: 疾病活動性和免疫抑制藥物兩方面均增加易感染性
- 長期使用類固醇/免疫抑制治療: T細胞功能下降和嗜中性球功能障礙
- 高齡: 隨年齡增長免疫功能全面下降(尤其是體液免疫和細胞免疫)
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”診斷基本方針
Section titled “診斷基本方針”當懷疑內源性眼內炎時,原則是不等檢查結果,優先治療。由於急性感染可在數小時內迅速惡化,一旦根據問診和臨床症狀懷疑眼內炎,應同時開始眼內液採集和抗菌藥物給藥。
確診最重要的檢查是眼內液(房水、玻璃體液)的塗片和培養檢查。
- 塗片檢查(革蘭氏染色等): 有助於早期診斷。可快速了解致病菌類型(革蘭氏陽性或陰性)
- 培養檢查: 必須用於鑑定致病菌和確認藥物敏感性。玻璃體液比房水檢出致病菌的陽性率更高
- PCR法(基因檢測): 即使在培養陰性病例中也能檢測到致病菌DNA,近年來應用日益普及
全身及輔助檢查
Section titled “全身及輔助檢查”| 檢查 | 目的 |
|---|---|
| B超檢查 | 玻璃體混濁導致眼底無法窺見時必須進行。確認玻璃體膿瘍的有無及程度 |
| 血液培養 | 確認內因性眼內炎及鑑定致病菌所必需1) |
| 血清β-D-葡聚糖 | 有助於鑑別真菌性眼內炎1) |
| 白血球數、CRP、PCT | 監測全身感染的嚴重程度 |
| 血糖、HbA1c | 評估基礎疾病(糖尿病) |
| 胸腹部CT | 尋找原發感染灶(如肝膿瘍、肺膿瘍等) |
| 心臟超音波 | 排除感染性心內膜炎 |
內因性眼內炎需與以下疾病進行鑑別。
-
與急性前葡萄膜炎的鑑別:雖然可伴有前房蓄膿和纖維素,但有以下不同點。
- 老年人急性前葡萄膜炎罕見
- 急性前葡萄膜炎很少引起眼瞼腫脹或結膜水腫
- 急性前葡萄膜炎時視力不會降至手動或光感
- 急性前葡萄膜炎時至少可見視盤(內源性眼內炎時玻璃體混濁無法看到)
- 內源性眼內炎先有發燒等全身感染症狀
-
外源性眼內炎:根據明確的眼科手術、外傷或玻璃體注射史進行鑑別1)
-
真菌性眼內炎:進展相對緩慢(數天至數週),細菌性為數小時至數天。β-D-葡聚糖陽性、視網膜白色滲出病灶(真菌球)為特徵1)
-
遲發性(慢性)細菌性眼內炎:由痤瘡丙酸桿菌引起,白內障術後1個月或更晚發病。特徵為慢性虹膜睫狀體炎和復發性前房積膿1)
前房積膿是眼內炎的特徵性表現,但也可見於急性前葡萄膜炎(HLA-B27相關、貝西氏症等)、感染性角膜炎蔓延和糖尿病虹膜炎。鑑別要點包括:①手術或外傷史(與外源性眼內炎鑑別),②發燒等全身感染症狀(與內源性眼內炎鑑別),③眼瞼腫脹和結膜水腫程度,④玻璃體混濁深度和眼底可見性,⑤視力下降速度。眼內炎時伴有全身症狀,玻璃體混濁嚴重,視力下降迅速。若懷疑,應在等待檢查結果前開始治療1)。
5. 標準治療方法
Section titled “5. 標準治療方法”治療基本原則
Section titled “治療基本原則”一旦懷疑眼內炎,應立即開始抗生素三途徑同時給藥,無需等待病原菌鑑定。三途徑包括:①玻璃體內注射,②頻繁滴用抗生素眼藥水,③全身給藥(靜脈滴注)。需與內科(消化科、感染科)協作,同時治療原發感染灶(如肝膿瘍)1)。
藥物治療方案(病原菌不明時)
Section titled “藥物治療方案(病原菌不明時)”| 給藥途徑 | 藥物(商品名) | 用法用量 | 備註 |
|---|---|---|---|
| 玻璃體內注射① | 鹽酸萬古黴素注射液 | 1 mg/0.1 mL 玻璃體內注射 | 健保不給付 |
| 玻璃體內注射② | 頭孢他啶(Modacin®)注射液 | 2 mg/0.1 mL 玻璃體內注射 | 健保不給付。與①同時或緊接其後進行。 |
| 眼藥水① | 左氧氟沙星眼藥水(Cravit®)1.5% | 每日6次點眼 | 作為頻繁點眼繼續使用 |
| 眼藥水② | 頭孢甲肟眼藥水(Bestron®)0.5% | 每日6次點眼 | 與①交替使用 |
| 點眼③ | 倍他米松點眼液(Rinderon®)0.1% | 每日6次點眼 | 用於抑制發炎的合併用藥 |
| 全身給藥① | Imipenem/cilastatin(Tienam®)注射劑 | 每次1g,每日2次,靜脈點滴,共5天 | 廣譜碳青黴烯類 |
| 全身給藥② | Levofloxacin(Cravit®)錠 500mg | 每次1錠,每日1次,口服,共5天 | 與全身給藥①合併使用 |
全身給藥亦可選擇第四代頭孢菌素類如Cefozopran(Firstcin®)等廣譜抗菌藥物。藥敏結果確定後,應更換為特異性更高的抗菌藥物繼續治療。若確認革蘭氏陰性桿菌(如肺炎克雷伯菌),則根據藥敏模式從碳青黴烯類、氟喹諾酮類、第三至四代頭孢菌素中選擇最佳藥物。
懷疑眼內炎時(臨床判斷),並行實施以下措施。
- 採集眼內液(前房水、玻璃體液)→ 塗片、培養、PCR
- 不等檢查結果,立即開始三途徑同時給藥:(1)玻璃體內注射,(2)頻繁點眼,(3)全身給藥
- 與內科協作並行實施全身檢查和原發感染灶治療(如肝膿瘍引流)
- 藥敏結果明確後,更換為特異性更高的抗菌藥物
- 藥物治療無效或進展的病例,立即轉為玻璃體手術
對藥物治療無反應的病例,在全身狀況允許的情況下,應盡早實施玻璃體手術。玻璃體手術可物理清除作為感染介質的玻璃體,並將抗菌藥物直接送達眼內。葡萄膜炎診療指引推薦,在進展迅速、玻璃體混濁導致眼底無法窺見或存在視網膜下膿瘍時,應早期在抗菌藥物灌注下進行玻璃體手術1)。
- 適應症:藥物治療無效、眼底無法窺見、視網膜下膿瘍形成
- 術式:玻璃體手術。必要時聯合水晶體切除術、眼內透鏡/水晶體囊摘除
- 灌注液:使用混合抗菌藥物(如萬古黴素)的灌注液
- 限制:全身狀況不佳(如敗血症管理中)時常無法進行手術,這是一個挑戰
在致病菌不明時,通過三途徑同時給予廣譜抗菌藥物。藥敏結果明確後,更換為更特異的藥物可提高療效。但革蘭陰性桿菌(如肺炎克雷伯菌)引起的眼內炎進展極快(以小時計),僅用抗菌滴眼液眼內移行不足,必須聯合玻璃體內注射和全身給藥。若藥物治療後眼底無法窺見的情況未改善或進展,應迅速考慮轉為玻璃體手術1)。
6. 病理生理學與詳細發病機轉
Section titled “6. 病理生理學與詳細發病機轉”血行性播散的機制
Section titled “血行性播散的機制”內因性細菌性眼內炎是由於其他器官的感染灶(如肝膿瘍、尿路感染等)中的細菌進入血流,經血行性播散至視網膜脈絡膜而發病。細菌在脈絡膜微血管床定植後,局部發炎反應迅速進展,從視網膜脈絡膜炎波及到玻璃體炎。
多發生於患有惡性腫瘤、糖尿病、膠原病、使用免疫抑制劑等基礎疾病的易感染宿主。這些宿主血液中細菌清除能力下降,容易發生眼內感染。
革蘭氏陰性桿菌內毒素引起的組織損傷
Section titled “革蘭氏陰性桿菌內毒素引起的組織損傷”當致病菌為革蘭氏陰性桿菌(如肺炎克雷伯菌、大腸桿菌、綠膿桿菌等)時,病情進展尤其迅速。革蘭氏陰性桿菌的內毒素(脂多醣,LPS)在眼內組織中引發強烈的發炎反應,並放大發炎連鎖反應,這是快速惡化的主要原因。由於此機制,與外因性眼內炎(主要由革蘭氏陽性菌引起)相比,預後往往較差。
病變進展順序
Section titled “病變進展順序”- 原發感染灶引起菌血症
- 細菌在脈絡膜微血管定植 → 形成脈絡膜炎和視網膜脈絡膜炎
- 發炎波及視網膜和玻璃體腔 → 快速玻璃體混濁和玻璃體炎
- 進展病例:形成玻璃體膿瘍 → 波及鞏膜和眼眶組織(全眼球炎)
視力預後不良的因素包括視網膜血管閉塞、視網膜壞死和視神經萎縮 1)。如果治療延遲,許多病例最終會失去光感,治療開始的速度直接關係到預後。
7. 預後與長期管理
Section titled “7. 預後與長期管理”內因性細菌性眼內炎的視力預後通常較差。當致病菌為革蘭氏陰性桿菌時,進展尤其迅速,預後更差;治療開始的延遲直接影響視力結果。即使治療後,也常遺留視神經萎縮、視網膜壞死和視網膜血管白線化等後遺症,許多病例視力預後不良 1)。治癒後也可能合併脈絡膜新生血管和黃斑病變 1)。
一項針對342例患者的系統性回顧顯示,大多數患者最終視力為20/200(0.1)或更差,僅有少數患者能維持適當視力2)。關於克雷伯氏肺炎桿菌肝膿瘍相關眼內炎的預後因子研究指出,初診時視力及玻璃體混濁程度是最終視力的主要預測因子3)。
在形成玻璃體膿瘍或進展為全眼球炎的病例中,有時必須進行眼球摘除。
基礎疾病的長期管理
Section titled “基礎疾病的長期管理”長期而言,基礎疾病(肝膿瘍、糖尿病、惡性腫瘤等)的適當管理對於預防復發及改善生命預後至關重要。透過內科及感染科的多科合作,持續治療原發感染灶,對眼科預後也有正面影響。眼科方面,術後定期進行眼底檢查及OCT檢查以追蹤視網膜及黃斑部非常重要。
患者與醫療團隊應共同認識到,透過多科合作(眼科、內科、感染科)進行早期診斷及原發感染灶的同步治療,對於改善視力預後及生命預後最為重要4)5)。
8. 參考文獻
Section titled “8. 參考文獻”- 日本眼炎症学会/日本眼科学会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635-696(「14. 眼内炎」節).
- Jackson TL, Paraskevopoulos T, Georgalas I. Systematic review of 342 cases of endogenous bacterial endophthalmitis. Surv Ophthalmol. 2014;59(6):627-635.
- Ang M, Jap A, Chee SP. Prognostic factors and outcomes in endogenous Klebsiella pneumoniae endophthalmitis. Am J Ophthalmol. 2011;151(2):338-344.
- Durand ML. Bacterial and fungal endophthalmitis. Clin Microbiol Rev. 2017;30(3):597-613.
- Sadiq MA, Hassan M, Agarwal A, et al. Endogenous endophthalmitis: diagnosis, management, and prognosis. J Ophthalmic Inflamm Infect. 2015;5:32.
