TD-OCT(第一代)
波長:810 nm
速度:400 A掃描/秒
軸向解析度:約10 μm
第一代技術透過可移動參考鏡改變光路長度來獲取斷層影像。目前基本已被SD-OCT取代。

光學同調斷層掃描(Optical Coherence Tomography; OCT)是一種利用近紅外光干涉現象非侵入性獲取眼底及前眼部斷層影像的診斷成像設備。其解析度約為2–5 μm,是眼科超音波的約100倍。它能高解析度評估視網膜和視神經的微細結構,有助於多種眼疾的早期發現和監測。
1991年由Huang等人引入後,OCT在眼科領域迅速普及。如今,它已成為視網膜疾病、青光眼、前眼部疾病和神經眼科等廣泛領域的標準檢查。保險點數為187點(眼底三維影像分析)。
OCT主要有三代技術。各代特性如下所示。
TD-OCT(第一代)
波長:810 nm
速度:400 A掃描/秒
軸向解析度:約10 μm
第一代技術透過可移動參考鏡改變光路長度來獲取斷層影像。目前基本已被SD-OCT取代。
SD-OCT(第二代)
波長:840 nm
速度:40,000–100,000 A掃描/秒
軸向解析度:3–7 μm
第二代技術使用光譜儀和傅立葉轉換一次性獲取深度資訊,是目前臨床標準。可精確評估黃斑部和視神經盤。代表機型:Cirrus(蔡司)、Spectralis(海德堡)、RS-3000(尼德克)、3D-OCT(拓普康)。
SS-OCT(第三代)
波長:1050 nm
速度:100,000~400,000 A掃描/秒
軸向解析度:約5 μm
採用掃頻雷射和雙平衡偵測器的第三代技術。由於波長較長,能更佳顯示脈絡膜等深層結構。優點是不需要EDI-OCT。
OCT是一種非侵入性、非接觸的檢查,完全無痛。可能需要使用散瞳眼藥水,但只需照射光線,不會接觸角膜或視網膜。檢查時間通常只需幾分鐘。
| 成像模式 | 特點/用途 |
|---|---|
| 交叉掃描 | 通過中心凹的基本掃描。首先進行。 |
| 5線 | 薄層掃描確認微細結構(如黃斑裂孔) |
| 放射狀掃描 | PCV息肉確認、中心外病灶評估 |
| 黃斑地圖 | 視網膜厚度圖。糖尿病黃斑水腫、RVO療效評估 |
| 青光眼分析(cpRNFL/GCA) | RNFL厚度、GCL+IPL厚度。青光眼診斷及進展判定 |
觀察部位分為後節OCT(黃斑部、視神經乳頭周圍、周邊部)和前節OCT(AS-OCT;角膜、前房、隅角)。
基本拍攝步驟如下。
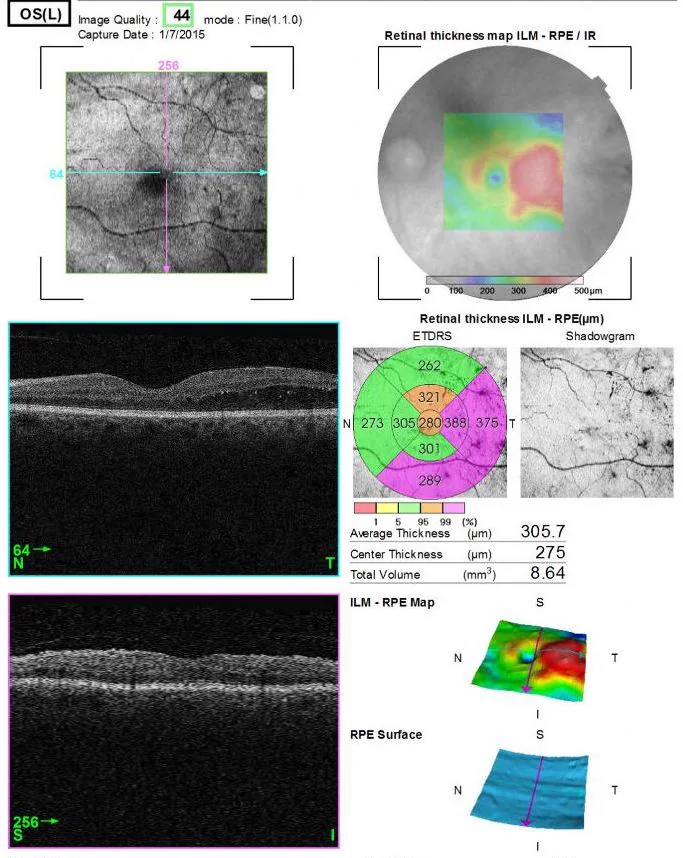
在中心凹掃描中,重要的是顯示中心凹凹陷且無視網膜內層的切片。黃斑疾病中,由於固視不良可能導致中心偏移,理解視網膜正常結構有助於提高檢查技能和診斷技能。
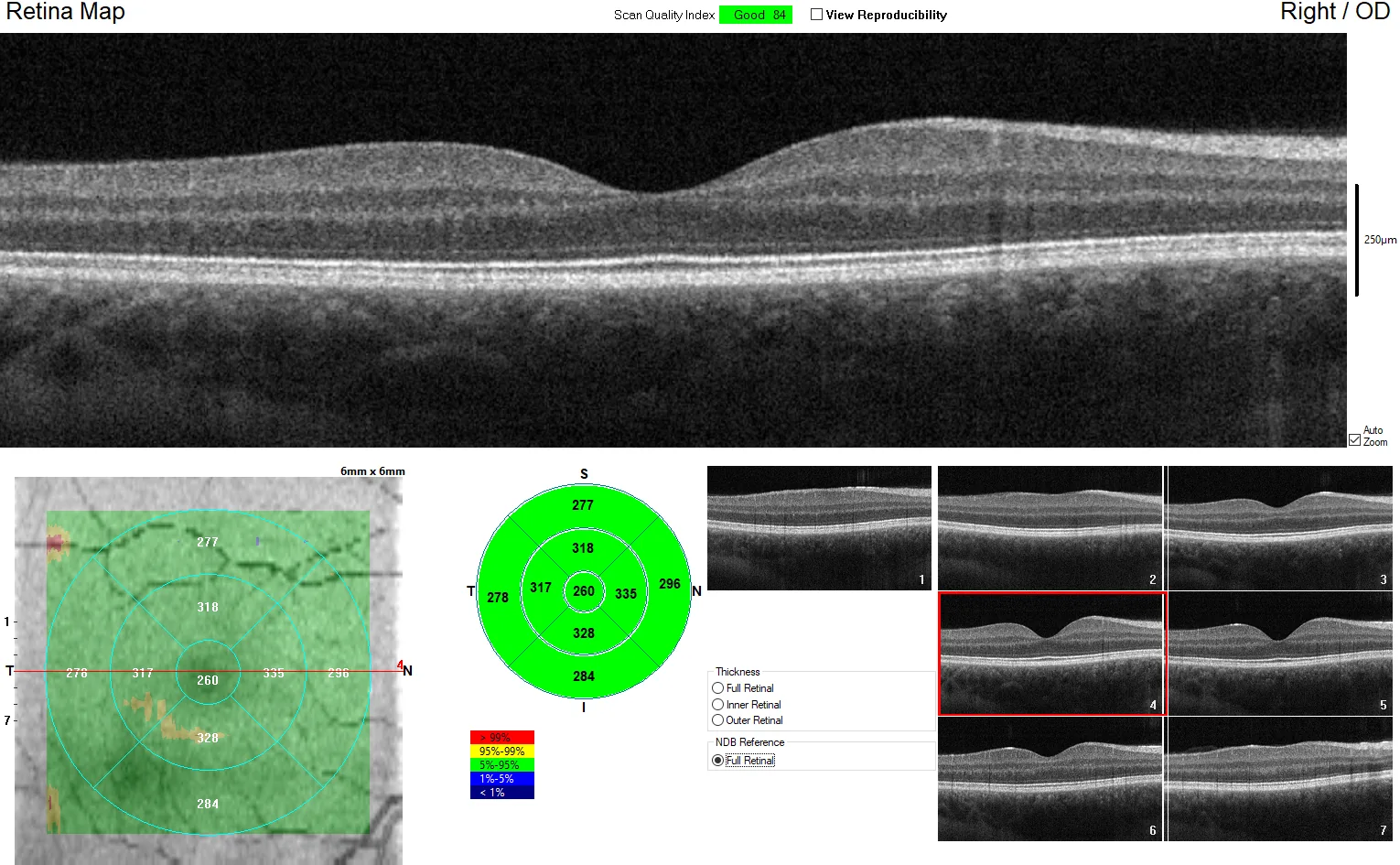
中心凹掃描的正常層結構(從內到外)由以下13層組成:
玻璃體 → 內界膜(ILM)→ 神經纖維層(RNFL)→ 神經節細胞層(GCL)→ 內叢狀層(IPL)→ 內核層(INL)→ 外叢狀層(OPL)→ 外核層(ONL)→ 外界膜(ELM)→ 橢圓體帶(EZ)→ 嵌合體帶(IZ)→ 視網膜色素上皮(RPE)→ 脈絡膜
各層的反射特性反映病理狀態,因此準確的層識別是判讀的基礎。
| 疾病 | 代表性OCT所見 |
|---|---|
| 黃斑裂孔 | 視網膜全層缺損±VMT |
| 黃斑前膜(ERM) | 內界膜上的高反射層 |
| 玻璃體黃斑牽引(VMT) | 後部玻璃體部分剝離伴黃斑牽引 |
| 糖尿病黃斑水腫 | 視網膜增厚、CME、DRIL、SRF |
| 視網膜靜脈阻塞(RVO) | 囊樣黃斑水腫、視網膜下液 |
| 年齡相關性黃斑變性(AMD) | CNV(1型/2型/3型)、色素上皮剝離 |
| 中心性漿液性脈絡膜視網膜病變(CSC) | 神經感覺視網膜剝離、EDI-OCT顯示脈絡膜增厚 |
| RPE撕裂 | RPE及外層結構突然消失 |
黃斑裂孔表現為視網膜全層缺損。SD-OCT是診斷黃斑裂孔最敏感且特異的檢查方法1)。
黃斑前膜(ERM) 在內界膜上表現為高反射層2)。關於術後視力,據報導80%的病例在玻璃體手術後獲得兩行或以上的視力改善2)。
糖尿病黃斑水腫:OCT定量測量視網膜厚度是抗VEGF治療啟動和再治療決策的指標3)。DRIL(視網膜內層紊亂)是視力預後不良的重要標誌。
RVO:OCT可定量評估黃斑水腫並檢測玻璃體視網膜界面變化4)。
AMD:RPE脫離分為漿液性、纖維血管性和玻璃膜疣樣色素上皮脫離,CNVM可分為1型(RPE下)、2型(RPE上)和3型(視網膜內新生血管)5)。
成像條件所致
鏡像偽影:由於成像範圍設置錯誤,實際圖像反轉並重疊顯示。
漸暈:周邊信號衰減,取決於照明光的入射角。
範圍外錯誤:超出設定深度範圍的結構被折疊顯示。
患者因素
軟體因素
分割錯誤:自動分層演算法錯誤識別視網膜層。在病變、嚴重白內障或高度近視眼中頻繁發生。
可透過手動校正或重新掃描來處理。如果訊號強度指數(SS)低於6,考慮重新檢查。
SD-OCT是一種非接觸、非侵入性的影像診斷技術,可客觀評估青光眼的結構損傷,在青光眼診斷中具有高度實用性6)。在前視野青光眼的診斷中尤其有用,能夠在視野缺損出現前捕捉到結構變化6)7)。
RNFL厚度
測量原理:量化內界膜(ILM)與RNFL邊界之間的厚度。
TSNIT圖:以視神經中心3.4mm直徑圓上的RNFL厚度,按T(顳側)→S(上方)→N(鼻側)→I(下方)→T(顳側)順序顯示。
正常模式:上下方向呈雙峰(反映弓狀神經纖維束的解剖分佈)6)。
青光眼檢測能力:平均RNFL厚度的敏感性83%,特異性88%(5%水平)。在1%水平,特異性100%,敏感性65%。
ONH參數
視神經乳頭分析:自動描繪視盤、杯凹和盤緣。
布魯赫膜參考:以布魯赫膜開口定義盤緣,並計算到ILM的最短距離。
診斷能力高的指標:垂直盤緣厚度、盤緣面積和垂直杯盤比具有最高的診斷性能7)。
BMO-MRW:以布魯赫膜開口為基準的視盤邊緣寬度評估,再現性優異6)
神經節細胞分析(GCA)
測量對象:黃斑周圍神經節細胞層(GCL)與內叢狀層(IPL)的複合厚度
不同設備名稱:Cirrus稱為GCIPL(GCL+IPL),Optovue稱為GCC(RNFL+GCL+IPL)
有用參數:最小值、顳下象限、平均值在診斷上最有用6)7)
與地板效應的關係:黃斑參數的地板效應出現晚於RNFL厚度,對晚期評估有用6)
與正常資料庫比較有用,但需注意以下因素導致的偽陽性和偽陰性。
青光眼進展判定有兩種方法:事件分析和趨勢分析。
Cirrus的GPA整合了這兩種方法7)。平均RNFL厚度的檢查間可重複性界限為3.89 μm,可重複性減少4 μm以上提示有統計學意義的顯著變化。
在進展期青光眼中,RNFL厚度趨於平穩,由於膠質組織和血管等非神經組織殘留,很少低於50 μm6)7)。這種「地板效應」降低了SD-OCT在終末期的臨床實用性,此時主要依靠視野檢查來判定進展。黃斑參數(GCIPL)的地板效應出現比RNFL厚度晚,因此在進展期仍保持一定的實用性6)。
在高度近視眼中,與正常資料庫的比較存在局限性。由於RNFL束向顳側移位,即使在正常眼中也可能被判定為「變薄」。對於此類病例,以患者自身基線進行縱向比較是有效的。透過一系列SD-OCT掃描評估進行性變薄。注意,即使在健康人群中,RNFL厚度也會因年齡增長每年減少約0.52 μm,因此需要考慮這種自然減少。
OCT在神經眼科領域的應用正在迅速擴展9)。視盤周圍RNFL(cpRNFL)厚度和黃斑部GCIPL(神經節細胞層+內叢狀層)是主要評估參數,有時可在明顯的臨床體徵或視功能障礙出現之前檢測到變化9)。
| 疾病 | 急性期表現 | 慢性期表現 |
|---|---|---|
| 視神經炎 | RNFL增厚(軸突水腫)或正常 | RNFL和GCIPL變薄(發病後至6個月) |
| 多發性硬化症(MS) | 無症狀時也有cpRNFL減少 | 進展型RNFL和GCIPL萎縮速度增加 |
| NMOSD | 視乳頭水腫 | 嚴重RNFL變薄(<30μm),微囊樣黃斑水腫(AQP4陽性者40%)9) |
| 壓迫性視神經病變(如垂體腺瘤) | GCIPL鼻側雙重變薄 | 蝶形RNFL萎縮(對應雙顳側偏盲) |
| NAION | 視乳頭水腫導致RNFL評估困難,GCIPL變薄先出現 | 水平下鼻側變薄 |
| 視乳頭玻璃膜疣(ODD) | EDI-OCT是檢測的黃金標準 | ODD體積大與RNFL變薄和視野缺損相關 |
| 視乳頭水腫 | cpRNFL增厚 | GCIPL變薄>10μm→1年後視功能不良9) |
視神經炎和多發性硬化症(MS):RNFL和GCIPL變薄是已確立的生物標誌物9)。即使沒有眼部症狀的MS患者也出現cpRNFL減少,死後研究證實99%的MS患者存在視神經脫髓鞘病灶。cpRNFL厚度與最佳矯正視力、對比敏感度、色覺和腦萎縮相關。
NMOSD以嚴重的視神經萎縮為特徵,微囊樣黃斑水腫的發生率(AQP4陽性約40%)顯著高於MS(5%)9)。在MOG-IgG相關視神經炎中,GCIPL相對保留,而在AQP4-IgG相關視神經炎中,GCIPL顯著喪失9)。
**視乳頭玻璃膜疣(ODD)**的檢測:EDI-OCT是金標準9)。ODD表現為位於篩板上方的低反射結構,具有高反射邊緣,在埋藏型玻璃膜疣的檢測能力上優於B超、自發螢光和CT。PHOMS(視乳頭周圍高反射卵圓形團塊樣結構)應作為與ODD不同的現象加以區分9)。
壓迫性視神經病變:術前RNFL厚度≥70μm是術後視力和視野改善的顯著預測因子9),術前OCT評估可用於預後預測。
由於不同設備的分割演算法和正常資料庫不同,不同設備之間的數值無法直接比較。建議縱向評估使用同一設備9)。
OCT基於邁克爾遜干涉儀的原理。近紅外光(波長840-1050nm)被分為測量光和參考光,分別照射到樣本(眼底)和參考鏡。兩者反射光重新結合時產生的干涉條紋(干涉圖)用於計算每個深度的反射強度。沿深度方向的反射強度剖面稱為A掃描,A掃描橫向排列形成B掃描(斷層圖像)。
在青光眼和視神經疾病中,優先評估以下三層9)。
隨著RGC損傷,RNFL會脫落。所有RGC中約50%集中在黃斑中心20°區域,即使在早期青光眼中,也可能有約50%的RGC已經消失6)。SD-OCT透過RNFL厚度評估RGC軸突的脫落,GCA評估包含細胞體的內層變薄。
最大的差異在於使用的波長和深層結構的可視化能力。SD-OCT使用840 nm波段,SS-OCT使用1050 nm波段。1050 nm受黑色素散射較少,更容易穿透RPE,因此SS-OCT在觀察脈絡膜和鞏膜方面更優。此外,SS-OCT的成像速度超過SD-OCT,便於進行廣角掃描。另一方面,兩者的軸向解析度都在5-7 μm左右,沒有顯著差異。
SS-OCT在1050 nm波長下的高速、廣角掃描能力推進了對厚脈絡膜疾病譜的評估。包括脈絡膜增厚(pachydysm)在內的中心性漿液性脈絡膜視網膜病變、息肉狀脈絡膜血管病變(PCV)和中心凹旁微血管擴張症的評估精度得到提高,有助於闡明病理機制。此外,正在嘗試在與黃斑部相同的掃描中評估包括周邊視網膜在內的廣泛區域的斷層影像。
針對青光眼、AMD和DME的自動診斷AI已經開發出來,診斷準確性的提升已有報告。基於深度學習的OCT影像分析正在實現分割精度的提高和報告自動生成,並逐步投入實際應用6)7)。
需要縱向研究來確立OCT作為阿茲海默症、帕金森病等神經退化性疾病篩檢和監測工具的有效性9)。REM睡眠行為障礙(RBD)患者的RNFL和GCIPL變薄作為前驅期帕金森病的替代標誌物受到關注9)。
American Academy of Ophthalmology Retina/Vitreous Panel. Idiopathic Macular Hole Preferred Practice Pattern. Ophthalmology. 2019.
American Academy of Ophthalmology Retina/Vitreous Panel. Idiopathic Epiretinal Membrane and Vitreomacular Traction Preferred Practice Pattern. Ophthalmology. 2019.
American Academy of Ophthalmology Retina/Vitreous Panel. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024.
American Academy of Ophthalmology Retina/Vitreous Panel. Retinal Vein Occlusions Preferred Practice Pattern. Ophthalmology. 2024.
American Academy of Ophthalmology Retina/Vitreous Panel. Age-Related Macular Degeneration Preferred Practice Pattern. Ophthalmology. 2024.
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
American Academy of Ophthalmology. Primary Open-Angle Glaucoma Preferred Practice Pattern®. 2020.
American Academy of Ophthalmology. Primary Open-Angle Glaucoma Suspect Preferred Practice Pattern®. 2020.
Lo C, Vuong LN, Micieli JA. Recent advances and future directions on the use of optical coherence tomography in neuro-ophthalmology. Taiwan J Ophthalmol. 2021;11(2):107-131.