TD-OCT (نسل اول)
طول موج: 810 نانومتر
سرعت: 400 اسکن A در ثانیه
وضوح محوری: حدود 10 میکرومتر
روش نسل اول که با تغییر طول مسیر نوری با استفاده از آینه مرجع متحرک، تصاویر مقطعی را به دست میآورد. امروزه تقریباً به طور کامل با SD-OCT جایگزین شده است.

توموگرافی انسجام نوری (OCT) یک دستگاه تصویربرداری تشخیصی است که با استفاده از پدیده تداخل نور مادون قرمز نزدیک، تصاویر مقطعی از فوندوس و بخش قدامی چشم را به صورت غیرتهاجمی به دست میآورد. وضوح آن حدود 2 تا 5 میکرومتر است که تقریباً 100 برابر سونوگرافی چشم میباشد. این دستگاه ساختارهای ریز شبکیه و عصب بینایی را با وضوح بالا ارزیابی کرده و به تشخیص زودهنگام و پایش بیماریهای مختلف چشمی کمک میکند.
پس از معرفی توسط هوانگ و همکاران در سال 1991، این فناوری به سرعت در چشمپزشکی گسترش یافت. امروزه OCT به عنوان یک آزمایش استاندارد در زمینههای گستردهای از جمله بیماریهای شبکیه، گلوکوم، بیماریهای بخش قدامی و نورو-افتالمولوژی در نظر گرفته میشود. نمره بیمه برای آنالیز سهبعدی تصاویر فوندوس 187 امتیاز تعیین شده است.
OCT عمدتاً دارای سه نسل از روشها است. ویژگیهای هر روش در زیر آورده شده است.
TD-OCT (نسل اول)
طول موج: 810 نانومتر
سرعت: 400 اسکن A در ثانیه
وضوح محوری: حدود 10 میکرومتر
روش نسل اول که با تغییر طول مسیر نوری با استفاده از آینه مرجع متحرک، تصاویر مقطعی را به دست میآورد. امروزه تقریباً به طور کامل با SD-OCT جایگزین شده است.
SD-OCT (نسل دوم)
طول موج: 840 نانومتر
سرعت: 40,000 تا 100,000 اسکن A در ثانیه
وضوح محوری: 3 تا 7 میکرومتر
روش نسل دوم که با استفاده از طیفسنج و تبدیل فوریه، اطلاعات عمق را به طور همزمان به دست میآورد. استاندارد بالینی فعلی. مناسب برای ارزیابی دقیق ماکولا و دیسک عصب بینایی. مدلهای نماینده: Cirrus (Carl Zeiss)، Spectralis (Heidelberg)، RS-3000 (Nidek)، 3D-OCT (Topcon).
SS-OCT (نسل سوم)
طول موج: 1050 نانومتر
سرعت: ۱۰۰,۰۰۰ تا ۴۰۰,۰۰۰ اسکن A در ثانیه
وضوح محوری: حدود ۵ میکرومتر
روش نسل سوم با استفاده از لیزر جاروب طول موج و آشکارساز تعادل دوگانه. به دلیل طول موج بلند، در تجسم ساختارهای عمیق مانند مشیمیه برتری دارد. مزیت آن عدم نیاز به EDI-OCT است.
OCT یک آزمایش غیرتهاجمی و غیرتماسی است و هیچ دردی ندارد. ممکن است نیاز به قطرههای گشادکننده مردمک باشد، اما فقط نور تابیده میشود و قرنیه یا شبکیه لمس نمیشود. زمان آزمایش معمولاً چند دقیقه است.
| حالت تصویربرداری | ویژگیها و کاربردها |
|---|---|
| اسکن متقاطع | اسکن پایه از طریق حفره مرکزی. ابتدا انجام میشود |
| 5 خط | بررسی ساختارهای ریز با برشهای نازک (مانند تأیید سوراخ ماکولا) |
| اسکن شعاعی | تأیید پولیپ در PCV، ارزیابی ضایعات خارج مرکزی |
| نقشه ماکولا | نقشه ضخامت شبکیه. ارزیابی اثر درمان در ادم ماکولای دیابتی و RVO |
| تحلیل گلوکوم (cpRNFL/GCA) | ضخامت RNFL و GCL+IPL. تشخیص و پیشرفت گلوکوم |
نواحی مشاهده به OCT بخش خلفی (ماکولا، اطراف دیسک بینایی، محیطی) و OCT بخش قدامی (AS-OCT؛ قرنیه، اتاق قدامی، زاویه) تقسیم میشوند.
مراحل پایه تصویربرداری به شرح زیر است:
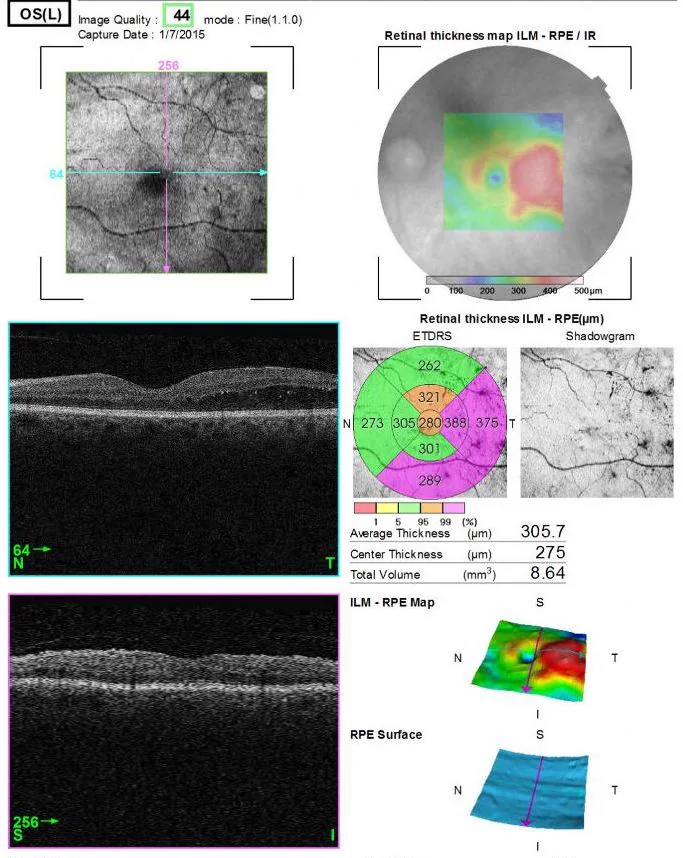
در اسکن حفره مرکزی، نمایش برشی که در آن فرورفتگی حفره مرکزی وجود داشته باشد و لایههای داخلی شبکیه دیده نشوند، مهم است. در بیماریهای لکه زرد، به دلیل تثبیت ضعیف، ممکن است مرکز جابهجا شود و درک ساختار طبیعی شبکیه به بهبود مهارتهای معاینه و تشخیص کمک میکند.
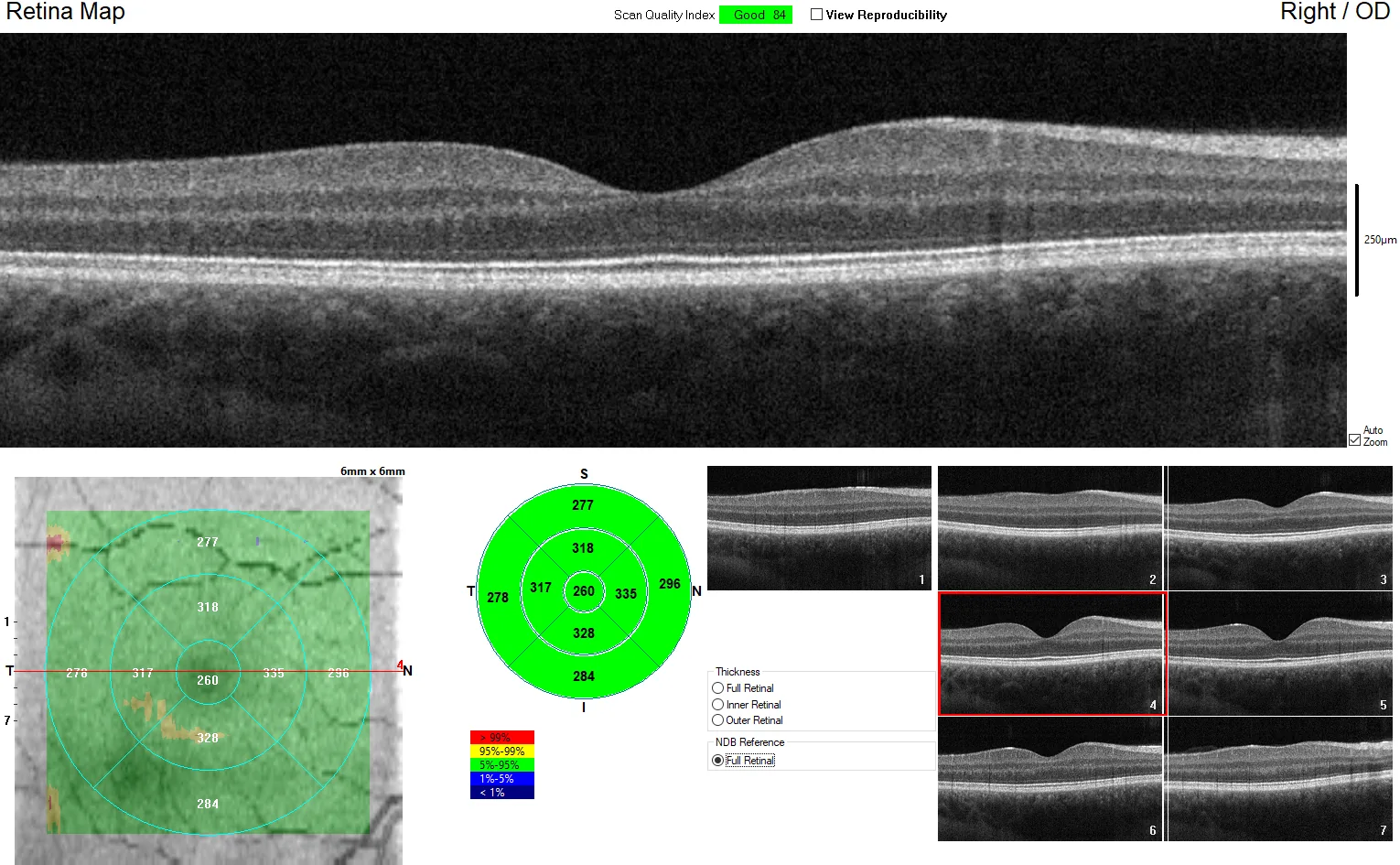
ساختار طبیعی لایهها در اسکن حفره مرکزی (از داخل به خارج) از ۱۳ لایه زیر تشکیل شده است:
زجاجیه ← غشای محدود کننده داخلی (ILM) ← لایه فیبرهای عصبی (RNFL) ← لایه سلولهای گانگلیونی (GCL) ← لایه شبکهای داخلی (IPL) ← لایه هستهای داخلی (INL) ← لایه شبکهای خارجی (OPL) ← لایه هستهای خارجی (ONL) ← غشای محدود کننده خارجی (ELM) ← ناحیه بیضیشکل (EZ) ← ناحیه بینانگشتی (IZ) ← اپیتلیوم رنگدانه شبکیه (RPE) ← مشیمیه
ویژگیهای بازتابی هر لایه منعکسکننده وضعیت پاتولوژیک است، بنابراین شناسایی دقیق لایهها اساس تفسیر تصاویر است.
| بیماری | یافتههای OCT شاخص |
|---|---|
| سوراخ ماکولا | نقص تمام ضخامت شبکیه ± VMT |
| غشای اپیرتینال (ERM) | لایه با بازتاب بالا روی غشای محدود کننده داخلی |
| کشیدگی زجاجیه-ماکولا (VMT) | جداشدگی جزئی زجاجیه خلفی و کشیدگی ماکولا |
| ادم ماکولای دیابتی | ضخیم شدن شبکیه، CME، DRIL، SRF |
| انسداد ورید شبکیه (RVO) | ادم ماکولای کیستی، مایع زیر شبکیه |
| دژنراسیون ماکولای وابسته به سن (AMD) | CNV (نوع 1/2/3)، جداشدگی اپیتلیوم رنگدانه |
| کوریورتینوپاتی سروز مرکزی (CSC) | جداشدگی شبکیه حسی-عصبی، ضخیم شدن مشیمیه در EDI-OCT |
| پارگی RPE | ناپدید شدن ناگهانی RPE و ساختار لایه خارجی |
سوراخ ماکولا به عنوان نقص تمام ضخامت شبکیه تصویر میشود. SD-OCT حساسترین و اختصاصیترین روش تشخیصی برای سوراخ ماکولا است1).
اپیرتینال ممبران (ERM) به عنوان یک لایه با بازتاب بالا روی غشای محدود کننده داخلی تشخیص داده میشود2). در مورد دید پس از جراحی، گزارش شده است که 80% موارد پس از ویترکتومی دو خط یا بیشتر بهبود بینایی دارند2).
در ادم ماکولای دیابتی، اندازهگیری کمی ضخامت شبکیه با OCT به عنوان شاخصی برای شروع درمان ضد VEGF و تصمیمگیری برای درمان مجدد استفاده میشود3). DRIL (Disorganization of Retinal Inner Layers) به عنوان یک نشانگر پیشآگهی ضعیف بینایی مهم است.
در RVO، OCT امکان ارزیابی کمی ادم ماکولا و تشخیص تغییرات سطح ویترئورتینال را فراهم میکند4).
در AMD، جداشدگی RPE به انواع سروزی، فیبروواسکولار و دروزنوئید طبقهبندی میشود و CNVM را میتوان به نوع 1 (زیر RPE)، نوع 2 (روی RPE) و نوع 3 (نئوواسکولاریزاسیون داخل شبکیه) تقسیم کرد5).
ناشی از شرایط تصویربرداری
آرتیفکت آینهای: به دلیل تنظیم نادرست محدوده تصویربرداری، تصویر واقعی به صورت معکوس و تکراری نمایش داده میشود.
وینیتینگ: تضعیف سیگنال در نواحی محیطی. به زاویه تابش نور بستگی دارد.
خطای خارج از محدوده: ساختارهایی که خارج از محدوده عمق تنظیم شده قرار دارند، به صورت تا شده نمایش داده میشوند.
عوامل مربوط به بیمار
آرتیفکت پلک زدن: پلک زدن در حین تصویربرداری باعث ایجاد نقص افقی میشود.
حرکت چشم: تثبیت ضعیف باعث جابجایی یا اعوجاج تصویر میشود.
جابجایی: ناشی از تغییر موقعیت سر در حین اسکن.
عوامل نرمافزاری
خطای سگمنتاسیون: الگوریتم جداسازی خودکار لایههای شبکیه را اشتباه تشخیص میدهد. این خطا در نواحی ضایعه، آب مروارید شدید یا نزدیکبینی بالا شایع است.
با اصلاح دستی یا اسکن مجدد قابل رفع است. اگر شاخص شدت سیگنال (SS) کمتر از 6 باشد، بررسی مجدد را در نظر بگیرید.
OCT بهویژه در تشخیص بیماریهای ناحیه ماکولا و قطب خلفی دقت بالایی دارد، اما برای تشخیص ضایعات شبکیه محیطی (مانند دژنراسیون شبکهای شبکیه و پارگی شبکیه) مناسب نیست. همچنین در موارد آب مروارید شدید یا کدورت زجاجیه، کیفیت تصویر کاهش یافته و قابلیت اطمینان تشخیص پایین میآید. برای ضایعات محیطی از عکسبرداری واید فاندوس و افتالموسکوپی غیرمستقیم استفاده میشود.
SD-OCT یک روش تصویربرداری غیرتماسی و غیرتهاجمی برای ارزیابی عینی آسیب ساختاری در گلوکوم است و در تشخیص گلوکوم کاربرد بالایی دارد 6). بهویژه در تشخیص گلوکوم پیش از بروز نقص میدان بینایی مفید است و میتواند تغییرات ساختاری را قبل از ظهور نقص میدان بینایی شناسایی کند 6)7).
ضخامت RNFL
اصل اندازهگیری: کمّیسازی ضخامت بین غشای محدود کننده داخلی (ILM) و مرز RNFL
نقشه TSNIT: ضخامت RNFL روی دایرهای به قطر 3.4 میلیمتر حول مرکز عصب بینایی به ترتیب T (گیجگاهی) → S (بالایی) → N (بینی) → I (پایینی) → T (گیجگاهی) نمایش داده میشود.
الگوی طبیعی: دو قله در جهت بالا و پایین نشان میدهد (منعکسکننده توزیع آناتومیک دستههای فیبر قوسی) 6)
قابلیت تشخیص گلوکوم: حساسیت 83% و ویژگی 88% برای میانگین ضخامت RNFL (سطح 5%). در سطح 1%، ویژگی 100% و حساسیت 65%.
پارامترهای ONH
تحلیل سر عصب بینایی: ترسیم خودکار سر عصب بینایی، حفره و لبه عصب
معیار غشای بروخ: لبه عصب با نقطه پایان غشای بروخ تعریف شده و کوتاهترین فاصله تا ILM محاسبه میشود.
شاخصهای با قدرت تشخیص بالا: ضخامت لبه عمودی، مساحت لبه و نسبت C/D عمودی بالاترین قدرت تشخیص را دارند 7)
BMO-MRW: ارزیابی عرض لبه بر اساس دهانه غشای بروخ با تکرارپذیری عالی 6)
تحلیل سلولهای گانگلیونی (GCA)
هدف اندازهگیری: ضخامت کمپلکس لایه سلولهای گانگلیونی (GCL) و لایه شبکهای داخلی (IPL) در اطراف ماکولا
نامهای مختلف بر اساس دستگاه: در Cirrus به نام GCIPL (GCL+IPL) و در Optovue به نام GCC (RNFL+GCL+IPL)
پارامترهای مفید: حداقل مقدار، بخش تمپورال تحتانی و مقدار متوسط از نظر تشخیصی مفیدترین هستند 6)7)
رابطه با اثر کف: پارامترهای ماکولا دیرتر از ضخامت RNFL دچار اثر کف میشوند و برای ارزیابی مراحل پیشرفته مفید هستند 6)
مقایسه با پایگاه داده چشمهای طبیعی مفید است، اما باید به علل زیر برای مثبت یا منفی کاذب توجه کرد.
برای تعیین پیشرفت گلوکوم دو رویکرد وجود دارد: تحلیل رویداد و تحلیل روند.
GPA در دستگاه Cirrus هر دو رویکرد را ادغام میکند7). حد قابل قبول تغییر در ضخامت متوسط RNFL بین ویزیتها 3.89 میکرومتر است و کاهش قابل تکرار بیش از 4 میکرومتر نشاندهنده تغییر آماری معنیدار است.
در گلوکوم پیشرفته، ضخامت RNFL تقریباً ثابت میماند و به دلیل باقیماندن بافتهای غیرعصبی مانند بافت گلیال و عروق، به ندرت به زیر 50 میکرومتر میرسد6)7). این «اثر کف» باعث کاهش کارایی بالینی SD-OCT در مراحل پایانی میشود و ارزیابی پیشرفت عمدتاً با تست میدان بینایی انجام میگیرد. پارامترهای ماکولا (GCIPL) دیرتر از ضخامت RNFL دچار اثر کف میشوند، بنابراین در مراحل پیشرفته نیز کارایی نسبی خود را حفظ میکنند6).
در چشمهای با نزدیکبینی شدید، مقایسه با پایگاه داده چشمهای طبیعی محدودیت دارد. دستههای RNFL به سمت تمپورال جابهجا میشوند، بنابراین حتی در حالت طبیعی نیز ممکن است «نازکشدگی» تشخیص داده شود. در این موارد، مقایسه سریالی با خط پایه خود بیمار مؤثر است. نازکشدگی پیشرونده در یک سری اسکنهای SD-OCT ارزیابی میشود. لازم به ذکر است که در افراد سالم نیز ضخامت RNFL با افزایش سن سالانه حدود 0.52 میکرومتر کاهش مییابد که باید در نظر گرفته شود.
استفاده از OCT در نورو-افتالمولوژی به سرعت در حال گسترش است9). ضخامت RNFL اطراف دیسک بینایی (cpRNFL) و GCIPL ماکولا (لایه سلولهای گانگلیونی + لایه پلکسیفرم داخلی) پارامترهای اصلی ارزیابی هستند و ممکن است تغییرات را قبل از بروز علائم بالینی آشکار یا اختلال عملکرد بینایی تشخیص دهند9).
| بیماری | یافتههای فاز حاد | یافتههای فاز مزمن |
|---|---|---|
| نوریت اپتیک | ضخیمشدگی RNFL (ادم آکسونی) یا طبیعی | نازکشدگی RNFL و GCIPL (6 ماه پس از شروع) |
| مولتیپل اسکلروزیس (MS) | کاهش cpRNFL حتی در موارد بدون علامت | در نوع پیشرونده، سرعت آتروفی RNFL و GCIPL افزایش مییابد |
| NMOSD | ادم پاپی | نازکشدگی شدید RNFL (<30 میکرومتر)، ادم ماکولار کیستیک میکرو (40% در AQP4 مثبت) 9) |
| نوروپاتی بینایی فشاری (مانند آدنوم هیپوفیز) | نازکشدگی دوگانه بینی GCIPL | آتروفی RNFL به شکل کراوات پروانهای (مطابق با همیانوپسی دوتمپورال) |
| NAION | ارزیابی RNFL به دلیل ادم پاپی دشوار است، نازکشدگی GCIPL زودتر رخ میدهد | نازکشدگی افقی تحتانی-بینی |
| درروزن عصب بینایی (ODD) | EDI-OCT استاندارد طلایی تشخیص است | حجم بالای ODD با نازکشدگی RNFL و نقص میدان بینایی مرتبط است |
| پاپیلای احتقانی | افزایش cpRNFL | نازک شدن GCIPL >10 میکرومتر → عملکرد بینایی ضعیف پس از 1 سال 9) |
نوریت اپتیک و مولتیپل اسکلروزیس (MS): نازک شدن RNFL و GCIPL یک بیومارکر تثبیتشده است 9). حتی در بیماران MS بدون علائم چشمی، کاهش cpRNFL مشاهده میشود و مطالعات پس از مرگ نشان داده است که 99٪ بیماران MS دارای ضایعات دمیلینه عصب بینایی هستند. ضخامت cpRNFL با بهترین دید اصلاحشده، حساسیت کنتراست، دید رنگی و آتروفی مغز همبستگی دارد.
NMOSD: با آتروفی شدید عصب بینایی مشخص میشود و فراوانی ادم ماکولار کیستیک میکرو (حدود 40٪ در AQP4 مثبت) به طور معنیداری بیشتر از MS (5٪) است 9). در نوریت اپتیک مرتبط با MOG-IgG، GCIPL نسبتاً حفظ میشود، در حالی که در مرتبط با AQP4-IgG به طور قابل توجهی از دست میرود 9).
درروزن سر عصب بینایی (ODD): EDI-OCT استاندارد طلایی برای تشخیص است 9). ODD ساختاری با بازتاب کم در بالای صفحه کریبریفرم با لبه بازتاب بالا است و توانایی تشخیصی بهتری نسبت به سونوگرافی B-scan، فلورسانس خودبهخودی و CT دارد. PHOMS (ساختارهای تخممرغی شکل با بازتاب بالا در اطراف پاپیلا) باید به عنوان پدیدهای جدا از ODD در نظر گرفته شود 9).
نوروپاتی فشاری عصب بینایی: ضخامت طبیعی RNFL قبل از عمل (≥70 میکرومتر) یک پیشبینیکننده معنیدار برای بهبود دید و میدان بینایی پس از عمل است 9) و ارزیابی OCT قبل از عمل برای پیشآگهی استفاده میشود.
از آنجایی که الگوریتمهای تقسیمبندی و پایگاههای داده نرمال بین دستگاهها متفاوت است، مقایسه عددی بین دستگاههای مختلف امکانپذیر نیست. برای ارزیابی طولی، استفاده از همان دستگاه توصیه میشود 9).
OCT بر اساس اصل تداخلسنج مایکلسون است. نور مادون قرمز نزدیک (طول موج 840-1050 نانومتر) به نور اندازهگیری و نور مرجع تقسیم میشود و به ترتیب به نمونه (فوندوس) و آینه مرجع تابانده میشود. با ترکیب مجدد نورهای بازتابی از هر دو، الگوی تداخل (اینترفرگرام) ایجاد میشود که از آن شدت بازتاب در هر عمق محاسبه میشود. پروفایل شدت بازتاب در جهت عمق، A-scan نامیده میشود و مجموعه A-scanها در جهت عرضی، B-scan (تصویر مقطعی) را تشکیل میدهد.
در گلوکوم و بیماریهای عصب بینایی، سه لایه زیر به طور اولویتدار ارزیابی میشوند9).
با آسیب RGC، RNFL تحلیل میرود. حدود 50٪ از کل RGCها در ناحیه 20 درجه مرکزی ماکولا متمرکز شدهاند و حتی در گلوکوم اولیه ممکن است حدود 50٪ از RGCها از بین رفته باشند6). SD-OCT تحلیل آکسونهای RGC را با ضخامت RNFL و نازکشدن لایه داخلی شامل اجسام سلولی را با GCA ارزیابی میکند.
تفاوت اصلی در طول موج استفاده شده و توانایی تجسم ساختارهای عمقی است. SD-OCT از باند 840 نانومتر و SS-OCT از باند 1050 نانومتر استفاده میکند. 1050 نانومتر پراکندگی کمتری توسط ملانین دارد و به راحتی از RPE عبور میکند، بنابراین SS-OCT برای مشاهده مشیمیه و صلبیه برتر است. همچنین سرعت تصویربرداری SS-OCT از SD-OCT بیشتر است و اسکن زاویه باز آسانتر است. از سوی دیگر، وضوح محوری هر دو حدود 5-7 میکرومتر است و تفاوت عمدهای ندارد.
قابلیت اسکن سریع و زاویه باز SS-OCT با طول موج 1050 نانومتر، ارزیابی طیف بیماری pachychoroid را پیشرفت داده است. دقت ارزیابی در کوریورتینوپاتی سروز مرکزی شامل ضخامت مشیمیه (pachydysm)، آنژیوپاتی پولیپوئیدال کوروئیدال (PCV) و تلانژکتازی پارافووهآل بهبود یافته و به روشنسازی پاتوفیزیولوژی کمک کرده است. همچنین تلاشهایی برای ارزیابی توموگرافی نواحی وسیع شامل شبکیه محیطی در همان تصویربرداری ماکولا در حال انجام است.
هوش مصنوعی تشخیص خودکار برای گلوکوم، AMD و DME توسعه یافته و بهبود دقت تشخیصی گزارش شده است. با تحلیل تصاویر OCT مبتنی بر یادگیری عمیق، بهبود دقت بخشبندی و تولید خودکار گزارشها در حال عملیاتی شدن است6)7).
برای اثبات کارایی OCT به عنوان ابزار غربالگری و پایش در بیماریهای تخریبکننده عصبی مانند آلزایمر و پارکینسون، مطالعات طولی مورد نیاز است9). نازک شدن RNFL و GCIPL در بیماران مبتلا به اختلال رفتاری خواب REM (RBD) به عنوان نشانگر جایگزین برای پارکینسون پیشدرمانی مورد توجه قرار گرفته است9).
American Academy of Ophthalmology Retina/Vitreous Panel. Idiopathic Macular Hole Preferred Practice Pattern. Ophthalmology. 2019.
American Academy of Ophthalmology Retina/Vitreous Panel. Idiopathic Epiretinal Membrane and Vitreomacular Traction Preferred Practice Pattern. Ophthalmology. 2019.
American Academy of Ophthalmology Retina/Vitreous Panel. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024.
American Academy of Ophthalmology Retina/Vitreous Panel. Retinal Vein Occlusions Preferred Practice Pattern. Ophthalmology. 2024.
American Academy of Ophthalmology Retina/Vitreous Panel. Age-Related Macular Degeneration Preferred Practice Pattern. Ophthalmology. 2024.
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
American Academy of Ophthalmology. Primary Open-Angle Glaucoma Preferred Practice Pattern®. 2020.
American Academy of Ophthalmology. Primary Open-Angle Glaucoma Suspect Preferred Practice Pattern®. 2020.
Lo C, Vuong LN, Micieli JA. Recent advances and future directions on the use of optical coherence tomography in neuro-ophthalmology. Taiwan J Ophthalmol. 2021;11(2):107-131.