
استئوما کوروئید
1. استئوم کوروئید چیست؟
Section titled “1. استئوم کوروئید چیست؟”استئوم کوروئید (choroidal osteoma) یک تومور خوشخیم است که در آن بافت استخوانی نابجا در داخل کوروئید تشکیل میشود. معمولاً در قطب خلفی چشم رخ میدهد و به صورت یک ضایعه زرد-سفید مسطح مشاهده میشود. علت ناشناخته است و نظریههای استئوم جداکننده (بافت استخوانی نابجا) و دخالت التهاب مطرح است.
در طول دوره، به دلیل پیگمانتاسیون، آتروفی اپیتلیوم رنگدانه شبکیه (RPE) و دکلسیفیکاسیون، یافتههای فوندوس تغییر میکند. تمایل به رشد آهسته دارد اما ضایعه در نهایت متوقف میشود.
اپیدمیولوژی
Section titled “اپیدمیولوژی”- یک تومور خوشخیم نسبتاً نادر است که بخش کوچکی از کل تومورهای داخل چشمی را تشکیل میدهد.
- در زنان جوان نسبتاً شایعتر است و ترشح هورمونها در ایجاد آن نقش دارد، اما علت آن ناشناخته است.
- ممکن است به صورت دوطرفه ایجاد شود.
- در قطب خلفی (به ویژه اطراف دیسک بینایی) شایعتر است.
مراحل پیشرفت بیماری
Section titled “مراحل پیشرفت بیماری”اگرچه سیستم طبقهبندی مشخصی وجود ندارد، مراحل زیر برای پیشرفت بیماری متمایز میشوند:
| مرحله | ویژگی |
|---|---|
| اولیه | ضایعات لکهای و مسطح به رنگ زرد-سفید یا زرد-نارنجی در قطب خلفی. برجستگی تقریباً وجود ندارد. |
| پیشرفته | دکلسیفیکاسیون، دژنراسیون و آتروفی لایههای RPE و خارجی شبکیه اضافه شده و نمای فوندوس تغییر میکند. |
| مرحله همراه با CNV | نئوواسکولاریزاسیون مشیمیه (CNV) ایجاد شده و منجر به خونریزی شبکیه و کاهش بینایی میشود. |
این یک تومور خوشخیم است که در آن بافت استخوانی نابجا در مشیمیه تشکیل میشود. معمولاً در قطب خلفی چشم رخ میدهد و در زنان جوان کمی شایعتر است. هیچ گزارشی از بدخیمی یا متاستاز وجود ندارد، اما اگر به ناحیه ماکولا گسترش یابد، باعث کاهش بینایی میشود. درمان قطعی وجود ندارد و پیگیری منظم اساس کار است.
2. علائم اصلی و یافتههای بالینی
Section titled “2. علائم اصلی و یافتههای بالینی”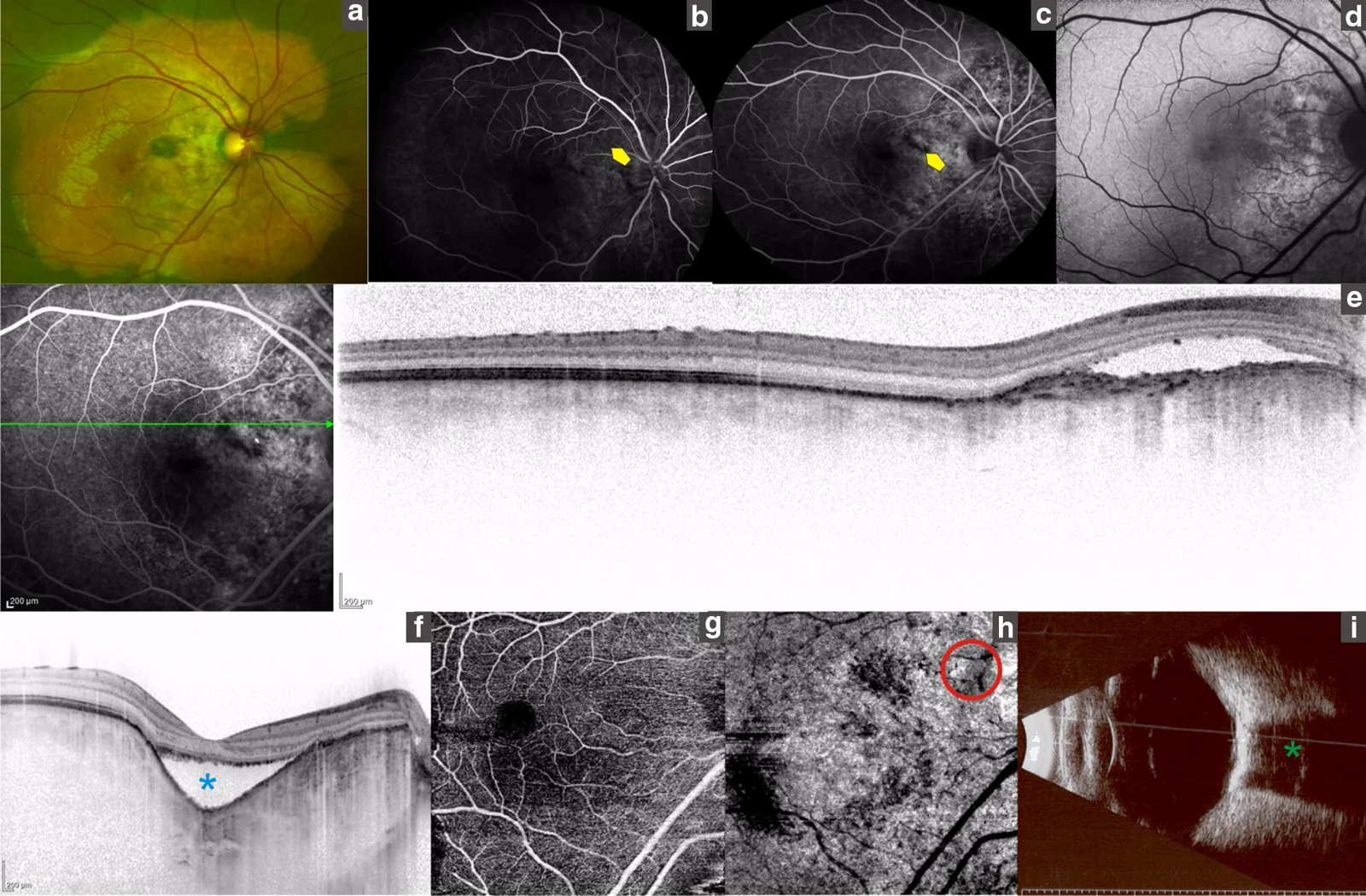
علائم ذهنی
Section titled “علائم ذهنی”- نقص میدان بینایی: متناسب با محل تومور ایجاد میشود. در مراحل اولیه ممکن است به سختی قابل توجه باشد.
- کاهش بینایی: اگر ضایعه به ماکولا گسترش یابد، کاهش شدید بینایی رخ میدهد.
- خونریزی شبکیه و زجاجیه: در صورت بروز CNV رخ میدهد و باعث کاهش ناگهانی بینایی میشود.
- اگر تومور به ماکولا گسترش نیابد، ممکن است علائم ذهنی کمی وجود داشته باشد.
یافتههای فوندوس
Section titled “یافتههای فوندوس”در قطب خلفی، به ویژه اطراف دیسک بینایی، یافتههای زیر مشاهده میشود:
- ضایعه لکهای به رنگ زرد-سفید تا زرد-نارنجی که تقریباً بدون برجستگی است و ممکن است ناهموار باشد.
- به صورت یک ضایعه برجسته زرد-سفید با مرز واضح و مسطح مشاهده میشود. اغلب با عروق ریز روی سطح تومور همراه است.
- با پیشرفت، دژنراسیون و آتروفی در RPE مجاور و لایههای خارجی شبکیه رخ میدهد و یافتههای فوندوس تغییر میکند.
یافتههای تصویربرداری
Section titled “یافتههای تصویربرداری”آنژیوگرافی فلورسین (FA):
- از مراحل اولیه، هیپرفلورسانس لکهای و دانهای منطبق با تومور دیده میشود.
- در مراحل بعدی، هیپرفلورسانس منتشر میشود.
- در صورت وجود CNV، نشت فلورسین مشاهده میشود.
سونوگرافی (B-mode):
- یک اکوی هایپررفلکتیو صفحهای در محل تومور و سایه آکوستیک (از بین رفتن یا کاهش اکو) در پشت آن مشاهده میشود.
سیتی اسکن (تشخیص قطعی):
- ناحیه تومور مقدار جذب بالایی (CT value بالا) مشابه استخوان نشان میدهد.
OCT:
- برای ارزیابی ارتفاع تومور، CNV و مایع زیرشبکیه مفید است.
3. علل و عوامل خطر
Section titled “3. علل و عوامل خطر”مکانیسم ایجاد استئوم کوروئید ناشناخته است. در حال حاضر فرضیههای زیر مطرح شدهاند:
- فرضیه کوریستوم: یک ناهنجاری مادرزادی که در آن بافت استخوانی نابجا در کوروئید تشکیل میشود.
- فرضیه التهابی: استخوانی شدن در پی التهاب رخ میدهد.
- فرضیه هورمونی: از آنجایی که در زنان جوان نسبتاً شایع است، ارتباط با ترشح هورمون مطرح شده است، اما مکانیسم دقیق آن مشخص نیست.
گزارشی از بدخیمی یا متاستاز وجود ندارد و خود تومور سیر خوشخیمی دارد.
4. تشخیص و روشهای آزمایش
Section titled “4. تشخیص و روشهای آزمایش”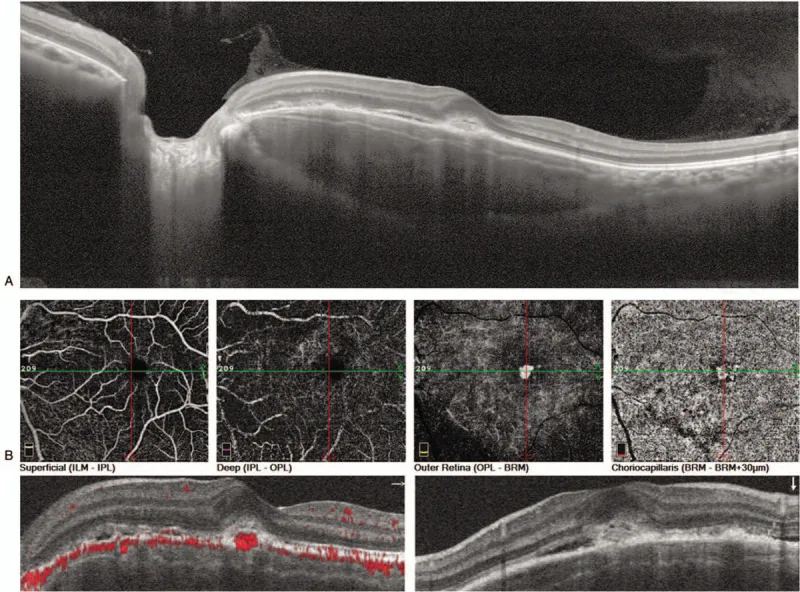
نکات تشخیصی
Section titled “نکات تشخیصی”ضایعه مسطح زرد-سفید در قطب خلفی (به ویژه اطراف دیسک بینایی) در معاینه فوندوس مشاهده میشود و تشخیص قطعی با CT و سونوگرافی انجام میشود.
- معاینه فوندوس: ضایعه مسطح زرد-سفید تا زرد-نارنجی در قطب خلفی. بزرگ شدن ضایعه، تغییرات RPE و وجود CNV ارزیابی میشود.
- CT (تشخیص قطعی): نشان دادن مقدار جذب بالا (CT value بالا) معادل استخوان در محل تومور، عامل تعیینکننده تشخیص قطعی است.
- سونوگرافی: تصویر بازتابی بالا به صورت صفحهای و سایه صوتی پشتی مشخصه است و از تشخیص حمایت میکند.
- آنژیوگرافی فلورسین (FA): هیپرفلورسانس لکهای-دانهای از مراحل اولیه و هیپرفلورسانس منتشر در مراحل پایانی مشاهده میشود. در صورت CNV، نشت فلورسین اضافه میشود.
- OCT: تغییرات RPE و شبکیه عصبی، مایع زیرشبکیه و وجود CNV را با جزئیات ارزیابی میکند.
تشخیص افتراقی
Section titled “تشخیص افتراقی”تشخیص افتراقی از بیماریهای همراه با کلسیفیکاسیون مهم است.
| بیماری | نکات افتراقی |
|---|---|
| رتینوبلاستوما | شایع در کودکان. توده سفید با کلسیفیکاسیون. ارزیابی با CT و سونوگرافی |
| آستروسیتومای هامارتوماتوز (مرتبط با توبروز اسکلروزیس) | ضایعه سفید در اطراف دیسک بینایی و قطب خلفی. همراه با کلسیفیکاسیون |
| ملانوم بدخیم کوروئید | برآمدگی گنبدی شکل و رنگدانهدار. الگوی دوگانه گردش خون در FA. بازتاب داخلی کم در سونوگرافی |
| متاستاز کوروئید | سابقه تومور بدخیم سیستمیک. ضایعات مسطح و متعدد. هیپرفلورسانس زودرس در FA |
| همانژیوم کوروئید | رنگ نارنجی-قرمز. الگوی مشخص در FA و ICGA. بازتاب بالا در سونوگرافی |
نشان دادن مقدار جذب بالا معادل استخوان در CT عامل تعیینکننده تشخیص قطعی است. همراه با سایه صوتی در سونوگرافی تشخیص داده میشود. در صورت مشاهده ضایعه مسطح زرد-سفید در قطب خلفی در معاینه فوندوس، به این بیماری مشکوک شده و با CT و سونوگرافی بررسی دقیق انجام میشود.
5. روشهای درمان استاندارد
Section titled “5. روشهای درمان استاندارد”اصول پایه: پیگیری
Section titled “اصول پایه: پیگیری”از آنجایی که درمان قطعی وجود ندارد، اساس کار پیگیری است. ارزیابی منظم بزرگ شدن تومور و وجود عروق جدید مهم است. تا زمانی که به ناحیه ماکولا گسترش نیابد، تأثیر بر عملکرد بینایی معمولاً جزئی است.
درمان هنگام بروز CNV
Section titled “درمان هنگام بروز CNV”در صورت تأیید وجود عروق جدید مشیمیه (CNV)، درمانهای علامتی زیر برای حفظ بینایی در نظر گرفته میشوند.
- انعقاد نوری (لیزر فوتوکوآگولاسیون): برای CNV انجام میشود. ضایعات خارج از ماکولا معمولاً مناسبتر هستند.
- درمان فتودینامیک (PDT): درمان فتودینامیک با ورتپورفین. اگرچه تحت پوشش بیمه نیست، اما اثرات مشخصی گزارش شده است.
- تزریق داخل زجاجیهای ضد VEGF: مانند رانیبیزوماب، آفلیبرسپت، بواسیزوماب. تحت پوشش بیمه نیست، اما انتظار میرود باعث پسرفت CNV شود.
اندیکاسیون و انتخاب درمان بر اساس موقعیت CNV، حدت بینایی و شرایط بیمار به صورت فردی تعیین میشود.
درمان قطعی وجود ندارد و اساساً پیگیری انجام میشود. در صورت بروز عروق جدید مشیمیه و کاهش بینایی، درمان علامتی با PDT یا تزریق داخل زجاجیهای ضد VEGF انجام میشود. از آنجایی که هر دو تحت پوشش بیمه نیستند، برنامه درمانی پس از مشورت کامل با پزشک معالج تعیین میشود.
۶. پاتوفیزیولوژی و مکانیسم دقیق بروز
Section titled “۶. پاتوفیزیولوژی و مکانیسم دقیق بروز”مکانیسم استخوانسازی نابجا
Section titled “مکانیسم استخوانسازی نابجا”ماهیت استئوم مشیمیه، استخوانسازی نابجا در داخل مشیمیه است. مکانیسم ایجاد بافت استخوانی در بافت طبیعی مشیمیه ناشناخته است، اما نکات زیر مشخص شده است.
- ضایعه به تدریج بزرگ میشود، اما تمایل به توقف در نهایت دارد.
- از آنجایی که در زنان جوان نسبتاً شایعتر است، نقش ترشح هورمونها حدس زده میشود، اما مکانیسم مولکولی ناشناخته است.
- نظریه کوریستوم استخوانی فرض میکند که بافت استخوانی به دلیل ناهنجاری جنینی در جای نادرست قرار گرفته است.
- نظریه التهابی القای استخوانسازی پس از التهاب را فرض میکند، اما اغلب سابقه التهابی واضحی تأیید نمیشود.
دکلسیفیکاسیون
Section titled “دکلسیفیکاسیون”در طول دوره، ممکن است دکلسیفیکاسیون تومور رخ دهد. هنگامی که دکلسیفیکاسیون رخ میدهد، مرز استئوم در فوندوس نامشخص شده و رنگ نیز تغییر میکند. گزارشهایی وجود دارد که پس از دکلسیفیکاسیون، CNV به راحتی ایجاد میشود. در مورد فراوانی دکلسیفیکاسیون و تأثیر کمی آن بر پیشآگهی بینایی، هنوز در حال جمعآوری موارد هستیم.
مکانیسم اختلال بینایی
Section titled “مکانیسم اختلال بینایی”- RPE و سلولهای گیرنده نوری که مستقیماً بالای تومور قرار دارند، به مرور زمان دچار دژنراسیون و آتروفی میشوند.
- هنگامی که CNV ایجاد میشود، نشت عروقی باعث مایع زیر شبکیه و خونریزی شبکیه شده و کاهش شدید بینایی رخ میدهد.
- اگر به ناحیه ماکولا گسترش یابد، گیرندههای نوری فووئا آسیب دیده و کاهش شدید بینایی رخ میدهد. کاهش بینایی که یک بار رخ داده است، بهبودی دشوار است.
پیشآگهی
Section titled “پیشآگهی”- تا زمانی که به ماکولا گسترش نیابد، اختلال عمدهای در عملکرد بینایی ایجاد نمیشود.
- اگر ضایعه به ماکولا برسد، کاهش شدید بینایی رخ میدهد و بهبودی قابل انتظار نیست.
- در موارد دوطرفه، حتی اگر پیشرفت یک چشم زودتر رخ دهد، باید به روند چشم دیگر توجه کرد.
- گزارشی از بدخیمی یا متاستاز وجود ندارد.
7. تحقیقات جدید و چشماندازهای آینده
Section titled “7. تحقیقات جدید و چشماندازهای آینده”کاربرد درمان ضد VEGF در CNV
Section titled “کاربرد درمان ضد VEGF در CNV”اگرچه تحت پوشش بیمه نیست، تزریق داخل زجاجیهای ضد VEGF با رانیبیزوماب یا آفلیبرسپت در موارد همراه با CNV استفاده شده است. گزارشهای موردی و سریهای کوچک، پسرفت CNV و بهبود بینایی را گزارش کردهاند، اما در حال حاضر هیچ کارآزمایی تصادفیسازی شدهای در مورد پروتکل درمانی (فاصله، تعداد، ترکیب با سایر درمانها) وجود ندارد. انتظار میرود شواهد بیشتری در آینده جمعآوری شود.
ارزیابی دقیق با OCT و OCT-A
Section titled “ارزیابی دقیق با OCT و OCT-A”پیشرفت در آنژیوگرافی OCT (OCT-A) امکان ارزیابی غیرتهاجمی و دقیق ساختار عروقی CNV را فراهم کرده است. ارزیابی کمی CNV با استفاده از OCT-A در استئوم کوروئید و کاربرد آن در پیگیری، از چالشهای آینده است.
شناسایی مکانیسم دکلسیفیکاسیون
Section titled “شناسایی مکانیسم دکلسیفیکاسیون”مکانیسم مولکولی علت دکلسیفیکاسیون و اینکه چرا پس از آن CNV مستعدتر رخ میدهد، هنوز ناشناخته است. تحقیقات در مورد ارتباط با عوامل متابولیسم استخوان (مانند RANKL و OPG) در حال انجام است.
8. منابع
Section titled “8. منابع”- Shields CL, Sun H, Demirci H, et al. Factors predictive of tumor growth, tumor decalcification, choroidal neovascularization, and visual outcome in 74 eyes with choroidal osteoma. Arch Ophthalmol. 2005;123(12):1658-1666.
- Shields JA, Shields CL. Intraocular Tumors: An Atlas and Textbook. 3rd ed. Philadelphia: Wolters Kluwer; 2015.
- Tsui I, Gillies MC, Barlow R, et al. Photodynamic therapy for choroidal neovascularization complicating choroidal osteoma. Retina. 2006;26(7):804-810.
- Nadarajah S, Blumenkranz MS. Intravitreal bevacizumab for choroidal neovascularization secondary to choroidal osteoma. Retina. 2009;29(6):888-890.
