
آنژیوم منتشر کوروئید
1. همانژیوم منتشر مشیمیه چیست؟
Section titled “1. همانژیوم منتشر مشیمیه چیست؟”تعریف و مفهوم
Section titled “تعریف و مفهوم”دو نوع همانژیوم مشیمیه وجود دارد: موضعی (انفرادی) و منتشر. نوع موضعی دارای مرز مشخص و پراکنده است، اما نوع منتشر اغلب تومور گسترده و با مرز نامشخص دارد. همانژیوم منتشر مشیمیه تقریباً همیشه با سندرم استورج-وبر (آنژیوماتوز صورت و مغز) مرتبط است.
سندرم استورج-وبر یکی از فاکوماتوزها (سندرمهای عصبی-پوستی) است که در اثر تکثیر نابجای سلولهای تاج عصبی در دوره جنینی ایجاد میشود. مشخصه آن تشکیل همانژیوم در صورت، چشم و لپتومننژ مغز است.
اپیدمیولوژی
Section titled “اپیدمیولوژی”فراوانی سندرم استورج-وبر 1 در 20000 تا 50000 نفر تخمین زده میشود. این بیماری ارثی نیست و عمدتاً ناشی از جهش موزاییک سوماتیک ژن GNAQ است که به صورت پراکنده رخ میدهد. این یک بیماری مادرزادی است که از بدو تولد وجود دارد و در دوران نوزادی یا کودکی تشخیص داده میشود. در بیمارانی که همانژیوم پوستی (لکه شرابی) در ناحیه توزیع شاخههای اول و دوم عصب سهقلو دارند، در همان سمت فوندوس چشم ایجاد میشود. دادههای واضحی در مورد تفاوت جنسیتی و نژادی وجود ندارد، اما به عنوان یک بیماری پراکنده میتواند در همه نژادها رخ دهد.
مقایسه با همانژیوم موضعی مشیمیه
Section titled “مقایسه با همانژیوم موضعی مشیمیه”| ویژگی | همانژیوم منتشر مشیمیه | همانژیوم موضعی (انفرادی) مشیمیه |
|---|---|---|
| سندرم همراه | همراه با سندرم استورج-وبر (اجباری) | بدون بیماری سیستمیک (پراکنده) |
| توزیع در فوندوس | گسترده و با مرز نامشخص | موضعی و با مرز نسبتاً مشخص |
| رنگ | فوندوس سس گوجهفرنگی | ضایعه برجسته نارنجی |
| همراهی با گلوکوم | بیش از نیمی از موارد | نادر |
| زمان بروز | مادرزادی / دوران نوزادی | بیشتر در بزرگسالی |
همانژیوم منتشر کوروئید تقریباً همیشه همراه با سندرم استورج-وبر (آنژیوماتوز صورت-مغز) رخ میدهد. در سندرم استورج-وبر، سهگانه لکه شرابی صورت، آنژیوم لپتومننژ، و علائم چشمی (همانژیوم منتشر کوروئید و گلوکوم) دیده میشود. شیوع آن 1 در 20,000 تا 50,000 نفر است و ارثی نیست. همانژیوم در فوندوس همان طرف لکه شرابی صورت ایجاد میشود.
2. علائم اصلی و یافتههای بالینی
Section titled “2. علائم اصلی و یافتههای بالینی”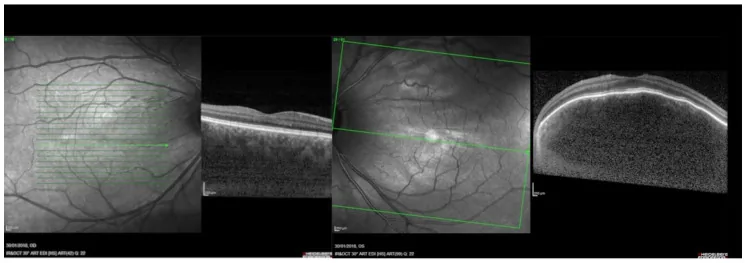
یافتههای فوندوس
Section titled “یافتههای فوندوس”بارزترین یافته فوندوسکوپی در همانژیوم منتشر کوروئید، «فوندوس سس گوجهفرنگی» است که در آن تمام فوندوس به طور گسترده به رنگ نارنجی-قرمز درمیآید. تومور ناحیه وسیعی از کوروئید را اشغال کرده و مرزهای آن نامشخص است. در عکسبرداری معمولی فوندوس، این حالت به صورت تفاوت قرمزی قابل توجه نسبت به فوندوس طبیعی قابل تشخیص است.
یافتههای اصلی فوندوسکوپی و چشمی به شرح زیر است:
- ضخیم شدن منتشر کوروئید: کوروئید از قطب خلفی تا نواحی محیطی به طور گسترده ضخیم میشود
- مرزهای نامشخص: برخلاف همانژیوم موضعی، لبه تومور واضح نیست
- جداشدگی سروزی شبکیه: علت اصلی کاهش بینایی. باعث نقص میدان بینایی و دگرگونی بینایی میشود
- دوربینی شدن: برجستگی کوروئید باعث تغییر انکسار در جهت محوری چشم میشود
- ضایعه برجسته نارنجی: در قطب خلفی به صورت برجستگی نارنجی قابل مشاهده است
یافتههای آنژیوگرافی فلورسئین و تصویربرداری
Section titled “یافتههای آنژیوگرافی فلورسئین و تصویربرداری”یافتههای مشخص در بررسیهای تصویربرداری مختلف به شرح زیر است:
- FA (آنژیوگرافی فلورسئین): از مراحل اولیه آنژیوگرافی، هیپرفلورسانس شبکهای در داخل تومور دیده میشود و در مراحل پایانی، تجمع رنگ افزایش مییابد (الگوی منتشر)
- ICGA (آنژیوگرافی با ایندوسیانین سبز): نسبت به FA در نمایش عروق کوروئید برتر است و ساختار عروقی داخل تومور به وضوح قابل تشخیص است
- OCT: به صورت برجستگی موضعی گسترده کوروئید در قطب خلفی مشاهده میشود. همچنین برای ارزیابی جداشدگی سروزی شبکیه مفید است
- سونوگرافی: به صورت ضایعه برجسته جامد دیده میشود. در B-scan ضخیم شدن گسترده کوروئید قابل تأیید است
- CT: مشابه سونوگرافی، به صورت ضایعه جامد دیده میشود
همراهی با گلوکوم
Section titled “همراهی با گلوکوم”در سندرم استورج-وبر، بیش از نیمی از موارد با گلوکوم همراه است. بر اساس زمان شروع، تقریباً نیمی از موارد در دوران نوزادی (نوع مادرزادی) و نیمی در دوران کودکی (نوع اکتسابی) مشاهده میشود.
- نوع شروع در دوران نوزادی: ویژگیهای گلوکوم مادرزادی مانند افزایش قطر قرنیه، بوفتالموس (بزرگ شدن قرنیه) و خطوط هاب را نشان میدهد. اغلب نیاز به جراحی دارد.
- نوع شروع در دوران کودکی: فشار چشم ابتدا در محدوده طبیعی تثبیت میشود، اما ممکن است در طول پیگیری افزایش یابد.
- همانژیوم اپیاسکلرال: در برخی موارد، همانژیوم در اپیاسکلر سمت مبتلا دیده میشود.
بیش از نیمی از موارد سندرم استورج-وبر با گلوکوم همراه است. نیمی از موارد در دوران نوزادی و نیمی در دوران کودکی شروع میشود و ممکن است در طول پیگیری افزایش فشار چشم رخ دهد. اگر گلوکوم به درستی مدیریت نشود، میتواند منجر به اختلال میدان بینایی و کاهش بینایی شود، بنابراین اندازهگیری منظم فشار چشم و معاینه فوندوس در طولانی مدت ضروری است. به ویژه، بوفتالموس و کدورت قرنیه در دوران نوزادی نیاز به مداخله فوری دارند.
3. علل و عوامل خطر
Section titled “3. علل و عوامل خطر”مکانیسم بروز
Section titled “مکانیسم بروز”بروز سندرم استورج-وبر و همانژیوم کوروئید منتشر ناشی از تکثیر نابجای سلولهای تاج عصبی در دوره جنینی است. هامارتوم عروقی کوروئید تشکیل میشود و ساختار طبیعی کوروئید به طور گسترده با بافت عروقی جایگزین میشود.
در سطح ژنتیکی، جهش در ژن GNAQ (پروتئین اتصالدهنده گوانین نوکلئوتید Gqα) (c.548G>A, p.Arg183Gln) در بسیاری از موارد شناسایی میشود. این جهش به صورت موزاییک سوماتیک رخ میدهد، بنابراین ارثی نیست و اصولاً از والدین به فرزند منتقل نمیشود. تصور میشود که جهش GNAQ فعالیت GTPase را کاهش داده و سیگنالهای رگزایی را به طور مداوم فعال میکند.
عوامل خطر و ویژگیهای اصلی
Section titled “عوامل خطر و ویژگیهای اصلی”- جهش موزاییک سوماتیک GNAQ: مهمترین جهش علتساز. جهش خط زایا نیست و ارثی نیست.
- بیماری مادرزادی: از بدو تولد وجود دارد، بنابراین جهش اتفاقی دوران جنینی عامل اصلی است تا زمینه ژنتیکی.
- عوامل محیطی: هیچ عامل خطر محیطی ثابت شدهای وجود ندارد.
- سابقه خانوادگی: اصولاً ارثی نیست، بنابراین تجمع خانوادگی معمولاً مشاهده نمیشود.
پاتوژنز گلوکوم
Section titled “پاتوژنز گلوکوم”دو مکانیسم اصلی در ایجاد گلوکوم در سندرم استورج-وبر نقش دارند.
- افزایش فشار وریدی اپیاسکلرا: همانژیوم اپیاسکلرا فشار وریدی را افزایش داده و مقاومت در برابر خروج زلالیه را زیاد میکند. این مکانیسم در گلوکوم پس از دوران کودکی شایعتر است.
- ناهنجاری زاویه اتاق قدامی: ناهنجاری رشدی زاویه اتاق قدامی باعث اختلال در خروج زلالیه میشود. این مکانیسم اغلب با گلوکوم دوران شیرخوارگی مرتبط است.
4. تشخیص و روشهای آزمایش
Section titled “4. تشخیص و روشهای آزمایش”رویکرد تشخیصی
Section titled “رویکرد تشخیصی”ترکیب لکه شرابی صورت (همانژیوم پوستی در ناحیه عصب سهقلو) و تغییرات فوندوس همطرف به شدت از تشخیص همانژیوم کوروئید منتشر حمایت میکند. برای تشخیص چشمی از آزمایشهای زیر استفاده میشود.
معاینه فوندوس و تصویربرداری:
- عکس فوندوس (شامل عکسبرداری واید): ثبت فوندوس سس گوجهای و پیگیری
- FA/ICGA: تأیید هیپرفلورسانس مشبک اولیه (الگوی منتشر)
- OCT: ارزیابی ضخیمشدگی گسترده کوروئید و جداشدگی سروز شبکیه
- سونوگرافی (A-scan و B-scan): تأیید ضایعه جامد و اندازهگیری ضخامت
بررسی سیستمیک:
- MRI مغز: آنژیوم لپتومننژ و کلسیفیکاسیون (همراه با یافتههای چشمی توسط متخصص مغز و اعصاب کودکان ارزیابی میشود)
- اندازهگیری فشار داخل چشم: غربالگری گلوکوم (در صورت نیاز تحت بیهوشی عمومی)
- گونیوسکوپی: ارزیابی ناهنجاریهای زاویه اتاق قدامی
تشخیص افتراقی
Section titled “تشخیص افتراقی”بیماریهایی که نیاز به تشخیص افتراقی با همانژیوم منتشر کوروئید دارند در زیر آورده شده است.
| بیماری افتراقی | تفاوتهای اصلی |
|---|---|
| همانژیوم موضعی کوروئید | مرز مشخص، موضعی، بدون سندرم سیستمیک |
| ملانوم بدخیم کوروئید (نوع منتشر) | یافتههای بدخیم، تغییرات رنگدانهای، خطر متاستاز |
| یووئیت خلفی | یافتههای التهابی، کدورت زجاجیه |
| تغییر رنگ طبیعی فوندوس | بدون یافتههای سیستمیک سندرم استورج-وبر |
نکات مهم در زمان تشخیص
Section titled “نکات مهم در زمان تشخیص”اگر ته چشم «به نوعی قرمز» به نظر برسد، به ویژه در نوزادان و کودکان خردسال همراه با لکه شرابی، باید به این بیماری مشکوک شد. در نوزادان و کودکان خردسال ممکن است معاینه نیاز به بیهوشی عمومی داشته باشد و همکاری با متخصص بیهوشی و پزشک اطفال مهم است.
5. روشهای درمانی استاندارد
Section titled “5. روشهای درمانی استاندارد”خلاصه رویکرد درمانی
Section titled “خلاصه رویکرد درمانی”درمان همانژیوم منتشر کوروئید به صورت مرحلهای و بر اساس وجود یا عدم وجود علائم و نوع عوارض انجام میشود. معمولاً خود همانژیوم کوروئید با جراحی برداشته نمیشود. هدف اصلی درمان، جداشدگی سروزی شبکیه (علت اصلی کاهش بینایی) و گلوکوم است.
1. پیگیری
Section titled “1. پیگیری”در صورت عدم وجود علائم و عدم مشکل در بینایی و فشار چشم، پیگیری منظم زیر ادامه مییابد:
- اندازهگیری فشار چشم (تشخیص زودهنگام گلوکوم)
- عکسبرداری از ته چشم و OCT برای بررسی وجود جداشدگی سروزی شبکیه
- بررسی بینایی و عیوب انکساری (ارزیابی دوربینی و تنبلی چشم)
- در صورت لزوم، پیگیری با FA/OCT
2. درمان جداشدگی سروزی شبکیه و کاهش عملکرد بینایی
Section titled “2. درمان جداشدگی سروزی شبکیه و کاهش عملکرد بینایی”در صورت مشاهده کاهش بینایی یا جداشدگی سروزی شبکیه، درمان فعال انجام میشود.
- تزریق داخل وریدی ورتپورفین (حساسکننده نوری) و سپس تابش لیزر با طول موج 689 نانومتر
- اثربخشی PDT برای همانژیوم مشیمیه گزارش شده است
- غیرقابل پوشش بیمه (برای همانژیوم منتشر مشیمیه)
- میتوان انتظار بهبود جداشدگی سروزی شبکیه و بهبود بینایی را داشت
- اثربخشی برای همانژیوم موضعی مشیمیه ثابت شده است، اما برای نوع منتشر به دلیل وسعت ناحیه تابش، محدودیتهای فنی وجود دارد
پرتو درمانی با دوز پایین:
- تابش با دوز پایین حدود 20 گری انجام میشود
- گاهی مؤثر است. میتوان انتظار بهبود جداشدگی شبکیه و بهبود بینایی را داشت
- اغلب از پرتودهی خارجی (تلهتراپی) استفاده میشود
معمولاً برداشت جراحی انجام نمیشود. همانژیوم منتشر مشیمیه به طور گسترده کل مشیمیه را درگیر میکند، بنابراین برداشت جراحی هم از نظر فنی و هم از نظر عملکردی دشوار است. برای جداشدگی سروزی شبکیه که باعث کاهش بینایی میشود، PDT یا پرتودرمانی با دوز پایین (حدود 20 گری) انجام میشود که اغلب مؤثر است. برای گلوکوم، فشار چشم با قطره یا جراحی کنترل میشود.
3. درمان گلوکوم
Section titled “3. درمان گلوکوم”از آنجایی که بیش از نیمی از موارد با گلوکوم همراه هستند، مدیریت آن یک موضوع درمانی مهم است.
درمان دارویی (قطره چشمی):
- داروهای مرتبط با پروستاگلاندین (مهار تولید زلالیه و افزایش خروج آن)
- مسدودکنندههای بتا (مهار تولید زلالیه)
- مهارکنندههای کربنیک آنهیدراز (موضعی یا خوراکی)
- با این حال، در گلوکوم ناشی از افزایش فشار ورید اپیاسکلرال، اثر قطرههای چشمی ممکن است محدود باشد
درمان جراحی:
- در نوع مادرزادی (شروع در شیرخوارگی) گونیوتومی و ترابکولوتومی انجام میشود
- در نوع بزرگسالی، جراحی فیلتراسیون (ترابکولکتومی و شانت لولهای) در نظر گرفته میشود
- در صورت بالا بودن فشار ورید اپیاسکلرال، مراقبتهای پس از ترابکولکتومی نیاز به دقت دارد
4. مدیریت سیستمیک
Section titled “4. مدیریت سیستمیک”- مدیریت صرع: کنترل تشنج با داروهای ضدصرع (متخصص مغز و اعصاب کودکان)
- مدیریت تأخیر رشد ذهنی: مداخله زودهنگام و ایجاد سیستم حمایتی
- سردرد و همیپارزی: پیگیری علائم عصبی و درمان علامتی
- همکاری چندتخصصی: هماهنگی بین چشمپزشک، متخصص مغز و اعصاب کودکان، متخصص پوست، متخصص صرع و تیم توانبخشی
6. پاتوفیزیولوژی و مکانیسم دقیق بروز
Section titled “6. پاتوفیزیولوژی و مکانیسم دقیق بروز”ماهیت به عنوان هامارتوم عروقی
Section titled “ماهیت به عنوان هامارتوم عروقی”آنژیوم منتشر کوروئید از نظر جنینشناسی به عنوان یک هامارتوم عروقی در نظر گرفته میشود. هامارتوم یک ضایعه خوشخیم شبه توموری است که در آن اجزای بافتی طبیعی آن ناحیه به طور غیرطبیعی تکثیر مییابند و با نئوپلاسم واقعی متفاوت است. در این بیماری، عناصر عروقی بالغ به طور بیش از حد در داخل کوروئید تکثیر میشوند و ساختار طبیعی لایه مویرگی کوروئید و عروق متوسط و بزرگ را جایگزین میکنند.
جهش ژن GNAQ و مکانیسم مولکولی
Section titled “جهش ژن GNAQ و مکانیسم مولکولی”به عنوان اساس مولکولی سندرم استورج-وبر، جهش موزاییک سوماتیک در ژن GNAQ (c.548G>A, p.Arg183Gln) در بسیاری از موارد شناسایی شده است.
- عملکرد GNAQ (Gqα): زیرواحد Gα درگیر در سیگنالدهی پاییندستی گیرندههای جفت شده با پروتئین G (GPCR)
- تأثیر جهش: جهش Arg183Gln باعث کاهش فعالیت GTPase میشود و GNAQ را در حالت فعال دائمی نگه میدارد
- سیگنالدهی پاییندستی: فعالسازی PLC-β از طریق Gq → تولید IP3/DAG → فعالسازی PKC → فعالسازی دائمی آبشار MAPK (MEK/ERK)
- تأثیر بر رگزایی: تصور میشود که تولید بیش از حد فاکتورهای رگزایی مانند VEGF افزایش یافته و باعث تشکیل عروق غیرطبیعی میشود
- اهمیت جهش موزاییک سوماتیک: از آنجایی که جهش تنها در برخی سلولها در اوایل جنینزایی رخ میدهد، الگوی بیان در افراد مختلف متفاوت است و منجر به تنوع علائم میشود
مکانیسم دقیق بروز گلوکوم
Section titled “مکانیسم دقیق بروز گلوکوم”حداقل دو مکانیسم برای بروز گلوکوم در سندرم استورج-وبر در نظر گرفته شده است.
مکانیسم 1: افزایش فشار ورید اپیاسکلرا همانژیوم در اپیاسکلرا (زیر تونکا تنون) فشار ورید اپیاسکلرا را افزایش میدهد و خروج زلالیه از کانال اشلم و ترابکولوم را مختل میکند. اگر فشار ورید اپیاسکلرا از مقدار طبیعی (حدود 10 میلیمتر جیوه) فراتر رود، فشار داخل چشم به همان میزان افزایش مییابد. این مکانیسم در گلوکوم اکتسابی که پس از دوران کودکی بروز میکند شایعتر است.
مکانیسم 2: ناهنجاری زاویه اتاق قدامی ناهنجاری رشدی زاویه اتاق قدامی (دیسژنزیس زاویه) باعث رشد ناقص ترابکولوم میشود و مسیر خروج زلالیه از نظر آناتومیک غیرعملکردی میشود. این مکانیسم اغلب با بروز در دوران نوزادی (نوع گلوکوم مادرزادی) مرتبط است.
مکانیسم بروز جداشدگی سروز شبکیه
Section titled “مکانیسم بروز جداشدگی سروز شبکیه”افزایش نفوذپذیری عروق در آنژیوم منتشر کوروئید باعث تراوش اجزای داخل عروقی به خارج از عروق و تجمع مایع در فضای زیر شبکیه میشود. این امر منجر به جداشدگی سروز شبکیه میشود که علت اصلی کاهش بینایی و نقص میدان بینایی است. با PDT یا پرتودرمانی، عروق توموری کاهش یافته، تراوش کاهش مییابد و شبکیه دوباره به جای خود برمیگردد.
پاتوفیزیولوژی خارج چشمی
Section titled “پاتوفیزیولوژی خارج چشمی”- مننژیوم عروقی مغز: همانژیوم قشر مغز باعث ایسکمی موضعی و کلسیفیکاسیون شده و علت صرع، تأخیر رشد ذهنی و همی پارزی میشود.
- لکه شراب پورت صورت: به صورت اتساع مویرگهای پوست از بدو تولد قابل مشاهده است.
- کلسیفیکاسیون: کلسیفیکاسیون به شکل «ریل راهآهن» در قشر مغز زیر مننژیوم عروقی، ویژگی تصویربرداری سندرم استورج-وبر است.
7. تحقیقات جدید و چشمانداز آینده
Section titled “7. تحقیقات جدید و چشمانداز آینده”درمان هدفمند مولکولی با هدف قرار دادن مسیر پاییندست GNAQ
Section titled “درمان هدفمند مولکولی با هدف قرار دادن مسیر پاییندست GNAQ”آبشار MAPK (مسیر MEK/ERK) که به دلیل جهش GNAQ به طور مداوم فعال شده است، در تحقیقات ملانوم یووه آ به عنوان هدف درمانی به طور گسترده مطالعه شده است. از آنجایی که ناهنجاری مولکولی یکسانی در سندرم استورج-وبر/همانژیوم کروئید منتشر وجود دارد، کاربرد مهارکنندههای MEK (مانند ترامتینیب، بینیمتینیب) و مهارکنندههای مستقیم GNAQ (مانند YM-254890) در سطح تحقیقات پایه در حال بررسی است.
در واقع، به عنوان درمان هدفمند مولکولی برای کل سندرم استورج-وبر، درمان با مهارکننده mTOR (سیرولیموس) و درمان هدفمند مسیر PI3K-AKT-mTOR به صورت آزمایشی انجام شده است و در برخی بیماران بهبود علائم گزارش شده است. با این حال، مطالعات بزرگی که به طور مستقیم اثربخشی را بر روی خود همانژیوم کروئید منتشر ارزیابی کنند، در حال حاضر محدود است.
بهینهسازی درمان PDT
Section titled “بهینهسازی درمان PDT”PDT در چندین گزارش موردی برای جداشدگی سروزی شبکیه ناشی از همانژیوم کروئید منتشر مؤثر نشان داده شده است، اما پروتکل (میدان تابش، انرژی، تعداد جلسات) برای ضایعات منتشر گسترده استاندارد نشده است. در مقایسه با همانژیوم کروئید موضعی، در نوع منتشر سطح تابش بزرگتر است و چالشهای فنی وجود دارد. انتظار میرود که در آینده با مطالعات آیندهنگر چندمرکزی تثبیت شود.
پیشرفتهای جدید در مدیریت گلوکوم
Section titled “پیشرفتهای جدید در مدیریت گلوکوم”جراحی فیلتراسیون سنتی برای گلوکوم ناشی از افزایش فشار ورید اپیاسکلرا، در شرایط فشار بالای ورید اپیاسکلرا خطر ترشح کروئید و گلوکوم بدخیم را دارد. در مقابل، تحقیقات در مورد اثربخشی جراحی شنت لولهای (دریچه احمد، لوله بائرولت) در حال پیشرفت است. همچنین، امکان کاربرد لیزر انتخابی ترابکولوپلاستی (SLT) نیز در حال بررسی است.
چشمانداز تشخیص ژنتیکی GNAQ
Section titled “چشمانداز تشخیص ژنتیکی GNAQ”تشخیص قطعی سندرم استورج-وبر با تشخیص جهش GNAQ در نمونههای بیوپسی پوست و خون در حال کاربرد است. انتظار میرود در آینده با تشخیص زودهنگام از طریق بیوپسی مایع (ctDNA) و بهبود نرخ تشخیص جهش، تشخیص قطعیتری ممکن شود.
8. منابع
Section titled “8. منابع”- Shirley MD, Tang H, Gallione CJ, et al. Sturge-Weber syndrome and port-wine stains caused by somatic mutation in GNAQ. N Engl J Med. 2013;368(21):1971-1979.
- Baselga E, Torrelo A, Mediero IG, et al. Sturge-Weber syndrome: report of 3 cases. Pediatr Dermatol. 2019;36(6):932-934.
- Bhatt A, Bhatt N. Sturge-Weber syndrome: a rare neurocutaneous disorder. J Pediatr Neurosci. 2021;16(1):1-6.
- Zreik O, Elabassy HM, Bakhurji E, Al-Johani SM. Sturge-Weber syndrome: an updated review. Clin Ophthalmol. 2023;17:2369-2381.
- Nassiri N, Rootman DB, Rootman J, Goldberg RA. Orbital and adnexal lymphangiomas: a review of management. Surv Ophthalmol. 2015;60(3):245-257.
