
หลอดเลือดดำคอรอยด์ผิดปกติแบบกระจาย
1. Hemangioma คอรอยด์แบบกระจายคืออะไร?
หัวข้อที่มีชื่อว่า “1. Hemangioma คอรอยด์แบบกระจายคืออะไร?”คำจำกัดความและแนวคิด
หัวข้อที่มีชื่อว่า “คำจำกัดความและแนวคิด”เนื้องอกหลอดเลือดคอรอยด์มีสองประเภท: แบบจำกัดขอบเขต (เดี่ยว) และแบบกระจาย แบบจำกัดขอบเขตมีขอบเขตชัดเจนและเกิดขึ้นเป็นครั้งคราว ในขณะที่แบบกระจายมีขอบเขตกว้างและมักไม่ชัดเจน เนื้องอกหลอดเลือดคอรอยด์แบบกระจายเกือบทั้งหมดเกี่ยวข้องกับกลุ่มอาการสเตอร์จ-เวเบอร์ (โรคหลอดเลือดสมอง-ใบหน้า)
กลุ่มอาการสเตอร์จ-เวเบอร์เป็นหนึ่งในโรคเนื้องอกผิวหนัง (กลุ่มอาการผิวหนัง-ประสาท) ซึ่งเกิดจากการเจริญเติบโตผิดตำแหน่งของเซลล์ประสาทคริสต้าในระยะตัวอ่อน มีลักษณะเฉพาะคือการเกิดเนื้องอกหลอดเลือดที่ใบหน้า ตา และเยื่อหุ้มสมองชั้นใน
ระบาดวิทยา
หัวข้อที่มีชื่อว่า “ระบาดวิทยา”อุบัติการณ์ของกลุ่มอาการสเตอร์จ-เวเบอร์ประมาณ 1 ใน 20,000 ถึง 50,000 คน ไม่มีการถ่ายทอดทางพันธุกรรม สาเหตุหลักคือการกลายพันธุ์แบบโมเสกในร่างกายของยีน GNAQ ที่เกิดขึ้นอย่างกะทันหัน เป็นโรคที่มีมาแต่กำเนิดตั้งแต่เกิด พบได้ในวัยทารกหรือเด็กเล็ก เกิดขึ้นที่จอตาด้านเดียวกับเนื้องอกหลอดเลือดที่ผิวหนัง (ปานสีไวน์) ในบริเวณที่เส้นประสาทไทรเจมินัลแขนงที่หนึ่งและสองเลี้ยง ยังไม่มีข้อมูลชัดเจนเกี่ยวกับความแตกต่างทางเพศหรือเชื้อชาติ แต่ในฐานะโรคที่เกิดขึ้นเป็นครั้งคราว สามารถเกิดได้ในทุกเชื้อชาติ
การเปรียบเทียบกับเนื้องอกหลอดเลือดคอรอยด์แบบจำกัดขอบเขต
หัวข้อที่มีชื่อว่า “การเปรียบเทียบกับเนื้องอกหลอดเลือดคอรอยด์แบบจำกัดขอบเขต”| ลักษณะ | เนื้องอกหลอดเลือดคอรอยด์แบบกระจาย | เนื้องอกหลอดเลือดคอรอยด์แบบจำกัดขอบเขต (เดี่ยว) |
|---|---|---|
| กลุ่มอาการร่วม | ร่วมกับกลุ่มอาการสเตอร์จ-เวเบอร์เสมอ | ไม่มีโรคทางระบบ (เกิดขึ้นเป็นครั้งคราว) |
| การกระจายในจอตา | กว้าง ขอบเขตไม่ชัดเจน | จำกัดขอบเขต ขอบเขตค่อนข้างชัดเจน |
| สี | จอตาสีซอสมะเขือเทศ | รอยโรคยกตัวสีส้ม |
| การเกิดร่วมกับต้อหิน | มากกว่าครึ่ง | พบได้น้อย |
| ช่วงเวลาที่เกิด | แต่กำเนิด / วัยทารก | มักเกิดในวัยผู้ใหญ่ |
Hemangioma คอรอยด์แบบกระจายมักเกิดร่วมกับกลุ่มอาการ Sturge-Weber (hemangiomatosis สมองและใบหน้า) เกือบทุกครั้ง กลุ่มอาการ Sturge-Weber มีสามลักษณะสำคัญ: ปานสีแดงไวน์บนใบหน้า, hemangioma ของเยื่อหุ้มสมองชั้นเลปโตเมนิงซ์, และอาการทางตา (hemangioma คอรอยด์แบบกระจาย, ต้อหิน) ความถี่ในการเกิดคือ 1 ใน 20,000–50,000 คน และไม่มีการถ่ายทอดทางพันธุกรรม Hemangioma เกิดขึ้นที่จอตาด้านเดียวกับปานสีแดงไวน์บนใบหน้า
2. อาการหลักและผลการตรวจทางคลินิก
หัวข้อที่มีชื่อว่า “2. อาการหลักและผลการตรวจทางคลินิก”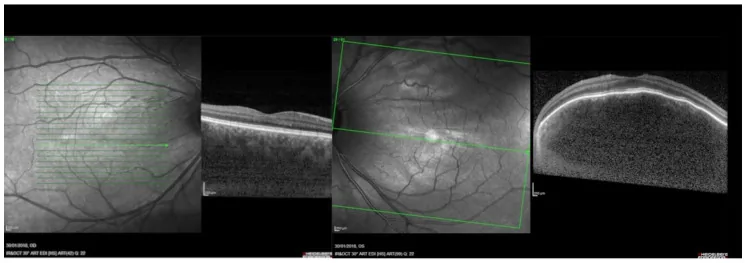
ผลการตรวจจอตา
หัวข้อที่มีชื่อว่า “ผลการตรวจจอตา”ลักษณะเฉพาะของจอประสาทตาที่พบได้บ่อยที่สุดใน hemangioma คอรอยด์ชนิดแพร่กระจายคือ จอประสาทตาทั้งหมดมีสีส้มแดงเป็นบริเวณกว้าง เรียกว่า “จอประสาทตาสีซอสมะเขือเทศ” เนื้องอกครอบครองคอรอยด์เป็นบริเวณกว้าง ขอบเขตไม่ชัดเจน ในภาพถ่ายจอประสาทตาทั่วไป จะเห็นความแตกต่างของสีแดงอย่างชัดเจนเมื่อเทียบกับจอประสาทตาปกติ
ผลการตรวจจอประสาทตาและทางจักษุวิทยาที่สำคัญแสดงไว้ด้านล่าง
- คอรอยด์หนาตัวแบบแพร่กระจาย: คอรอยด์หนาตัวเป็นบริเวณกว้างตั้งแต่ขั้วหลังไปจนถึงส่วนรอบนอก
- ขอบเขตไม่ชัดเจน: แตกต่างจาก hemangioma ชนิดเฉพาะที่ ขอบของเนื้องอกไม่ชัดเจน
- จอประสาทตาลอกชนิดมีน้ำใต้จอประสาทตา: สาเหตุหลักของการมองเห็นลดลง ทำให้เกิดความบกพร่องของลานสายตาและภาพบิดเบือน
- การเปลี่ยนแปลงไปทางสายตายาว: เกิดการเปลี่ยนแปลงค่าสายตาตามแนวแกนลูกตาเนื่องจากคอรอยด์นูนขึ้น
- รอยโรคสีส้มนูน: เห็นเป็นรอยนูนสีส้มที่ขั้วหลัง
การตรวจฟลูออเรสซีนแองจิโอกราฟฟีและผลการตรวจภาพ
หัวข้อที่มีชื่อว่า “การตรวจฟลูออเรสซีนแองจิโอกราฟฟีและผลการตรวจภาพ”ลักษณะเฉพาะในการตรวจภาพต่างๆ แสดงไว้ด้านล่าง
- FA (ฟลูออเรสซีนแองจิโอกราฟฟี): พบการเรืองแสงมากเกินแบบร่างแหภายในเนื้องอกตั้งแต่ระยะแรก และการสะสมของสีเพิ่มขึ้นในระยะหลัง (แบบแพร่กระจาย)
- ICGA (อินโดไซยานีนกรีนแองจิโอกราฟฟี): เหนือกว่า FA ในการแสดงภาพหลอดเลือดคอรอยด์ ทำให้เห็นโครงสร้างหลอดเลือดภายในเนื้องอกได้ชัดเจน
- OCT: สังเกตเห็นเป็นรอยนูนเฉพาะที่กว้างของคอรอยด์ที่ขั้วหลัง มีประโยชน์ในการประเมินจอประสาทตาลอกชนิดมีน้ำใต้จอประสาทตา
- การตรวจอัลตราซาวนด์: แสดงเป็นรอยโรคตันนูนขึ้น สามารถยืนยันคอรอยด์หนาตัวแบบแพร่กระจายได้ด้วย B-scan
- CT: แสดงเป็นรอยโรคตัน คล้ายกับอัลตราซาวนด์
ภาวะแทรกซ้อนของต้อหิน
หัวข้อที่มีชื่อว่า “ภาวะแทรกซ้อนของต้อหิน”ในกลุ่มอาการสเตอร์จ-เวเบอร์ โรคต้อหินเกิดร่วมในมากกว่าครึ่งหนึ่งของกรณี ตามช่วงเวลาที่เกิด พบว่าประมาณครึ่งหนึ่งเกิดในวัยทารก (ชนิดแต่กำเนิด) และอีกครึ่งหนึ่งเกิดในวัยเด็ก (ชนิดที่ได้มา)
- ชนิดเกิดในวัยทารก: แสดงลักษณะของต้อหินแต่กำเนิด เช่น เส้นผ่านศูนย์กลางกระจกตาใหญ่ ตาวัว (กระจกตาใหญ่) และรอยแฮบส์ มักต้องผ่าตัด
- ชนิดเกิดในวัยเด็ก: ความดันลูกตาอาจคงที่ในระดับปกติชั่วคราว แล้วเกิดความดันลูกตาสูงขึ้นระหว่างการติดตามผล
- หลอดเลือดแดงโป่งพองที่เยื่อบุตาชั้นนอก: บางกรณีมีหลอดเลือดแดงโป่งพองที่เยื่อบุตาชั้นนอกด้านที่ได้รับผลกระทบร่วมด้วย
โรคต้อหินเกิดร่วมในมากกว่าครึ่งหนึ่งของกรณีกลุ่มอาการสเตอร์จ-เวเบอร์ การเกิดในวัยทารกและวัยเด็กมีสัดส่วนครึ่งหนึ่ง และอาจเกิดความดันลูกตาสูงขึ้นภายหลังระหว่างการติดตามผล หากไม่จัดการต้อหินอย่างเหมาะสม อาจนำไปสู่ความเสียหายของลานสายตาและการมองเห็นลดลง ดังนั้นการวัดความดันลูกตาเป็นประจำและการสังเกตอวัยวะภายในตาในระยะยาวจึงจำเป็น โดยเฉพาะในวัยทารก ตาวัวและกระจกตาขุ่นต้องได้รับการแทรกแซงอย่างเร่งด่วน
3. สาเหตุและปัจจัยเสี่ยง
หัวข้อที่มีชื่อว่า “3. สาเหตุและปัจจัยเสี่ยง”กลไกการเกิด
หัวข้อที่มีชื่อว่า “กลไกการเกิด”กลุ่มอาการสเตอร์จ-เวเบอร์และหลอดเลือดแดงโป่งพองที่คอรอยด์แบบกระจายเกิดจากการเจริญเติบโตผิดตำแหน่งของเซลล์ประสาทคริสต้าในระยะตัวอ่อน เกิด hamartoma ของหลอดเลือดที่คอรอยด์ ซึ่งแทนที่โครงสร้างคอรอยด์ปกติอย่างกว้างขวางด้วยเนื้อเยื่อหลอดเลือด
ในระดับยีน พบการกลายพันธุ์ของยีน GNAQ (โปรตีนจับนิวคลีโอไทด์กัวนีน Gqα) (c.548G>A, p.Arg183Gln) ในหลายกรณี การกลายพันธุ์นี้เกิดขึ้นเป็นการกลายพันธุ์แบบโมเสกในเซลล์ร่างกาย จึงไม่ถ่ายทอดทางพันธุกรรม และโดยหลักการแล้วไม่ถ่ายทอดจากพ่อแม่สู่ลูก เชื่อว่าการกลายพันธุ์ GNAQ ลดการทำงานของ GTPase และกระตุ้นสัญญาณการสร้างหลอดเลือดอย่างต่อเนื่อง
ปัจจัยเสี่ยงและลักษณะสำคัญ
หัวข้อที่มีชื่อว่า “ปัจจัยเสี่ยงและลักษณะสำคัญ”- การกลายพันธุ์แบบโมเสกในเซลล์ร่างกายของ GNAQ: สำคัญที่สุดในฐานะการกลายพันธุ์ที่เป็นสาเหตุ ไม่ใช่การกลายพันธุ์ในเซลล์สืบพันธุ์ ไม่ถ่ายทอดทางพันธุกรรม
- โรคแต่กำเนิด: มีอยู่ตั้งแต่เกิด ดังนั้นการกลายพันธุ์โดยบังเอิญในระยะตัวอ่อนเป็นสาเหตุหลัก ไม่ใช่ภูมิหลังทางพันธุกรรม
- ปัจจัยสิ่งแวดล้อม: ไม่มีปัจจัยเสี่ยงด้านสิ่งแวดล้อมที่ชัดเจน
- ประวัติครอบครัว: โดยหลักการแล้วไม่ถ่ายทอดทางพันธุกรรม ดังนั้นจึงมักไม่พบการสะสมในครอบครัว
กลไกการเกิดต้อหิน
หัวข้อที่มีชื่อว่า “กลไกการเกิดต้อหิน”กลไกหลักสองประการเกี่ยวข้องกับการเกิดต้อหินในกลุ่มอาการ Sturge-Weber
- ความดันหลอดเลือดดำเอพิสเกลราสูงขึ้น: หลอดเลือดผิดปกติที่เอพิสเกลราทำให้ความดันหลอดเลือดดำเพิ่มขึ้น ส่งผลให้ความต้านทานการไหลออกของอารมณ์ขันในลูกตาเพิ่มขึ้น กลไกนี้พบได้บ่อยในต้อหินที่เกิดขึ้นหลังวัยเด็ก
- ความผิดปกติของการสร้างมุม: ความผิดปกติของพัฒนาการของมุมช่องหน้าม่านตาทำให้การไหลออกของอารมณ์ขันในลูกตาถูกขัดขวาง มักเกี่ยวข้องกับต้อหินที่เกิดขึ้นในวัยทารก
4. การวินิจฉัยและวิธีการตรวจ
หัวข้อที่มีชื่อว่า “4. การวินิจฉัยและวิธีการตรวจ”แนวทางการวินิจฉัย
หัวข้อที่มีชื่อว่า “แนวทางการวินิจฉัย”การรวมกันของปานสีแดงไวน์ (หลอดเลือดผิดปกติที่ผิวหนังในบริเวณที่เส้นประสาทไทรเจมินัลบนใบหน้าควบคุม) และการเปลี่ยนแปลงของจอตาข้างเดียวกันสนับสนุนการวินิจฉัยหลอดเลือดผิดปกติของคอรอยด์แบบกระจายอย่างมาก การตรวจทางจักษุวิทยาต่อไปนี้ใช้สำหรับการวินิจฉัย
การตรวจจอตาและการถ่ายภาพ:
- ภาพถ่ายจอตา (รวมถึงการถ่ายภาพมุมกว้าง): เพื่อบันทึกและติดตามจอตาที่มีลักษณะคล้ายซอสมะเขือเทศ
- FA/ICGA: เพื่อยืนยันการเรืองแสงมากเกินไปแบบร่างแหในระยะแรก (รูปแบบกระจาย)
- OCT: เพื่อประเมินความหนาของคอรอยด์อย่างกว้างขวางและจอตาลอกแบบเซรุ่ม
- อัลตราซาวนด์ (A-scan และ B-scan): เพื่อยืนยันรอยโรคตันและวัดความหนา
การค้นหาทั่วร่างกาย:
- MRI ศีรษะ: angioma เยื่อหุ้มสมองและหินปูน (ประเมินโดยกุมารแพทย์ระบบประสาทร่วมกับผลตรวจทางจักษุ)
- วัดความดันลูกตา: คัดกรองต้อหิน (ภายใต้การดมยาสลบหากจำเป็น)
- ตรวจมุมตา: ประเมินความผิดปกติของมุมตา
การวินิจฉัยแยกโรค
หัวข้อที่มีชื่อว่า “การวินิจฉัยแยกโรค”โรคที่ต้องแยกจาก hemangioma คอรอยด์แบบกระจายมีดังนี้
| โรคที่ต้องแยก | ข้อแตกต่างหลัก |
|---|---|
| Hemangioma คอรอยด์เฉพาะที่ | ขอบเขตชัดเจน เฉพาะที่ ไม่มีกลุ่มอาการทางระบบ |
| มะเร็งเมลาโนมาคอรอยด์ (ชนิดกระจาย) | ลักษณะร้าย การเปลี่ยนแปลงของเม็ดสี เสี่ยงต่อการแพร่กระจาย |
| ม่านตาอักเสบส่วนหลัง | อาการอักเสบ ขุ่นของวุ้นตา |
| การเปลี่ยนแปลงสีของจอตาปกติ | ไม่มีอาการทางระบบของกลุ่มอาการ Sturge-Weber |
ข้อควรระวังในการวินิจฉัย
หัวข้อที่มีชื่อว่า “ข้อควรระวังในการวินิจฉัย”เมื่อรู้สึกว่าจอประสาทตา “แดงเล็กน้อย” โดยเฉพาะในทารกที่มีปานสีแดงไวน์ ควรสงสัยโรคนี้อย่างมาก ในทารก การตรวจอาจต้องใช้การดมยาสลบ และความร่วมมือกับแผนกวิสัญญีและกุมารเวชศาสตร์เป็นสิ่งสำคัญ
5. การรักษามาตรฐาน
หัวข้อที่มีชื่อว่า “5. การรักษามาตรฐาน”สรุปแนวทางการรักษา
หัวข้อที่มีชื่อว่า “สรุปแนวทางการรักษา”การรักษา hemangioma คอรอยด์แบบกระจายจะดำเนินการเป็นขั้นตอนตามอาการและชนิดของภาวะแทรกซ้อน โดยปกติแล้วจะไม่ผ่าตัดเอา hemangioma คอรอยด์ออก เป้าหมายหลักของการรักษาคือ จอประสาทตาลอกชนิดมีน้ำใต้จอประสาทตา (สาเหตุหลักของการมองเห็นลดลง) และต้อหิน
1. การสังเกตอาการ
หัวข้อที่มีชื่อว่า “1. การสังเกตอาการ”หากไม่มีอาการและการมองเห็นและความดันลูกตาปกติ ให้ติดตามสังเกตเป็นระยะดังนี้:
- วัดความดันลูกตา (เพื่อตรวจหาต้อหินตั้งแต่แรก)
- ถ่ายภาพจอประสาทตาและ OCT เพื่อตรวจสอบว่ามีจอประสาทตาลอกชนิดมีน้ำใต้จอประสาทตาหรือไม่
- ตรวจการมองเห็นและการหักเหของแสง (ประเมินสายตายาวและตาขี้เกียจ)
- ติดตามเป็นระยะด้วย FA/OCT ตามความจำเป็น
2. การรักษาจอประสาทตาลอกชนิดมีน้ำใต้จอประสาทตาและการทำงานของการมองเห็นที่ลดลง
หัวข้อที่มีชื่อว่า “2. การรักษาจอประสาทตาลอกชนิดมีน้ำใต้จอประสาทตาและการทำงานของการมองเห็นที่ลดลง”หากมีการมองเห็นลดลงหรือจอประสาทตาลอกชนิดมีน้ำใต้จอประสาทตา ให้ทำการรักษาอย่างจริงจัง
PDT (การรักษาด้วยแสงไดนามิก):
- ฉีดเวอร์เทพออร์ฟิน (สารไวแสง) ทางหลอดเลือดดำ ตามด้วยการฉายเลเซอร์ความยาวคลื่น 689 นาโนเมตร
- มีรายงานประสิทธิภาพของ PDT ต่อ hemangioma คอรอยด์
- ไม่ครอบคลุมโดยประกัน (สำหรับ hemangioma คอรอยด์ชนิดกระจาย)
- คาดหวังให้จอประสาทตาลอกชนิดเซรุ่มยุบลงและการมองเห็นดีขึ้น
- ประสิทธิภาพใน hemangioma คอรอยด์ชนิดเฉพาะที่ได้รับการยืนยันแล้ว แต่การประยุกต์ใช้กับชนิดกระจายมีข้อจำกัดทางเทคนิคเนื่องจากพื้นที่ฉายรังสีกว้าง
การฉายรังสีปริมาณต่ำ:
- ให้การฉายรังสีปริมาณต่ำประมาณ 20 เกรย์
- บางครั้งได้ผล คาดหวังให้จอประสาทตาลอกยุบลงและการมองเห็นดีขึ้น
- มักใช้การฉายรังสีจากภายนอก (teletherapy)
โดยปกติไม่ทำการผ่าตัดเอาออก hemangioma คอรอยด์ชนิดกระจายแผ่กว้างไปทั่วคอรอยด์ ดังนั้นการผ่าตัดเอาออกจึงยากทั้งทางเทคนิคและหน้าที่ สำหรับจอประสาทตาลอกชนิดเซรุ่มที่ทำให้การมองเห็นลดลง จะทำ PDT หรือการฉายรังสีปริมาณต่ำ (ประมาณ 20 เกรย์) และมักได้ผล สำหรับต้อหิน จะควบคุมความดันลูกตาด้วยยาหยอดตาหรือการผ่าตัด
3. การรักษาต้อหิน
หัวข้อที่มีชื่อว่า “3. การรักษาต้อหิน”เนื่องจากมากกว่าครึ่งหนึ่งของผู้ป่วยมีต้อหินร่วมด้วย การจัดการจึงเป็นความท้าทายในการรักษาที่สำคัญ
การรักษาด้วยยา (ยาหยอดตา):
- ยาที่เกี่ยวข้องกับพรอสตาแกลนดิน (ยับยั้งการผลิตอารมณ์ขันในน้ำและเพิ่มการไหลออก)
- ยาปิดกั้นเบตา (ยับยั้งการผลิตอารมณ์ขันในน้ำ)
- ยายับยั้งเอนไซม์คาร์บอนิกแอนไฮเดรส (ใช้เฉพาะที่หรือรับประทาน)
- อย่างไรก็ตาม ในโรคต้อหินที่เกิดจากความดันหลอดเลือดดำอีพิสเคลาสูง ผลของยาหยอดตาอาจมีจำกัด
การรักษาโดยการผ่าตัด:
- ในกรณีที่เริ่มมีอาการในวัยทารก (ชนิดพิการแต่กำเนิด) อาจลองทำการผ่าตัดโกนิโอโตมีหรือทราเบคิวโลโตมี
- ในชนิดผู้ใหญ่ พิจารณาการผ่าตัดกรอง (ทราเบคิวเลกโตมีหรือการผ่าตัดใส่ท่อระบาย)
- หากความดันหลอดเลือดดำอีพิสเคลาสูง ต้องระมัดระวังในการดูแลหลังการผ่าตัดทราเบคิวเลกโตมี
4. การจัดการทั่วร่างกาย
หัวข้อที่มีชื่อว่า “4. การจัดการทั่วร่างกาย”- การจัดการโรคลมชัก: ควบคุมอาการชักด้วยยาต้านโรคลมชัก (ประสาทวิทยาเด็ก)
- การจัดการกับพัฒนาการทางจิตที่ล่าช้า: การแทรกแซง早期และการจัดระบบสนับสนุน
- อาการปวดศีรษะและอัมพาตครึ่งซีก: การสังเกตอาการทางระบบประสาทและการรักษาตามอาการ
- ความร่วมมือแบบสหสาขาวิชา: การประสานงานระหว่างจักษุวิทยา ประสาทวิทยาเด็ก ผิวหนัง ผู้เชี่ยวชาญโรคลมชัก และทีมแทรกแซง早期
6. พยาธิสรีรวิทยาและกลไกการเกิดโรคโดยละเอียด
หัวข้อที่มีชื่อว่า “6. พยาธิสรีรวิทยาและกลไกการเกิดโรคโดยละเอียด”ลักษณะพื้นฐานเป็น hamartoma ของหลอดเลือด
หัวข้อที่มีชื่อว่า “ลักษณะพื้นฐานเป็น hamartoma ของหลอดเลือด”hemangioma คอรอยด์ชนิดแพร่กระจาย (diffuse choroidal hemangioma) ถูกจัดประเภททางเอ็มบริโอวิทยาว่าเป็น hamartoma ของหลอดเลือด Hamartoma คือรอยโรคคล้ายเนื้องอกชนิดไม่ร้ายแรงที่เกิดจากการเจริญเติบโตผิดปกติของส่วนประกอบเนื้อเยื่อที่ปกติมีอยู่บริเวณนั้น และแตกต่างจากเนื้องอกแท้จริง (neoplasm) ในโรคนี้ องค์ประกอบของหลอดเลือดที่เจริญเต็มที่จะเพิ่มจำนวนมากเกินไปภายในคอรอยด์ แทนที่โครงสร้างของเส้นเลือดฝอยคอรอยด์ปกติและหลอดเลือดขนาดกลางและใหญ่
การกลายพันธุ์ของยีน GNAQ และกลไกระดับโมเลกุล
หัวข้อที่มีชื่อว่า “การกลายพันธุ์ของยีน GNAQ และกลไกระดับโมเลกุล”ในฐานะพื้นฐานระดับโมเลกุลของกลุ่มอาการ Sturge-Weber การกลายพันธุ์แบบโมเสกในเซลล์ร่างกายของยีน GNAQ (c.548G>A, p.Arg183Gln) ถูกระบุในหลายกรณี
- หน้าที่ของ GNAQ (Gqα): หน่วยย่อย Gα ที่เกี่ยวข้องกับการส่งสัญญาณต่อเนื่องจากตัวรับที่จับกับโปรตีน G (GPCR)
- ผลของการกลายพันธุ์: การกลายพันธุ์ Arg183Gln ลดการทำงานของ GTPase ทำให้ GNAQ อยู่ในสถานะถูกกระตุ้นอย่างต่อเนื่อง
- สัญญาณต่อเนื่อง: การกระตุ้น PLC-β ผ่าน Gq → การผลิต IP3/DAG → การกระตุ้น PKC → การกระตุ้นอย่างต่อเนื่องของ cascade MAPK (MEK/ERK)
- ผลต่อการสร้างหลอดเลือด: การผลิตปัจจัยสร้างหลอดเลือด เช่น VEGF มากเกินไป被认为ส่งเสริมการสร้างหลอดเลือดผิดปกติ
- ความสำคัญของการกลายพันธุ์แบบโมเสกในเซลล์ร่างกาย: เนื่องจากการกลายพันธุ์เกิดขึ้นเฉพาะในเซลล์บางส่วนในช่วงต้นของการพัฒนาเอ็มบริโอ รูปแบบการแสดงออกจึงแตกต่างกันระหว่างบุคคล ทำให้เกิดความหลากหลายของอาการ
กลไกโดยละเอียดของการเกิดต้อหิน
หัวข้อที่มีชื่อว่า “กลไกโดยละเอียดของการเกิดต้อหิน”ในกลุ่มอาการ Sturge-Weber มีการสันนิษฐานกลไกอย่างน้อยสองกลไกที่ทำให้เกิดต้อหิน
กลไกที่ 1: ความดันหลอดเลือดดำอีพิสเกลราสูงขึ้น hemangioma ใต้เยื่อหุ้มตาชั้นนอก (ใต้แคปซูลเทนอน) ทำให้ความดันหลอดเลือดดำอีพิสเกลราสูงขึ้น ขัดขวางการไหลของอารมณ์ขันจากคลองชเลมม์และ trabecular meshwork เมื่อความดันหลอดเลือดดำอีพิสเกลราเกินค่าปกติ (ประมาณ 10 มิลลิเมตรปรอท) ความดันลูกตาจะเพิ่มขึ้นตามส่วนที่เพิ่มขึ้น กลไกนี้พบบ่อยในต้อหินที่เกิดขึ้นภายหลังวัยเด็ก
กลไกที่ 2: ความผิดปกติของการสร้างมุม ความผิดปกติในการพัฒนามุมของช่องหน้าม่านตา (angle dysgenesis) ทำให้ trabecular meshwork พัฒนาไม่สมบูรณ์ ทำให้ทางเดินของอารมณ์ขันไม่ทำงานทางกายวิภาค กลไกนี้มักเกี่ยวข้องกับต้อหินแต่กำเนิดที่ปรากฏในวัยทารก
กลไกการเกิดจอประสาทตาลอกชนิดมีน้ำใต้จอประสาทตา
หัวข้อที่มีชื่อว่า “กลไกการเกิดจอประสาทตาลอกชนิดมีน้ำใต้จอประสาทตา”การเพิ่มขึ้นของการซึมผ่านของหลอดเลือดใน hemangioma คอรอยด์ชนิดแพร่กระจายทำให้ส่วนประกอบภายในหลอดเลือดรั่วออกนอกหลอดเลือด และของเหลวสะสมในช่องใต้จอประสาทตา สิ่งนี้ทำให้เกิดจอประสาทตาลอกชนิดมีน้ำใต้จอประสาทตา ซึ่งเป็นสาเหตุหลักของการมองเห็นลดลงและข้อบกพร่องของลานสายตา การรักษาด้วยการส่องไฟแบบไดนามิก (PDT) หรือการฉายรังสีจะลดหลอดเลือดของเนื้องอก ทำให้สารคัดหลั่งลดลงและจอประสาทตากลับเข้าที่
พยาธิสรีรวิทยานอกตา
หัวข้อที่มีชื่อว่า “พยาธิสรีรวิทยานอกตา”- หลอดเลือดผิดปกติในเยื่อหุ้มสมองชั้นเลปโตเมนิงซ์: หลอดเลือดผิดปกติในคอร์เทกซ์สมองทำให้เกิดภาวะขาดเลือดเฉพาะที่และการกลายเป็นปูน นำไปสู่อาการชัก พัฒนาการทางจิตช้า และอัมพาตครึ่งซีก
- ปานแดงพอร์ตไวน์บนใบหน้า: ปรากฏตั้งแต่แรกเกิดเป็นเส้นเลือดฝอยขยายตัวบนผิวหนัง
- การกลายเป็นปูน: การกลายเป็นปูนรูป “รางรถไฟ” ในคอร์เทกซ์สมองใต้หลอดเลือดผิดปกติในเยื่อหุ้มสมองชั้นเลปโตเมนิงซ์เป็นลักษณะเฉพาะทางภาพของกลุ่มอาการสเตอร์จ-เวเบอร์
7. งานวิจัยล่าสุดและแนวโน้มในอนาคต
หัวข้อที่มีชื่อว่า “7. งานวิจัยล่าสุดและแนวโน้มในอนาคต”การรักษาแบบมุ่งเป้าระดับโมเลกุลที่กำหนดเป้าหมายปลายน้ำของ GNAQ
หัวข้อที่มีชื่อว่า “การรักษาแบบมุ่งเป้าระดับโมเลกุลที่กำหนดเป้าหมายปลายน้ำของ GNAQ”แกนสัญญาณ MAPK (วิถี MEK/ERK) ที่ถูกกระตุ้นอย่างต่อเนื่องเนื่องจากการกลายพันธุ์ของ GNAQ ได้รับการศึกษาอย่างกว้างขวางในฐานะเป้าหมายการรักษาในการวิจัยมะเร็งผิวหนังชนิดยูเวียล เนื่องจากความผิดปกติระดับโมเลกุลเดียวกันนี้มีอยู่ในกลุ่มอาการสเตอร์จ-เวเบอร์/หลอดเลือดผิดปกติในคอรอยด์แบบกระจาย การประยุกต์ใช้สารยับยั้ง MEK (trametinib, binimetinib ฯลฯ) และสารยับยั้ง GNAQ โดยตรง (YM-254890 ฯลฯ) จึงอยู่ระหว่างการพิจารณาในระดับการวิจัยพื้นฐาน
ในความเป็นจริง การรักษาแบบมุ่งเป้าระดับโมเลกุลสำหรับกลุ่มอาการสเตอร์จ-เวเบอร์ทั้งหมดด้วยสารยับยั้ง mTOR (sirolimus) และการรักษาที่กำหนดเป้าหมายวิถี PI3K-AKT-mTOR ได้ดำเนินการในเชิงทดลอง โดยมีรายงานการปรับปรุงอาการในผู้ป่วยบางราย อย่างไรก็ตาม การศึกษาขนาดใหญ่ที่ประเมินประสิทธิผลโดยตรงต่อหลอดเลือดผิดปกติในคอรอยด์แบบกระจายนั้นยังมีจำกัดในปัจจุบัน
การปรับปรุงการรักษาด้วย PDT
หัวข้อที่มีชื่อว่า “การปรับปรุงการรักษาด้วย PDT”PDT ได้รับการพิสูจน์แล้วว่ามีประสิทธิภาพสำหรับจอประสาทตาลอกชนิดมีน้ำใต้จอประสาทตาจากหลอดเลือดผิดปกติในคอรอยด์แบบกระจายในรายงานผู้ป่วยหลายฉบับ แต่ยังไม่มีมาตรฐานสำหรับระเบียบวิธี (พื้นที่ฉายรังสี พลังงาน จำนวนครั้ง) สำหรับรอยโรคแบบกระจายกว้าง เมื่อเทียบกับหลอดเลือดผิดปกติในคอรอยด์แบบเฉพาะที่ พื้นที่ฉายรังสีจะใหญ่กว่าในชนิดกระจาย ซึ่งก่อให้เกิดความท้าทายทางเทคนิค คาดว่าจะมีการกำหนดระเบียบวิธีผ่านการศึกษาไปข้างหน้าแบบหลายศูนย์ในอนาคต
ความก้าวหน้าใหม่ในการจัดการโรคต้อหิน
หัวข้อที่มีชื่อว่า “ความก้าวหน้าใหม่ในการจัดการโรคต้อหิน”การผ่าตัดกรองแบบดั้งเดิมสำหรับโรคต้อหินจากความดันเลือดดำในชั้นเอพิสเกลราสูงมีความเสี่ยงต่อการมีน้ำใต้คอรอยด์และต้อหินชนิดร้ายแรงในภาวะความดันเลือดดำในชั้นเอพิสเกลราสูง กำลังมีการวิจัยเกี่ยวกับประสิทธิผลของการผ่าตัดใส่ท่อระบาย (ลิ้นอาห์เม็ด, ท่อแบร์เวลต์) นอกจากนี้ยังกำลังศึกษาความเป็นไปได้ของการใช้เลเซอร์ trabeculoplasty แบบเลือกสรร (SLT)
แนวโน้มการวินิจฉัยทางพันธุกรรมของ GNAQ
หัวข้อที่มีชื่อว่า “แนวโน้มการวินิจฉัยทางพันธุกรรมของ GNAQ”การตรวจหาการกลายพันธุ์ของ GNAQ ในชิ้นเนื้อผิวหนังและตัวอย่างเลือดกำลังถูกนำมาใช้เพื่อการวินิจฉัยที่แน่นอนของกลุ่มอาการสเตอร์จ-เวเบอร์ ในอนาคต คาดว่าการวินิจฉัยตั้งแต่ระยะแรกผ่านการตรวจชิ้นเนื้อของเหลว (ctDNA) และการปรับปรุงอัตราการตรวจพบการกลายพันธุ์จะช่วยให้การวินิจฉัยแม่นยำยิ่งขึ้น
8. เอกสารอ้างอิง
หัวข้อที่มีชื่อว่า “8. เอกสารอ้างอิง”- Shirley MD, Tang H, Gallione CJ, et al. Sturge-Weber syndrome and port-wine stains caused by somatic mutation in GNAQ. N Engl J Med. 2013;368(21):1971-1979.
- Baselga E, Torrelo A, Mediero IG, et al. Sturge-Weber syndrome: report of 3 cases. Pediatr Dermatol. 2019;36(6):932-934.
- Bhatt A, Bhatt N. Sturge-Weber syndrome: a rare neurocutaneous disorder. J Pediatr Neurosci. 2021;16(1):1-6.
- Zreik O, Elabassy HM, Bakhurji E, Al-Johani SM. Sturge-Weber syndrome: an updated review. Clin Ophthalmol. 2023;17:2369-2381.
- Nassiri N, Rootman DB, Rootman J, Goldberg RA. Orbital and adnexal lymphangiomas: a review of management. Surv Ophthalmol. 2015;60(3):245-257.
