
びまん性脈絡膜血管腫
1. びまん性脈絡膜血管腫とは
Section titled “1. びまん性脈絡膜血管腫とは”脈絡膜血管腫には限局性(孤立性)と びまん性の2型がある。限局性は境界明瞭で散発性に発生するが、びまん性は腫瘍が広範囲にわたり境界も不明瞭なことが多い。びまん性脈絡膜血管腫はほぼ必ずSturge-Weber症候群(脳顔面血管腫症)に関連して発生する。
Sturge-Weber症候群は母斑症(神経皮膚症候群)の一つであり、胎生期の神経堤細胞(しんけいていさいぼう)の異所性増殖によって引き起こされる。顔面と眼、および脳軟膜に血管腫が形成されることが特徴である。
Sturge-Weber症候群の発生頻度は2〜5万人に1人とされる。遺伝性はなく、突発的に発生するGNAQ遺伝子の体細胞モザイク変異が主因である。生下時から存在する先天性疾患であり、乳幼児期から発見される。顔面三叉神経第1〜2枝支配領域に皮膚血管腫(ポートワイン斑)が存在する患者の同側の眼底に発生する。男女差・人種差についての明確なデータは乏しいが、散発性疾患として全人種に生じうる。
限局性脈絡膜血管腫との比較
Section titled “限局性脈絡膜血管腫との比較”| 特徴 | びまん性脈絡膜血管腫 | 限局性(孤立性)脈絡膜血管腫 |
|---|---|---|
| 合併症候群 | Sturge-Weber症候群に必発 | 全身疾患なし(散発性) |
| 眼底分布 | 広範囲・境界不明瞭 | 局所・境界比較的明瞭 |
| 色調 | トマトケチャップ眼底 | 橙色隆起性病変 |
| 緑内障合併 | 半数以上 | まれ |
| 発症時期 | 先天性・乳幼児期 | 成人期が多い |
びまん性脈絡膜血管腫はほぼ必ずSturge-Weber症候群(脳顔面血管腫症)に伴って発生する。Sturge-Weber症候群では顔面ポートワイン斑・脳軟膜血管腫・眼科症状(びまん性脈絡膜血管腫・緑内障)の三徴が認められる。発生頻度は2〜5万人に1人で、遺伝性はない。顔面のポートワイン斑と同側の眼底に血管腫が生じる。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”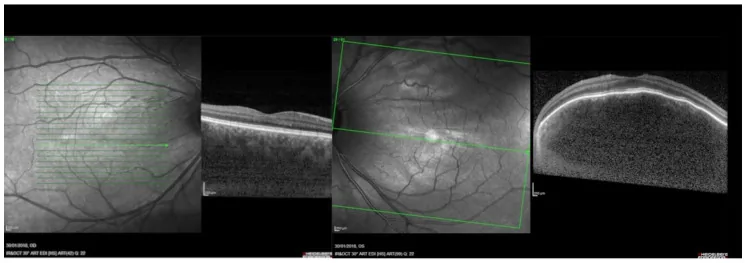
びまん性脈絡膜血管腫の最も特徴的な眼底所見は、眼底全体が広範囲にわたって橙赤色を帯びる「トマトケチャップ眼底」である。腫瘍は広範囲に脈絡膜を占拠し、境界は不明瞭である。通常の眼底写真では正常眼底と比較して著明な赤みの差として認識できる。
主な眼底・眼科的所見を以下に示す。
- びまん性脈絡膜肥厚:後極から周辺部にかけて広範に脈絡膜が肥厚する
- 境界不明瞭:限局性血管腫と異なり、腫瘍辺縁が不明確
- 漿液性網膜剥離:視力低下の主な原因。視野障害・変視症を呈する
- 遠視化:脈絡膜の隆起により眼軸方向に屈折変化が生じる
- 橙色隆起性病変:後極部に橙色の隆起として認識される
蛍光眼底造影・画像所見
Section titled “蛍光眼底造影・画像所見”各種画像検査での特徴的所見を以下に示す。
- FA(蛍光眼底造影):造影早期より腫瘍内に網目状の過蛍光を認め、造影後期に蛍光色素の貯留が増加する(びまん性パターン)
- ICGA(インドシアニングリーン造影):FAよりも脈絡膜血管の描出に優れ、腫瘍内血管構造が明瞭に把握できる
- OCT:後極部脈絡膜の広範な局所的隆起として観察される。漿液性網膜剥離の評価にも有用
- 超音波検査:充実性の隆起性病変として描出される。B-scan で脈絡膜の広範な肥厚が確認できる
- CT:超音波と同様、充実性病変として描出される
緑内障の合併
Section titled “緑内障の合併”Sturge-Weber症候群では半数以上の症例に緑内障が合併する。発症時期により乳児期発症(先天緑内障型)と小児期発症(後天型)がほぼ半数ずつ認められる。
- 乳児期発症型:角膜径拡大・牛眼(角膜拡大)・Haab’s striaなどの先天緑内障の特徴を呈する。手術が必要となる場合が多い
- 小児期発症型:眼圧は正常域でいったん落ち着いた後、経過観察中に眼圧上昇が生じることがある
- 上強膜の血管腫:患側の上強膜に血管腫を合併する症例もある
Sturge-Weber症候群の半数以上に緑内障が合併する。乳児期発症と小児期発症が半数ずつであり、経過観察中に後から眼圧上昇が生じることもある。緑内障は適切に管理されなければ視野障害・視力低下につながるため、長期にわたる定期的な眼圧測定と眼底観察が不可欠である。特に乳児期の牛眼・角膜混濁は緊急性の高い介入を要する。
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”Sturge-Weber症候群およびびまん性脈絡膜血管腫の発症は、胎生期における神経堤細胞の異所性増殖によって引き起こされる。脈絡膜の血管過誤腫(hamartoma)が形成され、正常な脈絡膜構造が広範に血管性組織に置き換わる。
遺伝子レベルでは、GNAQ遺伝子(グアニンヌクレオチド結合タンパク質Gqα)の変異(c.548G>A, p.Arg183Gln)が多くの症例で検出される。この変異は体細胞モザイク変異として生じるため、遺伝性はなく、親から子への遺伝は原則として生じない。GNAQ変異はGTPase活性を低下させ、血管形成シグナルを恒常的に活性化させると考えられている。
主なリスク要因・特徴
Section titled “主なリスク要因・特徴”- GNAQ体細胞モザイク変異:原因変異として最も重要。生殖細胞系列変異ではなく、遺伝性なし
- 先天性疾患:生下時から存在するため、遺伝的背景よりも胎生期の偶発的変異が主因
- 環境要因:確立した環境リスク因子はない
- 家族歴:原則として遺伝しないため、家族内集積は通常認めない
緑内障の発症機序
Section titled “緑内障の発症機序”Sturge-Weber症候群における緑内障の発症には主に2つの機序が関与する。
- 上強膜静脈圧上昇:上強膜の血管腫が静脈圧を上昇させ、房水流出抵抗が増大する。小児期以降の緑内障に多い機序
- 隅角形成異常:前房隅角の発達異常により房水流出が障害される。乳児期発症の緑内障に関わることが多い
4. 診断と検査方法
Section titled “4. 診断と検査方法”診断のアプローチ
Section titled “診断のアプローチ”顔面のポートワイン斑(顔面三叉神経支配領域の皮膚血管腫)と同側の眼底変化の組み合わせがびまん性脈絡膜血管腫の診断を強く支持する。眼科的診断には以下の検査が用いられる。
眼底検査・画像:
- 眼底写真(広角眼底撮影を含む):トマトケチャップ眼底の記録と経過観察
- FA/ICGA:早期の網目状過蛍光(びまん性パターン)の確認
- OCT:脈絡膜の広範な肥厚と漿液性網膜剥離の評価
- 超音波(Aスキャン・Bスキャン):充実性病変の確認と厚みの計測
全身検索:
- 頭部MRI:脳軟膜血管腫・石灰化(眼科的所見と並行して小児脳神経専門医が評価)
- 眼圧測定:緑内障スクリーニング(必要に応じて全身麻酔下)
- 隅角鏡検査:隅角形成異常の評価
びまん性脈絡膜血管腫との鑑別を要する疾患を以下に示す。
| 鑑別疾患 | 主な相違点 |
|---|---|
| 限局性脈絡膜血管腫 | 境界明瞭・局所性・全身症候群なし |
| 脈絡膜悪性黒色腫(びまん性型) | 悪性所見・色素変化・転移リスク |
| 後部ブドウ膜炎 | 炎症所見・硝子体混濁 |
| 正常眼底の色調変化 | Sturge-Weber症候群の全身所見なし |
診断時の留意点
Section titled “診断時の留意点”眼底が「なんとなく赤い」と感じた場合、特にポートワイン斑を伴う乳幼児では本疾患を積極的に疑う必要がある。乳幼児では診察に全身麻酔が必要となる場合があり、麻酔科・小児科との協力体制が重要である。
5. 標準的な治療法
Section titled “5. 標準的な治療法”治療方針の概要
Section titled “治療方針の概要”びまん性脈絡膜血管腫の治療は、症状の有無と合併症の種類に応じて段階的に行われる。脈絡膜血管腫自体を外科的に摘出することは通常行わない。主な治療対象は漿液性網膜剥離(視力低下の主因)と緑内障である。
1. 経過観察
Section titled “1. 経過観察”無症状で視力・眼圧に問題がない場合は、以下の定期観察を継続する。
2. 漿液性網膜剥離・視機能低下への治療
Section titled “2. 漿液性網膜剥離・視機能低下への治療”視力低下や漿液性網膜剥離が認められる場合には積極的治療を行う。
PDT(光線力学療法):
- ベルテポルフィン(光増感剤)を静脈内投与後に689nm波長レーザーを照射する
- 脈絡膜血管腫に対するPDTの有効性が報告されている
- 保険適用外(びまん性脈絡膜血管腫に対して)
- 漿液性網膜剥離の消退・視力改善が期待できる
- 限局性脈絡膜血管腫への有効性は確立されているが、びまん性への適用は照射範囲の広さから技術的制約がある
低線量放射線照射:
- 約20Gy程度の低線量照射が行われる
- 有効なことがある。網膜剥離の消退・視力改善が期待できる
- 外部照射(teletherapy)が用いられることが多い
外科的に摘出することは通常行わない。びまん性脈絡膜血管腫は広範に脈絡膜全体に及ぶため、外科的摘出は技術的にも機能的にも困難である。視力低下をきたす漿液性網膜剥離に対してはPDTや低線量放射線照射(約20Gy)が行われ、有効なことが多い。緑内障については点眼薬や手術で眼圧をコントロールする。
3. 緑内障治療
Section titled “3. 緑内障治療”半数以上の症例で緑内障が合併するため、その管理は重要な治療課題である。
薬物療法(点眼):
- プロスタグランジン関連薬(房水産生抑制・流出促進)
- β遮断薬(房水産生抑制)
- 炭酸脱水酵素阻害薬(局所または内服)
- ただし、上強膜静脈圧上昇による緑内障では点眼薬の効果が限定的なことがある
外科的治療:
- 乳児期発症(先天緑内障型)には房角切開術・線維柱帯切開術が試みられる
- 成人型では濾過手術(線維柱帯切除術・チューブシャント手術)が考慮される
- 上強膜静脈圧が高い場合は線維柱帯切除術の術後管理に注意が必要
4. 全身管理
Section titled “4. 全身管理”- てんかん管理:抗てんかん薬による発作コントロール(小児脳神経科)
- 精神発達遅滞への対応:早期療育・支援体制の整備
- 頭痛・片麻痺:神経症状の経過観察と対症療法
- 多科連携:眼科・小児神経科・皮膚科・てんかん専門医・療育チームの協力体制
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”血管過誤腫としての本態
Section titled “血管過誤腫としての本態”びまん性脈絡膜血管腫は、発生学的には血管過誤腫(hamartoma)と位置づけられる。過誤腫とは、本来その部位に存在する組織成分が異常に増殖した良性腫瘍様病変であり、真の腫瘍(neoplasm)とは異なる。本疾患では成熟した血管要素が脈絡膜内に過剰に増殖し、正常な脈絡膜毛細管板や中・大血管の構造が置き換わる。
GNAQ遺伝子変異と分子機序
Section titled “GNAQ遺伝子変異と分子機序”Sturge-Weber症候群の分子基盤として、GNAQ遺伝子の体細胞モザイク変異(c.548G>A, p.Arg183Gln)が多くの症例で同定されている。
- GNAQ(Gqα)の機能:Gタンパク質共役受容体(GPCR)の下流シグナルに関わるGαサブユニット
- 変異の影響:Arg183Gln変異によりGTPase活性が低下し、GNAQが恒常的に活性化状態に維持される
- 下流シグナル:Gqを介したPLC-β活性化→IP3/DAG産生→PKC活性化→MAPKカスケード(MEK/ERK)の恒常的活性化
- 血管形成への影響:VEGF等の血管新生因子の過剰産生が促進され、異常血管形成が引き起こされると考えられる
- 体細胞モザイク変異の意義:胎生早期の一部の細胞にのみ変異が生じるため、発現パターンが個人によって異なり、症状の多様性をもたらす
緑内障の詳細な発症機序
Section titled “緑内障の詳細な発症機序”Sturge-Weber症候群における緑内障発症には少なくとも2つの機序が想定されている。
機序1: 上強膜静脈圧上昇 上強膜(テノン嚢下)の血管腫が上強膜静脈圧を上昇させ、Schlemm管・線維柱帯からの房水流出が障害される。上強膜静脈圧の正常値(約10mmHg)を超えた場合、眼圧はその上昇分だけ付加的に高まる。この機序は小児期以降に発症する後天型緑内障に多い。
機序2: 隅角形成異常 前房隅角の発達異常(前房隅角異形成)により、線維柱帯の発達が不完全となり、房水流出路が解剖学的に機能しない。この機序は乳児期発症(先天緑内障型)に関わることが多い。
漿液性網膜剥離の発症機序
Section titled “漿液性網膜剥離の発症機序”びまん性脈絡膜血管腫の血管透過性が亢進することにより、血管内成分が血管外へ滲出し、網膜下腔に液体が貯留する。これが漿液性網膜剥離を引き起こし、視力低下・視野障害の主因となる。PDTや放射線照射によって腫瘍血管が減少すると、滲出液が減少し網膜が復位する。
眼以外の病態生理
Section titled “眼以外の病態生理”- 脳軟膜血管腫:大脳皮質の血管腫が局所的虚血・石灰化を引き起こし、てんかん・精神発達遅滞・片麻痺の原因となる
- 顔面ポートワイン斑:皮膚の毛細血管拡張として生後より認められる
- 石灰化:脳軟膜血管腫下の大脳皮質に生じる「鉄道レール状」の石灰化がSturge-Weber症候群の画像的特徴
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”GNAQ下流を標的とした分子標的治療
Section titled “GNAQ下流を標的とした分子標的治療”GNAQ変異によって恒常的に活性化されたMAPKカスケード(MEK/ERK経路)は、ブドウ膜メラノーマ研究において治療ターゲットとして広く研究されている。Sturge-Weber症候群/びまん性脈絡膜血管腫においても同一の分子異常が存在することから、MEK阻害薬(trametinib, binimetinib等)や GNAQ直接阻害薬(YM-254890等)の応用が基礎研究レベルで検討されている。
実際にSturge-Weber症候群全体に対する分子標的治療として、mTOR阻害薬(sirolimus)やPI3K-AKT-mTOR経路を標的とした治療が試験的に行われており、一部の患者で症状改善の報告がある。ただし、びまん性脈絡膜血管腫自体への有効性を直接評価した大規模研究は現時点では限られる。
PDTの治療最適化
Section titled “PDTの治療最適化”PDTはびまん性脈絡膜血管腫の漿液性網膜剥離に対して有効であることが複数の症例報告で示されているが、びまん性の広範病変に対するプロトコール(照射野・エネルギー・セッション数)は標準化されていない。限局性脈絡膜血管腫と比較して、びまん性では照射面積が大きく技術的課題がある。今後の多施設前向き研究での確立が期待される。
緑内障管理の新展開
Section titled “緑内障管理の新展開”上強膜静脈圧上昇を機序とする緑内障に対する従来の濾過手術は、上強膜静脈圧亢進状態では脈絡膜滲出・悪性緑内障のリスクがある。これに対してチューブシャント手術(Ahmed弁・Baerveldt管)の有効性に関する研究が進んでいる。また、選択的レーザー線維柱帯形成術(SLT)の応用可能性も検討されている。
GNAQ遺伝子診断の展望
Section titled “GNAQ遺伝子診断の展望”Sturge-Weber症候群の確定診断に皮膚生検・血液検体でのGNAQ変異検出が応用されつつある。将来的には液体生検(ctDNA)による早期診断や、変異検出率の改善によってより確実な診断が可能になると期待される。
8. 参考文献
Section titled “8. 参考文献”- Shirley MD, Tang H, Gallione CJ, et al. Sturge-Weber syndrome and port-wine stains caused by somatic mutation in GNAQ. N Engl J Med. 2013;368(21):1971-1979.
- Baselga E, Torrelo A, Mediero IG, et al. Sturge-Weber syndrome: report of 3 cases. Pediatr Dermatol. 2019;36(6):932-934.
- Bhatt A, Bhatt N. Sturge-Weber syndrome: a rare neurocutaneous disorder. J Pediatr Neurosci. 2021;16(1):1-6.
- Zreik O, Elabassy HM, Bakhurji E, Al-Johani SM. Sturge-Weber syndrome: an updated review. Clin Ophthalmol. 2023;17:2369-2381.
- Nassiri N, Rootman DB, Rootman J, Goldberg RA. Orbital and adnexal lymphangiomas: a review of management. Surv Ophthalmol. 2015;60(3):245-257.
