پراکنده (شایعترین)
الگوی وراثت: غیروراثتی (پراکنده)
توزیع ضایعه: یکطرفه، شبکیه محیطی
سیر بالینی: معمولاً غیرپیشرونده، بدون علامت
عوارض سیستمیک: ندارد

همانژیوم غاری شبکیه (retinal cavernous hemangioma) یک ناهنجاری عروقی شبکیه است که از تجمع وریدهای گشاد شده با جریان کم تشکیل میشود. معمولاً غیرارثی، یکطرفه و غیرپیشرونده است و به صورت منفرد در شبکیه محیطی رخ میدهد. مواردی با درگیری سر عصب بینایی یا ماکولا و مواردی با الگوی اتوزومال غالب همراه با ضایعات پوستی، سیستم عصبی مرکزی و کبد نیز گزارش شده است.
این بیماری دقیقاً تومور نیست، بلکه به عنوان ناهنجاری عروقی طبقهبندی میشود. این توده عروقی از سلولهای اندوتلیال، سلولهای عضله صاف و سلولهای استرومایی تشکیل شده است و تکثیر یک سلول نیست. در طبقهبندی انجمن بینالمللی مطالعه ناهنجاریهای عروقی (ISSVA) به عنوان ناهنجاری وریدی با جریان کم (venous malformation) طبقهبندی میشود و در دستورالعملهای تشخیص و درمان همانژیوم و ناهنجاریهای عروقی نیز گنجانده شده است.
پراکنده (شایعترین)
الگوی وراثت: غیروراثتی (پراکنده)
توزیع ضایعه: یکطرفه، شبکیه محیطی
سیر بالینی: معمولاً غیرپیشرونده، بدون علامت
عوارض سیستمیک: ندارد
خانوادگی (وراثت اتوزومال غالب)
الگوی وراثت: اتوزومال غالب
توزیع ضایعه: یک یا دو چشم، چندگانه
سیر بالینی: همراه با عوارض مغزی، پوستی و کبدی
عوارض سیستمیک: آنژیوم غاری مغز (CCM)، آنژیوم پوستی، آنژیوم کبدی
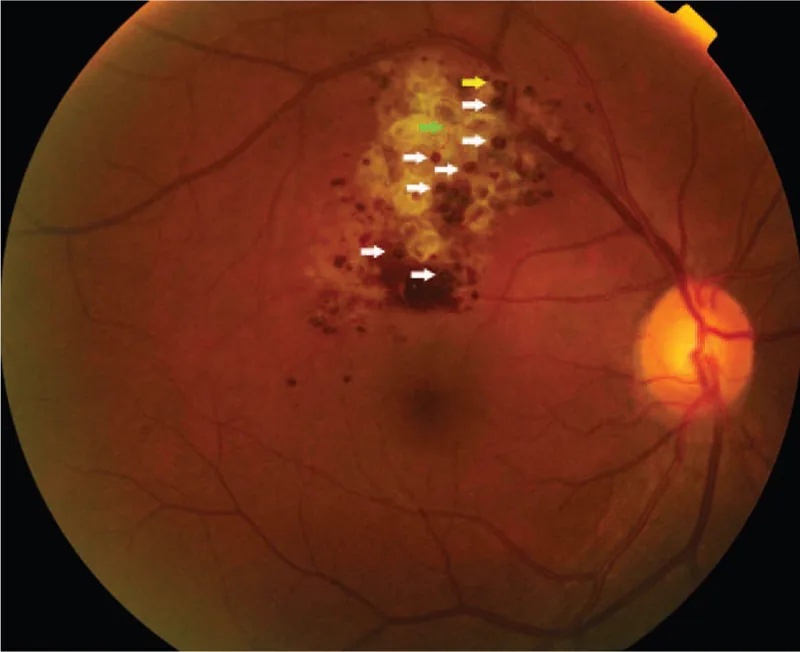
هنگامی که ضایعه به ناحیه محیطی محدود باشد، معمولاً بدون علامت است و اغلب به طور تصادفی در معاینه فوندوس کشف میشود. در مواردی که ضایعه به دیسک بینایی یا ماکولا گسترش یابد، ممکن است اختلال بینایی و نقص میدان بینایی ایجاد شود. اگر یک غشای فیبروپرولیفراتیو روی تومور تشکیل شود و با کشش باعث ترشح یا خونریزی شود، تأثیر بر عملکرد بینایی آشکار میشود.
یافتههای فوندوس در تشخیص این بیماری بسیار مهم هستند. یافتههای مشخصه در زیر آورده شده است.
آنژیوگرافی فلورسین مفیدترین آزمایش برای تشخیص افتراقی است. یافتههای مشخصه در زیر آورده شده است.
در توموگرافی انسجام نوری (OCT)، این ضایعه به صورت یک توده برجسته و کیستیک با بازتاب بالا که از لایههای داخلی شبکیه بیرون زده است، دیده میشود. در آنژیوگرافی توموگرافی انسجام نوری (OCT-A)، جریان خون داخلی ضعیف بوده و ویژگیهای یک ناهنجاری عروقی با جریان کم تأیید میشود.
مکانیسم دقیق ایجاد همانژیوم غاری شبکیه به طور کامل شناخته نشده است. تصور میشود که ناهنجاری در رشد عروق جنینی، یعنی تغییر هامارتوماتوز موضعی سیستم وریدی، علت آن باشد. عوامل خطر محیطی برای موارد پراکنده در حال حاضر شناسایی نشدهاند.
در موارد خانوادگی (با وراثت اتوزومال غالب)، زمینه ژنتیکی مشترکی با ناهنجاری غاری مغز (CCM) وجود دارد. سه ژن زیر به عنوان ژنهای ایجادکننده ناهنجاری غاری مغز شناسایی شدهاند و ارتباط آنها با ناهنجاریهای عروقی سیستمیک از جمله ضایعات چشمی گزارش شده است1).
| ژن | نام دیگر | پروتئین کدشونده | عملکرد اصلی |
|---|---|---|---|
| CCM1 | KRIT1 | Krev interaction trapped 1 | چسبندگی سلولی و هموستاز اندوتلیال عروقی |
| CCM2 | MGC4607 | Malcavernin | اتصال به CCM1 و انتقال سیگنال |
| CCM3 | PDCD10 | Programmed cell death 10 | کنترل آپوپتوز و نفوذپذیری عروق |
این جهشهای ژنی در چسبندگی سلولی، انتقال سیگنال و کنترل نفوذپذیری سلولهای اندوتلیال عروق نقش دارند و منجر به گشاد شدن وریدها و ضعیف شدن دیواره عروق میشوند2).
دادههای دقیق در مورد میزان بروز محدود است، اما آنژیوم کاورنوی شبکیه یک بیماری نادر محسوب میشود3). شیوع مبتنی بر جمعیت آنژیوم کاورنوی مغزی 0.1 تا 0.5٪ تخمین زده میشود، اما نسبت موارد با درگیری چشمی حتی کمتر است. دادههای واضحی در مورد سن شایع و تفاوت جنسیتی وجود ندارد. موارد خانوادگی نادر هستند، اما چندین خانواده با موارد همراه با آنژیوم مغزی، پوستی و کبدی گزارش شده است.
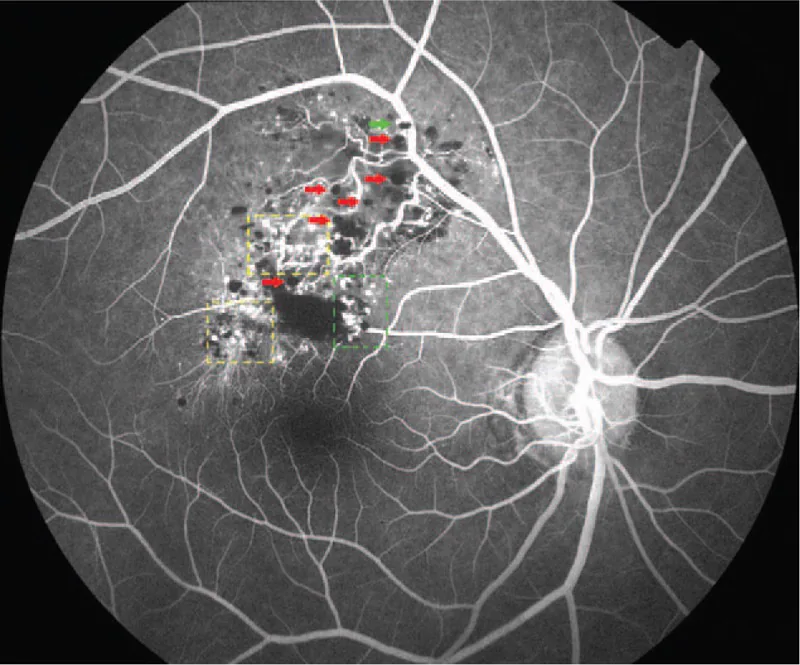
تشخیص عمدتاً بر اساس یافتههای مشخص افتالموسکوپی (توده چندکیستی قرمز تیره به شکل خوشه انگور) و یافتههای آنژیوگرافی فلورسین (علامت کلاهک فلورسنت، الگوی پر شدن وریدی با نشت کم فلورسین) انجام میشود. در موارد معمولی، نیاز به بیوپسی نیست و تشخیص بالینی امکانپذیر است.
در آنژیوم کاورنو شبکیه خانوادگی (اتوزومال غالب)، ارتباط ژنتیکی با آنژیوم کاورنو مغزی (CCM) وجود دارد. جهشهای ژن CCM1، CCM2 و CCM3 علت مشترک هستند و ناهنجاریهای عروقی متعدد در شبکیه، مغز، پوست و کبد ایجاد میکنند. در موارد خانوادگی، MRI مغز با کنتراست ضروری است تا ضایعات مغزی ناشناخته (که میتوانند باعث صرع یا خونریزی مغزی شوند) رد شوند. در موارد پراکنده، ارتباطی با ضایعات مغزی نشان داده نشده است.
مهمترین تشخیص افتراقی آنژیوم کاورنو شبکیه، همانژیوم مویرگی شبکیه (بیماری VHL) است. یافتههای آنژیوگرافی فلورسئین مهمترین نکته برای افتراق دو بیماری است.
| بیماری | یافتههای فوندوس | یافتههای FA | عوارض سیستمیک | درمان |
|---|---|---|---|---|
| آنژیوم کاورنو شبکیه | توده چندکیستیک قرمز تیره (شبیه خوشه انگور) | پر شدن وریدی آهسته، علامت کلاهک فلورسنت، نشت کم | CCM (خانوادگی) | معمولاً پیگیری |
| همانژیوم مویرگی شبکیه (بیماری VHL) | تومور نیمهشفاف نارنجی-قرمز همراه با عروق ورودی و خروجی گشاد شده | پر شدن سریع در فاز شریانی، نشت شدید فلورسین | تومورهای VHL (مانند کارسینوم سلول کلیوی) | لیزر، جراحی، ضد VEGF |
| بیماری کوتس | جداشدگی اگزوداتیو شبکیه، آنوریسم مویرگی | نشت شدید از آنوریسم مویرگی | ندارد (بیشتر در کودکان) | لیزر، جراحی |
| تومور پرولیفراتیو عروقی شبکیه | توده زرد-سفید محیطی | پر شدن تدریجی و نشت | ندارد | لیزر، PDT |
هر دو بیماری ضایعات عروقی شبکیه هستند، اما با آنژیوگرافی فلورسئین به وضوح قابل تشخیص هستند. در همانژیوم مویرگی شبکیه (بیماری VHL)، تومور نارنجی-قرمز با عروق ورودی و خروجی گشاد شده مشخص میشود و در FA از فاز شریانی به سرعت پر شده و نشت شدید فلورسئین دیده میشود. در مقابل، همانژیوم غاری شبکیه با پر شدن آهسته در فاز پر شدن وریدی و علامت کلاهک فلورسنت مشخص میشود و حتی در مراحل پایانی نشت فلورسئین کمی دارد. در معاینه فوندوس، همانژیوم غاری شبکیه به صورت تودههای قرمز تیره چندکیسهای شبیه خوشه انگور دیده میشود و معمولاً تشخیص افتراقی امکانپذیر است.
همانژیوم غاری شبکیه غیرپیشرونده است و معمولاً نیازی به درمان ندارد. ممکن است غشای فیبروواسکولار روی ضایعه تشکیل شود که میتواند باعث ترشح یا خونریزی ناشی از کشش شود. در موارد بدون علامت و بدون عارضه، پیگیری با معاینات منظم فوندوس انجام میشود.
در صورت بروز عوارض زیر، درمان در نظر گرفته میشود.
ویترکتومی: در صورت بروز جداشدگی شبکیه کششی ناشی از غشای فیبروواسکولار یا خونریزی زجاجیه همراه با کشش، ویترکتومی در نظر گرفته میشود. از آنجایی که این ضایعه یک ناهنجاری عروقی با جریان کم است، خطر خونریزی حین و بعد از عمل مشابه جراحی معمول شبکیه است. نتایج جراحی عمدتاً بر اساس گزارش موارد است و شواهد گسترده محدود است4).
فتوکوآگولاسیون لیزری: به دلیل جریان کم در ناهنجاری عروقی، پاسخ به فتوکوآگولاسیون ضعیف است. در حال حاضر به طور فعال توصیه نمیشود.
در موارد خانوادگی، علاوه بر مدیریت ضایعات چشمی، مدیریت نورولوژیک برای آنژیوم کاورنوی مغزی اهمیت دارد. برای ضایعات مغزی، در صورت بدون علامت بودن، پیگیری پایه است، اما در صورت بروز تشنج یا علائم عصبی، درمان دارویی یا مداخله جراحی در نظر گرفته میشود5).
معمولاً نیازی به درمان نیست. این یک ناهنجاری عروقی غیرپیشرونده است و در موارد بدون علامت، پیگیری با معاینات منظم فوندوسکوپی رویکرد اصلی است. تنها در صورت بروز عوارض کششی ناشی از غشای فیبروپرولیفراتیو (جداشدگی کششی شبکیه یا خونریزی زجاجیه) جراحی ویترکتومی اندیکاسیون دارد. فوتوکواگولاسیون لیزری به دلیل جریان کم مؤثر نیست و معمولاً انجام نمیشود. در موارد خانوادگی، علاوه بر پیگیری چشمی، مدیریت سیستمیک آنژیوم مغزی ضروری است.
آنژیوم کاورنوی شبکیه یک تومور نیست، بلکه یک ناهنجاری عروقی است. این توده عروقی متشکل از سلولهای اندوتلیال عروقی، سلولهای عضله صاف و سلولهای بینابینی است و ویژگی اصلی آن عدم تکثیر سلولی (رشد توموری) است. در طبقهبندی اصلاحشده ISSVA (انجمن بینالمللی ناهنجاریهای عروقی) در سال 2018، به عنوان ناهنجاری وریدی کمجریان (venous malformation) طبقهبندی میشود و از ناهنجاری شریانی-وریدی (جریان بالا) متمایز است6).
در موارد خانوادگی (اتوزومال غالب)، جهشهای از دستدهنده عملکرد در ژنهای CCM نقش اصلی را ایفا میکنند. CCM1 (KRIT1) مسیر اینتگرین را که در چسبندگی بین سلولی نقش دارد، تنظیم میکند. CCM2 (malcavernin) به عنوان پروتئین داربستی برای CCM1 عمل میکند. CCM3 (PDCD10) در تنظیم آپوپتوز و نفوذپذیری عروقی نقش دارد2). این جهشها منجر به فروپاشی چسبندگی بین سلولی سلولهای اندوتلیال عروقی، انتقال اندوتلیال به مزانشیمی (endothelial-to-mesenchymal transition)، اتساع عروق و افزایش نفوذپذیری میشوند.
در موارد پراکنده (غیرارثی)، جهشهای سوماتیک (somatic mutation) به عنوان علت ناهنجاری موضعی عروقی مطرح است. تصور میشود که ناهنجاری در فرآیند تکامل عروق شبکیه در دوره جنینی منجر به تشکیل اتساعهای وریدی کیستیک چندگانه به شکل خوشه انگور میشود، اما مکانیسم دقیق هنوز ناشناخته است.
ناهنجاری وریدی کمجریان بودن ویژگی بالینی این بیماری را تعیین میکند. به دلیل جریان خون کم، ویژگیهای زیر ایجاد میشود:
در سطح ناهنجاری عروقی (سمت زجاجیه) ممکن است کلاهک گلیوز (gliotic cap) یا غشای پرولیفراتیو فیبروز تشکیل شود. انقباض این غشا میتواند باعث جداشدگی کششی شبکیه یا خونریزی زجاجیه شود. غشای پرولیفراتیو فیبروز تومورال نیست، بلکه یک پرولیفراسیون واکنشی ثانویه است.
شناسایی مکانیسمهای مولکولی ناشی از جهشهای ژن CCM در حال پیشرفت است. در مطالعات حیوانی، مهارکنندههای سیگنالینگ Rho/ROCK و مهارکنندههای مسیر PI3K/Akt/mTOR نتایج امیدوارکنندهای در مدلهای آنژیوم کاورنوی مغزی نشان دادهاند7). کاربرد آن در ضایعات چشمی نیاز به تحقیقات بیشتر دارد.
آزمایش پانل چندژنی با توالییابی نسل بعدی (NGS) رایجتر شده و برای تشخیص قطعی موارد خانوادگی، تشخیص ناقلان و مشاوره ژنتیک خانوادهها استفاده میشود. تفسیر واریانتهای پاتوژنیک جهشهای ژن CCM نیز در حال انباشته شدن است1).
در مورد مدیریت عوارض کششی با ویترکتومی، مقالات در سطح گزارش مورد و سری موارد در حال انباشته شدن است4,8). هیچ کارآزمایی تصادفیسازی شده در مقیاس بزرگ وجود ندارد و تحقیقات آیندهنگر مورد انتظار است.
Fischer A, Zalvide J, Faurobert E, et al. Cerebral cavernous malformations: from CCM genes to endothelial cell homeostasis. Trends Mol Med. 2013;19(5):302-308.
Couteulx SL, Jung HH, Labauge P, et al. Truncating mutations in CCM1, encoding KRIT1, cause hereditary cavernous angiomas. Nat Genet. 1999;23(2):189-193.
Gass JDM. Cavernous hemangioma of the retina. A neuro-oculocutaneous syndrome. Am J Ophthalmol. 1971;71(4):799-814.
Messmer EP, Font RL, Laqua H, et al. Cavernous hemangioma of the retina. Immunohistochemical and ultrastructural observations. Arch Ophthalmol. 1984;102(3):413-418.
Haller JA Jr, Dortz J, Goldberg MF. Familial retinal cavernous hemangiomas. Arch Ophthalmol. 1979;97(5):879-883.
ISSVA Classification of Vascular Anomalies. International Society for the Study of Vascular Anomalies. 2018 update. Available at: https://www.issva.org.
Lewis RA, Cohen BH, Wise GN. Cavernous haemangioma of the retina and optic disc. A report of three cases and a review of the literature. Br J Ophthalmol. 1975;59(8):422-434.
Shields JA, Shields CL, Timmers E, et al. Spectrum of vitreoretinal surgery. Retina. 1992;12(1):1-11.