散发性(最常见)
遗传方式:非遗传性(散发性)
病变分布:单眼、周边视网膜
临床经过:通常为非进行性、无症状
全身并发症:无

视网膜海绵状血管瘤(retinal cavernous hemangioma)是由低流量扩张静脉聚集形成的视网膜血管畸形。通常为非遗传性、单眼、非进行性,在周边视网膜散发发生。也有病变位于视盘或黄斑部、以及呈常染色体显性遗传并合并皮肤、中枢神经和肝血管瘤的病例报道。
本病严格来说不是肿瘤,而是血管畸形。它是由血管内皮细胞、平滑肌细胞和间质细胞等构成的血管团块,并非单一细胞增殖。根据国际血管畸形研究学会(ISSVA)分类,它属于低流量静脉畸形,也是血管瘤和血管畸形诊疗指南的靶向疾病。
散发性(最常见)
遗传方式:非遗传性(散发性)
病变分布:单眼、周边视网膜
临床经过:通常为非进行性、无症状
全身并发症:无
家族性(常染色体显性遗传)
遗传方式:常染色体显性
病变分布:单眼或双眼、多发性
临床经过:可伴有脑、皮肤、肝脏并发症
全身并发症:脑海绵状血管瘤(CCM)、皮肤血管瘤、肝血管瘤
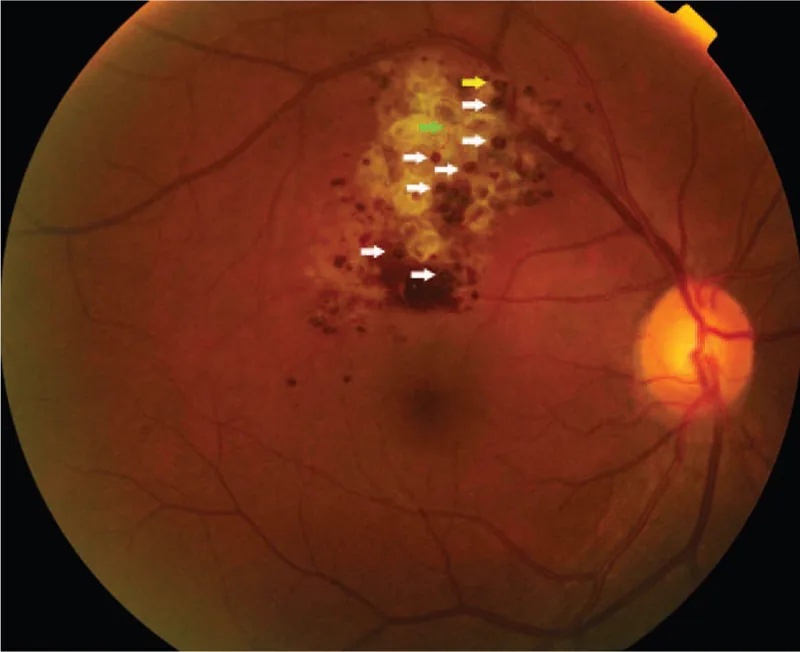
当病变局限于周边部时,通常无症状,常在眼底检查中偶然发现。当病变累及视乳头或黄斑时,可能出现视力障碍和视野缺损。当纤维增殖膜在肿瘤上形成,并因牵拉导致渗出或出血时,对视觉功能的影响会变得明显。
眼底所见对本病的诊断最为重要。特征性表现如下所示。
荧光眼底造影是鉴别诊断最有用的检查。特征性表现如下所示。
在光学相干断层扫描(OCT)上,表现为从视网膜内层突出的囊状隆起性高反射肿块。OCT血管成像(OCT-A)显示内部血流稀少,证实其作为低流量血管畸形的特征。
视网膜海绵状血管瘤的确切发生机制尚未完全阐明。目前认为是由胚胎期血管发育异常,即静脉系统局灶性错构瘤样改变所致。目前尚未确定散发病例的环境危险因素。
家族性病例(常染色体显性遗传)与脑海绵状血管畸形(CCM)具有共同的遗传背景。目前已鉴定出以下三个脑海绵状血管畸形的致病基因,并报道其与包括眼部病变在内的全身性血管畸形相关1)。
| 基因 | 别名 | 编码蛋白 | 主要功能 |
|---|---|---|---|
| CCM1 | KRIT1 | Krev相互作用捕获蛋白1 | 细胞黏附与血管内皮稳态 |
| CCM2 | MGC4607 | Malcavernin | 与CCM1结合及信号转导 |
| CCM3 | PDCD10 | 程序性细胞死亡10 | 调节细胞凋亡和血管通透性 |
这些基因突变参与血管内皮细胞的细胞黏附、信号转导和通透性调控,导致静脉扩张和血管壁脆弱化2)。
准确的发病率数据有限,但视网膜海绵状血管瘤被认为是一种罕见疾病3)。脑海绵状血管瘤的人群患病率为0.1%–0.5%,但伴有眼部病变的比例更低。关于发病年龄和性别差异的明确数据缺乏。家族性病例罕见,但已有多个合并脑、皮肤和肝脏血管瘤的家系报道。
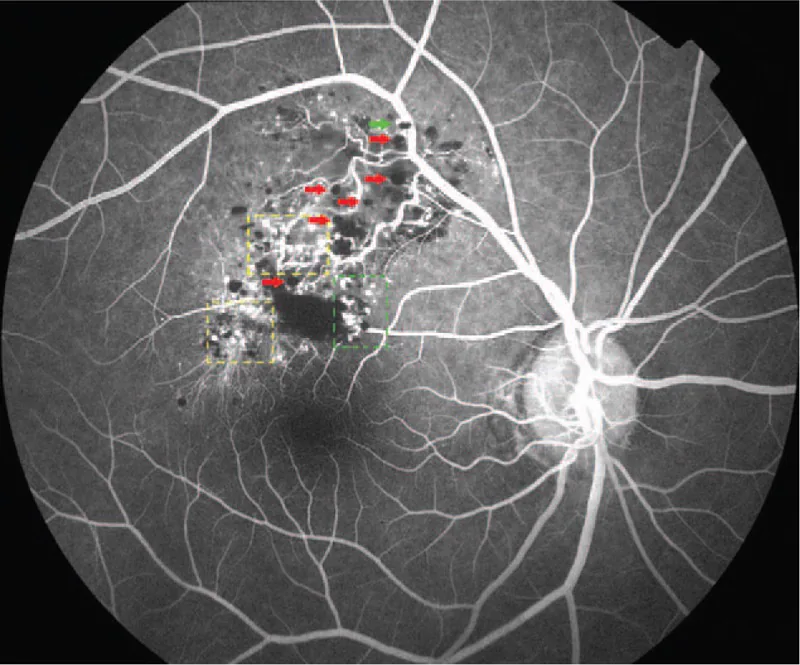
诊断主要基于特征性眼底表现(葡萄串样多囊性暗红色肿块)和荧光眼底造影表现(荧光帽征、静脉期填充模式且无明显渗漏)。典型病例无需活检即可临床诊断。
家族性(常染色体显性遗传)视网膜海绵状血管瘤与脑海绵状血管瘤(CCM)有遗传关联。CCM1、CCM2、CCM3基因突变是共同原因,导致视网膜、脑、皮肤、肝脏多发血管畸形。家族性病例必须进行脑部增强MRI,以排除未发现的脑部病变(可能引起癫痫或脑出血)。散发性病例未显示与脑部病变相关。
视网膜海绵状血管瘤最重要的鉴别诊断是视网膜毛细血管瘤(VHL病)。荧光眼底造影结果是区分两者的关键。
| 疾病 | 眼底所见 | FA所见 | 全身并发症 | 治疗 |
|---|---|---|---|---|
| 视网膜海绵状血管瘤 | 多囊状暗红色肿块(葡萄串样) | 缓慢静脉充盈、荧光帽征、渗漏少 | CCM(家族性) | 通常观察 |
| 视网膜毛细血管瘤(VHL病) | 橙红色半透明肿瘤 + 扩张的输入和输出血管 | 动脉期快速充盈,大量荧光素渗漏 | VHL肿瘤(如肾细胞癌) | 激光、手术、抗VEGF |
| Coats病 | 渗出性视网膜脱离、毛细血管瘤 | 毛细血管瘤大量渗漏 | 无(多见于儿童) | 激光、手术 |
| 视网膜血管增生性肿瘤 | 周边部黄白色肿块 | 渐进性充盈和渗漏 | 无 | 激光、PDT |
两种疾病都是视网膜的血管性病变,但可通过荧光眼底血管造影明确区分。视网膜毛细血管瘤(VHL病)的特征是伴有扩张的流入和流出血管的橙红色肿瘤,FA显示从动脉期快速充盈并出现强烈的荧光渗漏。而视网膜海绵状血管瘤的特征是静脉充盈期缓慢充盈和荧光帽征,即使在晚期荧光渗漏也很少。眼底检查中,视网膜海绵状血管瘤表现为葡萄串样的多囊性暗红色肿块,通常可以鉴别。
视网膜海绵状血管瘤是非进行性的,通常不需要治疗。病变上可能形成纤维增殖膜,可能因牵引导致渗出或出血。在无症状且无并发症的病例中,通过定期眼底检查进行随访。
出现以下并发症时考虑治疗。
玻璃体手术: 当纤维增殖膜导致牵引性视网膜脱离或牵引导致玻璃体出血时,考虑玻璃体手术。由于是低流量血管畸形,术中及术后出血风险与一般视网膜手术相当。手术结果多为病例报告,缺乏大规模证据4)。
激光光凝: 由于是低流量血管畸形,对光凝反应差。目前不积极推荐。
在家族性病例中,不仅需要管理眼部病变,还需要对脑海绵状血管瘤进行神经内科管理。对于脑部病变,无症状时以观察为主,但如果出现癫痫发作或神经症状,应考虑药物治疗或外科干预 5)。
视网膜海绵状血管瘤不是肿瘤,而是血管畸形。它是由血管内皮细胞、平滑肌细胞和间质细胞等构成的血管团块,本质特征不是单一细胞的增殖(即肿瘤性增殖)。在国际血管畸形研究学会(ISSVA)2018年修订分类中,它被归类为低流量静脉畸形,与动静脉畸形(高流量)相区别 6)。
在家族性(常染色体显性遗传)病例中,CCM基因的功能丧失突变起核心作用。CCM1(KRIT1)调节参与细胞间黏附的整合素通路,CCM2(malcavernin)作为CCM1的支架蛋白,CCM3(PDCD10)参与凋亡调控和血管通透性调节 2)。这些突变导致血管内皮细胞间黏附破坏,进而引起内皮-间质转化、血管扩张和通透性增加。
在散发性(非遗传性)病例中,提示体细胞突变导致局部血管发育异常。胚胎期视网膜血管发育过程中的异常可能形成葡萄串样多囊状静脉扩张,但详细机制尚不明确。
低流量静脉畸形的特性决定了本病的临床特征。由于血流量少,产生以下特点:
血管畸形表面(玻璃体侧)可能形成胶质帽或纤维增殖膜。该膜收缩可导致牵拉性视网膜脱离或玻璃体出血。纤维增殖膜并非肿瘤性,而是继发性反应性增殖。
CCM基因突变导致的分子机制正在逐步阐明。在动物实验中,Rho/ROCK信号传导抑制剂、PI3K/Akt/mTOR通路抑制剂等在脑海绵状血管瘤模型中显示出有希望的结果7)。应用于眼部病变需要进一步研究。
基于下一代测序(NGS)的多基因面板检测已普及,用于家族性病例的确诊、携带者诊断和家族遗传咨询。CCM基因突变的致病性变异解读也在积累中1)。
关于玻璃体手术治疗牵拉性并发症,病例报告和病例系列文献正在积累中4,8)。尚无大规模随机对照试验,期待未来的前瞻性研究。
Fischer A, Zalvide J, Faurobert E, et al. Cerebral cavernous malformations: from CCM genes to endothelial cell homeostasis. Trends Mol Med. 2013;19(5):302-308.
Couteulx SL, Jung HH, Labauge P, et al. Truncating mutations in CCM1, encoding KRIT1, cause hereditary cavernous angiomas. Nat Genet. 1999;23(2):189-193.
Gass JDM. Cavernous hemangioma of the retina. A neuro-oculocutaneous syndrome. Am J Ophthalmol. 1971;71(4):799-814.
Messmer EP, Font RL, Laqua H, et al. Cavernous hemangioma of the retina. Immunohistochemical and ultrastructural observations. Arch Ophthalmol. 1984;102(3):413-418.
Haller JA Jr, Dortz J, Goldberg MF. Familial retinal cavernous hemangiomas. Arch Ophthalmol. 1979;97(5):879-883.
ISSVA Classification of Vascular Anomalies. International Society for the Study of Vascular Anomalies. 2018 update. Available at: https://www.issva.org.
Lewis RA, Cohen BH, Wise GN. Cavernous haemangioma of the retina and optic disc. A report of three cases and a review of the literature. Br J Ophthalmol. 1975;59(8):422-434.
Shields JA, Shields CL, Timmers E, et al. Spectrum of vitreoretinal surgery. Retina. 1992;12(1):1-11.