桑葚样(mulberry型)

视网膜星形细胞瘤
一目了然的要点
Section titled “一目了然的要点”1. 什么是视网膜星形细胞瘤?
Section titled “1. 什么是视网膜星形细胞瘤?”视网膜星形细胞错构瘤是由视网膜星形胶质细胞过度增殖形成的良性肿瘤。错构瘤是指该部位正常存在的成熟组织成分以异常比例混合形成的肿瘤样病变。不会恶变。
本病可伴发于结节性硬化症(TSC),也可为不伴TSC的散发。结节性硬化症是一种常染色体显性多系统疾病,可在多种器官发生错构瘤,表现为颅内病变引起的癫痫、皮肤皮脂腺瘤、肾血管平滑肌脂肪瘤、视网膜错构瘤等多种症状。
已知致病基因有两个:TSC1(9号染色体)和TSC2(16号染色体)。TSC1编码hamartin,TSC2编码tuberin,两者功能异常导致mTOR(雷帕霉素靶蛋白)通路调控障碍。
存在不伴TSC的散发。散发者双眼发病罕见,无全身并发症,以眼科管理为主。而TSC伴发者需多器官管理,因此确诊时鉴别TSC很重要。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”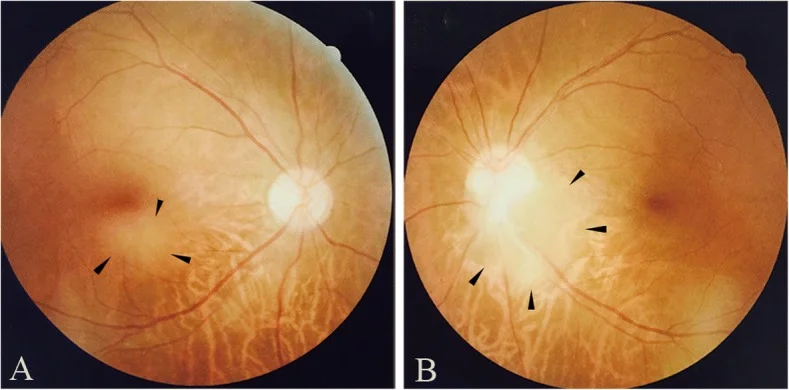
视网膜星形细胞错构瘤通常无症状,常在结节性硬化症的筛查眼底检查中偶然发现。少数情况下可能出现视力下降或飞蚊症。当肿瘤位于黄斑部时,对视力影响较大。
眼底出现特征性的白色隆起病变。根据外观不同分为以下两型。
荧光眼底造影所见
Section titled “荧光眼底造影所见”荧光眼底造影(FAG)中,早期可见肿瘤内微细血管显影。晚期无荧光渗漏是本病的特征性所见,是与晚期出现荧光渗漏的视网膜母细胞瘤的重要鉴别点。
在光学相干断层扫描(OCT)上,肿瘤表现为从视网膜内层隆起的强反射肿块。其特征是内部层状结构紊乱,与周围正常视网膜边界相对清晰。
3. 病因与风险因素
Section titled “3. 病因与风险因素”结节性硬化症(TSC)为常染色体显性遗传。患病率约为每6000至10000人中有1人。据报道,TSC患者中视网膜错构瘤的合并率约为50%,可表现为双眼性和多发性。
TSC1基因(9号染色体q34)突变倾向于引起较轻的症状,而TSC2基因(16号染色体p13.3)突变更可能导致严重的全身性病变。新生突变也很常见,因此即使没有家族史也不能排除TSC。
在散发性病例(非TSC)中,遗传背景不同,可能涉及局限的体细胞突变。散发性病例通常为单眼、单发,不伴有全身并发症。
- 结节性硬化症(TSC)的家族史或确诊
- 已知的TSC基因突变(TSC1或TSC2)
- 多发性中枢神经系统、皮肤或肾脏病变病史
未见明确的性别差异。在TSC相关病例中,出生后早期即可发现眼底病变,建议将眼底检查作为儿科筛查的一部分。散发性病例也可在成人中发现,但均呈良性经过。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”视网膜星形细胞错构瘤的诊断需结合特征性眼底表现和结节性硬化症的全身表现。
眼底检查的鉴别要点:
- 白色隆起病变呈桑葚样或扁平型
- 荧光眼底造影无晚期荧光渗漏
- 隆起轻微,边缘平滑
- 随访观察无增大
- 即使有钙化,黄色调也较强
最重要的鉴别疾病是视网膜母细胞瘤。当儿童出现白色隆起视网膜病变时,首先需排除视网膜母细胞瘤。
| 疾病名称 | 鉴别要点 |
|---|---|
| 视网膜母细胞瘤 | 快速增大、晚期荧光渗漏、钙化(白色调) |
| 视网膜细胞瘤 | 非活动性、钙化退缩像、无增大 |
| 孤立性脉络膜血管瘤 | 橙红色,荧光眼底造影显示增强 |
结节性硬化症的诊断
Section titled “结节性硬化症的诊断”当发现视网膜错构瘤时,应根据TSC诊断标准(Northrup修订版2012年1))进行全身评估。主要标准包括面部血管纤维瘤、癫痫和鲨革斑。确诊TSC需要与儿科和神经科协作。
5. 标准治疗方法
Section titled “5. 标准治疗方法”视网膜星形细胞错构瘤通常不增大。若无症状且无增大,则无需治疗,以观察为主。应定期进行眼底检查,以确认有无增大或出血。
治疗适应症和手术方式
Section titled “治疗适应症和手术方式”如果反复出血,可考虑以下治疗。
玻璃体手术
适应症:反复出血导致玻璃体积血,或伴有牵拉性视网膜改变时。
目的:清除玻璃体积血,解除牵拉,维持视功能。
预后:若手术适应症恰当,可望维持视力。
视网膜光凝
适应症:肿瘤边缘渗出或出血轻微时的辅助治疗。
目的:封闭肿瘤血管的出血源,预防再出血。
注意:黄斑部病变时需谨慎判断光凝适应症。
如果眼部病变不增大,则无需积极治疗。在结节性硬化症伴发的情况下,应与儿科和神经科医生共同管理中枢神经系统病变(癫痫、室管膜下巨细胞星形细胞瘤SEGA)、肾血管平滑肌脂肪瘤等全身病变。
**mTOR抑制剂(依维莫司)**对结节性硬化症相关的全身肿瘤(SEGA和肾血管平滑肌脂肪瘤)有医保适应症,作为全身TSC治疗的一部分,已有肿瘤缩小效果的报道2)3)。对视网膜错构瘤的直接有效性证据有限,但在全身TSC治疗背景下给药的患者中有缩小的报道。
如果无症状且不增大,则无需治疗,定期眼底检查随访是基本原则。仅在反复出血时进行玻璃体手术或视网膜光凝。在结节性硬化症伴发的情况下,眼科管理与全身疾病管理并行非常重要。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”TSC1/TSC2-mTOR通路障碍
Section titled “TSC1/TSC2-mTOR通路障碍”视网膜星形细胞错构瘤的病理源于TSC1(错构瘤蛋白)和TSC2(马铃薯球蛋白)基因产物的功能丧失。
错构瘤蛋白和马铃薯球蛋白形成复合物,作为肿瘤抑制因子抑制mTOR(雷帕霉素靶蛋白)复合物1(mTORC1)的活性。当TSC1或TSC2突变导致这种mTOR调节功能丧失时,mTORC1过度激活。
mTORC1过度激活通过S6激酶(S6K)和4E-BP1的磷酸化促进细胞增殖、蛋白质合成和血管生成。结果,星形细胞异常增殖,形成错构瘤(良性肿瘤)。
二次打击假说
Section titled “二次打击假说”肿瘤的发生被认为与“二次打击假说”有关。在生殖细胞系中携带TSC1或TSC2一个等位基因突变的个体中,视网膜细胞发生体细胞突变(第二次打击),导致剩余正常等位基因功能丧失(LOH:杂合性缺失),mTOR通路调控完全崩溃,从而形成肿瘤。
错构瘤的组织学特征
Section titled “错构瘤的组织学特征”视网膜星形细胞错构瘤是由星形胶质细胞增殖构成的良性肿瘤,不会发生恶性转化。组织学上,异常增殖的星形胶质细胞密集排列,部分伴有钙沉积(钙化)。细胞分裂速度缓慢,与肿瘤缓慢增大的临床特征相对应。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”mTOR抑制剂在结节性硬化症相关肿瘤中的应用
Section titled “mTOR抑制剂在结节性硬化症相关肿瘤中的应用”依维莫司(everolimus)作为一种mTORC1抑制剂,用于治疗结节性硬化症相关肿瘤。在EXIST-1试验(针对SEGA)2)中,依维莫司组SEGA体积减少≥50%的患者比例显著高于安慰剂组。EXIST-2试验(针对肾血管平滑肌脂肪瘤)3)也报告了类似的肿瘤缩小效果。
关于mTOR抑制剂对TSC相关视网膜错构瘤的眼科疗效,目前仅有有限的病例报告。有报道称,作为全身性TSC治疗的一部分接受依维莫司的患者观察到视网膜错构瘤缩小,但尚未建立大规模前瞻性试验的证据。
预后与长期随访的挑战
Section titled “预后与长期随访的挑战”眼底错构瘤通常不增大,但少数病例可能增大并引起出血或渗出。关于增大风险因素的识别、长期视力变化的预测以及适当干预时机的判断,需要进一步的病例积累和前瞻性研究。
散发性视网膜星形细胞错构瘤的病理
Section titled “散发性视网膜星形细胞错构瘤的病理”不伴有TSC的散发性病例的遗传背景和分子机制尚未完全阐明。有研究表明体细胞突变导致的局部mTOR通路异常可能参与其中,但详细机制的阐明是未来的研究课题。
8. 参考文献
Section titled “8. 参考文献”-
Northrup H, Krueger DA; International Tuberous Sclerosis Complex Consensus Group. Tuberous sclerosis complex diagnostic criteria update: recommendations of the 2012 International Tuberous Sclerosis Complex Consensus Conference. Pediatr Neurol. 2013;49(4):243-254.
-
Franz DN, Belousova E, Sparagana S, et al. Efficacy and safety of everolimus for subependymal giant cell astrocytomas associated with tuberous sclerosis complex (EXIST-1): a multicentre, randomised, placebo-controlled phase 3 trial. Lancet. 2013;381(9861):125-132.
-
Bissler JJ, Kingswood JC, Radzikowska E, et al. Everolimus for angiomyolipoma associated with tuberous sclerosis complex or sporadic lymphangioleiomyomatosis (EXIST-2): a multicentre, randomised, double-blind, placebo-controlled trial. Lancet. 2013;381(9869):817-824.
-
Shields CL, Shields JA, Kiratli H, et al. Familial retinal astrocytoma. Retina. 2002;22(1):95-97.
-
Rowley SA, O’Callaghan FJ, Osborne JP. Ophthalmic manifestations of tuberous sclerosis: a population based study. Br J Ophthalmol. 2001;85(4):420-423.
-
Zimmer-Galler I, Robertson DM. Long-term observation of retinal lesions in tuberous sclerosis. Am J Ophthalmol. 1995;119(3):318-324.
-
Lucchese NJ, Goldberg MF. Iris and fundus pigmentary changes in tuberous sclerosis. J Pediatr Ophthalmol Strabismus. 1981;18(4):45-48.
