뽕나무형 (mulberry형)

망막 성상세포종
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 망막성상세포종이란?
섹션 제목: “1. 망막성상세포종이란?”망막성상세포과오종은 망막의 별아교세포(성상세포)가 과도하게 증식한 양성 종괴이다. 과오종(hamartoma)이란 원래 그 부위에 존재하는 성숙 조직의 구성 성분이 비정상적인 비율로 혼재된 종괴양 병변을 말한다. 악성화되지 않는다.
이 질환은 결절성경화증(tuberous sclerosis complex; TSC)에 동반되는 경우와 TSC 없이 발생하는 산발적인 경우가 모두 존재한다. 결절성경화증은 여러 장기에 과오종을 일으키는 상염색체 우성의 다계통 질환으로, 두개내 병변에 의한 간질, 피부의 피지선종, 신혈관근지방종, 망막과오종 등 다양한 증상을 나타낸다.
원인 유전자는 TSC1(9번 염색체)과 TSC2(16번 염색체) 두 가지가 알려져 있다. TSC1은 하마르틴(hamartin), TSC2는 튜베린(tuberin)을 각각 코딩하며, 두 유전자의 기능 이상이 mTOR(mechanistic target of rapamycin) 경로의 조절 장애를 유발한다.
TSC를 동반하지 않은 산발적인 경우가 존재한다. 산발적인 경우 양안성은 드물고, 전신 합병증이 없으므로 안과적 관리가 주가 된다. 반면 TSC 동반 예에서는 전신의 다장기 관리가 필요하므로, 확진 시 TSC의 감별이 중요하다.
2. 주요 증상과 임상 소견
섹션 제목: “2. 주요 증상과 임상 소견”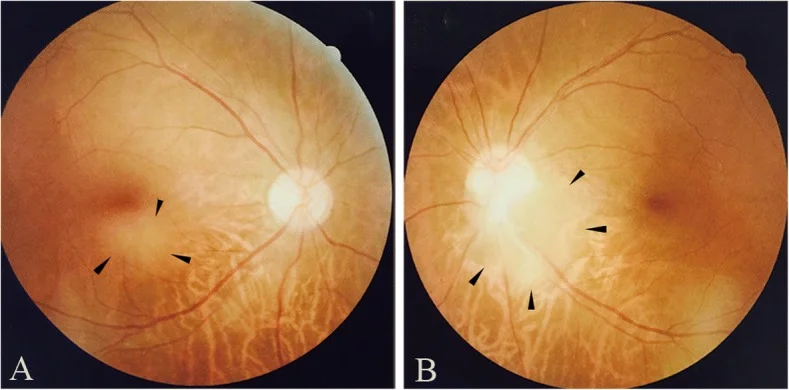
자각 증상
섹션 제목: “자각 증상”망막 성상세포 과오종은 종종 무증상이며, 결절성 경화증 선별 안저 검사에서 우연히 발견됩니다. 드물게 시력 저하나 비문증이 발생할 수 있습니다. 종양이 황반부에 위치하면 시력에 미치는 영향이 큽니다.
안저 소견
섹션 제목: “안저 소견”안저에 특징적인 흰색 융기 병변이 나타납니다. 외관의 차이에 따라 다음 두 가지 유형으로 분류됩니다.
평탄형
형광 안저 조영 소견
섹션 제목: “형광 안저 조영 소견”형광 안저 조영술(FAG)에서는 조기에 종양 내 미세 혈관이 묘사됩니다. 후기에도 형광 누출을 보이지 않는 것이 본 질환의 특징적인 소견이며, 후기에 형광 누출을 보이는 망막모세포종과의 중요한 감별점이 됩니다.
OCT 소견
섹션 제목: “OCT 소견”광간섭단층촬영(OCT)에서 종양은 망막 내층에서 융기하는 고반사 종괴로 나타납니다. 내부 층상 구조의 혼란과 주변 정상 망막과의 경계가 비교적 명확한 점이 특징적입니다.
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”유전적 배경
섹션 제목: “유전적 배경”결절성 경화증(TSC)은 상염색체 우성 유전 양식을 따릅니다. 유병률은 약 6,000~10,000명당 1명으로 알려져 있습니다. TSC 환자에서 망막 과오종의 동반율은 약 50%로 보고되며, 양안성 및 다발성으로 나타날 수 있습니다.
TSC1 유전자(9번 염색체 q34) 돌연변이는 경증 경향을, TSC2 유전자(16번 염색체 p13.3) 돌연변이는 더 중증의 전신 병변을 유발하기 쉽습니다. 새로 발생한 돌연변이도 많아 가족력이 없더라도 TSC를 배제할 수 없습니다.
산발성(비TSC) 사례에서는 유전적 배경이 다르며, 국소적 체세포 돌연변이가 관여할 수 있습니다. 산발성 사례는 일반적으로 단안성, 단발성이며 전신 합병증을 동반하지 않습니다.
위험 요인
섹션 제목: “위험 요인”- 결절성 경화증(TSC)의 가족력 또는 확진
- 알려진 TSC 유전자 돌연변이(TSC1 또는 TSC2)
- 다발성 중추신경계, 피부 또는 신장 병변의 병력
명확한 성별 차이는 보고되지 않았습니다. TSC 동반 사례에서는 출생 후 조기에 안저 병변이 확인될 수 있으며, 소아과적 선별 검사의 일환으로 안저 검사가 권장됩니다. 산발성 사례는 성인에서도 발견될 수 있지만, 모두 양성 경과를 보입니다.
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”임상 진단
섹션 제목: “임상 진단”망막성상세포과오종의 진단은 특징적인 안저 소견과 결절성 경화증의 전신 소견을 조합하여 이루어집니다.
안저 검사의 감별 포인트:
- 백색 융기 병변이 오디 모양 또는 편평형을 보임
- 형광 안저 촬영에서 후기 형광 누출이 없음
- 융기가 경미하고 가장자리가 완만함
- 경과 관찰 중 크기 증가가 없음
- 석회화가 있어도 황색조가 강함
감별 진단
섹션 제목: “감별 진단”가장 중요한 감별 질환은 망막모세포종입니다. 소아에서 백색 융기 망막 병변이 발견되면 먼저 망막모세포종을 배제해야 합니다.
| 질환명 | 감별 포인트 |
|---|---|
| 망막모세포종 | 급속 성장, 후기 형광 누출, 칼슘 침착(백색조) |
| 망막세포종 | 비활동성, 석회화 퇴축 소견, 크기 증가 없음 |
| 고립성 맥락막 혈관종 | 주황색, 형광 안저 조영술에서 조영 증강 |
결절성 경화증의 진단
섹션 제목: “결절성 경화증의 진단”망막 과오종이 발견된 경우, TSC 진단 기준(Northrup 개정판 2012년1))에 따라 전신 평가를 시행합니다. 주요 기준으로는 안면 혈관 섬유종, 간질, 샤그린 반점 등이 포함됩니다. TSC의 확진을 위해서는 소아과 및 신경과와의 협력이 필수적입니다.
5. 표준 치료법
섹션 제목: “5. 표준 치료법”기본 방침
섹션 제목: “기본 방침”망막 성상 세포 과오종은 일반적으로 커지지 않습니다. 무증상이고 크기 증가가 없는 경우 치료가 필요 없으며 경과 관찰이 기본입니다. 정기적인 안저 검사를 통해 크기 증가나 출혈 여부를 확인합니다.
치료 적응증과 수술법
섹션 제목: “치료 적응증과 수술법”출혈이 반복되는 경우 다음 치료를 고려합니다.
유리체 절제술
적응증: 출혈이 반복되어 유리체 출혈이 발생한 경우 또는 견인성 망막 변화를 동반한 경우.
목적: 유리체 출혈 제거, 견인 해소를 통한 시기능 유지.
예후: 적절한 수술 적응증이라면 시력 유지가 기대됩니다.
망막 광응고
적응증: 종양 가장자리에서 삼출이나 출혈이 경미한 경우의 보조적 치료.
목적: 종양 혈관의 출혈원을 차단하여 재출혈을 예방합니다.
주의: 황반부 병변에서는 광응고 적응증을 신중히 판단합니다.
전신 관리
섹션 제목: “전신 관리”안구 병변이 커지지 않으면 적극적인 치료가 필요하지 않습니다. 결절성 경화증 동반 사례에서는 중추신경계 병변(간질, 뇌실막밑 거대세포 별아교세포종 SEGA), 신장 혈관근지방종 등 전신 병변의 관리를 소아과·신경과 의사와 함께 수행합니다.
**mTOR 억제제(에베로리무스)**는 결절성 경화증에 동반된 전신 종양(SEGA 및 신장 혈관근지방종)에 대해 보험 적용이 있으며, 전신 TSC 치료의 일환으로 종양 축소 효과가 보고되었습니다2)3). 망막 과오종에 대한 직접적인 유효성 증거는 제한적이지만, 전신 TSC 치료 맥락에서 투여된 사례에서 축소 보고가 있습니다.
무증상이고 커지지 않는 경우 치료는 불필요하며 정기적인 안저 검사를 통한 경과 관찰이 기본입니다. 출혈이 반복되는 경우에만 유리체 절제술 또는 망막 광응고를 시행합니다. 결절성 경화증 동반 사례에서는 안과적 관리와 병행하여 전신 질환의 관리가 중요합니다.
6. 병태생리학·상세한 발병 기전
섹션 제목: “6. 병태생리학·상세한 발병 기전”TSC1/TSC2-mTOR 경로의 장애
섹션 제목: “TSC1/TSC2-mTOR 경로의 장애”망막 별아교세포 과오종의 병태는 TSC1(하마르틴) 및 TSC2(투베린) 유전자 산물의 기능 상실에 기인합니다.
하마르틴과 투베린은 복합체를 형성하여 mTOR(rapamycin의 기계적 표적) 복합체 1(mTORC1)의 활성을 억제하는 종양 억제 인자로 기능합니다. TSC1 또는 TSC2의 돌연변이로 인해 이 mTOR 조절 기능이 상실되면 mTORC1이 과활성화됩니다.
mTORC1의 과활성화는 S6 키나아제(S6K) 및 4E-BP1의 인산화를 통해 세포 증식, 단백질 합성, 혈관 신생을 촉진합니다. 그 결과, 별아교세포가 비정상적으로 증식하여 과오종(양성 종괴)이 형성됩니다.
2-hit 가설
섹션 제목: “2-hit 가설”종양 발생에는 ‘2-히트 가설’이 관여하는 것으로 생각됩니다. 생식세포 계열에 TSC1 또는 TSC2의 한쪽 대립유전자 돌연변이를 가진 개체에서 망막 세포의 체세포 돌연변이(2nd hit)가 발생하면 남아 있는 정상 대립유전자의 기능이 상실되고(LOH: loss of heterozygosity), mTOR 경로 조절이 완전히 붕괴되어 종양이 형성됩니다.
과오종의 조직학적 특징
섹션 제목: “과오종의 조직학적 특징”망막 성상세포 과오종은 성상세포 유래 증식으로 구성된 양성 종괴이며, 악성 전환은 일어나지 않습니다. 조직학적으로는 비정상적으로 증식한 성상세포가 밀집되어 배열되고, 일부에 칼슘 침착(석회화)이 동반됩니다. 세포 분열 속도가 느린 것이 종양이 서서히만 커지는 임상적 특징과 일치합니다.
7. 최신 연구와 향후 전망
섹션 제목: “7. 최신 연구와 향후 전망”mTOR 억제제의 결절성 경화증 관련 종양에의 응용
섹션 제목: “mTOR 억제제의 결절성 경화증 관련 종양에의 응용”에베롤리무스(everolimus)는 mTORC1 억제제로서 결절성 경화증 관련 종양 치료에 사용됩니다. EXIST-1 시험(SEGA 대상) 2)에서는 에베롤리무스 투여군에서 SEGA 부피가 50% 이상 감소한 비율이 위약군에 비해 유의하게 높았습니다. EXIST-2 시험(신혈관근지방종 대상) 3)에서도 유사한 종양 축소 효과가 보고되었습니다.
TSC 관련 망막 과오종에 대한 mTOR 억제제의 안과적 유효성에 대해서는 현재 시점에서 제한된 증례 보고만 존재합니다. 전신 TSC 치료의 일환으로 에베롤리무스를 투여받은 환자에서 망막 과오종의 축소가 관찰되었다는 보고가 있지만, 대규모 전향적 시험의 근거는 확립되지 않았습니다.
예후와 장기 추적 관찰의 과제
섹션 제목: “예후와 장기 추적 관찰의 과제”안저 과오종은 일반적으로 커지지 않지만, 드물게 커져서 출혈이나 삼출을 일으키는 증례가 있습니다. 성장 위험 인자의 동정, 장기 경과에서 시력 변화의 예측, 적절한 개입 시기의 판단에 대해서는 추가적인 증례 축적과 전향적 연구가 필요합니다.
고립성 망막 성상세포 과오종의 병태
섹션 제목: “고립성 망막 성상세포 과오종의 병태”TSC를 동반하지 않는 고립성 증례의 유전적 배경이나 분자 기전은 충분히 밝혀지지 않았습니다. 체세포 돌연변이에 의한 국소적 mTOR 경로 이상이 관여할 가능성이 시사되고 있지만, 상세한 기전의 해명은 향후 연구 과제입니다.
8. 참고문헌
섹션 제목: “8. 참고문헌”-
Northrup H, Krueger DA; International Tuberous Sclerosis Complex Consensus Group. Tuberous sclerosis complex diagnostic criteria update: recommendations of the 2012 International Tuberous Sclerosis Complex Consensus Conference. Pediatr Neurol. 2013;49(4):243-254.
-
Franz DN, Belousova E, Sparagana S, et al. Efficacy and safety of everolimus for subependymal giant cell astrocytomas associated with tuberous sclerosis complex (EXIST-1): a multicentre, randomised, placebo-controlled phase 3 trial. Lancet. 2013;381(9861):125-132.
-
Bissler JJ, Kingswood JC, Radzikowska E, et al. Everolimus for angiomyolipoma associated with tuberous sclerosis complex or sporadic lymphangioleiomyomatosis (EXIST-2): a multicentre, randomised, double-blind, placebo-controlled trial. Lancet. 2013;381(9869):817-824.
-
Shields CL, Shields JA, Kiratli H, et al. Familial retinal astrocytoma. Retina. 2002;22(1):95-97.
-
Rowley SA, O’Callaghan FJ, Osborne JP. Ophthalmic manifestations of tuberous sclerosis: a population based study. Br J Ophthalmol. 2001;85(4):420-423.
-
Zimmer-Galler I, Robertson DM. Long-term observation of retinal lesions in tuberous sclerosis. Am J Ophthalmol. 1995;119(3):318-324.
-
Lucchese NJ, Goldberg MF. Iris and fundus pigmentary changes in tuberous sclerosis. J Pediatr Ophthalmol Strabismus. 1981;18(4):45-48.
