桑の実様(mulberry型)
外観:表面に凹凸を伴うドーム状の隆起。「桑の実」に例えられる特徴的な形態。
石灰化:石灰化を伴うことが多い。網膜芽細胞腫との石灰化の差異として、黄色調が強い点が特徴的である。
辺縁:細胞分裂が遅いことを反映し、隆起は軽度で辺縁の立ち上がりがなだらかである。

網膜星細胞過誤腫(retinal astrocytic hamartoma)は、網膜の星状膠細胞(アストロサイト)が過剰増殖した良性腫瘤である。過誤腫(hamartoma)とは、本来その部位に存在する成熟組織の構成成分が、異常な比率で混在した腫瘤状病変を指す。悪性化することはない。
本疾患は、結節性硬化症(tuberous sclerosis complex; TSC)に随伴する場合と、TSCを伴わない孤発例の両方が存在する。結節性硬化症は、種々の臓器に過誤腫を生じる常染色体優性の多系統疾患であり、頭蓋内病変によるてんかん、皮膚の皮脂腺腫、腎血管筋脂肪腫、網膜過誤腫などの多彩な症状を呈する。
原因遺伝子はTSC1(9番染色体)とTSC2(16番染色体)の2つが知られている。TSC1はハマルチン(hamartin)、TSC2はチュベリン(tuberin)をそれぞれコードし、両者の機能異常がmTOR(mechanistic target of rapamycin)経路の制御障害を引き起こす。
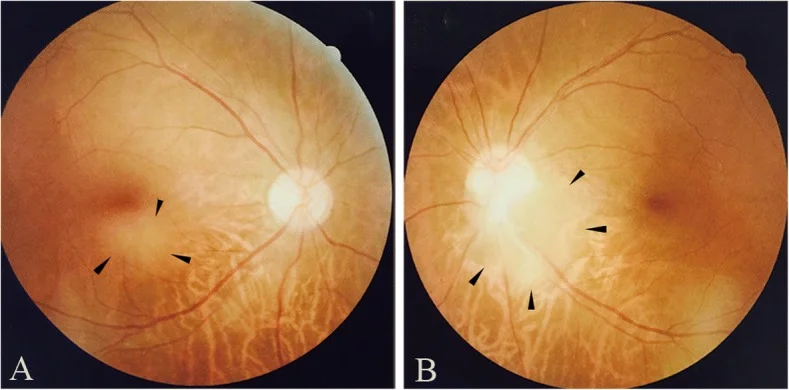
網膜星細胞過誤腫はしばしば無症状で、結節性硬化症のスクリーニング眼底検査で偶然発見される。まれに視力低下や飛蚊症が生じることがある。腫瘍が黄斑部に存在する場合は視力への影響が大きい。
眼底に特徴的な白色隆起病変を生じる。外観の違いから以下の2型に分類される。
桑の実様(mulberry型)
外観:表面に凹凸を伴うドーム状の隆起。「桑の実」に例えられる特徴的な形態。
石灰化:石灰化を伴うことが多い。網膜芽細胞腫との石灰化の差異として、黄色調が強い点が特徴的である。
辺縁:細胞分裂が遅いことを反映し、隆起は軽度で辺縁の立ち上がりがなだらかである。
平坦型
蛍光眼底造影(FAG)では、早期に腫瘍内の微細血管が描出される。後期においても蛍光漏出を認めないことが本疾患の特徴的所見であり、後期に蛍光漏出を示す網膜芽細胞腫との重要な鑑別点となる。
光干渉断層計(OCT)では、腫瘤が網膜内層から隆起する高反射腫瘤として描出される。腫瘤内部の層構造の乱れと、周囲正常網膜との境界が比較的明瞭な点が特徴的である。
結節性硬化症(TSC)は常染色体優性遺伝形式をとる。有病率は約6,000〜10,000人に1人とされる。TSC患者における網膜過誤腫の合併率は約50%と報告されており、両眼性・多発性にみられることもある。
TSC1遺伝子(9番染色体q34)変異では軽症傾向、TSC2遺伝子(16番染色体p13.3)変異ではより重症の全身病変をきたしやすいとされる。新生変異(de novo mutation)も多く、家族歴がない例でもTSCを否定できない。
孤発例(非TSC)では、遺伝子的背景は異なり、限局した体細胞変異が関与している可能性がある。孤発例は通常片眼性・単発性で、全身合併症を伴わない。
明確な性差は報告されていない。TSC随伴例では出生後早期から眼底病変が確認されることがあり、小児科的スクリーニングの一環として眼底検査が推奨される。孤発例は成人でも発見されうるが、いずれも良性経過をたどる。
網膜星細胞過誤腫の診断は、特徴的な眼底所見と結節性硬化症の全身所見を組み合わせて行う。
眼底検査での鑑別ポイント:
最も重要な鑑別疾患は網膜芽細胞腫である。小児に白色隆起網膜病変を認めた場合、まず網膜芽細胞腫を除外する必要がある。
| 疾患名 | 鑑別ポイント |
|---|---|
| 網膜芽細胞腫 | 急速増大、後期蛍光漏出あり、カルシウム沈着(白色調) |
| 網膜細胞腫 | 非活動性・石灰化退縮像、増大なし |
| 孤立性脈絡膜血管腫 | 橙赤色、蛍光眼底造影で造影増強 |
網膜過誤腫が発見された場合、TSCの診断基準(Northrup改訂版 2012年1))に基づき全身評価を行う。主要基準として皮脂腺腫(顔面血管線維腫)、てんかん、脳内結節(Shagreen patch)などが含まれる。TSCの確定診断のためには、小児科・神経科との連携が不可欠である。
網膜星細胞過誤腫は通常増大せず、無症状・増大なしの場合は治療不要で経過観察が基本となる。定期的な眼底検査を行い、増大や出血の有無を確認する。
出血を繰り返す場合には、以下の治療を検討する。
硝子体手術
網膜光凝固
適応:腫瘍辺縁からの滲出や出血が軽度の場合の補助的治療。
目的:腫瘍の血管からの出血源を封鎖し、再出血を予防する。
注意:黄斑部病変では光凝固適応を慎重に判断する。
眼病変が増大しなければ、積極的な治療を行う必要はない。結節性硬化症随伴例では、中枢神経病変(てんかん・上衣下巨細胞性星細胞腫 SEGA)、腎血管筋脂肪腫など全身病変の管理を小児科・神経科医師とともに行う。
**mTOR阻害薬(エベロリムス)**は結節性硬化症に伴う全身腫瘍(SEGAや腎血管筋脂肪腫)に対して保険適用があり、全身TSC治療の一環として腫瘍縮小効果が報告されている2)3)。網膜過誤腫への直接的な有効性エビデンスは限定的であるが、TSCの全身治療の文脈で投与された症例での縮小報告がある。
無症状で増大していない場合、治療は不要で定期的な眼底検査による経過観察が基本である。出血を繰り返す場合にのみ硝子体手術または網膜光凝固を行う。結節性硬化症随伴例では眼科的管理と並行して全身疾患の管理が重要となる。
網膜星細胞過誤腫の病態は、TSC1(ハマルチン)およびTSC2(チュベリン)遺伝子産物の機能喪失に起因する。
ハマルチンとチュベリンは複合体を形成し、mTOR(mechanistic target of rapamycin)複合体1(mTORC1)の活性を抑制する腫瘍抑制因子として機能する。TSC1またはTSC2の変異により、このmTOR制御機能が失われると、mTORC1が過活性化する。
mTORC1の過活性化は、S6キナーゼ(S6K)および4E-BP1のリン酸化を通じて、細胞増殖・タンパク質合成・血管新生を促進する。その結果、アストロサイトが異常増殖し、過誤腫(良性腫瘤)が形成される。
腫瘍発生には「2-hit仮説」が関与すると考えられている。生殖細胞系列にTSC1またはTSC2の片方のアレル変異を持つ個体で、網膜細胞における体細胞変異(2nd hit)が生じることで、残存する正常アレルの機能が失われ(LOH: loss of heterozygosity)、mTOR経路の制御が完全に破綻して腫瘍が形成される。
網膜星細胞過誤腫は、アストロサイト由来の増殖から構成される良性腫瘤であり、悪性転化することはない。組織学的には、異常増殖したアストロサイトが密に配列し、一部にカルシウム沈着(石灰化)を伴う。細胞分裂速度が遅いことが、腫瘍が緩徐にしか増大しない臨床的特徴と対応する。
エベロリムス(everolimus)は、mTORC1阻害薬として結節性硬化症関連腫瘍の治療に用いられる。EXIST-1試験(SEGAを対象)2)では、エベロリムス投与群においてSEGA体積が50%以上減少した割合がプラセボ群と比較して有意に高かった。EXIST-2試験(腎血管筋脂肪腫を対象)3)でも同様の腫瘍縮小効果が報告されている。
TSC関連網膜過誤腫に対するmTOR阻害薬の眼科的有効性については、現時点では限られた症例報告が存在するのみである。全身TSC治療の一環としてエベロリムスを投与された患者で、網膜過誤腫の縮小が観察されたという報告があるが、大規模な前向き試験のエビデンスは確立されていない。
眼底過誤腫は通常増大しないが、まれに増大して出血や滲出を引き起こす症例がある。増大リスク因子の同定、長期経過における視力変化の予測、および適切な介入時機の判断については、さらなる症例集積と前向き研究が必要である。
TSCを伴わない孤発性症例の遺伝的背景や分子機序は十分に解明されていない。体細胞変異による局所的mTOR経路の異常が関与している可能性が示唆されているが、詳細な機序の解明は今後の研究課題である。
Northrup H, Krueger DA; International Tuberous Sclerosis Complex Consensus Group. Tuberous sclerosis complex diagnostic criteria update: recommendations of the 2012 International Tuberous Sclerosis Complex Consensus Conference. Pediatr Neurol. 2013;49(4):243-254.
Franz DN, Belousova E, Sparagana S, et al. Efficacy and safety of everolimus for subependymal giant cell astrocytomas associated with tuberous sclerosis complex (EXIST-1): a multicentre, randomised, placebo-controlled phase 3 trial. Lancet. 2013;381(9861):125-132.
Bissler JJ, Kingswood JC, Radzikowska E, et al. Everolimus for angiomyolipoma associated with tuberous sclerosis complex or sporadic lymphangioleiomyomatosis (EXIST-2): a multicentre, randomised, double-blind, placebo-controlled trial. Lancet. 2013;381(9869):817-824.
Shields CL, Shields JA, Kiratli H, et al. Familial retinal astrocytoma. Retina. 2002;22(1):95-97.
Rowley SA, O’Callaghan FJ, Osborne JP. Ophthalmic manifestations of tuberous sclerosis: a population based study. Br J Ophthalmol. 2001;85(4):420-423.
Zimmer-Galler I, Robertson DM. Long-term observation of retinal lesions in tuberous sclerosis. Am J Ophthalmol. 1995;119(3):318-324.
Lucchese NJ, Goldberg MF. Iris and fundus pigmentary changes in tuberous sclerosis. J Pediatr Ophthalmol Strabismus. 1981;18(4):45-48.