生理性飞蚊症

发现飞蚊症时的就诊指南
一目了然的要点
Section titled “一目了然的要点”1. 什么是飞蚊症
Section titled “1. 什么是飞蚊症”飞蚊症是玻璃体(填充眼球内部的透明凝胶状组织)的混浊投影到视网膜上引起的症状。在白墙、明亮的天空、窗户等明亮背景下,看到蚊子、烟尘、环状物等随眼球运动而飘动。
飞蚊症是眼科门诊日常主诉之一 3)。其背景包括从年龄相关的生理性变化到视网膜裂孔、视网膜脱离等紧急疾病。因此,需要仔细确认症状的性质、发病经过和伴随症状,以免漏诊病理性飞蚊症。
与飞蚊症混淆的症状
Section titled “与飞蚊症混淆的症状”蓝视野内视现象是在看蓝天等明亮蓝光时,视野内出现小白点随机移动的现象,与飞蚊症不同。这是感知到视网膜内白细胞运动的结果,并非病态。
玻璃体后脱离(PVD)是50岁以上人群常见的年龄相关变化,是飞蚊症最常见的原因。报告显示,出现急性症状的PVD患者中约14%发现视网膜裂孔 1),无症状经过的情况并不少见。单眼急性飞蚊症伴闪光感时,必须进行眼底检查 3)。
2. 飞蚊症的类型(生理性 vs 病理性)
Section titled “2. 飞蚊症的类型(生理性 vs 病理性)”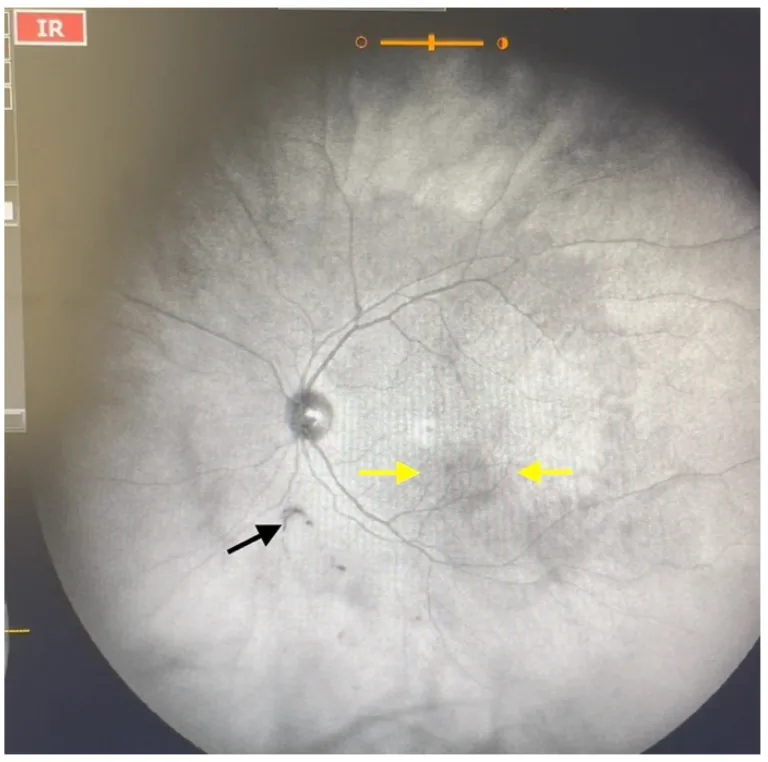
生理性飞蚊症与病理性飞蚊症的鉴别
Section titled “生理性飞蚊症与病理性飞蚊症的鉴别”| 特征 | 生理性飞蚊症 | 病理性飞蚊症 |
|---|---|---|
| 发病方式 | 缓慢(数周至数月) | 急剧(数天至数小时) |
| 飞蚊的数量和性状 | 少量、环形、线状 | 大量、烟雾状(烟草尘) |
| 合并闪光感 | 通常无 | 有(牵拉性) |
| 视野缺损 | 无 | 可能有(视网膜脱离) |
| 视力下降 | 通常无 | 可能有(玻璃体出血等) |
| 是否需要治疗 | 不需要(观察) | 需要(根据病因治疗) |
需要注意的是,星状玻璃体病变(玻璃体内钙结晶沉积)中的玻璃体混浊是一种例外情况,通常不被患者感知为飞蚊症。
生理性飞蚊症无需治疗,随着玻璃体液化进展,通常会逐渐变得不那么明显。病理性飞蚊症可能通过治疗原发病而改善。典型治疗包括视网膜裂孔的激光光凝、视网膜脱离的手术、玻璃体积血的病因治疗等。对于生理性飞蚊症的积极治疗(YAG激光玻璃体消融术、玻璃体切除术)仅在生活质量显著下降时有限考虑。
3. 飞蚊症的病因(鉴别诊断)
Section titled “3. 飞蚊症的病因(鉴别诊断)”
| 病因 | 主要特征 | 紧急程度 |
|---|---|---|
| 后玻璃体脱离(PVD) | 最常见。随年龄增长玻璃体与视网膜分离。典型表现为Weiss环。50岁以上高发 | 低(但需确认是否合并裂孔) |
| 视网膜裂孔 | PVD时玻璃体牵拉导致视网膜撕裂。常伴有烟尘状混浊和闪光感2) | 高(紧急眼底检查、激光光凝) |
| 视网膜脱离(孔源性) | 液体通过视网膜裂孔进入视网膜下。视野缺损、幕状视野障碍4) | 紧急(手术) |
| 玻璃体积血 | 主要由糖尿病视网膜病变和视网膜静脉阻塞引起5)。飞蚊突然增多、视力下降 | 高(查明原因、治疗) |
| 葡萄膜炎 | 玻璃体内的炎症细胞被感知为飞蚊症。可能伴有充血和眼痛 | 中至高(控制炎症) |
| 高度近视(病理性近视) | 玻璃体液化从年轻时就开始进展,容易产生飞蚊症6)。周边视网膜变性的风险也高 | 低至中(定期随访) |
4. 需要就诊的危险信号
Section titled “4. 需要就诊的危险信号”按紧急程度就诊指南
Section titled “按紧急程度就诊指南”| 紧急程度 | 症状组合 | 建议行动 |
|---|---|---|
| 当日就诊 | 视野缺损、烟尘样、闪光感合并、飞蚊急剧增多伴视力下降 | 当天到眼科就诊。最好选择能处理急诊的医疗机构。 |
| 早期就诊(数日内) | 突然出现飞蚊症、飞蚊数量明显增多、形状改变 | 1至3天内到眼科就诊。 |
| 定期随访观察 | 原有飞蚊症无变化,仅在明亮背景下晃动 | 继续定期眼科检查 |
PVD发生后6周内是视网膜裂孔最容易发生的高风险期2),在此期间如果症状发生变化,需要及时就医。
飞蚊症突然增多或性状改变(数量增加、形状改变、出现像烟草灰一样的新黑点)可能提示病理性飞蚊症。特别是同时出现闪光感时,是视网膜裂孔的危险信号,需要尽早眼科就诊。如果原有的飞蚊症持续无变化,很可能是生理性飞蚊症,但仍建议定期进行眼底检查。
5. 眼科检查与治疗
Section titled “5. 眼科检查与治疗”眼科就诊后,首先判断飞蚊症是生理性还是病理性。使用裂隙灯显微镜和非接触式双凸透镜进行玻璃体检查,以视乳头前胶质环(Weiss环)的存在作为PVD的指标,并确认玻璃体混浊情况。
在玻璃体检查中,重要的是将裂隙光宽度调窄、照明强度调至最大,动态观察玻璃体的运动。如果仅有PVD而无明显的玻璃体混浊(除视乳头前胶质环外),可诊断为生理性飞蚊症。但如果观察到烟草灰样混浊、出血或闪辉,则需要详细检查眼底。
滴用散瞳药后,广泛检查眼底周边部,确认有无视网膜裂孔、视网膜脱离和玻璃体出血。
治疗方法一览
Section titled “治疗方法一览”| 病态 | 治疗方法 | 详细说明 |
|---|---|---|
| 生理性飞蚊症 | 观察 | 无需治疗。随着玻璃体液化进展,自觉症状可能减轻。 |
| 生理性飞蚊症(生活质量显著下降) | YAG激光玻璃体消融术 | RCT报告显示与假手术对照相比症状显著改善(p=0.02)7)。适应症有限。 |
| 生理性飞蚊症(严重生活质量障碍) | 玻璃体手术(玻璃体切除术) | 症状改善率高,但需充分考虑手术风险(白内障、视网膜脱离等)8)。 |
| 视网膜裂孔(仅裂孔) | 激光光凝术 | 凝固裂孔周围,预防进展为视网膜脱离。 |
| 视网膜脱离(孔源性) | 玻璃体手术/巩膜扣带术4) | 早期手术可改善视力预后。需要紧急处理。 |
| 玻璃体出血 | 治疗原发疾病(DR、RVO等)5) | 若出血不吸收,考虑玻璃体手术 |
| 葡萄膜炎 | 控制炎症(类固醇等) | 需要检查和治疗基础疾病 |
使用散瞳药(如托吡卡胺)滴眼后,瞳孔通常在4~6小时内恢复。在此期间,光线刺眼且近视力模糊,因此应避免驾驶汽车或自行车。建议携带太阳镜。散瞳药的效果因人而异,恢复时间可能长达6~8小时。
6. 飞蚊症的病理生理
Section titled “6. 飞蚊症的病理生理”玻璃体的年龄相关变化
Section titled “玻璃体的年龄相关变化”玻璃体是填充眼球的透明凝胶状组织,主要由胶原纤维和透明质酸构成。随着年龄增长,胶原纤维聚集变性,导致玻璃体液化(玻璃体浓缩)。液化区域形成液腔,周围残留的凝胶变得混浊,散射光线。这种混浊投影到视网膜上,被感知为飞蚊症。
后玻璃体脱离(PVD)的机制
Section titled “后玻璃体脱离(PVD)的机制”随着玻璃体液化进展,玻璃体与视网膜的粘附减弱,最终后玻璃体膜从视网膜分离(后玻璃体脱离:PVD)。PVD发生后立即,视乳头前胶质环(Weiss环)位于视网膜正上方,因此飞蚊症感觉强烈。随着玻璃体液化进一步进展为完全性PVD,Weiss环远离视网膜,自觉症状趋于减轻。
视网膜裂孔的形成机制
Section titled “视网膜裂孔的形成机制”在PVD发生时,玻璃体与视网膜局部粘附较强的部位(如格子状变性区),玻璃体分离时牵引力集中,可能导致视网膜撕裂(视网膜裂孔)2)。这种牵引刺激视网膜,被感知为闪光感。如果液体通过裂孔进入视网膜下腔,可进展为孔源性视网膜脱离4)。
高度近视与飞蚊症
Section titled “高度近视与飞蚊症”在高度近视中,由于眼轴延长导致眼球容积增大,玻璃体液化从年轻时就开始进展6)。此外,视网膜周边部的格子样变性和视网膜裂孔的发生频率较高,飞蚊症也相对容易在较年轻时出现。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”飞蚊症与生活质量
Section titled “飞蚊症与生活质量”即使飞蚊症不伴有视力下降,也会给患者带来较大的精神负担,并对生活质量产生显著影响。Wagle等人(2011年)的研究显示,与飞蚊症相关的效用值平均为0.98,但症状较重的患者生活质量评分显著降低9)。不应将飞蚊症视为轻微症状,而应充分倾听患者的诉求。
YAG激光玻璃体消融术的疗效
Section titled “YAG激光玻璃体消融术的疗效”Shah等人(2017年)的随机对照试验显示,对于有症状的玻璃体混浊,YAG激光玻璃体消融术与假手术对照相比,能显著改善症状(53.3% vs 8.7%,p=0.02)7)。但该手术对操作者技术依赖性高,且存在并发症风险(眼压升高、晶状体损伤、视网膜损伤),因此设施和适应症的选择至关重要。
药物性玻璃体消融
Section titled “药物性玻璃体消融”一种通过向玻璃体内注射酶(ocriplasmin)来化学解除玻璃体牵拉的治疗方法正在研究中。Stalmans等人(2012年)的随机对照试验证明了ocriplasmin对玻璃体黄斑牵拉和黄斑裂孔的有效性10)。将其应用于飞蚊症本身仍处于研究阶段。
PVD后随访时机的优化
Section titled “PVD后随访时机的优化”Byer等人(1994年)在PVD发生后的自然病程研究中指出,后玻璃体脱离发生后的初期是视网膜裂孔风险最高的时期2)。后续研究也表明,急性症状性PVD发生后6周内的随访观察是预防裂孔和脱离的主要策略,随访时机的标准化正在推进中3)。
8. 参考文献
Section titled “8. 参考文献”- Hollands H, Johnson D, Brox AC, et al. Acute-onset floaters and flashes: is this patient at risk for retinal detachment? JAMA. 2009;302(20):2243-2249.
- Byer NE. Natural history of posterior vitreous detachment with early management as the premier line of defense against retinal detachment. Ophthalmology. 1994;101(9):1503-1514.
- Kahawita S, Simon S, Engelbrecht T. Acute symptomatic posterior vitreous detachment and the prevalence of associated retinal tears: a systematic review. Eye (Lond). 2024;38(5):825-833.
- Feltgen N, Walter P. Rhegmatogenous retinal detachment—an ophthalmologic emergency. Dtsch Arztebl Int. 2014;111(1-2):12-22.
- 日本糖尿病眼学会. 糖尿病網膜症診療ガイドライン(第1版). 日眼会誌. 2020;124(12):955-981.
- Ohno-Matsui K, Lai TY, Lai CC, Cheung CMG. Updates of pathologic myopia. Prog Retin Eye Res. 2016;52:156-187. PMID:26769165. doi:10.1016/j.preteyeres.2015.12.001.
- Shah CP, Heier JS. YAG laser vitreolysis vs sham YAG vitreolysis for symptomatic vitreous floaters: a randomized clinical trial. JAMA Ophthalmol. 2017;135(9):918-923.
- de Nie S, Crama N, Coppens JE, et al. Pars plana vitrectomy for disturbing primary vitreous floaters: clinical outcome and patient satisfaction. Graefes Arch Clin Exp Ophthalmol. 2013;251(5):1373-1382.
- Wagle AM, Lim WY, Yap TP, et al. Utility values associated with vitreous floaters. Am J Ophthalmol. 2011;152(1):60-65.e1.
- Stalmans P, Benz MS, Gandorfer A, et al. Enzymatic vitreolysis with ocriplasmin for vitreomacular traction and macular holes. N Engl J Med. 2012;367(7):606-615. PMID:22894573. doi:10.1056/NEJMoa1110823.
