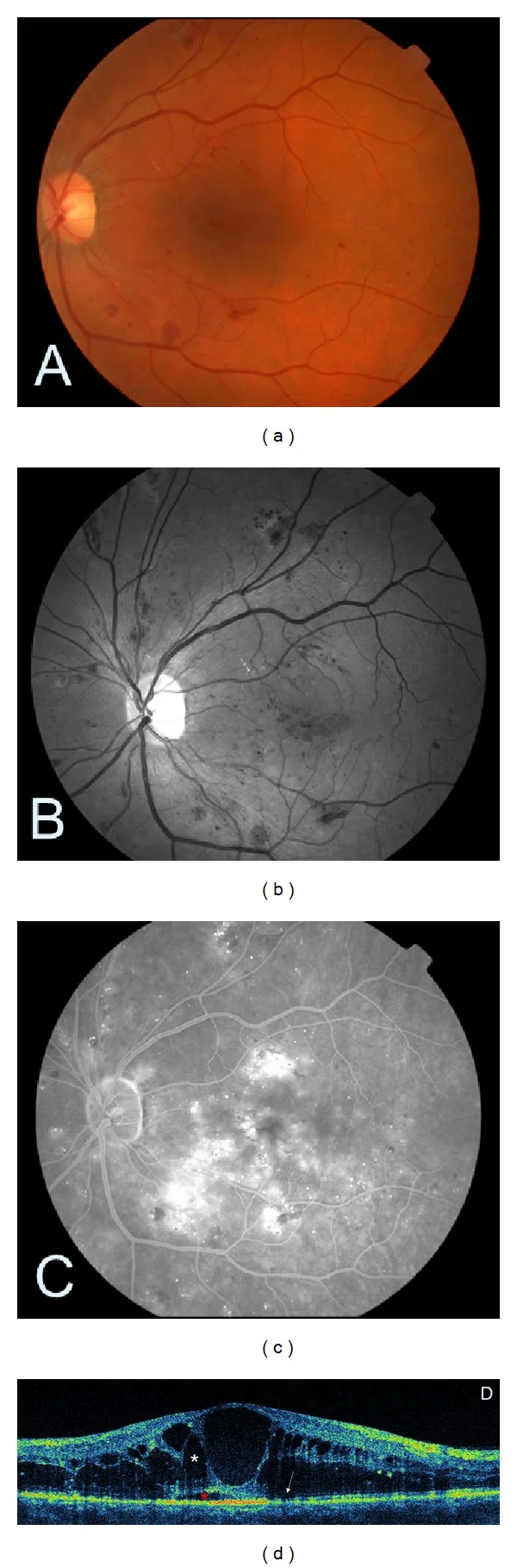
单纯性视网膜病变
微血管瘤:DR的最早期所见。荧光眼底造影显示为点状强荧光。
视网膜出血:点状或斑片状出血。红细胞从毛细血管漏出所致。
硬性渗出:血管通透性增高导致血浆成分漏出,脂质沉积形成。

糖尿病视网膜病变(DR)是由高血糖引起的代谢异常导致多种细胞因子和趋化因子诱导的视网膜微血管病变。继发性引起多种眼底病变,与糖尿病神经病变和糖尿病肾病并称为三大并发症。近年来,它被重新定义为“神经血管疾病”,而不仅仅是微血管疾病2)。
它是获得性视力障碍的第二大原因,每年约3000人因DR失明。
糖尿病黄斑水肿(DME)是糖尿病黄斑病变中最常见的类型。糖尿病黄斑病变包括黄斑水肿、缺血性黄斑病变和视网膜色素上皮病变三种类型,其中黄斑水肿最常见,是临床上重要的视力下降原因。DME可在DR的任何阶段发生。DME的病理生理复杂,涉及血管通透性增加、血管闭塞引起的血流障碍、胶体渗透压降低和后玻璃体膜牵拉等多因素。
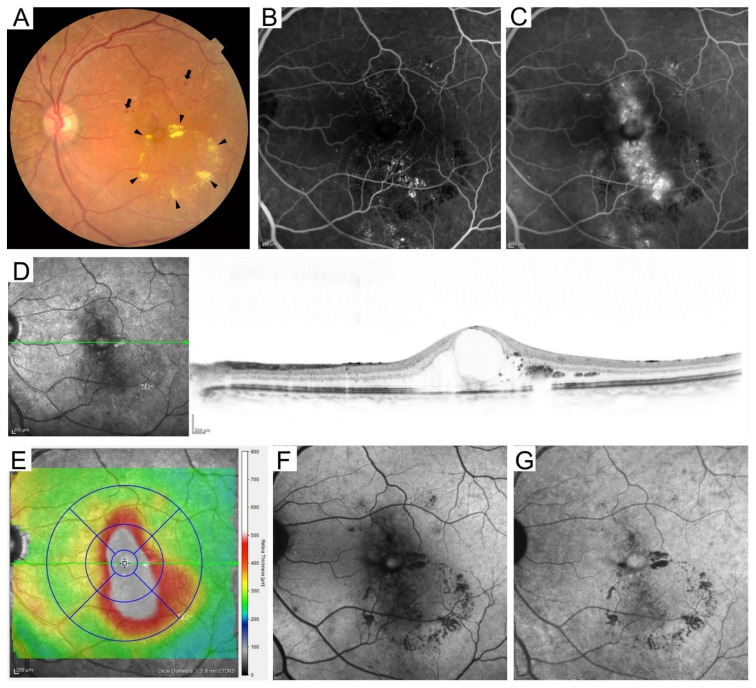
日本的主要流行病学数据如下所示1)。
在全球范围内,34.6%的糖尿病患者(约9300万人)患有DR2)。2020年估计DR患者1.312亿人,威胁视力的DR(VTDR)2854万人,临床有意义的黄斑水肿(CSME)1883万人,预计到2045年将增至1.605亿人2)。1型糖尿病发病20年后约90%出现DR11)。
在日本大型队列中,DR的年发病率为3.8-4.0%,2型糖尿病诊断时已有约30%的患者患有DR1)。全球范围内,34.6%的糖尿病患者(约9300万人)患有DR2),1型糖尿病发病20年后约90%出现DR11)。
早期DR常无症状进展。当出现症状时,通常已存在中度或更严重的病变。
各期的主要眼底所见如下所示。
单纯性视网膜病变
微血管瘤:DR的最早期所见。荧光眼底造影显示为点状强荧光。
视网膜出血:点状或斑片状出血。红细胞从毛细血管漏出所致。
硬性渗出:血管通透性增高导致血浆成分漏出,脂质沉积形成。
增殖前期视网膜病变
软性渗出(棉絮斑):视神经纤维轴浆运输受阻导致的局部梗死灶。反映视网膜缺血。
串珠状静脉扩张和迂曲形成:出现在血管闭塞区域附近。
IRMA(视网膜内微血管异常):无灌注区周围的分流形成。荧光造影中无明显渗漏是与新生血管的鉴别要点。
增殖性视网膜病变
新生血管:由于广泛毛细血管闭塞导致VEGF过度产生,出现在视网膜和视乳头上。荧光造影显示旺盛的荧光渗漏。
纤维血管性增殖膜:新生血管周围成纤维细胞样细胞增殖形成。
牵拉性视网膜脱离:增殖膜与视网膜粘连加上玻璃体牵拉而发生。累及黄斑时视力预后不良。
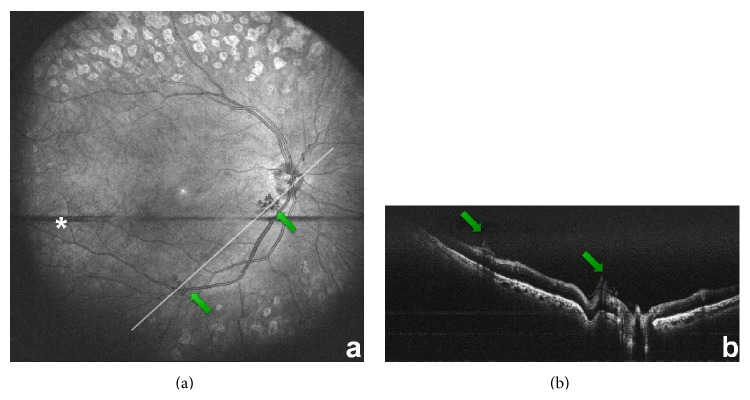
重度NPDR由“4-2-1规则”定义2),即满足以下任一条件:
新福田分类1)大致分为良性(A组)和恶性(B组)。
| 分类 | 分期 | 所见 |
|---|---|---|
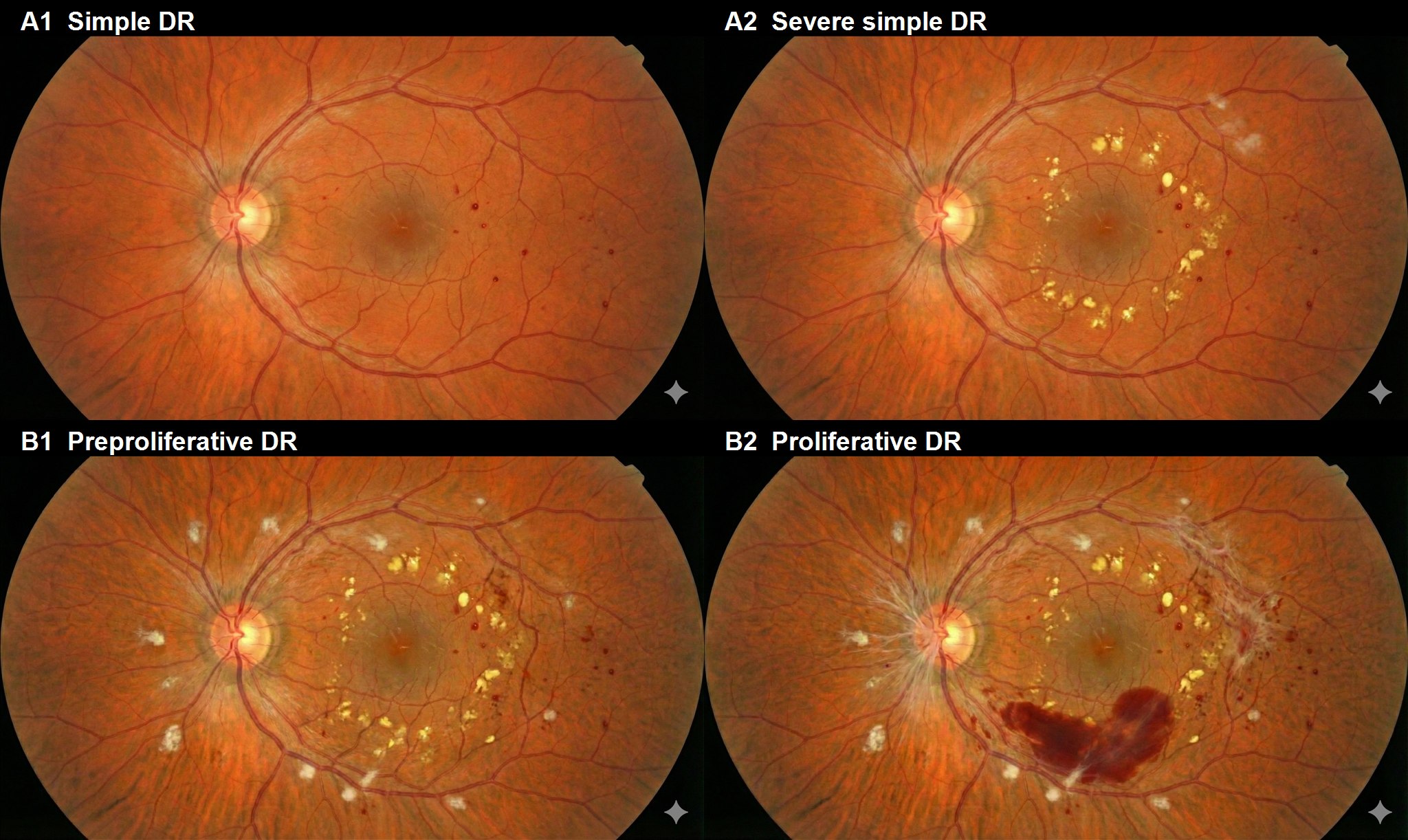
| A1 | 轻度非增殖性 | 微血管瘤、点状出血 |
| A2 | 中度非增殖性 | 片状出血、硬性渗出、少量软性渗出 |
| B1 | 增殖前期 | 软性渗出、静脉串珠、IRMA、荧光血管造影显示无灌注区 |
| B2 | 早期增殖性 | 不与视乳头直接相连的新生血管 |
| B3 | 中度增殖性 | 与视乳头直接相连的新生血管 |
| B4 | 晚期增殖 | 玻璃体出血/视网膜前出血 |
| B5 | 晚期增殖 | 纤维血管增殖组织 |
| A3~A5 | 增殖静止 | 陈旧性新生血管/VH/增殖组织 |
治疗后病情稳定6个月以上称为增殖静止性视网膜病变。并发症标注为M(黄斑病变)、D(牵拉性RD)、G(NVG)、N(缺血性视神经病变)、P(光凝)、V(玻璃体手术)。
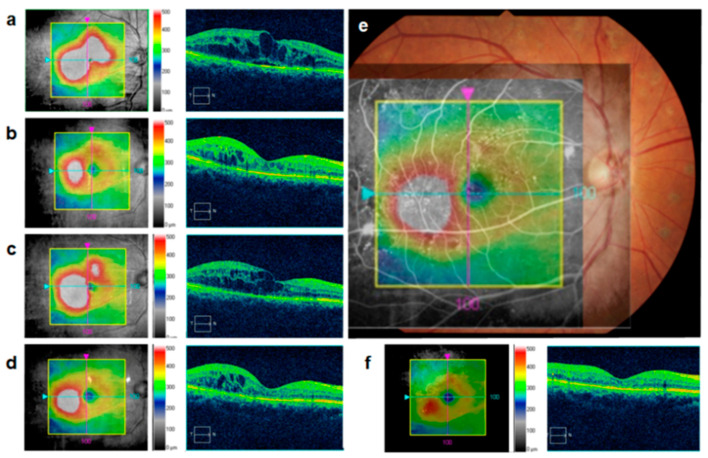
黄斑水肿的OCT断层图像根据视网膜膨化、囊样黄斑水肿和浆液性视网膜脱离三种基本类型的组合进行评估。
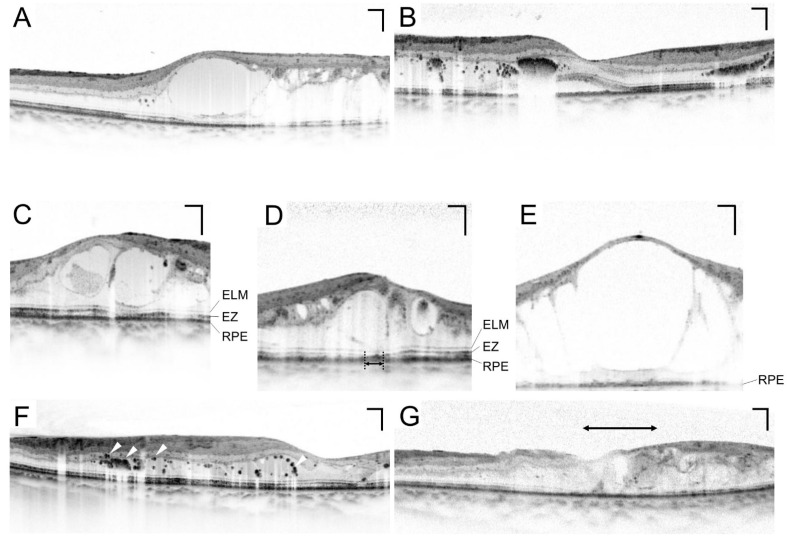
临床上有意义的黄斑水肿(CSME)根据ETDRS定义满足以下任一条件2):
SD-OCT中心视网膜厚度≥300μm作为累及中心凹的DME阈值(按设备:Spectralis 320/305μm,Cirrus 305/290μm,Stratus 250/250μm,男/女)1)。DME的国际严重程度分级分为轻度(远离中心凹的增厚或硬性渗出)、中度(靠近中心凹但未累及)和重度(累及中心凹)三级。DME随NPDR进展而增加,轻度NPDR合并1.7–6.3%,中度NPDR合并20.3–63.2%1)。
与DR进展相关的主要风险因素如下所示。
| 风险因素 | 主要证据 |
|---|---|
| 病程 | 最大的风险因素。2型糖尿病诊断时约30%已存在DR1) |
| 血糖控制 | HbA1c<7.0%可预防微血管并发症(熊本研究)。HbA1c降低1%使微血管并发症风险降低37%(UKPDS)1) |
| 高血压 | WESDR:收缩压升高10mmHg使早期DR风险增加10%,增殖性DR/DME风险增加15%。UKPDS:收缩压降低10mmHg使DR进展减少35%,视力下降减少47%1) |
| 血脂异常 | 非诺贝特(FIELD研究):光凝导入减少31%,增殖性DR减少30%,DME减少31%。ACCORD眼研究:DR进展几率降低40%1) |
| 肾功能障碍 | 蛋白尿和GFR下降与DR患病率相关。肾病→PDR进展风险增加29%1) |
| 妊娠 | 无既往DR→妊娠期间DR发生率为8 |
| 严重低血糖 | DR发生率增加约4倍(JDCS)1) |
多项大规模试验表明,严格的血糖控制可有效预防和延缓DR的进展1)。
另一方面,长期血糖控制不佳的患者如果快速改善血糖,可能会出现一过性DR恶化的“早期恶化”。由于约50%的病例视力下降会持续,因此希望缓慢改善血糖,与内科的协作很重要1)。
此外,曾暴露于高血糖的视网膜细胞会发生表观遗传改变,即使在血糖正常化后病变仍持续或进展,这被称为“代谢记忆”11)。SOD2下调和线粒体DNA过度甲基化被认为是其机制。
以HbA1c低于7.0%为目标可预防微血管并发症(熊本研究)1)。HbA1c降低1%可使微血管并发症风险降低37%(UKPDS)1)。由于曾暴露于高血糖的细胞会残留“代谢记忆”,即使血糖正常化也需要长期随访11)。
| 检查方法 | 主要用途 | 备注 |
|---|---|---|
| 散瞳眼底检查(间接检眼镜/前置镜) | 分期分级的金标准 | 未散瞳时仅约50%能准确分类2) |
| 裂隙灯显微镜检查 | 评估角膜损伤、虹膜红变、白内障及前房炎症 | 通过前置镜详细观察黄斑 |
| 彩色眼底照相 | 客观记录及纵向比较 | ETDRS 7方位照相。超广角SLO可记录周边部3) |
| 荧光素眼底血管造影(FA) | 识别无灌注区、新生血管及渗漏点。鉴别局灶性与弥漫性DME | FA总不良反应率1.1%~11.2%,严重者0.005%~0.48%,死亡0.0005%~0.002%1) |
| 光学相干断层扫描(OCT) | 黄斑水肿的定量评估与随访 | SD-OCT深度分辨率5μm。中心视网膜厚度≥300μm提示中心凹DME1) |
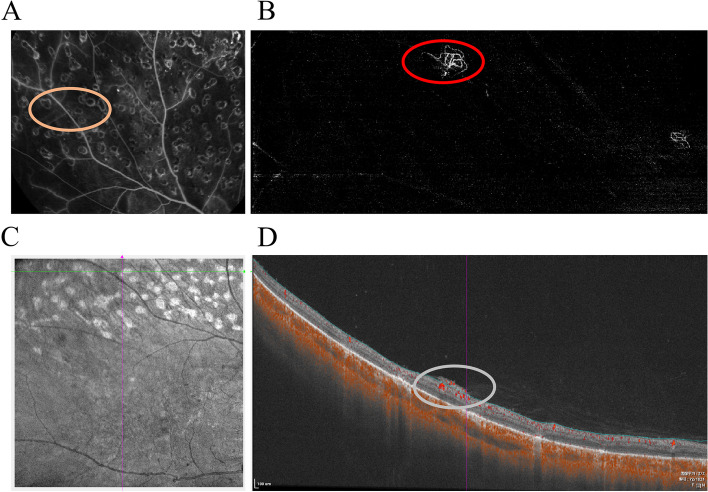
| OCTA | 不使用造影剂评估毛细血管脱落、无灌注区(NPA)和新生血管 | 无创。还可定量FAZ3) |
| 超声检查 | 屈光间质混浊时评估视网膜与玻璃体关系 | 了解牵拉性视网膜脱离范围及增殖膜位置 |
| 视网膜电图(ERG) | 客观评估视网膜功能 | OP潜伏期延长在DR早期出现。负波型ERG提示术后视力不良1) |
| 分期(改良Davis分类) | 推荐间隔 |
|---|---|
| 糖尿病(无视网膜病变) | 每年一次 |
| 单纯性糖尿病视网膜病变(轻至中度NPDR) | 每6个月一次 |
| 增殖前期糖尿病视网膜病变(重度NPDR) | 每2个月一次 |
| 增殖性糖尿病视网膜病变 | 每月一次 |
(AAO PPP建议重度NPDR每3-4个月一次,与GL表3的值略有不同)1)2)
主要的鉴别诊断包括高血压性视网膜病变、视网膜动静脉阻塞、Eales病、Coats病、血液疾病(贫血、白血病、霍奇金病)、干扰素视网膜病变、放射性视网膜病变、Purtscher病、高安病、葡萄膜炎(白塞病、结节病、SLE)。
2型糖尿病在诊断时约30%已存在DR,因此建议在诊断时进行眼底检查1)。1型糖尿病应在诊断后5年内进行1)。若合并妊娠,应在妊娠早期尽早检查,妊娠期间需每3个月随访一次1)。
全身危险因素管理是预防和抑制DR进展的根本,应贯穿所有分期持续进行。
抗VEGF疗法
一线治疗:累及中心凹的DME的标准治疗 1)。
雷珠单抗(Lucentis):0.5 mg/0.05 mL玻璃体内注射。每月一次直至视力稳定。
阿柏西普2 mg(Eylea):2 mg/0.05 mL。每月一次×5次负荷剂量,之后每2个月一次。
法瑞西单抗(Vabysmo):6 mg/0.05 mL。抗VEGF+抗Ang-2双特异性抗体。YOSEMITE/RHINE试验中,50-70%维持12-16周间隔 9)。
布罗鲁珠单抗(Beovu):6 mg/0.05 mL。分子量26 kDa。KESTREL/KITE试验中,>50%维持q12w 5)。
再给药方案:三种方式:PRN(按需给药)、固定给药和TAE(治疗并延长间隔)1)。
类固醇疗法
激光光凝(DME)
适应症:不累及中心凹的DME的选择1)。
直接光凝:直接照射渗漏源的微动脉瘤。
格栅样光凝:照射弥漫性渗漏或无灌注区。
改良ETDRS法:避免照射黄斑中心500μm以内区域,采用低功率、大间距进行1)。
注意:存在萎缩性瘢痕扩展和视网膜下纤维增殖的风险1)。
| 药物名称(商品名) | 剂量 | 特点 |
|---|---|---|
| 雷珠单抗(Lucentis) | 0.5mg/0.05mL | Fab片段。每月一次给药。持续至视力稳定。 |
| 阿柏西普 2mg(Eylea) | 2mg/0.05mL | VEGF-A/B和PlGF结合融合蛋白。5次负荷剂量后每2个月一次。 |
| 阿柏西普 8mg(Eylea 8mg) | 8mg/0.07mL | 高剂量。最长间隔16周 2) |
| 布罗珠单抗(Beovu) | 6mg/0.05mL | 分子量26kDa。超过50%每12周一次。注意眼内炎症风险 5)7) |
| 法瑞西单抗(Vabysmo) | 6mg/0.05mL | 抗VEGF+抗Ang-2。最长每16周一次 9) |
对于累及中心凹且视力良好(20/25或以上)的DME,将治疗推迟至视力降至20/30或以下是一种选择2)。
对于累及中心凹的DME,抗VEGF治疗是一线选择1)。雷珠单抗、阿柏西普、法瑞西单抗和布罗鲁珠单抗均有效,其中法瑞西单抗(最长q16w)和布罗鲁珠单抗(≥50% q12w)因可延长给药间隔而备受关注5)9)。若抗VEGF效果不佳,可考虑使用曲安奈德或地塞米松植入物进行类固醇治疗2)。
DR的基本病理改变大致分为三类:血管通透性增加、血管闭塞和新生血管形成。单纯性视网膜病变、增殖前期视网膜病变和增殖性视网膜病变各期基本对应这些基本病理改变。
在高血糖状态下,四条主要代谢途径被激活,通过氧化应激和炎症导致视网膜损伤11)。
| 途径 | 主要产物/变化 | 主要下游损伤 |
|---|---|---|
| 多元醇途径 | 山梨醇积累 | NADPH耗竭→谷胱甘肽降低→氧化应激放大 |
| AGEs形成 | RAGE激活 | NF-κB↑→VEGF↑,周细胞凋亡 |
| PKC活化 | PKC-β活化 | VEGF/Nox上调 |
| 己糖胺途径 | UDP-GlcNAc过量 | TGF-β/PAI-1增加 |
内侧BRB(视网膜毛细血管内皮细胞的紧密连接)和外侧BRB(RPE细胞间的紧密连接)均受到损害8)。
视网膜存在独立于循环系统的局部RAAS9)。经典途径(ACE/AngII/AT1R轴)促进周细胞凋亡、白细胞停滞和BRB破坏,而保护性途径(ACE2/Ang-(1-7)/Mas轴)则拮抗之。视网膜内AngII浓度高于循环中,DIRECT试验显示坎地沙坦治疗使DR消退34%9)。
曾暴露于高血糖的视网膜细胞即使在血糖正常化后仍会持续存在表观遗传学改变(SOD2抑制、线粒体DNA过度甲基化)11)。其机制包括线粒体电子传递链复合物I/III产生的ROS增加、Drp1/OPA1失衡导致的线粒体过度碎片化,以及通过Nrf2/KEAP1和SIRT1介导的抗氧化反应受损。
DR已被重新定义为“神经血管疾病”2),在血管病变出现之前,OCT即可检测到GCIPL变薄13)。黄斑NFL每年变薄0.25 μm,GCIPL每年变薄0.29 μm。还观察到Müller细胞胶质化(GFAP升高)和小胶质细胞活化。Fractalkine(CX3CL1)由视网膜神经节细胞产生,作用于CX3CR1受体,发挥抗炎和神经保护作用10)。
糖尿病患者玻璃体中葡萄糖浓度升高,胶原纤维的糖化反应进展。糖化程度与DR进展相关,胶原结构变化促进液化、玻璃体皮质收缩和后玻璃体脱离(PVD)。如果发生无牵拉的完全性PVD,则几乎不会进展为增殖性DR。相反,不完全性PVD(玻璃体与增殖组织紧密粘连)会导致持续的玻璃体牵拉,容易发生牵拉性视网膜脱离和玻璃体出血。
血糖控制对于预防和延缓DR进展最为重要,目标HbA1c低于7.0%1)。然而,根据“代谢记忆”的概念,曾暴露于高血糖的细胞会保留表观遗传学改变,即使在血糖正常化后,病变也可能持续或进展11)。DCCT/EDIC随访研究表明,早期强化治疗组在长期内抑制了DR进展。
阿柏西普8mg于2023年获批用于DME适应症,预计可延长至最多16周间隔2)。在DRCR Protocol W中,对重度NPDR进行预防性抗VEGF治疗可预防PDR/DME的发生,但长期视力结果与初始观察组相当2)。
LumineticsCore(原IDx-DR)是2018年FDA批准的首个无需医生解读的自主AI眼底诊断系统3)。深度学习模型报告灵敏度96.8%、特异度87%3),EyeArt、AEYE-DS等新系统也在开发中2)。
给予可溶性分形趋化因子表达AAV载体(rAAV-sFKN)可改善视力、减少纤维蛋白渗漏、使小胶质细胞正常化10)。其具有不同于抗VEGF疗法的神经保护和抗炎机制。
EUROCONDOR II-III期试验(NCT01726075)评估了生长抑素和溴莫尼定滴眼液,但整体分析未显示疗效;然而,在基线mfERG异常的亚组中,神经功能障碍的进展停止13)。一项为期36个月的胞磷胆碱联合维生素B12滴眼液双盲RCT报告,在轻度DR中可抑制功能、结构和血管的进展13)。
miRNA作为整合调节DR病理多轴(氧化应激、炎症、神经变性、血管功能障碍)的“主调控因子”而受到关注14)。已显示通过抑制miR-195稳定SIRT1、通过miR-497a-5p抑制VEGF-A翻译的可能性;视网膜中表达约350种miRNA,其中86种以上在DR模型中异常表达。
二甲双胍通过AMPK激活具有抗氧化、抗炎、抗血管生成和神经保护等多效作用,观察性研究显示使用者发生STDR(威胁视力的DR)的aHR=0.2912)。但目前眼科适应症的RCT数据尚不充分。
非甾体MR拮抗剂非奈利酮在临床前模型中显示可减轻BRB破坏、血管新生和炎症,MR作为DR独立治疗靶点的意义正在研究中9)。