단순 망막병증

당뇨망막병증 및 당뇨황반부종
1. 당뇨망막병증 및 당뇨황반부종이란?
섹션 제목: “1. 당뇨망막병증 및 당뇨황반부종이란?”당뇨망막병증(DR)은 고혈당으로 인한 대사 이상으로 다양한 사이토카인과 케모카인이 유도되어 발생하는 망막의 미세혈관 장애입니다. 이차적으로 다양한 안저 병변이 초래되며, 당뇨신경병증, 당뇨신병증과 함께 3대 합병증으로 불립니다. 최근에는 미세혈관 질환에 그치지 않고 ‘신경혈관 질환’으로 재정의되고 있습니다2).
후천적 시각 장애 원인의 2위이며, 연간 약 3,000명이 DR로 실명합니다.
당뇨황반부종(DME)은 당뇨황반병증 중 가장 빈도가 높은 병형입니다. 당뇨황반병증에는 황반부종, 허혈성 황반병증, 망막색소상피병증의 3형이 포함되지만, 황반부종의 빈도가 가장 높고 임상적으로 중요한 시력 저하 원인입니다. DME는 DR의 모든 단계에서 발생할 수 있습니다. DME의 병태는 혈관 투과성 항진, 혈관 폐쇄로 인한 혈류 장애, 교질 삼투압 저하, 후유리체막의 견인 등 여러 요인이 관여하는 복잡한 것입니다.
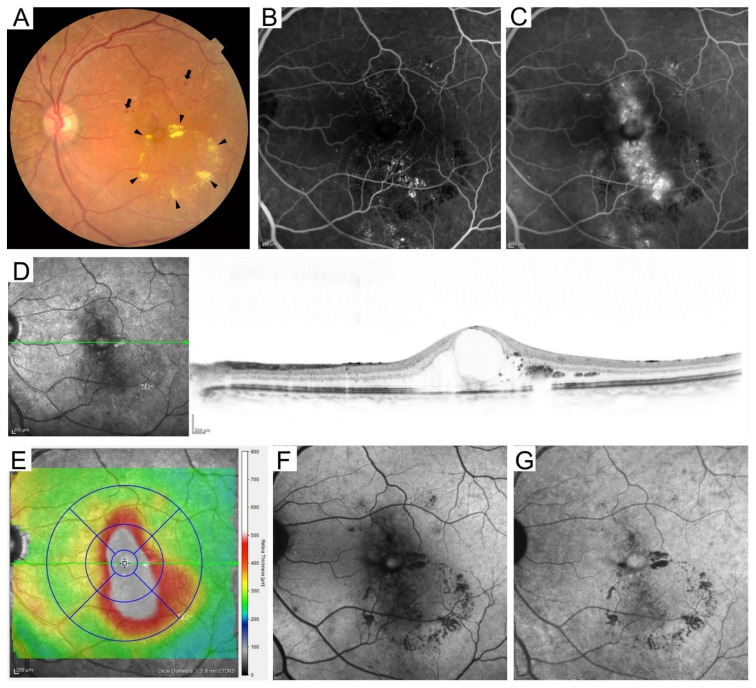
일본의 주요 역학 데이터는 아래와 같습니다1).
- 일본인 2형 당뇨병 환자 976명을 평균 8.3년 추적: DR 발생률 연 3.98%
- JDCS (1,221명, 평균 58.2세, HbA1c 8.2%) 8년 추적: DR 발생률 연 3.83%
- JDCS 410명: 경증 NPDR → 중증 NPDR/PDR 진행률 연 2.11%
- 일본을 포함한 아시아 지역의 DR 유병률 19.9%
- 일본의 DR 유병률 23.5% (경증~중등증 NPDR 18.5%, DME 3.7%)
- 2형 당뇨병 진단 시 이미 약 30%가 DR 발병
세계적으로 당뇨병 환자의 34.6%(약 9,300만 명)가 DR을 가지고 있습니다2). 2020년 추정으로 DR 1억 312만 명, 시력을 위협하는 DR(VTDR) 2,854만 명, 임상적으로 유의한 황반부종(CSME) 1,883만 명으로 보고되었으며, 2045년에는 1억 6,050만 명으로 증가할 것으로 예측됩니다2). 1형 당뇨병에서는 발병 20년 후 약 90%에서 DR이 발생합니다11).
일본의 대규모 코호트에서는 연 3.8~4.0%의 빈도로 DR이 발생하며, 2형 당뇨병 진단 시 이미 약 30%가 DR을 가지고 있습니다1). 세계적으로 당뇨병 환자의 34.6%(약 9,300만 명)가 DR을 가지고 있으며2), 1형 당뇨병 발병 20년 후에는 약 90%에서 나타납니다11).
2. 주요 증상과 임상 소견
섹션 제목: “2. 주요 증상과 임상 소견”자각 증상
섹션 제목: “자각 증상”초기 DR은 무증상으로 진행되는 경우가 많습니다. 증상이 나타난 시점에는 이미 중등도 이상의 병변이 존재하는 경우가 많습니다.
- 시력 저하: DME 동반 시 또는 유리체 출혈 발생 시 나타납니다.
- 변시증(왜곡): 황반 부종이 중심와에 미칠 때.
- 비문증: 유리체 출혈로 인한 갑작스러운 다수의 부유물 출현.
- 시야 결손: 견인성 망막박리, 광범위한 무관류 영역 또는 전망막광응고술 후에 발생할 수 있습니다.
- 급속한 시야 협착 진행: 신생혈관녹내장(NVG)으로 인한 현저한 고안압이 원인이 될 수 있습니다.
임상 소견
섹션 제목: “임상 소견”병기별 주요 안저 소견은 다음과 같습니다.
증식전 망막병증
증식성 망막병증
신생혈관: 광범위한 모세혈관 폐쇄로 인한 VEGF 과잉 생성으로 망막 및 시신경 유두에 나타납니다. 형광 혈관조영술에서 활발한 형광 누출을 보입니다.
섬유혈관 증식막: 신생혈관 주변에 섬유아세포 유사 세포가 증식하여 형성됩니다.
견인성 망막박리: 증식막과 망막의 유착에 유리체 견인이 더해져 발생합니다. 황반을 침범하면 시력 예후가 좋지 않습니다.
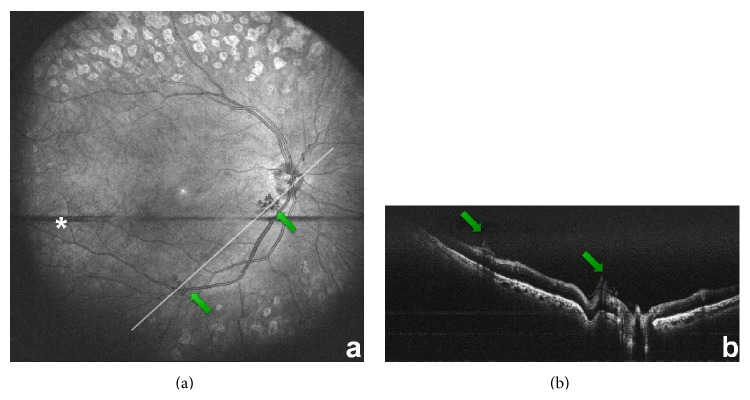
국제 당뇨망막병증 중증도 분류 (ICDR) 및 신후쿠다 분류
섹션 제목: “국제 당뇨망막병증 중증도 분류 (ICDR) 및 신후쿠다 분류”중증 NPDR은 ‘4-2-1 규칙’으로 정의됩니다2). 즉, 다음 중 하나 이상을 충족하는 경우입니다.
- 4사분면 각각 20개 이상의 망막 출혈
- 2사분면 이상의 명확한 구슬모양 정맥 확장
- 1사분면 이상의 명확한 IRMA
신후쿠다 분류1)는 양성(A군)과 악성(B군)으로 크게 나뉩니다.
| 분류 | 병기 | 소견 |
|---|---|---|
| A1 | 경증 비증식성 | 미세동맥류, 점상출혈 |
| A2 | 중등도 비증식성 | 얼룩출혈, 경성백반, 소수의 연성백반 |
| B1 | 증식전 | 연성백반, 정맥비딩, IRMA, 형광안저조영술에서 무관류부위 |
| B2 | 초기 증식성 | 시신경유두에 직접 연결되지 않은 신생혈관 |
| B3 | 중등도 증식성 | 시신경유두에 직접 연결된 신생혈관 |
| B4 | 말기 증식 | 유리체 출혈/망막전 출혈 |
| B5 | 말기 증식 | 섬유혈관 증식 조직 |
| A3~A5 | 증식 정지 | 구신생혈관/VH/증식 조직 |
치료 후 6개월 이상 안정화되면 증식 정지 망막병증이라고 합니다. 합병증 표기로 M(황반 병변), D(견인성 RD), G(NVG), N(허혈성 시신경병증), P(광응고), V(유리체 절제술)를 추가합니다.
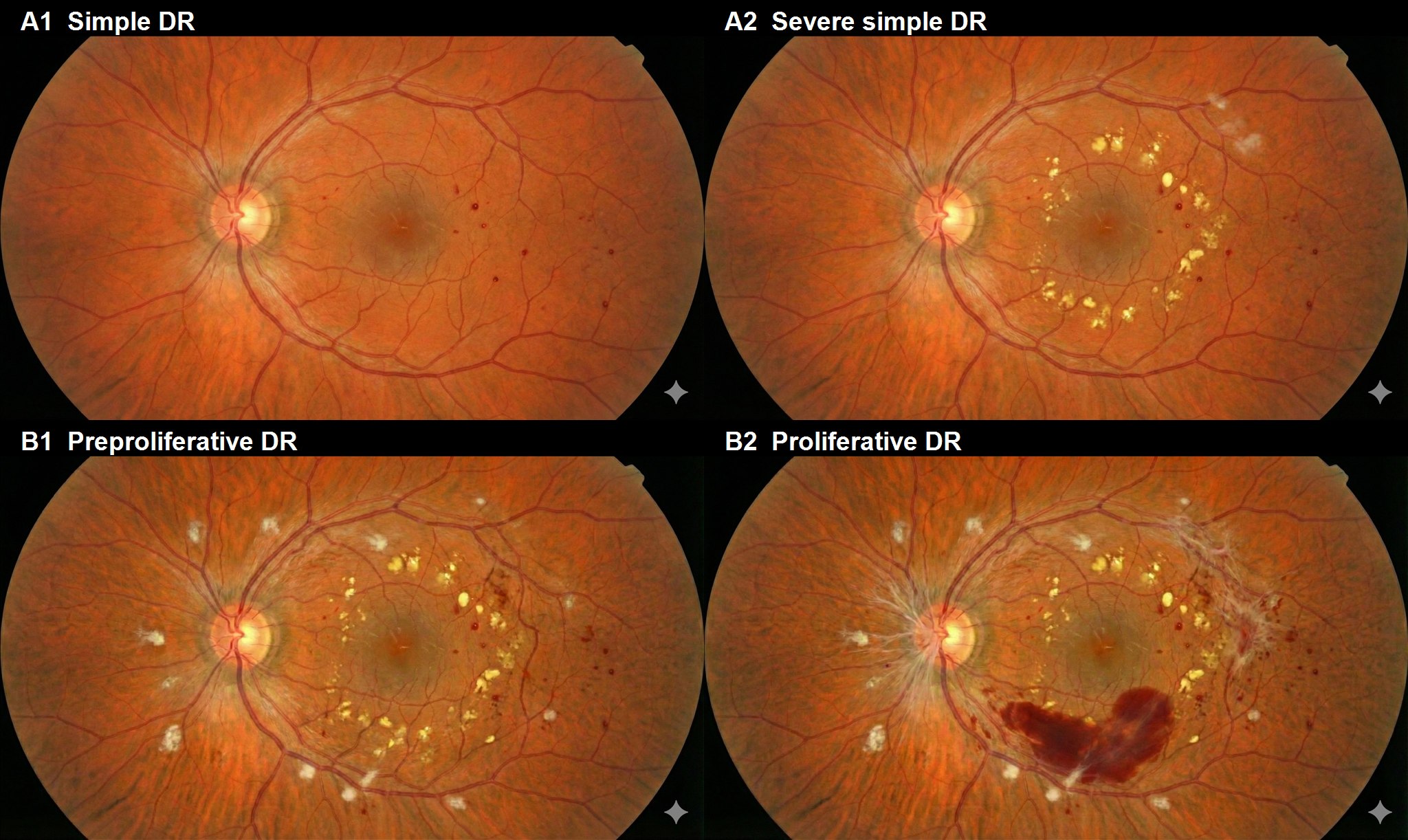
DME의 임상 소견
섹션 제목: “DME의 임상 소견”황반 부종의 OCT 단층상은 망막 팽창, 낭포황반부종, 장액망막박리의 세 가지 기본형의 조합으로 평가합니다.
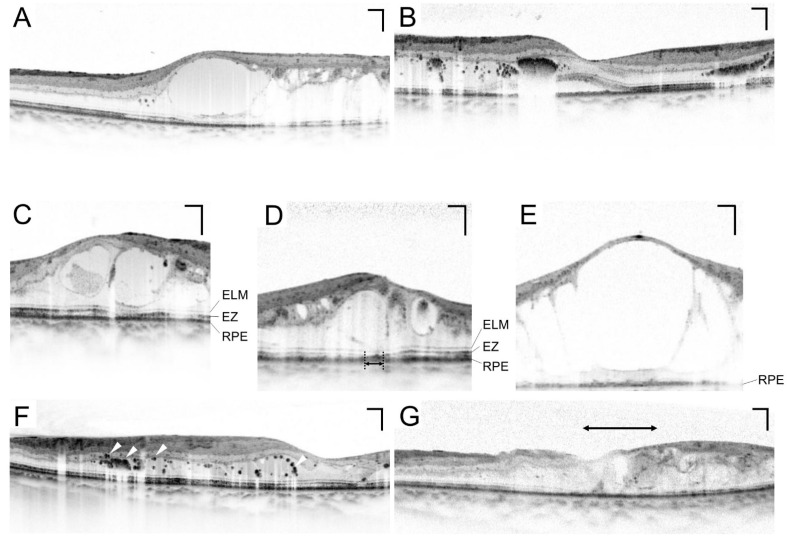
임상적으로 유의한 황반부종(CSME)은 ETDRS 정의에 따라 다음 중 하나를 충족하는 것입니다2):
- A. 중심와 500μm 이내의 망막 비후
- B. 중심와 500μm 이내의 경성 백반과 인접 망막 비후
- C. 1유두면적 이상의 비후가 있고 그 일부가 중심와에서 1,500μm 이내
SD-OCT 중심 망막 두께 300μm 이상을 중심와를 포함하는 DME의 역치로 합니다(기종별: Spectralis 320/305μm, Cirrus 305/290μm, Stratus 250/250μm, 남성/여성)1). DME의 국제 중증도 분류는 경증(황반 중심에서 떨어진 비후·경성 백반), 중등증(중심에 가깝지만 포함하지 않음), 중증(중심와 포함)의 3단계입니다. DME는 NPDR의 진행과 함께 증가하며, 경증 NPDR 1.76.3%, 중등증 NPDR 20.363.2%에서 합병됩니다1).
3. 원인과 위험 요인
섹션 제목: “3. 원인과 위험 요인”DR 진행과 관련된 주요 위험 인자는 다음과 같습니다.
| 위험 인자 | 주요 근거 |
|---|---|
| 유병 기간 | 가장 큰 위험 인자. 2형 당뇨병 진단 시 약 30%가 이미 DR을 가지고 있습니다1) |
| 혈당 조절 | HbA1c 7.0% 미만에서 미세혈관 합병증이 예방됩니다(구마모토 연구). HbA1c 1% 감소 → 미세혈관 합병증 위험 37% 감소(UKPDS)1) |
| 고혈압 | WESDR: 수축기 10mmHg 상승 → 초기 DR 10%·증식성 DR/DME 15% 위험 증가. UKPDS: 10mmHg 감소 → DR 진행 35% 감소·시력 저하 47% 감소1) |
| 이상지질혈증 | 페노피브레이트(FIELD 연구): 광응고 도입 31% 감소, 증식성 DR 30% 감소, DME 31% 감소. ACCORD 안 연구: DR 진행 오즈 40% 감소1) |
| 신기능 장애 | 단백뇨 및 GFR 감소가 DR 유병률과 상관관계. 신증 → PDR 진행 위험 29% 증가1) |
| 임신 | 기존 DR 없음 → 임신 중 DR 발생 8 |
| 중증 저혈당 | DR 발생률 약 4배 증가(JDCS)1) |
혈당 관리의 근거
섹션 제목: “혈당 관리의 근거”여러 대규모 임상시험에서 엄격한 혈당 조절이 DR 예방 및 진행 억제에 효과적임이 입증되었습니다1).
- Kumamoto 연구: HbA1c 7.0% 미만(NGSP 환산)으로 미세혈관 합병증 예방
- UKPDS: HbA1c 1% 감소 시 미세혈관 합병증 위험 37% 감소
- DCCT/EDIC: 조기 집중 인슐린 요법군이 장기 추적에서도 DR 진행 및 DME 발생을 유의하게 억제
- J-DOIT3: 다인자 중재 치료군에서 DR 진행 위험 감소
- Steno-2 연구: 다인자 집중 요법으로 DR 진행 위험 58% 감소
반면, 장기간 혈당 조절이 불량한 환자에서 급속히 혈당을 개선하면 일시적으로 DR이 악화되는 “조기 악화(early worsening)“가 발생할 수 있습니다. 약 50%의 증례에서 시력 저하가 지속되므로, 완만한 혈당 개선이 바람직하며, 내과와의 협력이 중요합니다 1).
또한, 한 번 고혈당에 노출된 망막 세포에는 후성유전학적 변화가 각인되어 혈당이 정상화된 후에도 병변이 지속·진행되는 “대사 기억(metabolic memory)“이 알려져 있습니다 11). SOD2의 하향 조절 및 미토콘드리아 DNA의 과메틸화가 그 메커니즘으로 보고되었습니다.
지질 관리 및 RAS 억제제
섹션 제목: “지질 관리 및 RAS 억제제”- 페노피브레이트: FIELD 연구 및 ACCORD Eye Study에서 광응고 빈도 및 DR 진행을 유의하게 억제함 1).
- 스타틴: 레지스트리 데이터에서 비복용자 대비 DR 발병 위험 40% 감소 1).
- RAS 억제제: DIRECT 시험에서 칸데사르탄 투여로 DR이 34% 퇴축. ACE 억제제가 ARB보다 더 효과적이라는 보고도 있음 1)9).
HbA1c 7.0% 미만을 목표로 하면 미세혈관 합병증이 예방됩니다 (Kumamoto Study) 1). HbA1c 1% 감소로 미세혈관 합병증 위험이 37% 감소합니다 (UKPDS) 1). 한 번 고혈당에 노출된 세포에는 “대사 기억”이 남아 있으므로, 혈당이 정상화되어도 장기간 추적 관찰이 필요합니다 11).
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”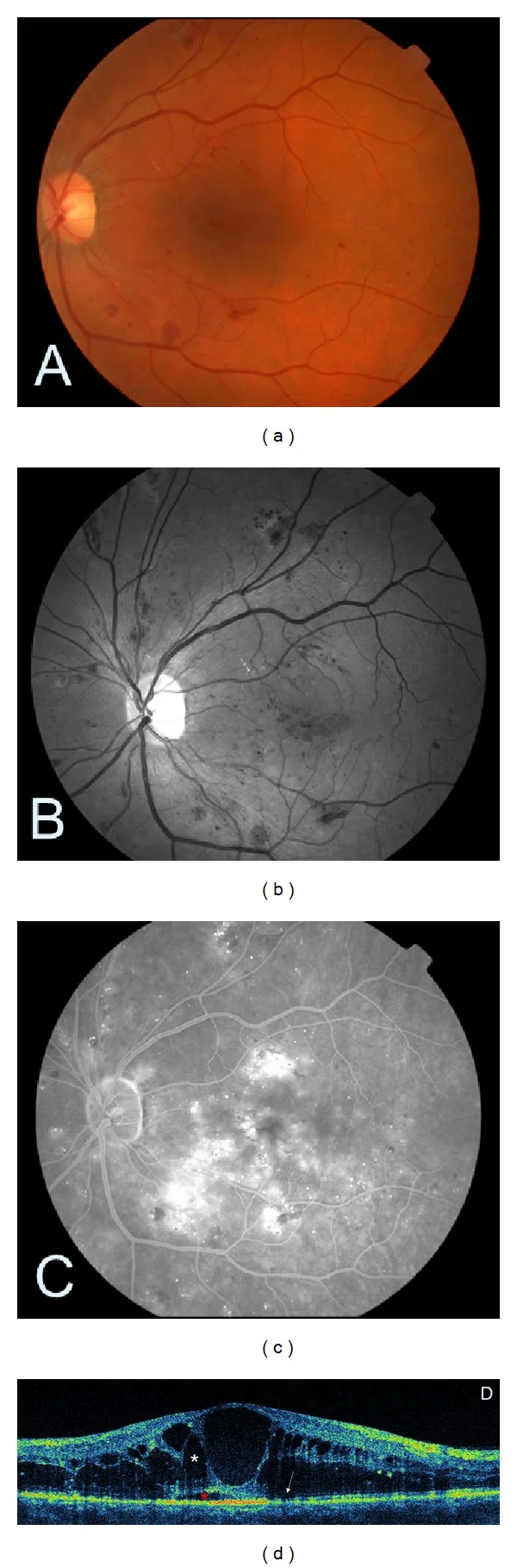
표준 검사법
섹션 제목: “표준 검사법”| 검사법 | 주요 용도 | 비고 |
|---|---|---|
| 산동 안저 검사 (도상경/전치렌즈) | 병기 분류의 표준 기준 | 산동 없이 약 50%만 정확히 분류됨2) |
| 세극등 현미경 검사 | 각막 손상, 홍수색소침착, 백내장, 전방 염증 확인 | 전치렌즈를 이용한 황반 세부 관찰 |
| 컬러 안저 사진 | 객관적 기록 및 경시적 비교 | ETDRS 7방향 촬영. 초광각 SLO로 주변부도 기록 가능3) |
| 형광 안저 혈관 조영 (FA) | 무관류 부위, 신생혈관, 누출점 확인. 국소성/미만성 DME 감별 | FA 전체 부작용 1.1 |
| 광간섭 단층촬영 (OCT) | 황반 부종의 정량 평가 및 경과 관찰 | SD-OCT 깊이 분해능 5μm. 중심 망막 두께 300μm 이상에서 중심와 DME1) |
| OCTA | 조영제 없이 모세혈관 소실, 무관류 영역(NPA), 신생혈관 평가 | 비침습적. FAZ 정량화도 가능3) |
| 초음파 검사 | 중간 굴절매체 혼탁 시 망막 및 유리체 관계 평가 | 견인성 망막박리 범위 및 증식막 위치 파악 |
| 망막전위도(ERG) | 망막 기능의 객관적 평가 | OP 잠복기 연장은 DR 초기부터 나타남. 음성 ERG는 수술 후 시력 불량을 시사1) |
선별검사 시작 시기
섹션 제목: “선별검사 시작 시기”- 1형 당뇨병: 진단 후 5년 이내 (사춘기 전 시력 저하는 드물다)1)2)
- 2형 당뇨병: 진단 시 안과 진료 (진단 시 이미 약 30%에서 DR 발생)1)
- 임신 합병 당뇨병: 첫 삼분기 초기에 진료. 임신 중 3개월마다 추적1)
- 임신성 당뇨병(GDM): 안과 진료 불필요2)
권장 안과 검진 간격
섹션 제목: “권장 안과 검진 간격”| 병기(수정된 Davis 분류) | 권장 간격 |
|---|---|
| 당뇨병(망막병증 없음) | 1년에 1회 |
| 단순 당뇨망막병증(경증~중등도 NPDR) | 6개월에 1회 |
| 증식전 당뇨망막병증(중증 NPDR) | 2개월에 1회 |
| 증식성 당뇨망막병증 | 1개월에 1회 |
(AAO PPP에서는 중증 NPDR에 대해 3~4개월마다를 권장하며, GL 표 3의 값과 약간 다름) 1)2)
감별 진단
섹션 제목: “감별 진단”주요 감별 대상으로는 고혈압성 망막병증, 망막동정맥폐쇄증, Eales병, Coats병, 혈액 질환(빈혈, 백혈병, 호지킨병), 인터페론 망막병증, 방사선 망막병증, Purtscher병, 고안병, 포도막염(베체트병, 사르코이드증, SLE)이 있습니다.
2형 당뇨병은 진단 시 약 30%가 이미 DR을 가지고 있으므로 진단 시 안저 검사를 받는 것이 권장됩니다1). 1형 당뇨병은 진단 후 5년 이내를 기준으로 합니다1). 임신을 동반한 경우 첫 삼분기에 가능한 한 조기에 검사를 받고, 임신 중에는 3개월마다 추적 관찰이 필요합니다1).
5. 표준 치료법
섹션 제목: “5. 표준 치료법”전신 관리 (모든 병기 공통)
섹션 제목: “전신 관리 (모든 병기 공통)”전신 위험인자 관리는 DR 예방과 진행 억제의 근본이며, 모든 병기를 통해 지속합니다.
- 혈당 조절: HbA1c 7.0% 미만을 목표 1). 급속한 개선은 early worsening의 위험이 있습니다.
- 혈압 관리: UKPDS: 10mmHg 감소로 DR 진행 35% 감소, 시력 저하 47% 감소 1).
- 지질 관리: Fenofibrate로 DR 진행 오즈비 40% 감소 (ACCORD Eye Study) 1).
- 다인자 중재 치료: Steno-2 Study에서 DR 진행 위험 58% 감소 1).
당뇨병성 황반 부종 (DME)의 치료
섹션 제목: “당뇨병성 황반 부종 (DME)의 치료”항VEGF 요법
1차 선택: 중심와를 포함하는 DME에 대한 표준 치료 1).
라니비주맙 (루센티스): 0.5mg/0.05mL 유리체강내 주사. 시력 안정까지 월 1회 투여.
아플리버셉트 2mg (아일리아): 2mg/0.05mL. 월 1회×5회 도입 후 2개월마다.
파리시맙 (바비스모): 6mg/0.05mL. 항VEGF+항Ang-2 이중특이성 항체. YOSEMITE/RHINE 시험에서 5070%가 1216주 간격 유지 9).
브롤루시주맙 (베오뷰): 6mg/0.05mL. 분자량 26kDa. KESTREL/KITE 시험에서 50% 이상이 q12w 유지 5).
재투여 요법: PRN (필요시 투여), 고정 투여, TAE (treat and extend)의 3가지 방식 1).
스테로이드 요법
레이저 광응고술 (DME)
대상: 중심와를 포함하지 않는 DME에 대한 선택지1).
직접 응고: 누출원인 모세혈관류에 직접 조사.
격자형 응고: 미만성 누출 또는 무관류 부위에 조사.
변형 ETDRS법: 황반 중심 500μm 이내 조사를 피하고, 저출력·광간격으로 시행1).
주의: 위축성 반흔 확장 및 망막하 섬유증식 위험이 있습니다1).
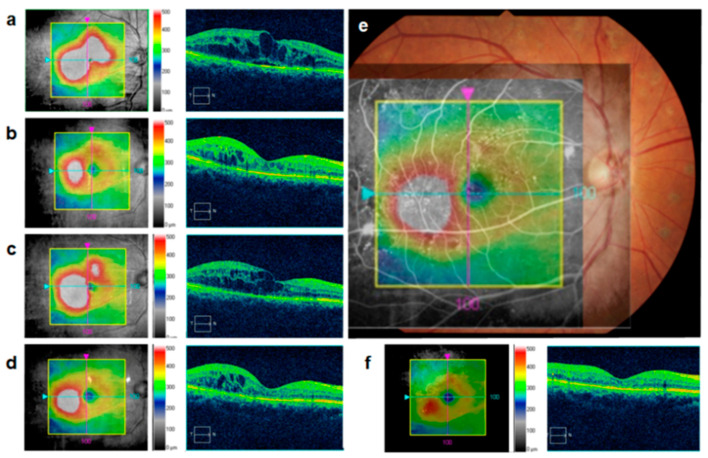
항VEGF 약물 비교
섹션 제목: “항VEGF 약물 비교”| 약제명 (상품명) | 용량 | 특징 |
|---|---|---|
| 라니비주맙 (루센티스) | 0.5mg/0.05mL | Fab 단편. 월 1회 투여. 시력 안정 시까지 지속. |
| 아플리버셉트 2mg (아일리아) | 2mg/0.05mL | VEGF-A/B 및 PlGF 결합 융합 단백질. 5회 부하 투여 후 2개월마다. |
| 아플리버셉트 8mg (아일리아 8mg) | 8mg/0.07mL | 고용량. 최대 16주 간격 2) |
| 브롤루시주맙 (베오뷰) | 6mg/0.05mL | 분자량 26kDa. 50% 이상이 12주 간격. 안내 염증 위험 주의 5)7) |
| 파리시맙 (바비스모) | 6mg/0.05mL | 항VEGF + 항Ang-2. 최대 16주 간격 9) |
중심와를 포함하고 시력이 양호한(20/25 이상) DME에서는 시력이 20/30 이하로 떨어질 때까지 치료를 연기하는 것도 선택지입니다2).
증식전~증식망막병증의 치료
섹션 제목: “증식전~증식망막병증의 치료”- 범망막광응고술(PRP): 허혈망막을 응고하여 VEGF 생성을 감소시키고 신생혈관을 퇴축시킵니다. 고위험 PDR에는 예외 없이 시행합니다1). NPA 3사분면 이상에서 권장1). ETDRS 기준에서는 조사 시간 0.2초, 200μm, 200mW가 표준입니다1).
- 선택적 망막광응고술: FA에서 NPA를 확인하고 해당 부위에 선택적으로 시행합니다. 증식전 DR에 자주 시행됩니다1).
- 항VEGF(PDR): DRCR Protocol S에서 라니비주맙 유리체강내 주사가 PRP에 비해 비열등함을 보였습니다(2년 추적)2). 그러나 투여 중단 시 신생혈관이 재증식할 위험이 있어 지속적인 외래 관리가 전제되어야 합니다.
- DRCR Protocol W: NPDR에 대한 예방적 항VEGF 투여는 PDR/DME 발병을 예방하지만, 장기 시력 결과는 초기 관찰과 동등합니다2).
- 유리체절제술 적응증: 황반을 위협하는 견인망막박리, 열공병발형, 지속/재발성 유리체출혈, 신생혈관녹내장1). 최소절개유리체절제술(MIVS)의 보급으로 저침습화가 진행되고 있습니다. 트리암시놀론을 이용한 유리체 가시화, 브릴리언트블루G(BBG)를 이용한 내경계막 염색으로 수술 정밀도가 향상되었습니다.
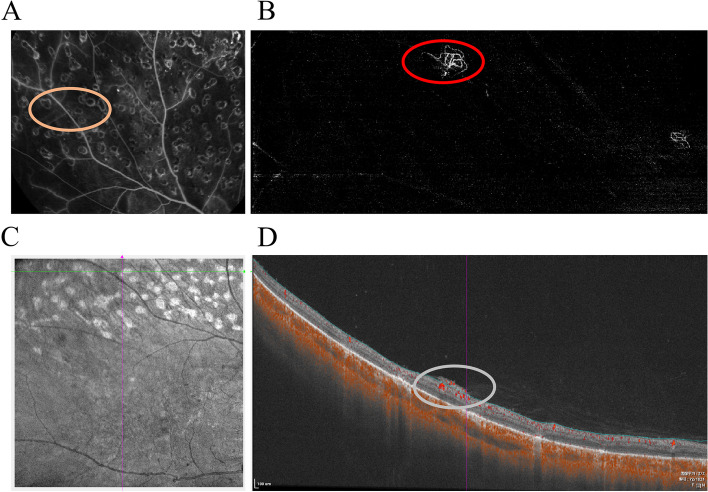
중심와를 포함하는 DME에 대해 항VEGF 요법이 일차 선택입니다1). 라니비주맙, 아플리버셉트, 파리시맙, 브롤루시주맙 모두 효과적이며, 투여 간격 연장이 가능한 점에서 파리시맙(최대 q16w)과 브롤루시주맙(50% 이상 q12w)이 주목받고 있습니다5)9). 항VEGF 효과가 불충분한 경우 트리암시놀론 또는 덱사메타손 임플란트를 이용한 스테로이드 요법을 고려합니다2).
6. 병태생리학 및 상세한 발병 기전
섹션 제목: “6. 병태생리학 및 상세한 발병 기전”DR의 기본 병태는 혈관 투과성 항진, 혈관 폐쇄, 혈관 신생의 세 가지로 크게 나뉘며, 단순 망막증, 증식전 망막증, 증식 망막증의 각 병기는 이러한 기본 병태에 거의 대응합니다.
고혈당에 의한 4대 대사 경로
섹션 제목: “고혈당에 의한 4대 대사 경로”고혈당 상태에서는 4가지 주요 대사 경로가 활성화되어 산화 스트레스와 염증을 통해 망막 손상이 진행됩니다11).
| 경로 | 주요 생성물/변화 | 주요 하류 손상 |
|---|---|---|
| 폴리올 경로 | 소르비톨 축적 | NADPH 고갈 → 글루타티온 감소 → 산화 스트레스 증폭 |
| AGEs 형성 | RAGE 활성화 | NF-κB↑ → VEGF↑, 주세포 세포자멸사 |
| PKC 활성화 | PKC-β 활성화 | VEGF/Nox 증가 |
| 헥소사민 경로 | UDP-GlcNAc 과잉 | TGF-β/PAI-1 증가 |
혈액-망막 장벽(BRB) 파괴의 메커니즘
섹션 제목: “혈액-망막 장벽(BRB) 파괴의 메커니즘”내측 BRB(망막 모세혈관 내피의 치밀연접)와 외측 BRB(RPE 세포 간 치밀연접) 모두 손상됩니다8).
- TNF-α → PKCζ → claudin-5/ZO-1 감소 → 내측 BRB 파괴
- IL-1β → 백혈구 동원 → 내측 BRB 파괴
- CCL2 → 단핵구 침윤 → VEGF/TNF-α 분비 (피드포워드)
- 주세포 소실: DR의 가장 초기 변화. AngII에 의한 세포자멸사 유도가 주원인9)
국소 RAAS
섹션 제목: “국소 RAAS”망막에는 순환계와 독립적인 국소 RAAS가 발현되어 있습니다9). 고전적 경로(ACE/AngII/AT1R 축)는 주세포 세포자멸사, 백혈구 정체, BRB 파괴를 촉진하고, 보호 경로(ACE2/Ang-(1-7)/Mas 축)는 이에 길항합니다. 망막 내 AngII 농도는 순환 중보다 높으며, DIRECT 시험에서 칸데사르탄 투여로 DR이 34% 퇴축되었습니다9).
대사 기억과 후성유전학적 변화
섹션 제목: “대사 기억과 후성유전학적 변화”일단 고혈당에 노출된 망막 세포는 혈당이 정상화된 후에도 후성유전학적 변화(SOD2 억제, 미토콘드리아 DNA 과메틸화)가 지속됩니다11). 미토콘드리아 전자전달계 복합체 I/III에서 ROS 생성 증가, Drp1/OPA1 불균형으로 인한 미토콘드리아 과도한 단편화, Nrf2/KEAP1 및 SIRT1을 통한 항산화 반응 장애가 그 메커니즘으로 보고되었습니다.
DR에서의 신경변성
섹션 제목: “DR에서의 신경변성”DR은 “신경혈관 질환”으로 재정의되었으며2), 혈관 병변에 앞서 OCT에서 GCIPL 얇아짐을 감지할 수 있습니다13). 황반 NFL은 연간 0.25μm, GCIPL은 연간 0.29μm씩 얇아집니다. 뮐러 세포의 교세포증(GFAP 상승)과 미세아교세포 활성화도 확인되었습니다. Fractalkine(CX3CL1)은 망막 신경절 세포가 생성하며, CX3CR1 수용체에 작용하여 항염증 및 신경보호 효과를 발휘합니다10).
유리체 변화와 DR의 관계
섹션 제목: “유리체 변화와 DR의 관계”당뇨병 환자에서는 유리체 내 포도당 농도가 상승하고, 콜라겐 섬유의 당화 반응이 진행됩니다. 당화 정도는 DR 진행도와 상관관계가 있으며, 콜라겐 구조 변화는 액화, 유리체 피질 수축, 후유리체 박리(PVD)를 일으키기 쉽게 만듭니다. 견인이 없는 완전 PVD가 발생하면 증식성 DR로의 진행은 거의 없습니다. 반면, 불완전 PVD(유리체와 증식 조직의 강한 유착)에서는 유리체 견인이 지속되어 견인성 망막박리나 유리체 출혈이 발생하기 쉽습니다.
혈당 조절은 DR 예방 및 진행 억제에 가장 중요하며, HbA1c 7.0% 미만을 목표로 합니다1). 그러나 “대사 기억” 개념에 따르면, 일단 고혈당에 노출된 세포는 후성유전학적 변화가 남아 있어 혈당이 정상화된 후에도 병변이 지속되거나 진행될 수 있습니다11). DCCT/EDIC 추적 연구에서는 조기 집중 치료군이 장기간에 걸쳐 DR 진행을 억제한 것으로 나타났습니다.
7. 최신 연구와 향후 전망
섹션 제목: “7. 최신 연구와 향후 전망”신규 항VEGF 약물 및 장기 지속형 제제
섹션 제목: “신규 항VEGF 약물 및 장기 지속형 제제”Aflibercept 8mg은 2023년 DME 적응증으로 승인되었으며, 최대 16주 간격까지 연장이 기대됩니다2). DRCR Protocol W에서는 중증 NPDR에 대한 예방적 항VEGF 투여가 PDR/DME 발병을 예방하는 반면, 장기 시력 결과는 초기 관찰과 동등한 것으로 나타났습니다2).
AI 선별검사
섹션 제목: “AI 선별검사”LumineticsCore(구 IDx-DR)는 2018년 FDA가 승인한, 의사의 판독이 필요 없는 최초의 자율 AI 안저 진단 시스템입니다3). 딥러닝 모델에서 민감도 96.8%, 특이도 87%가 보고되었으며3), EyeArt, AEYE-DS 등의 새로운 시스템도 개발되고 있습니다2).
프랙탈카인 유전자 치료
섹션 제목: “프랙탈카인 유전자 치료”가용성 프랙탈카인 발현 AAV 벡터(rAAV-sFKN) 투여로 시력 개선, 피브린 누출 감소, 미세아교세포 정상화가 입증되었습니다10). 항VEGF 요법과는 다른 신경보호 및 항염증 기전을 가지고 있습니다.
신경보호제의 임상시험
섹션 제목: “신경보호제의 임상시험”EUROCONDOR 2-3상 시험(NCT01726075)에서는 소마토스타틴과 브리모니딘 점안액이 평가되었으나 전체 분석에서는 유효성을 보이지 않았으며, 기준선 mfERG 이상 하위군에서 신경 기능 장애의 진행 중단이 인정되었습니다13). 시티콜린+비타민 B12 점안액의 36개월 이중맹검 RCT에서는 경도 DR에 대한 투여로 기능적, 구조적, 혈관성 진행 억제가 보고되었습니다13).
miRNA 표적 치료
섹션 제목: “miRNA 표적 치료”miRNA는 DR 병태의 여러 축(산화 스트레스, 염증, 신경변성, 혈관 기능 장애)을 통합적으로 조절하는 ‘마스터 조절자’로 주목받고 있습니다14). miR-195 억제를 통한 SIRT1 안정화, miR-497a-5p에 의한 VEGF-A 번역 억제 가능성이 제시되었으며, 약 350개의 miRNA가 망막에서 발현되고 86개 이상이 DR 모델에서 비정상 발현됩니다.
메트포르민의 망막 보호 효과
섹션 제목: “메트포르민의 망막 보호 효과”메트포르민은 AMPK 활성화를 통한 항산화, 항염증, 항혈관신생, 신경보호의 다면적 작용을 가지며, 관찰 연구에서 사용자에서 STDR(시력 위협 DR)의 aHR=0.29가 보고되었습니다12). 그러나 안과 적응증에 대한 RCT 데이터는 현재 충분하지 않습니다.
피네레논의 가능성
섹션 제목: “피네레논의 가능성”비스테로이드성 MR 길항제 피네레논은 전임상 모델에서 BRB 파괴, 혈관신생, 염증 감소가 입증되었으며, DR에 대한 독립적인 치료 표적으로서 MR의 의의가 검토되고 있습니다9).
8. 참고문헌
섹션 제목: “8. 참고문헌”- 日本糖尿病眼学会診療ガイドライン委員会. 糖尿病網膜症診療ガイドライン(第1版). 日眼会誌. 2020;124(12):955-981.
- Flaxel CJ, Adelman RA, Bailey ST, et al. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024;131(1):P49-P130.
- Huang Y, et al. Advances in diabetic retinopathy: epidemiology, pathogenesis, diagnosis, and treatment. Front Endocrinol. 2025;16:1664604.
- Beuran DI, et al. Sterile endophthalmitis after intravitreal injection of triamcinolone acetonide. Rom J Ophthalmol. 2024;68(1):2-7.
- Chakraborty D, et al. Off-label intravitreal brolucizumab for recalcitrant diabetic macular edema: a case series. Am J Ophthalmol Case Rep. 2021;24:101197.
- Kikuchi Y, et al. Renal thrombotic microangiopathy induced by intravitreal aflibercept for diabetic macular edema. BMC Nephrology. 2022;23(1):348.
- Hirano T, et al. Retinal arterial occlusive vasculitis after brolucizumab injection for diabetic macular edema. Am J Ophthalmol Case Rep. 2023;29:101788.
- O’Leary F, Campbell M. The blood-retina barrier in health and disease. FEBS J. 2023;290(4):878-891.
- Li X, et al. The role of the renin-angiotensin-aldosterone system in diabetic retinopathy: mechanisms and therapies. Arch Endocrinol Metab. 2024;68:e230292.
- Lee CY, Yang CH. The role of fractalkine and its receptor CX3CR1 in diabetic retinopathy. Int J Mol Sci. 2025;26(1):378.
- He W, et al. Oxidative stress and diabetic retinopathy: molecular mechanisms, pathological roles, and therapeutic implications. Front Immunol. 2025;16:1571576.
- Alasbily H, et al. Metformin and diabetic retinopathy: a comprehensive review. Cureus. 2025;17(7):e87455.
- Bianco L, Arrigo A, Aragona E, et al. Neuroinflammation and neurodegeneration in diabetic retinopathy. Front Aging Neurosci. 2022;14:937999.
- Chen J, Zhang J, Li C, et al. Targeting microRNAs in diabetic retinopathy: from pathogenic mechanisms to therapeutic potentials. Front Endocrinol. 2025;16:1664604.
