황반전막 박리

황반상막
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 황반상막이란?
섹션 제목: “1. 황반상막이란?”황반상막(Epiretinal Membrane; ERM)은 망막 내경계막(ILM) 위에 형성되는 섬유세포 증식 조직입니다. 황반주름, 셀로판 황반증, 망막전황반섬유증, 유리체황반경계증후군이라고도 합니다11). 황반상막은 이차적으로 망막주름, 황반부종, 견인성 망막박리를 일으킬 수 있습니다.
황반상막은 특발성과 속발성으로 분류됩니다. 속발성은 황반주름(macular pucker)이라고도 합니다11).
특발성 황반상막은 후유리체박리(PVD)와 관련되어 발생하며 50세 이상에서 많습니다. 속발성 황반상막은 망막열공, 열공성 망막박리, 안내 수술, 외상, 망막혈관폐쇄, 포도막염, 당뇨망막병증, 망막색소변성증 등을 계기로 다양한 안질환에 속발하여 발생합니다.
유병률은 검사법과 대상 집단에 따라 다르며 다양한 보고가 있습니다. 각 연구의 유병률을 아래에 요약합니다.
| 연구 | 대상 집단 | 유병률 | 검사법 |
|---|---|---|---|
| 베이징 안구 연구 | 중국 도시 지역 | 2.2% | 안저 사진 |
| 한단 안구 연구 | 중국 농촌 지역 | 3.4% | 안저 사진 |
| 블루 마운틴 안구 연구 | 호주 | 7.0% | 안저 사진 |
| 멜버른 코호트 | 호주 | 8.9% | 안저 사진 |
| Los Angeles Latino Eye Study | 히스패닉계 | 18.8% | 안저 사진 |
| MESA | 미국 다인종 | 28.9% | 안저 사진 |
| Beaver Dam Eye Study (20년) | 미국 백인 (평균 74.1세) | 34.1% | SD-OCT15) |
셀로판 황반증(무증상 ERM)의 유병률은 1.825.1%, 증상성 ERM(망막전황반섬유증)은 0.73.9%로 보고된다12). 미국에서는 약 3000만 명이 이환된 것으로 추정된다12). 양측성은 20~35%에서 나타난다11). 인종 차이도 보고되었으며, MESA 연구에서는 중국계 39.0%, 히스패닉 29.3%, 백인 27.5%, 흑인 26.2%로 나타났다16).
자연 경과
섹션 제목: “자연 경과”5년 동안 ERM의 29%가 진행, 26%가 퇴축, 39%가 안정을 보인다(Blue Mountains Eye Study)14). 셀로판 황반증의 진행은 5년에 20%에 불과하다. PVD가 동반된 ERM의 자연 분리는 1.5%(1,091안 중 16안), PVD가 없는 ERM의 자연 분리는 13.6%(157안 중 21안, 평균 33개월 추적)이다12). 증상 발현까지 수술을 연기해도 즉시 수술과 비교하여 예후가 악화되지 않는 것으로 알려져 있다12). 후유리체박리가 없는 젊은 환자에서는 드물게 자연 박리가 일어날 수 있으므로 주의 깊게 경과 관찰한다.
제2형 신경섬유종증(NF2)에서 황반상막 유병률은 80%에 이릅니다 9). 유리체황반견인(VMT)의 유병률은 0.4~2.0%(63세 이상)이며, ERM과 VMT는 종종 동반됩니다 12).
중증도 분류(Gass 분류)
섹션 제목: “중증도 분류(Gass 분류)”임상적 중증도 분류로 Gass 분류가 널리 사용됩니다.
| 등급 | 소견 | 시력 기준 |
|---|---|---|
| 0등급 | 투명한 얇은 막(셀로판 황반증). 망막 내층 변형 없음 | 양호 |
| 1등급 | 막 수축으로 인한 망막 주름. 망막 모세혈관이 불명확해짐 | 보통 0.5 이상 |
| 2등급 | 회색 불투명 두꺼운 막. 황반 주름이 현저함 | 감소 |
모든 황반상막이 수술 적응증이 되는 것은 아닙니다. 무증상, 증상이 경미하거나 시력이 양호한 경우 경과 관찰을 선택합니다. 자연 경과에서 5년 동안 29%가 진행, 26%가 퇴축, 39%가 안정적이라고 보고되었으며14), 증상이 나타날 때까지 수술을 연기해도 예후가 악화되지 않는다고 알려져 있습니다12). 수술은 일반적으로 교정시력 0.7 이하이고 변시증이 심한 경우, 또는 시력 저하가 비교적 급성이며 황반상막에 의한 장애로 생각되는 경우에 고려됩니다. 최종적으로는 환자의 자각 증상과의 균형을 고려하여 판단합니다.
2. 주요 증상과 임상 소견
섹션 제목: “2. 주요 증상과 임상 소견”자각 증상
섹션 제목: “자각 증상”황반상막은 무증상인 경우가 많으며, 건강검진이나 다른 질환의 경과 관찰 중 우연히 발견되는 예도 적지 않습니다. 증상이 있는 경우 다음과 같은 증상을 나타냅니다.
- 변시증(왜곡): 직선이 왜곡되어 보입니다. 가장 특징적이고 환자가 호소하기 쉬운 증상입니다.
- 시력 저하: 막의 수축·비후가 진행됨에 따라 발생합니다.
- 소시증: 물체가 작게 보입니다. 막의 견인에 의한 황반 변형이 원인입니다.
- 대시증: 물체가 실제보다 크게 보이는 경우도 있습니다.
- 단안 복시: 한쪽 눈으로 두 개로 보입니다.
- 독서 곤란, 운전 곤란, 양안시 곤란: 일상생활에 미치는 영향으로 빈도가 높은 주된 호소입니다12).
Amsler grid는 변시증의 자가 모니터링 도구로서 유용하며, 증상의 진행을 환자 스스로 확인하는 수단으로 활용됩니다12).
임상 소견
섹션 제목: “임상 소견”세극등 현미경에서는 황반부 표면의 광택, 망막 주름, 혈관 사행이 확인됩니다. 슬릿 빛의 폭을 넓게 하여 황반부를 관찰함으로써 막의 두께나 분포 영역을 OCT 이미지와 결합하여 평가할 수 있습니다. 초기에는 water silk reflex(비단 같은 광택)로 포착되는 반짝이는 반사가 특징적입니다. 병변이 진행되면 황반 부종, 가성 황반원공을 나타낼 수 있습니다.
두껍고 흰색 불투명한 막일수록 증상이 나타나기 쉽고, 황반 편위(ectopia)를 일으키기 쉽습니다12). 정상적인 중심와 함몰의 소실, 황반의 낭포양 변화, 층판 황반원공, 전층 황반원공으로의 진행도 가능합니다.
유리체유두견인(Vitreopapillary traction): 시신경유두 주변의 유리체 유착이 ERM에 동반될 수 있습니다. 시신경유두부종(울혈유두)으로 오진될 수 있으므로 주의가 필요합니다12).
광간섭단층혈관조영(OCTA)에서는 중심와무혈관영역(FAZ)의 형태 변화가 확인됩니다. 황반전막이 있는 눈의 FAZ 면적은 0.11 mm²로, 건강한 눈의 0.24 mm²와 비교하여 유의하게 좁아져 있습니다2).
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”황반전막의 가장 중요한 관련 인자는 후유리체박리(PVD)입니다. 기존 가설에서는 PVD 후 잔류한 피질 유리체가 내경계막(ILM)의 열상을 유발하고, 신경교세포와 망막색소상피세포가 유리체강으로 이동하여 섬유아세포 유사 세포로 분화 및 증식함으로써 황반전막이 형성된다고 생각되었습니다11).
최근 지지를 얻고 있는 새로운 가설에서는 ILM 열상이 필수적이지 않다고 합니다. ILM 위에 잔류하는 유리체 피질 내의 세포가 근섬유아세포로 활성화되어 막 형성 및 수축을 초래하는 기전이 제안되고 있습니다12).
유리체 주머니 이론에 의한 병태
섹션 제목: “유리체 주머니 이론에 의한 병태”후유리체박리가 발생하지 않은 단계에서도 후유리체 젤 내에는 액화강(후유리체 피질 전 주머니)이 존재합니다. 주머니의 후벽은 얇고 탄력성이 풍부한 유리체 피질이며, 이 황반 전에 존재하는 후유리체 피질에 세포 증식 등의 변형이 가해짐으로써 황반전막이 형성된다고 생각됩니다.
후유리체가 박리되지 않은 상태로 황반에 부착된 주머니의 후벽이 망막을 견인하는 증례와, 완전 PVD가 발생했을 때 망막 쪽에 남겨진 주머니의 후벽이 황반을 왜곡시키는 증례가 있습니다. 유리체 주머니의 후벽 위에 세포가 증식하여 황반전막을 형성하는 경우가 있으며, 이들은 속발성 또는 젊은 연령에서 흔히 관찰됩니다. 후유리체박리가 발생할 때 자연 박리가 일어날 수 있습니다.
참고로, 수술 시 후유리체가 부착되어 있던 증례가 20.1%에서 확인되었으며, Weiss ring의 존재가 반드시 후유리체의 완전 분리를 의미하지는 않는다는 점에 유의해야 합니다12).
NF2 관련 황반전막에서는 면역염색에서 GFAP 약양성, 네스틴 중등도 양성이 확인되어, 뮐러세포 유래 성분이 주체임이 시사됩니다9).
주요 위험 요인은 다음과 같습니다.
- 노화: 50세 이상에서 급증하고, 75세 이상에서 더욱 유병률이 상승합니다.
- 후유리체박리(PVD): 특발성 황반전막의 가장 큰 유발 요인.
- 여성: 체계적 문헌고찰(49,000예 초과)에서 유의한 위험 인자로 확인되었습니다13).
- 망막열공/망막박리: 속발성 황반전막의 주요 원인.
- 안내 수술력: 백내장 수술은 속발성 ERM의 확립된 위험 인자입니다12).
- 당뇨병 및 고지혈증: 셀로판 황반병증의 위험 인자(MESA data)12).
- 망막 혈관 폐쇄 및 포도막염: 염증 후 증식 반응으로 발생합니다.
- 망막색소변성증: 속발성 ERM의 원인 중 하나입니다.
- 방사선 치료: 양성자선 조사 후 속발성 망막앞막이 보고되었습니다3).
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”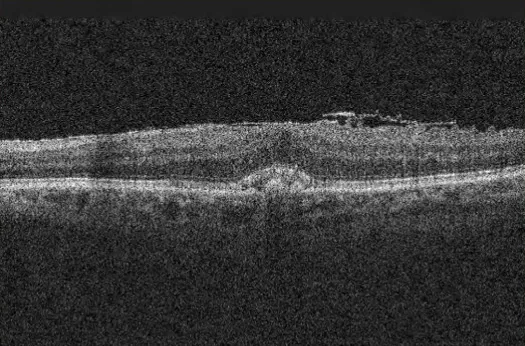
검사법 개요
섹션 제목: “검사법 개요”각 검사의 역할을 요약합니다.
| 검사 | 주요 목적 | 특징 |
|---|---|---|
| OCT | 막 묘사, 두께 평가, 망막 견인 확인 | 가장 중요, 비침습적 |
| OCTA | 혈관 흐름 평가 | FAZ 면적, 신생혈관 검출 |
| FA | 혈관 투과성, 무관류 평가 | 합병 질환의 감별 |
| 안저 검사 | 표면 광택, 주름 확인 | 선별 검사 |
**광간섭단층촬영(OCT)**이 진단의 핵심입니다. ERM은 OCT에서 내표면의 과반사층으로 나타나며, 종종 내망막 표면의 다리(pegs)로 부착되어 물결 모양의 단면을 보입니다. 중심와 함몰 소실, 망막 외층 융기, 낭포성 변화 등이 관찰됩니다. OCT를 통해 유리체나 막 조직에 의한 망막 견인, 망막 팽윤, 낭포성 변화, 망막박리 유무 및 타원체대(EZ) 상태도 파악할 수 있습니다. 수술 전 ILM 결손 예측에는 en face OCT가 유용하며, 22.7%의 증례에서 수술 전 ILM 결손이 확인되었습니다1).
ERM+VMT 동반은 ERM 안의 57%에서 관찰되며, VMT 안의 65%에서 ERM이 동반된다는 보고가 있습니다12).
**OCTA(광간섭단층혈관조영술)**에서는 표층 모세혈관망(SCP)의 혈관면적밀도(VAD) 상승이 확인됩니다2). 황반전막 유발 망막내 신생혈관 검출에도 유용합니다6).
형광안저조영술(FA): 초기 ERM에서는 비교적 정상 소견을 보입니다. 막 수축이 진행되면 견인 중심 부근에서 혈관 구불거림, 주변에서 혈관 직선화가 관찰됩니다. 견인 하의 모세혈관에서 누출 패턴도 관찰됩니다. 낭포강 내 염료 저류가 발생하는 경우, 위수정체안 CME와의 감별이 필요합니다(CME는 더 꽃잎 모양 패턴으로 시신경유두 과형광을 동반함) 12). FA/OCTA는 합병된 망막혈관폐쇄, 당뇨망막병증, 황반모세혈관확장증, 맥락막신생혈관 검출에도 유용합니다 12).
EZ/IZ 완전성과 예후 예측
섹션 제목: “EZ/IZ 완전성과 예후 예측”수술 전 OCT에서 타원체대(EZ)와 상호디지털화대(IZ, 원추세포외절끝선)가 온전한 경우, 수술 후 시력이 좋은 경향이 있습니다 12). 외망막, EZ, 광수용체외절 길이는 수술 후 호전 및 정상화될 수 있습니다(각 매개변수는 시력 개선과 상관관계). 시간영역OCT를 이용한 101안 연구에서는 광수용체층 손상이 수술 후 시력 불량의 예측인자로 보고되었습니다 12).
황반가구멍과의 감별
섹션 제목: “황반가구멍과의 감별”망막앞막의 특수형으로 황반가구멍이 있습니다. 망막앞막의 수축으로 중심와 함몰이 원통형이 되어 황반구멍과 유사한 소견을 나타냅니다.
임상적 감별점으로, 황반가구멍에서는 시력이 비교적 잘 유지되는 경우가 많습니다. 세극등검사에서 Watzke-Allen 징후가 감별에 유용하며, 황반구멍에서는 슬릿광을 비추면 잘록함을 자각하지만(양성), 황반가구멍에서는 균일한 폭의 세극광으로 인식됩니다(음성). OCT를 사용하면 둘의 감별이 용이합니다.
수술 적응증 판단 기준
섹션 제목: “수술 적응증 판단 기준”시력 장애와 망막 비후가 있는 것이 수술 적응증의 전제입니다. 시력이 좋아도 망막 비후가 현저하고 변시증이 심한 경우, 또는 전층 황반구멍을 합병한 경우도 수술 적응증이 됩니다.
시력 저하가 비교적 급성인 것, 백내장 정도에 비해 시력 장애가 망막앞막에 의한 것으로 생각되는 경우도 수술 적응증입니다. 증상 진행 속도, 환자의 직업 및 생활에 미치는 영향(독서 곤란, 운전 곤란)을 구체적으로 청취하고, 최종적으로는 환자의 자각 증상과의 균형을 고려하여 판단합니다. 수술은 선택적이며, 긴급성은 없습니다 12).
OCT(광간섭단층촬영)가 가장 중요한 검사입니다. 망막 표면의 고휘도 막상 구조와 망막 비후를 비침습적으로 묘사할 수 있으며, 진단, 수술 적응증 판단, 수술 후 경과 관찰 모두에 활용됩니다. 중심와 함몰 소실, 타원체대 상태, 망막 내 낭포성 변화 등도 평가할 수 있습니다. 수술 전 EZ/IZ 완전성은 수술 후 예후 예측에도 유용합니다 12).
5. 표준적 치료법
섹션 제목: “5. 표준적 치료법”유리체절제술
섹션 제목: “유리체절제술”황반전막 치료의 표준 수술법은 섬모체평면부 유리체절제술(PPV) + 황반전막 박리 + ILM 박리입니다. 23G, 25G, 27G 미세절개 유리체절제술(MIVS)이 표준이며, 최소 침습 및 조기 회복이 가능합니다.
ILM 박리
목적: 황반전막의 재발을 방지하고 망막의 더 완전한 신전을 촉진합니다.
ILM 경계부 처리: 황반전막만 절제하려고 해도 일반적으로 ILM에 균열이 생깁니다. 박리된 ILM과 그렇지 않은 부분의 경계가 황반을 통과하지 않도록 추가 박리를 시행합니다. 수술 전 en face OCT에서 22.7%의 증례에서 ILM 결손을 인지하며1), 결손 가장자리 박리술(defect-edge technique)이 유용합니다1).
염색제 사용: ILM/ERM 염색에는 brilliant blue G(BBG, TISSUEBLUE®)가 FDA 승인(2019년)을 받아 널리 사용됩니다. ICG, trypan blue, triamcinolone도 off-label로 사용됩니다. 저농도에서는 안전한 것으로 간주되지만, 광노출 시간 최소화가 중요하며 논의는 계속되고 있습니다12). 주변 유리체 쉐이빙(캐뉼라 근처를 중점적으로)을 통해 의인성 망막열공 위험을 줄일 수 있습니다.
수술 성적
섹션 제목: “수술 성적”- 시력 개선율: 약 80%의 증례에서 Snellen 2단계 이상의 시력 개선이 얻어집니다12)(기존 보고에서는 73%11)). 10~20%는 시력 불변 또는 악화입니다.
- 시력 개선 정도: logMAR 0.4에서 0.1로 개선(수술 전후 비교)2).
- 변시증 개선: 수술 전 56%가 변시증을 가지고 있었으며, 수술 후 13%로 감소11).
- VFQ-25 점수: 수술 후 6개월 및 24개월에 유의하게 개선됩니다12).
- 장기 성적(Elhusseiny 2020, 49안, 평균 111개월 추적): BCVA 0.56(20/72) → 1년 0.33(20/42) → 3년 0.25(20/35) → 10년 0.28(20/38)로, 수술 후 3년까지 개선이 지속되고 10년까지 안정을 유지했습니다17).
- 시력 회복 경과: 수술 후 3~6개월에 걸쳐 점차 개선되며, 수술 후 12개월까지 완만한 개선이 지속될 수 있습니다. 수술 후 1년에도 망막 비후 및 이에 따른 시기능 장애가 남아 있는 경우가 있습니다. 수술 후 시력은 수술 전 시력과 잘 상관관계가 있으므로, 시력이 너무 저하되기 전에 수술을 시행하는 것이 중요합니다.
ILM 박리의 증거
섹션 제목: “ILM 박리의 증거”ILM 박리는 ERM 재발 방지에 효과적이며 현재 표준 수술에 포함되어 있습니다12).
- 재발 방지 효과: ILM 박리 없이 ERM 재발률 8.6
21%, ILM 박리 시 02.6%12). - Ducloyer 2024 RCT(213안): 자연 박리 101안, 능동적 ILM 박리 51안, 비박리 49안 비교. 재발률은 능동적 박리군 0% vs 비박리군 19.6%로 유의한 차이. 그러나 능동적 ILM 박리군에서 BCVA 및 미세시야 회복이 다소 지연됨18).
- 2017년 메타분석: 시력 개선에는 명확한 차이가 없는 반면, ERM 재발 억제에서는 ILM 박리군이 우월하다고 보고됨19).
- 결론: ILM 박리는 재발 방지에 효과적이나 시력에 대한 우월성은 명확하지 않음. 내망막 소실(DONFL)이 발생할 수 있으나 기능적 영향은 불명.
VMT(유리체황반견인)의 관리
섹션 제목: “VMT(유리체황반견인)의 관리”VMT(유리체황반견인)는 ERM과 밀접하게 관련되어 있으며 종종 동반됩니다.
- VMT ≤1500μm: 23
47%가 12년 내 자연 소실. 시력이 안정적이면 경과 관찰이 선택지12). - 광범위 VMT(>1500μm), 황반박리 동반, 시력 불량: 자연 호전 기대 어려워 유리체 수술 적응12).
기체성 유리체 용해술(가스 주입을 통한 VMT 해소): 유리체내 C3F8 0.3ml 주입으로 85.7%의 VMT 해소율을 보인 연구가 있으나, DRCR Retina Network RCT에서는 망막열공 및 망막박리 발생률이 예상보다 높아 안전성 우려로 조기 중단됨12). 현재 명확한 증거가 부족하며, 위험과 이점의 개별 판단이 필요합니다.
오크리플라스민(Ocriplasmin): 재조합 프로테아제. 2012년 FDA 승인(증후성 VMA/VMT 치료). 3상 시험에서 VMA 해소율 27% vs 위약 10%(P<0.001)12). ERM 동반 VMT에 대한 효과는 제한적(VMA 해소율 8.7% vs 위약 1.5%)이며, ERM 단독에는 무효12). 부작용으로 유리체 부유물, 광시증, 안통, 시야 흐림(약 10%, 첫 주)이 있음. 심각한 부작용으로 급성 중증 시력 저하, ERG 이상, 색각 장애가 드물게 보고되나 대부분 가역적12).
수술 후 관리
섹션 제목: “수술 후 관리”- 수술 후 1일째 내원, 수술 후 1~2주 재진(안압, 전안부, 중심망막, 주변망막 평가)12).
- 복시 또는 양안시 어려움이 지속되는 경우: 사시 전문의 또는 시능 훈련사로의 의뢰 고려12).
비수술적 치료의 보고
섹션 제목: “비수술적 치료의 보고”표준 치료는 수술이지만, 다음과 같은 비수술적 자연 박리 또는 유발 박리가 보고되었습니다(모두 증례 보고 수준).
- 덱사메타손 유리체내 임플란트(DEX implant): 유리체내 투여 후 망막앞막의 자연 박리가 관찰된 증례가 보고되었습니다7).
- 항VEGF + 광역학치료(PDT) 후 자연 박리: 광역학치료 시행 후 망막앞막의 자발적 박리가 발생한 증례가 보고되었습니다4).
이들은 증례 보고에 불과하며, 현재 표준 치료는 아닙니다.
ILM 박리는 황반전막 재발 방지에 효과적이며 현재 표준 수술에 포함되어 있습니다. 재발률은 ILM 박리 시 02.6%, 비박리 시 8.621%로 보고됩니다 12). 수술 전 en face OCT에서 ILM 결손이 확인되는 경우(22.7%에서 존재) 결손 가장자리부터 박리 술기가 필요합니다 1). 그러나 기술적 난이도가 높고 RPE 위축 등의 합병증 위험과의 균형을 고려하여 판단합니다. 활동성 ILM 박리군에서는 시력 회복이 다소 지연될 수 있습니다 18).
시력 회복은 수술 후 3~6개월에 걸쳐 서서히 진행되며, 수술 후 12개월까지 개선이 지속되기도 합니다. 수술 후 1년에도 망막 비후와 이에 따른 시기능 장애가 남아 있을 수 있어 장기적인 경과 관찰이 중요합니다. 장기 성적에서는 수술 후 3년까지 개선이 지속되고 10년까지 안정이 유지된다고 보고됩니다 17). 수술 전 망막 변형 정도와 EZ 완전성이 회복 전망을 좌우합니다.
6. 병태생리학 및 상세 발병 기전
섹션 제목: “6. 병태생리학 및 상세 발병 기전”황반전막의 형성은 다음 단계를 거치는 창상 치유 유사 반응으로 이해됩니다 11).
- PVD와 잔류 유리체 피질: PVD 시 일부 유리체 피질이 ILM 위에 잔류합니다.
- ILM 미세 파열(기존 가설): 잔류 유리체 피질의 견인으로 ILM에 미세한 틈이 생깁니다.
- 세포 이동: ILM 파열 부위를 통해 망막 신경교세포(Müller 세포, 별아교세포), RPE 세포, 대식세포가 유리체강으로 이동합니다.
- 증식 및 섬유아세포 분화: 이동한 세포가 증식하고 섬유아세포 유사 수축성 세포로 분화하여 황반전막을 형성합니다.
유리체세포(hyalocyte)의 역할
섹션 제목: “유리체세포(hyalocyte)의 역할”특발성 ERM의 주요 세포 성분으로 라미노사이트(후유리체막 유래 유리체세포) 가 주목받고 있습니다 12). 유리체세포는 골수 유래 세포에서 기원하며 지속적으로 재생됩니다. 신경교세포와 유리체세포가 섬유아세포/근섬유아세포로 분화하여 세포외기질 형성 및 섬유화를 유발함으로써 ERM 형성에 이릅니다. ERM의 구성은 다양하며 기원과 원인도 여러 가지입니다.
ILM 파열을 필요로 하지 않는 새로운 가설에서는 ILM 위 잔류 유리체 피질 내 유리체세포가 근섬유아세포로 활성화되어 직접 ERM을 형성하고 수축시킨다고 합니다 12).
병리조직학적 기전
섹션 제목: “병리조직학적 기전”특발성의 경우 유리체 피질 내 섬유아세포, 근섬유아세포, 신경교세포, 대식세포, 염증 세포, 유리체 세포, 망막색소상피세포 등의 증식과 세포외기질의 변화가 더해져 막 조직을 형성합니다.
속발성의 경우, 혈액-망막 장벽의 파괴로 사이토카인이 방출되어 망막색소상피세포와 신경아교세포 등이 유리체 피질이나 내경계막 위에서 증식하여 막을 형성합니다.
혈관에 미치는 영향: 황반전막의 견인은 중심와무혈관대(FAZ) 면적을 감소시키고 표층모세혈관망(SCP)의 혈관면적밀도(VAD)를 유의하게 증가시킵니다2). FAZ 면적과 최대교정시력(BCVA) 사이에는 유의한 역상관 관계(r = −0.683)가 인정되며2), FAZ 형태는 시기능의 중요한 지표입니다.
NF2 관련 황반전막에서는 종양억제유전자의 기능 상실로 인해 뮐러세포 유사 신경아교 성분이 비정상적으로 증식하여 황반전막을 형성합니다. 면역염색에서는 GFAP 약양성, 네스틴 중등도 양성 패턴을 보입니다9).
7. 최신 연구와 향후 전망 (연구 단계 보고)
섹션 제목: “7. 최신 연구와 향후 전망 (연구 단계 보고)”ILM 박리 RCT (Ducloyer 2024)
섹션 제목: “ILM 박리 RCT (Ducloyer 2024)”Ducloyer 등(2024)의 213안을 대상으로 한 RCT(자연 박리 101안, 능동 ILM 박리 51안, 비박리 49안)에서 재발률이 능동 박리군 0% 대 비박리군 19.6%로 유의한 차이를 보였습니다18). 그러나 능동 ILM 박리군에서는 수술 후 BCVA 및 미세시야 회복이 다소 지연되었습니다. 재발 방지와 시기능 회복 간의 상충 관계에 대해 향후 장기 성적 검토가 필요합니다.
장기 수술 성적 (Elhusseiny 2020)
섹션 제목: “장기 수술 성적 (Elhusseiny 2020)”Elhusseiny 등(2020)의 49안, 평균 추적 111개월(약 9.3년) 보고에서 BCVA가 수술 전 0.56에서 1년 0.33, 3년 0.25, 10년 0.28로, 수술 후 3년까지 개선이 지속되고 10년까지 안정을 유지하는 것으로 나타났습니다17). 장기적인 시기능 유지 관점에서 조기 수술 중재가 지지됩니다.
OCTA를 통한 수술 전후 혈관 흐름 평가
섹션 제목: “OCTA를 통한 수술 전후 혈관 흐름 평가”Frisina 등(2023)은 특발성 황반전막안에서 FAZ 면적이 건강한 눈의 약 절반(0.11 mm² 대 0.24 mm²)으로 감소하고 SCP의 VAD가 유의하게 증가함을 OCTA로 확인했습니다2). 또한 FAZ 면적과 BCVA 사이에 유의한 역상관 관계(r = −0.683)를 보고하여 OCTA가 수술 전 예후 예측 도구로서 유망함을 보여주었습니다. logMAR 시력은 수술 후 0.4에서 0.1로 유의하게 개선되었습니다.
en face OCT를 이용한 ILM 결손의 수술 전 예측
섹션 제목: “en face OCT를 이용한 ILM 결손의 수술 전 예측”Sasajima와 Zako(2023)는 수술 전 en face OCT에서 22.7%의 증례에서 ILM 결손을 발견했으며, ILM 결손 가장자리에서 박리하는 기법(defect-edge technique)이 안전하고 효과적이라고 보고했습니다 1). 수술 전 결손 부위를 확인함으로써 수술 계획의 정확도 향상이 기대됩니다.
AI 진단의 전망
섹션 제목: “AI 진단의 전망”안저 사진이나 검안경 검사로부터의 AI 기반 ERM 진단이 평가 단계에 있습니다 12). 가격과 접근성 면에서 장점이 있다는 지적이 있으며, 선별 검사에의 활용이 기대됩니다. 그러나 진단 정확도 검증은 아직 진행 중이며, OCT가 ERM 진단의 사실상 표준으로서 여전히 중심적인 역할을 담당합니다.
황반상막 유발 망막내 신생혈관
섹션 제목: “황반상막 유발 망막내 신생혈관”Giachos 등(2021)은 당뇨병이 없는 환자에서 황반상막 견인이 유인이 되어 망막내 신생혈관이 형성된 증례를 보고했습니다 6). OCTA를 통해 혈관의 상세한 평가가 가능하며, 황반상막 수술 후 신생혈관이 퇴축되는 것도 확인되었습니다.
BBG 염색제의 안전성 프로토콜
섹션 제목: “BBG 염색제의 안전성 프로토콜”Venkatesh 등(2022)은 BBG와 내조명광의 조합으로 인한 황반 장애 증례를 보고하고 10), BBG 사용 시 노광 시간 제한과 적절한 광량 관리의 중요성을 제시했습니다. 안전한 염색 프로토콜의 확립이 향후 과제입니다.
PAMM 유사 합병증의 인식과 예방
섹션 제목: “PAMM 유사 합병증의 인식과 예방”Koiwa 등(2024)은 황반상막 유리체 수술 후 PAMM 유사 중심와주위 망막 허혈이 발생한 증례를 보고하고 5), 수술 전 혈류 평가와 수술 중 안압 관리가 합병증 예방에 중요하다고 지적했습니다.
8. 참고문헌
섹션 제목: “8. 참고문헌”- Sasajima H, Zako M. Internal limiting membrane peeling technique from internal limiting membrane defect edge. Clin Case Rep. 2023;11(5):e7279. doi:10.1002/ccr3.7279. PMID: 37155426.
- Frisina R, De Salvo G, Tozzi L, et al. Effects of physiological fluctuations on the estimation of vascular flow in eyes with idiopathic macular pucker. Eye (Lond). 2023;37(7):1470-1478. doi:10.1038/s41433-022-02158-4. PMID: 35794376.
- Mashayekhi A, Shields CL, Shields JA, et al. Malignant epiretinal membrane after proton beam radiation. J Ophthalmic Vis Res. 2023;18(4):445-451. doi:10.18502/jovr.v18i4.14558.
- Munoz-Solano J, Preziosa C, Staurenghi G, Pellegrini M. Resolution of epiretinal membrane after anti-VEGF and photodynamic therapy of retinal hemangioblastoma. Am J Ophthalmol Case Rep. 2024;33:101994. doi:10.1016/j.ajoc.2024.101994. PMID: 38303898. PMCID: PMC10831802.
- Koiwa C, Chi P, Yamamoto S, Nakao S. Extramacular paracentral acute middle maculopathy-like retinal ischemia after vitrectomy for epiretinal membrane. Am J Ophthalmol Case Rep. 2024;36:102221. doi:10.1016/j.ajoc.2024.102221. PMID: 39634097. PMCID: PMC11615521.
- Giachos I, et al. ERM-induced intraretinal neovascularization. Am J Ophthalmol Case Rep. 2021;23:101180.
- Alshahrani ST, Al Zoba A, Uwaydah Z. Epiretinal membrane separation following dexamethasone intravitreal implant in diabetic macular edema: a case report. Ophthalmol Ther. 2022;11(2):737-742. doi:10.1007/s40123-022-00472-4. PMID: 35362248.
- Rivera-Valdivia N, et al. RPE atrophy after ERM/ILM peeling. Rom J Ophthalmol. 2022;66(1):79-83.
- Kunikata H, Nishiguchi KM, Watanabe M, Nakazawa T. Surgical outcome and pathological findings in macular epiretinal membrane caused by neurofibromatosis type 2. Digit J Ophthalmol. 2022;28(1):12-16. doi:10.5693/djo.02.2021.06.001. PMID: 35573141.
- Venkatesh R, Yadav NK, Pereira A, et al. Phototoxic maculopathy following brilliant blue G-assisted internal limiting membrane peeling. J Curr Ophthalmol. 2022;34(2):267-270. doi:10.4103/joco.joco_46_22.
- Flaxel CJ, Adelman RA, Bailey ST, et al. Idiopathic Epiretinal Membrane and Vitreomacular Traction Preferred Practice Pattern. Ophthalmology. 2020;127(2):P145-P183.
- Bailey ST, Vemulakonda GA, et al. Idiopathic Epiretinal Membrane and Vitreomacular Traction Preferred Practice Pattern. Ophthalmology. 2025;132(2):P203-P237.
- Xiao W, Chen X, Yan W, et al. Prevalence and risk factors of epiretinal membranes: a systematic review and meta-analysis of population-based studies. BMJ Open. 2017;7:e014644. doi:10.1136/bmjopen-2016-014644. PMID: 28951399.
- Fraser-Bell S, Guzowski M, Rochtchina E, et al. Five-year cumulative incidence and progression of epiretinal membranes: the Blue Mountains Eye Study. Ophthalmology. 2003;110(1):34-40. PMID: 12511343.
- Meuer SM, Myers CE, Klein BE, et al. The epidemiology of vitreoretinal interface abnormalities as detected by spectral-domain optical coherence tomography: the Beaver Dam Eye Study. Ophthalmology. 2015;122(4):787-795.
- Ng CH, Cheung N, Wang JJ, et al. Prevalence and risk factors for epiretinal membranes in a multi-ethnic United States population. Ophthalmology. 2011;118(4):694-699. doi:10.1016/j.ophtha.2010.08.009.
- Elhusseiny AM, Smiddy WE, Flynn HW Jr, et al. Long-term visual and anatomical outcomes after epiretinal membrane peeling. Retina. 2020;40(10):1952-1959. doi:10.1097/IAE.0000000000002705. PMID: 31764264.
- Ducloyer JB, et al. Pros and cons of internal limiting membrane peeling during epiretinal membrane surgery: a randomised clinical trial with microperimetry (PEELING). Br J Ophthalmol. 2024. doi:10.1136/bjo-2023-324990. PMID: 38901960.
- Chang WC, Lin C, Lee CH, et al. Vitrectomy with or without internal limiting membrane peeling for idiopathic epiretinal membrane: a meta-analysis. PLoS One. 2017;12(6):e0179105. doi:10.1371/journal.pone.0179105. PMID: 28622372. PMCID: PMC5476241.
