เยื่อเหนือจอตา (ERM ) เป็นเนื้อเยื่อที่มีการเพิ่มจำนวนของเซลล์เส้นใยที่ก่อตัวบนเยื่อชั้นในสุด (ILM ) ของจอตา และเป็นสาเหตุสำคัญของภาพบิดเบี้ยว และการมองเห็น ลดลง
แบ่งออกเป็น 2 ประเภทหลัก: ไม่ทราบสาเหตุ (หลังการหลุดของวุ้นตา ส่วนหลัง พบมากในอายุ >50 ปี) และทุติยภูมิ (เรียกอีกอย่างว่า รอยย่นจอตา)
ประเมินความรุนแรงโดยใช้การจำแนกของ Gass (Grade 0-2) Grade 0 คือ เซลโลเฟนแมคคูโลพาธี Grade 1 มักมีสายตา ≥0.5
ความชุกอยู่ระหว่าง 2.2% ถึง 34.1% ขึ้นอยู่กับวิธีการตรวจและประชากรที่ศึกษา พบทั้งสองข้าง 20-35% ในทางธรรมชาติ 29% ลุกลาม 26% หายไป และ 39% คงที่ใน 5 ปี 14)
OCT เป็นเครื่องมือวินิจฉัยที่สำคัญที่สุด ประเมินโครงสร้างเยื่อบางสะท้อนแสงสูง การหายไปของรอยบุ๋มจอตา และความสมบูรณ์ของ ellipsoid zoneการผ่าตัด (ตัดวุ้นตา + ลอกเยื่อเหนือจอตา ± ลอก ILM ) ช่วยให้สายตาดีขึ้น ≥2 แถวในประมาณ 80% ของกรณี 12) การลอก ILM ลดอัตราการกลับเป็นซ้ำ (0% เทียบกับ 16-20%) แต่อาจทำให้การฟื้นฟูสายตาช้าลงเล็กน้อย 18)
ภาวะแทรกซ้อน ได้แก่ ต้อกระจก ที่ลุกลาม (เกือบทุกกรณี) จอตาฉีกขาด (1%) รูจอตาจากการรักษา (2.1%) จอตาขาดเลือดแบบ PAMM และการฝ่อของ RPE การให้ข้อมูลและขอความยินยอมก่อนผ่าตัดมีความสำคัญ 12)
เยื่อเหนือจอตา (ERM ) คือเนื้อเยื่อที่มีการเจริญเกินของเซลล์เส้นใยที่ก่อตัวบนเยื่อลิมิตติ้งชั้นใน (ILM ) ของจอตา เรียกอีกอย่างว่า macular pucker, เซลโลเฟนแมคคูโลพาธี, พังผืดก่อนจอตา, หรือกลุ่มอาการรอยต่อวุ้นตา -จอตา 11) ERM อาจทำให้เกิดรอยย่นของจอตา จอตาบวมน้ำ จอตาลอกจากการดึงรั้ง เป็นต้น
ERM แบ่งเป็น ไม่ทราบสาเหตุ และ ทุติยภูมิ ชนิดทุติยภูมิเรียกอีกอย่างว่า macular pucker 11)
ERM ไม่ทราบสาเหตุวุ้นตา ส่วนหลัง (PVD ) และพบบ่อยในอายุ >50 ปี ERM ทุติยภูมิม่านตาอักเสบ จอตาจากเบาหวาน จอตาอักเสบชนิดรงควัตถุ เป็นต้น
ความชุกแตกต่างกันไปตามวิธีการตรวจและประชากรที่ศึกษา โดยมีรายงานที่หลากหลาย ตารางต่อไปนี้สรุปความชุกจากการศึกษาต่างๆ
การศึกษา ประชากร ความชุก วิธีการตรวจ การศึกษาดวงตาปักกิ่ง เขตเมืองของจีน 2.2% ภาพถ่ายจอตา การศึกษาดวงตาหานตาน เขตชนบทของจีน 3.4% ภาพถ่ายจอตา การศึกษาดวงตาบลูเมาน์เทนส์ ออสเตรเลีย 7.0% ภาพถ่ายจอตา กลุ่มเมลเบิร์น ออสเตรเลีย 8.9% ภาพถ่ายจอตา การศึกษา Los Angeles Latino Eye Study เชื้อสายฮิสแปนิก 18.8% ภาพถ่ายจอตา MESA หลายเชื้อชาติในสหรัฐฯ 28.9% ภาพถ่ายจอตา การศึกษา Beaver Dam Eye Study (20 ปี) คนผิวขาวในสหรัฐฯ (อายุเฉลี่ย 74.1 ปี) 34.1% SD-OCT 15)
ความชุกของเซลโลเฟนแมคูลา (ERM ที่ไม่มีอาการ) รายงานอยู่ที่ 1.8–25.1% และ ERM ที่มีอาการ (พังผืดก่อนจุดรับภาพ) อยู่ที่ 0.7–3.9%12) ในสหรัฐฯ ประมาณการว่ามีผู้ป่วยประมาณ 30 ล้านคน12) การเกิดสองข้างพบได้ 20–35%11) มีรายงานความแตกต่างทางเชื้อชาติด้วย ในการศึกษา MESA พบในคนจีน 39.0% ฮิสแปนิก 29.3% คนผิวขาว 27.5% และคนผิวดำ 26.2%16)
ภายใน 5 ปี ERM 29% แย่ลง 26% ดีขึ้น และ 39% คงที่ (การศึกษา Blue Mountains Eye Study)14) การดำเนินของเซลโลเฟนแมคูลามีเพียง 20% ใน 5 ปี การแยกตัวของ ERM เองเมื่อมีภาวะวุ้นตา หลุด (PVD ) เกิดขึ้น 1.5% (16 ใน 1091 ตา) และเมื่อไม่มี PVD เกิดขึ้น 13.6% (21 ใน 157 ตา ติดตามเฉลี่ย 33 เดือน)12) การเลื่อนการผ่าตัดจนกว่าจะมีอาการไม่ทำให้พยากรณ์โรคแย่ลงเมื่อเทียบกับการผ่าตัดทันที12) ในผู้ป่วยอายุน้อยที่ไม่มี PVD การแยกตัวเองเกิดขึ้นได้น้อย ดังนั้นควรติดตามอย่างใกล้ชิด
ในโรคนิวโรไฟโบรมาโตซิสชนิดที่ 2 (NF 2) ความชุกของเยื่อเหนือจอประสาทตา สูงถึง 80% 9) ความชุกของการดึงรั้งวุ้นตา -จอประสาทตา (VMT ) อยู่ที่ 0.4–2.0% (อายุ ≥63 ปี) และ ERM และ VMT มักเกิดร่วมกัน 12)
การจำแนกของ Gass ถูกใช้อย่างแพร่หลายในการจำแนกความรุนแรงทางคลินิก
ระดับ ลักษณะที่พบ ค่าประมาณการมองเห็น ระดับ 0 เยื่อบางใส (โรคจอประสาทตา แบบกระดาษแก้ว) ไม่มีการเสียรูปของชั้นในจอตา ดี ระดับ 1 รอยย่นของจอตาจากการหดตัวของเยื่อ หลอดเลือดเล็กในจอตาไม่ชัดเจน โดยปกติ 0.5 หรือมากกว่า ระดับ 2 เยื่อหนาสีเทาไม่โปร่งใส รอยย่นของจอประสาทตา ชัดเจน ลดลง
Q
เยื่อเหนือจอประสาทตาจำเป็นต้องผ่าตัดเสมอหรือไม่?
A
ไม่ใช่ทุกกรณีของเยื่อเหนือจอประสาทตา ที่ต้องผ่าตัด หากไม่มีอาการ อาการเล็กน้อย หรือการมองเห็น ดี สามารถเลือกสังเกตอาการได้ ตามรายงาน ในระยะเวลา 5 ปี พบว่า 29% แย่ลง 26% ดีขึ้น และ 39% คงที่ 14) และการเลื่อนการผ่าตัดจนกว่าอาการจะปรากฏไม่ทำให้ผลการรักษาแย่ลง 12) โดยทั่วไปจะพิจารณาผ่าตัดเมื่อค่าสายตาที่แก้ไขแล้วเท่ากับ 0.7 หรือน้อยกว่า ร่วมกับภาพบิดเบี้ยว รุนแรง หรือเมื่อการมองเห็น ลดลงค่อนข้างเฉียบพลันและเชื่อว่าเกิดจากเยื่อเหนือจอประสาทตา การตัดสินใจขั้นสุดท้ายขึ้นอยู่กับอาการที่ผู้ป่วยรู้สึก
เยื่อเหนือจอประสาทตา มัก ไม่มีอาการ และไม่ใช่เรื่องแปลกที่จะพบโดยบังเอิญระหว่างการตรวจสุขภาพหรือการติดตามโรคอื่นๆ เมื่อมีอาการ อาจแสดงอาการดังต่อไปนี้
ภาพบิดเบี้ยว (ความโค้ง)การมองเห็น ลดลงเห็นวัตถุเล็กลง (micropsia) : วัตถุดูเล็กกว่าปกติ เกิดจากจอประสาทตา ผิดรูปเนื่องจากการดึงรั้งของเยื่อเห็นวัตถุใหญ่ขึ้น (macropsia) : วัตถุอาจดูใหญ่กว่าความเป็นจริงเห็นภาพซ้อน ในตาเดียวเห็นภาพซ้อน ด้วยตาข้างเดียวอ่านหนังสือลำบาก ขับรถลำบาก และมองเห็นด้วยสองตาลำบาก : ข้อร้องเรียนที่พบบ่อยซึ่งส่งผลต่อชีวิตประจำวัน 12)
ตาราง Amsler เป็นเครื่องมือที่มีประโยชน์สำหรับการติดตามภาพบิดเบี้ยว ด้วยตนเอง ผู้ป่วยใช้เพื่อตรวจสอบความก้าวหน้าของอาการ 12)
ด้วยกล้องจุลทรรศน์ชนิดกรีด สามารถสังเกตความมันวาวของผิวจอประสาทตา รอยย่นของจอประสาทตา และการคดเคี้ยวของหลอดเลือด โดยการขยายความกว้างของแสงกรีดและสังเกตจอประสาทตา ส่วนกลาง สามารถประเมินความหนาของเยื่อและพื้นที่การกระจายร่วมกับภาพ OCT ในระยะแรก จะเห็นการสะท้อนคล้ายแพรน้ำ ซึ่งเป็นประกายแวววาวที่มีลักษณะเฉพาะ เมื่อโรคดำเนินไป อาจเกิดจอประสาทตา บวมน้ำหรือรอยหลุมจอประสาทตา เทียม
เยื่อหนา สีขาวทึบแสง มักทำให้เกิดอาการและทำให้จอประสาทตา เคลื่อน 12) อาจเกิดการหายไปของรอยบุ๋มจอประสาทตา ปกติ การเปลี่ยนแปลงแบบถุงน้ำของจอประสาทตา รอยหลุมจอประสาทตา แบบชั้น และรอยหลุมจอประสาทตา ทะลุตลอดความหนา
การดึงรั้งของวุ้นตา บนหัวประสาทตา (Vitreopapillary traction) : การยึดเกาะของวุ้นตา รอบหัวประสาทตาอาจเกิดร่วมกับ ERM ต้องระวังเพราะอาจวินิจฉัยผิดเป็น papilledema (ขั้วประสาทตาคั่ง)12)
การตรวจ Optical coherence tomography angiography (OCTA ) แสดงการเปลี่ยนแปลงรูปร่างของบริเวณหลอดเลือดฝอยรอบรอยบุ๋มจอตา (FA Z) พื้นที่ FA Z ในตาที่มีเยื่อเหนือจอตาเท่ากับ 0.11 มม.² ซึ่งแคบลงอย่างมีนัยสำคัญเมื่อเทียบกับ 0.24 มม.² ในตาปกติ2)
ปัจจัยที่เกี่ยวข้องที่สำคัญที่สุดของเยื่อเหนือจอตาคือภาวะวุ้นตา หลุดจากจอตาส่วนหลัง (PVD ) สมมติฐานดั้งเดิมเสนอว่าส่วนคอร์เทกซ์ของวุ้นตา ที่เหลืออยู่หลัง PVD ทำให้เกิดการฉีกขาดของเยื่อลิมิตติงชั้นใน (ILM ) ทำให้เซลล์เกลียและเซลล์เยื่อบุผิวรงควัตถุจอตา (RPE ) เคลื่อนย้ายเข้าไปในช่องวุ้นตา แยกความแตกต่างและเพิ่มจำนวนเป็นเซลล์คล้ายไฟโบรบลาสต์ ก่อตัวเป็นเยื่อเหนือจอตา11)
สมมติฐานใหม่ที่กำลังได้รับการสนับสนุนเมื่อเร็วๆ นี้ระบุว่าการฉีกขาดของ ILM ไม่จำเป็น เชื่อว่าเซลล์ในคอร์เทกซ์วุ้นตา ที่เหลืออยู่บน ILM ถูกกระตุ้นให้กลายเป็นไมโอไฟโบรบลาสต์ ทำให้เกิดการสร้างและการหดรั้งของเยื่อ12)
แม้ไม่มี PVD ก็ยังมีโพรงที่กลายเป็นของเหลวภายในเจลวุ้นตา ส่วนหลัง (ถุงก่อนคอร์เทกซ์วุ้นตา ส่วนหลัง) ผนังด้านหลังของถุงนี้คือคอร์เทกซ์วุ้นตา ที่บางและยืดหยุ่น และเชื่อว่าการเปลี่ยนแปลง เช่น การเพิ่มจำนวนเซลล์บนคอร์เทกซ์วุ้นตา ส่วนหลังที่อยู่ด้านหน้าต่อรอยบุ๋มจอตา นี้ ทำให้เกิดเยื่อเหนือจอตา
มีกรณีที่วุ้นตา ส่วนหลังยังคงติดอยู่กับรอยบุ๋มจอตา และผนังด้านหลังของถุงดึงรั้งจอตา และกรณีที่หลัง PVD สมบูรณ์ ผนังด้านหลังของถุงยังคงอยู่ด้านจอตาและทำให้รอยบุ๋มจอตา บิดเบี้ยว การเพิ่มจำนวนเซลล์บนผนังด้านหลังของถุงวุ้นตา สามารถก่อตัวเป็นเยื่อเหนือจอตา ซึ่งมักพบในกรณีทุติยภูมิหรือในคนหนุ่มสาว การหลุดออกเองอาจเกิดขึ้นเมื่อเกิด PVD
ควรสังเกตว่าใน 20.1% ของกรณีผ่าตัด วุ้นตา ส่วนหลังยังคงติดอยู่ และการมีวงแหวนไวส์ (Weiss ring) ไม่ได้หมายถึงการแยกตัวสมบูรณ์ของวุ้นตา ส่วนหลังเสมอไป12)
ในเยื่อเหนือจอตาที่เกี่ยวข้องกับ NF 2 การย้อมอิมมูโนแสดง GFA P บวกอ่อนและ nestin บวกปานกลาง บ่งชี้ว่าส่วนประกอบส่วนใหญ่มาจากเซลล์มุลเลอร์9)
ปัจจัยเสี่ยงหลักแสดงดังต่อไปนี้:
อายุ : เพิ่มขึ้นอย่างรวดเร็วหลังอายุ 50 ปี และความชุกเพิ่มขึ้นอีกหลังอายุ 75 ปีภาวะวุ้นตา หลุดจากจอตาส่วนหลัง (PVD ) : ตัวกระตุ้นที่ใหญ่ที่สุดของเยื่อเหนือจอตาไม่ทราบสาเหตุเพศหญิง : ได้รับการยืนยันว่าเป็นปัจจัยเสี่ยงที่มีนัยสำคัญในการทบทวนอย่างเป็นระบบ (มากกว่า 49,000 ราย)13) จอตาฉีกขาดและจอตาหลุดลอก : สาเหตุหลักของเยื่อเหนือจอตาทุติยภูมิประวัติการผ่าตัดภายในลูกตา : การผ่าตัดต้อกระจก เป็นปัจจัยเสี่ยงที่ได้รับการยืนยันสำหรับ ERM ทุติยภูมิ 12) .เบาหวานและไขมันในเลือดสูง : ปัจจัยเสี่ยงของจอประสาทตา เสื่อมแบบเซลโลเฟน (ข้อมูล MESA) 12) .การอุดตันของหลอดเลือดจอตาและม่านตาอักเสบ : เกิดขึ้นเป็นปฏิกิริยาการเจริญเติบโตหลังการอักเสบจอประสาทตา เสื่อมชนิดเม็ดสีERM ทุติยภูมิการฉายรังสีรักษา : มีรายงาน ERM ทุติยภูมิหลังการฉายรังสีโปรตอน 3) .
ERM ไม่ทราบสาเหตุส่วนใหญ่เกี่ยวข้องกับอายุ และยากที่จะป้องกันโดยตรงด้วยการปรับเปลี่ยนวิถีชีวิต ควรตรวจตาเป็นประจำเพื่อค้นหาโรคตั้งแต่ระยะแรก หากสังเกตเห็นภาพบิดเบี้ยว หรือสายตาลดลง ควรรีบไปพบจักษุแพทย์โดยเร็ว
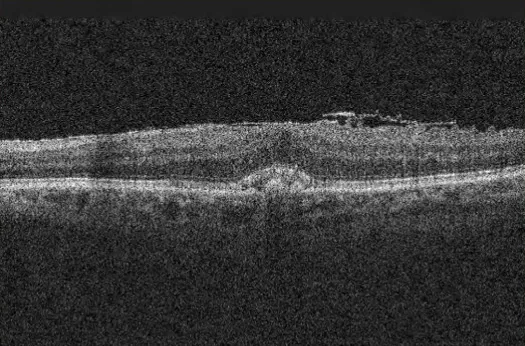
ภาพ OCT ของเยื่อเหนือจอตา Wikimedia Commons. File:EpiretinalMembrane_OCT.png. License: CC BY-SA.
ภาพถ่ายด้วยเครื่องเอกซเรย์การเชื่อมโยงกันด้วยแสง (OCT ) ของเยื่อเหนือจอตาในชายอายุ 89 ปี สอดคล้องกับเยื่อเหนือจอตาที่กล่าวถึงในหัวข้อ “4. การวินิจฉัยและวิธีการตรวจ”
สรุปบทบาทของการตรวจแต่ละอย่าง
การตรวจ วัตถุประสงค์หลัก ลักษณะเฉพาะ OCT การแสดงภาพเยื่อ การประเมินความหนา การยืนยันการดึงรั้งจอตา สำคัญที่สุดและไม่รุกราน OCTA การประเมินการไหลของหลอดเลือด พื้นที่ FA Z และการตรวจหาหลอดเลือดใหม่ การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน การประเมินการรั่วซึมของหลอดเลือดและการขาดเลือด การแยกโรคที่เกิดร่วม การตรวจอวัยวะภายในตา การยืนยันความมันวาวผิวและรอยย่น การคัดกรอง
เครื่องตรวจการเชื่อมโยงกันเชิงแสง (OCT ) เป็นหัวใจสำคัญของการวินิจฉัย เยื่อเหนือจอตา (ERM ) ใน OCT จะปรากฏเป็นชั้นสะท้อนแสงสูงบนพื้นผิวด้านใน มักยึดติดด้วยขา (pegs) จากพื้นผิวจอตาชั้นใน และมีลักษณะเป็นคลื่นในภาพตัดขวาง พบ การหายไปของรอยบุ๋มจอตา การโป่งของชั้นนอกจอตา และการเปลี่ยนแปลงแบบถุงน้ำ การใช้ OCT ยังสามารถประเมินการดึงรั้งจอตาจากวุ้นตา หรือเยื่อ อาการบวมจอตา การเปลี่ยนแปลงแบบถุงน้ำ การมีจอตาลอก และสถานะของ โซนรูปไข่ (EZ ) ได้อีกด้วย OCT แบบ en face มีประโยชน์ในการทำนายความบกพร่องของเยื่อจำกัดชั้นใน (ILM ) ก่อนผ่าตัด และพบความบกพร่องของ ILM ก่อนผ่าตัดใน 22.7% ของกรณี1) .
การเกิดร่วมของ ERM +VMT พบใน 57% ของตาที่มี ERM และพบ ERM ใน 65% ของตาที่มี VMT ตามรายงาน12) .
OCTA (การตรวจหลอดเลือดด้วยการเชื่อมโยงกันเชิงแสง)2) และยังมีประโยชน์ในการตรวจหาหลอดเลือดใหม่ในจอตาที่เกิดจากเยื่อเหนือจอตา6) .
การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน (FA ) : ใน ERM ระยะแรก FA จะแสดงภาพที่ค่อนข้างปกติ เมื่อเยื่อหดตัวมากขึ้น จะสังเกตเห็นความคดเคี้ยวของหลอดเลือดใกล้ศูนย์กลางการดึงรั้ง และการเหยียดตรงของหลอดเลือดบริเวณรอบนอก นอกจากนี้ยังสังเกตรูปแบบการรั่วซึมจากเส้นเลือดฝอยภายใต้การดึงรั้ง หากมีการสะสมของสีในโพรงถุงน้ำ จำเป็นต้องแยกจาก CME ในตาที่มีเลนส์แก้วตาเทียม (CME มีรูปแบบกลีบดอกไม้ร่วมกับการเรืองแสงเกินของจานประสาทตา ) 12) FA /OCTA ยังมีประโยชน์ในการตรวจหาภาวะหลอดเลือดจอประสาทตา อุดตันร่วม เบาหวานขึ้นจอประสาทตา ภาวะหลอดเลือดฝอยจอประสาทตา ขยาย และเส้นเลือดใหม่ในคอรอยด์ 12)
ความสมบูรณ์ของ EZ /IZ และการพยากรณ์โรค : หากบริเวณ ellipsoid (EZ ) และบริเวณ interdigitation (IZ, เส้นปลายของส่วนนอกเซลล์รูปกรวย ) อยู่ในสภาพสมบูรณ์ในการตรวจ OCT ก่อนผ่าตัด การมองเห็น หลังผ่าตัดมักจะดีกว่า 12) จอประสาทตา ชั้นนอก EZ และความยาวส่วนนอกของเซลล์รับแสง สามารถดีขึ้นและกลับมาเป็นปกติหลังผ่าตัด (แต่ละพารามิเตอร์สัมพันธ์กับการมองเห็น ที่ดีขึ้น) ในการศึกษา 101 ตาโดยใช้ OCT แบบโดเมนเวลา ความเสียหายของชั้นเซลล์รับแสง ถูกรายงานว่าเป็นปัจจัยทำนายการมองเห็น ที่ไม่ดีหลังผ่าตัด 12)
เยื่อเหนือจอประสาทตา ชนิดพิเศษคือ รอยหลุมจอประสาทตา เทียม การหดตัวของเยื่อเหนือจอประสาทตา ทำให้รอยบุ๋มฟอเวียกลายเป็นรูปทรงกระบอก คล้ายกับรอยหลุมจอประสาทตา
จุดแยกทางคลินิก: ในรอยหลุมจอประสาทตา เทียม การมองเห็น มักจะยังคงค่อนข้างดี ในการตรวจด้วยกล้องจุลทรรศน์กรีด สัญญาณ Watzke-Allen มีประโยชน์ในการแยกความแตกต่าง ในรอยหลุมจอประสาทตา ผู้ป่วยจะรู้สึกถึงการหดตัวของแสงกรีด (บวก) ในขณะที่รอยหลุมจอประสาทตา เทียม แสงกรีดจะถูกรับรู้เป็นเส้นที่มีความกว้างสม่ำเสมอ (ลบ) การใช้ OCT ทำให้การแยกความแตกต่างทั้งสองทำได้ง่าย
การมีความบกพร่องทางการมองเห็น และจอประสาทตา หนาตัว เป็นข้อกำหนดเบื้องต้นสำหรับการผ่าตัด แม้ว่าการมองเห็น จะดี แต่ถ้าจอประสาทตา หนาตัวอย่างมีนัยสำคัญร่วมกับภาพบิดเบี้ยว รุนแรง หรือมีรอยหลุมจอประสาทตา ทะลุทั้งชั้นร่วมด้วย ก็เป็นข้อบ่งชี้ในการผ่าตัด
การมองเห็น ลดลงค่อนข้างเฉียบพลันการมองเห็น ที่คิดว่าเกิดจากเยื่อเหนือจอประสาทตา เมื่อเทียบกับระดับต้อกระจก ก็เป็นข้อบ่งชี้ในการผ่าตัด ควรสอบถามความเร็วของการดำเนินของอาการ ผลกระทบต่ออาชีพและการใช้ชีวิตของผู้ป่วย (อ่านหนังสือลำบาก ขับรถลำบาก) อย่างละเอียด และ ในที่สุดการตัดสินใจขึ้นอยู่กับอาการที่ผู้ป่วยรู้สึกร่วมด้วย การผ่าตัดเป็นแบบเลือก (ไม่เร่งด่วน) 12)
Q
การตรวจที่สำคัญที่สุดในการวินิจฉัยเยื่อเหนือจอประสาทตาคืออะไร?
A
OCT (เครื่องตรวจชั้นจอประสาทตา ด้วยแสง) คือการตรวจที่สำคัญที่สุด สามารถแสดงโครงสร้างเยื่อสะท้อนแสงสูงบนพื้นผิวจอประสาทตา และความหนาของจอประสาทตา ได้โดยไม่ต้องผ่าตัด ใช้ในการวินิจฉัย การตัดสินใจผ่าตัด และการติดตามผลหลังผ่าตัด นอกจากนี้ยังสามารถประเมินการหายไปของรอยบุ๋มฟอเวีย สถานะของบริเวณ ellipsoid และการเปลี่ยนแปลงแบบถุงน้ำในจอประสาทตา ความสมบูรณ์ของ EZ /IZ ก่อนผ่าตัดยังมีประโยชน์ในการพยากรณ์โรคหลังผ่าตัด 12)
การผ่าตัดมาตรฐานสำหรับรักษาเยื่อเหนือจอประสาทตา คือ การตัดน้ำวุ้นตา ผ่านพาร์สพลานา (PPV ) + การลอกเยื่อเหนือจอประสาทตา + การลอกเยื่อจำกัดชั้นใน (ILM ) การผ่าตัดน้ำวุ้นตา แบบแผลเล็ก (MIVS) ด้วยขนาด 23G, 25G และ 27G เป็นมาตรฐาน ช่วยให้บาดเจ็บน้อยและฟื้นตัวเร็ว
การลอกเยื่อเหนือจอประสาทตา
วัตถุประสงค์ : กำจัดเยื่อเจริญที่ทำให้เกิดแรงดึง และฟื้นฟูสัณฐานของจอประสาทตา
เทคนิค : ใช้คีมจับน้ำวุ้นตา (ไมโครฟอร์เซปส์) จับขอบเยื่อแล้วลอกออกอย่างนุ่มนวลออกจากรอยบุ๋มจอตา เพื่อหลีกเลี่ยงการเกิดรูที่จุดรับภาพ ในกรณีที่ไม่มีภาวะน้ำวุ้นตา หลุดจากจอประสาทตา ส่วนหลัง การทำให้น้ำวุ้นตา หลุดเทียมอาจทำให้เยื่อหลุดออกพร้อมกัน
การลอกเยื่อจำกัดชั้นใน (ILM)
วัตถุประสงค์ : ป้องกันการกลับเป็นซ้ำของเยื่อเหนือจอประสาทตา และส่งเสริมการยืดตัวของจอประสาทตา ที่สมบูรณ์ยิ่งขึ้น
การจัดการขอบ ILM : แม้ว่าจะตัดเฉพาะเยื่อเหนือจอประสาทตา มักเกิดรอยฉีกขาดใน ILM ทำการลอกเพิ่มเติมเพื่อให้แน่ใจว่าขอบระหว่างบริเวณที่ลอก ILM และไม่ได้ลอกไม่ผ่านจอประสาทตา ส่วนกลาง OCT แบบเอนเฟซก่อนผ่าตัดพบข้อบกพร่องของ ILM ใน 22.7% ของกรณี 1) และเทคนิคการลอกจากขอบข้อบกพร่อง (defect-edge technique) มีประโยชน์ 1)
การใช้สีย้อม : สำหรับการย้อมสี ILM /ERM มีการใช้ brilliant blue G (BBG, TISSUEB LUE®) ซึ่งได้รับการรับรองจาก FDA (2019) อย่างแพร่หลาย ICG, trypan blue และ triamcinolone ก็ใช้แบบนอกข้อบ่งชี้เช่นกัน แม้ว่าความเข้มข้นต่ำจะถือว่าปลอดภัย แต่การลดระยะเวลาในการสัมผัสแสงเป็นสิ่งสำคัญ และยังคงมีการถกเถียงกันอยู่ 12) การโกนน้ำวุ้นตา ส่วนปลาย (โดยเฉพาะใกล้แคนนูลา) สามารถลดความเสี่ยงของการฉีกขาดของจอประสาทตา จากการรักษา
อัตราการมองเห็น ดีขึ้น : ประมาณ 80% ของกรณีมีการมองเห็น ดีขึ้น 2 แถวหรือมากกว่าบนตารางสนีลเลน 12) (73% ในรายงานก่อนหน้า 11) ) 10-20% ไม่เปลี่ยนแปลงหรือแย่ลงระดับการมองเห็น ดีขึ้น : logARM ดีขึ้นจาก 0.4 เป็น 0.1 (เปรียบเทียบก่อนและหลังผ่าตัด) 2) อาการภาพบิดเบือนดีขึ้น : ก่อนผ่าตัด 56% มีอาการภาพบิดเบือน หลังผ่าตัดลดลงเหลือ 13% 11) คะแนน VFQ-25 : ดีขึ้นอย่างมีนัยสำคัญที่ 6 และ 24 เดือนหลังผ่าตัด 12) ผลระยะยาว (Elhusseiny 2020, 49 ตา, ติดตามเฉลี่ย 111 เดือน): BCVA 0.56 (20/72) ก่อนผ่าตัด → 1 ปี 0.33 (20/42) → 3 ปี 0.25 (20/35) → 10 ปี 0.28 (20/38) โดยการมองเห็น ดีขึ้นต่อเนื่องถึง 3 ปีและคงที่ถึง 10 ปี 17) แนวทางการมองเห็น ดีขึ้น : ค่อยๆ ดีขึ้นในช่วง 3-6 เดือนหลังผ่าตัด และอาจดีขึ้นอย่างช้าๆ ต่อไปถึง 12 เดือน อาจยังมีความหนาของจอประสาทตา และความผิดปกติทางการมองเห็น ที่เกี่ยวข้องหลงเหลืออยู่ที่ 1 ปีหลังผ่าตัด เนื่องจากการมองเห็น หลังผ่าตัดสัมพันธ์อย่างดีกับการมองเห็น ก่อนผ่าตัด จึงเป็นสิ่งสำคัญที่จะผ่าตัดก่อนที่การมองเห็น จะลดลงมากเกินไป
การลอก ILM มีประสิทธิภาพในการป้องกันการกลับเป็นซ้ำของ ERM และเป็นส่วนหนึ่งของการผ่าตัดมาตรฐานในปัจจุบัน 12) .
ผลการป้องกันการกลับเป็นซ้ำ : หากไม่ลอก ILM อัตราการกลับเป็นซ้ำของ ERM อยู่ที่ 8.6–21% หากลอก ILM อยู่ที่ 0–2.6% 12) .RCT ของ Ducloyer 2024 (213 ตา) : เปรียบเทียบ 101 ตาที่มีการหลุดเอง 51 ตาที่ลอก ILM แบบ active และ 49 ตาที่ไม่ลอก อัตราการกลับเป็นซ้ำ 0% ในกลุ่ม active เทียบกับ 19.6% ในกลุ่มไม่ลอก แตกต่างอย่างมีนัยสำคัญ อย่างไรก็ตาม การฟื้นตัวของ BCVA และ microperimetry ช้ากว่าเล็กน้อยในกลุ่มลอก ILM แบบ active 18) .การวิเคราะห์อภิมานปี 2017 : ไม่มีความแตกต่างชัดเจนในการพัฒนาการมองเห็น ขณะที่กลุ่มลอก ILM เหนือกว่าในการยับยั้งการกลับเป็นซ้ำของ ERM 19) .สรุป : การลอก ILM มีประสิทธิภาพในการป้องกันการกลับเป็นซ้ำ แต่ความเหนือกว่าด้านการมองเห็น ยังไม่ชัดเจน อาจเกิดการสูญเสียจอประสาทตา ชั้นใน (DONF L) แต่ผลกระทบต่อการทำงานยังไม่ทราบแน่ชัด
VMT (การดึงรั้งของวุ้นตา -จอประสาทตา ส่วนกลาง) สัมพันธ์อย่างใกล้ชิดกับ ERM และมักพบร่วมกัน
VMT ≤1500 ไมครอนการมองเห็น คงที่ การสังเกตเป็นทางเลือก 12) .VMT กว้าง (>1500 ไมครอน)จอประสาทตา หลุดลอก หรือการมองเห็น ไม่ดี: ไม่คาดว่าจะดีขึ้นเอง และควรพิจารณาผ่าตัดวุ้นตา 12) .
การสลายวุ้นตา ด้วยแก๊ส (Pneumatic vitreolysis) : การฉีด C3F8 0.3 มล. เข้าในวุ้นตา แสดงอัตราการคลาย VMT 85.7% ในบางการศึกษา แต่ใน RCT ของ DRCR Retina Network อุบัติการณ์ของจอประสาทตาฉีกขาด และจอประสาทตา หลุดลอกสูงกว่าที่คาดไว้ ทำให้ต้องหยุดการทดลองก่อนกำหนดเนื่องจากข้อกังวลด้านความปลอดภัย 12) ปัจจุบันหลักฐานยังไม่เพียงพอ จำเป็นต้องประเมินความเสี่ยง-ประโยชน์เป็นรายบุคคล
Ocriplasmin : โปรตีเอสลูกผสม ได้รับการอนุมัติจาก FDA ในปี 2012 สำหรับ VMA/VMT ที่มีอาการ การทดลองระยะที่ 3 พบว่าอัตราการคลาย VMA 27% เทียบกับ 10% ในกลุ่มยาหลอก (P<0.001) 12) ผลจำกัดใน VMT ที่มี ERM ร่วม (อัตราการคลาย VMA 8.7% เทียบกับ 1.5% ในกลุ่มยาหลอก) และไม่ได้ผลใน ERM เพียงอย่างเดียว 12) ผลข้างเคียง ได้แก่ ภาพลอยในวุ้นตา ภาพแสงวาบ ปวดตา และตามัว (ประมาณ 10% ในสัปดาห์แรก) ผลข้างเคียงร้ายแรง เช่น การมองเห็น ลดลงเฉียบพลันรุนแรง ความผิดปกติของ ERG และความผิดปกติของการมองเห็นสี พบได้น้อย แต่ส่วนใหญ่สามารถกลับคืนได้ 12) .
ตรวจในวันแรกหลังผ่าตัด และนัดติดตามใน 1–2 สัปดาห์ (ประเมินความดันลูกตา ส่วนหน้าของลูกตา จอประสาทตา ส่วนกลางและส่วนปลาย) 12) .
หากภาพซ้อน หรือการมองเห็น สองตาลำบากยังคงอยู่: พิจารณาส่งต่อผู้เชี่ยวชาญด้านตาเหล่ หรือนักทัศนมาตรศาสตร์ 12) .
การรักษามาตรฐานคือการผ่าตัด แต่มีรายงานการลอกตัวเองหรือการลอกโดยการกระตุ้นโดยไม่ผ่าตัดดังต่อไปนี้ (ทั้งหมดเป็นรายงานผู้ป่วย)
การปลูกถ่ายเดกซาเมทาโซนในน้ำวุ้นตา (DEX implant) : มีรายงานผู้ป่วยที่พบการลอกตัวของเยื่อเหนือจอประสาทตา เองหลังการฉีดยาในน้ำวุ้นตา 7) .การลอกตัวเองหลังการให้สารต้าน VEGF ร่วมกับการรักษาด้วยแสงไดนามิก (PDT ) : มีรายงานผู้ป่วยที่เกิดการลอกตัวของเยื่อเหนือจอประสาทตา เองหลังการรักษาด้วยแสงไดนามิก 4) .
เหล่านี้เป็นเพียงรายงานผู้ป่วยและยังไม่ใช่การรักษามาตรฐานในปัจจุบัน
Q
จำเป็นต้องลอกเยื่อหุ้มชั้นใน (ILM) เสมอหรือไม่?
A
การลอก ILM มีประสิทธิภาพในการป้องกันการกลับเป็นซ้ำของเยื่อเหนือจอตา และเป็นส่วนหนึ่งของการผ่าตัดมาตรฐานในปัจจุบัน อัตราการกลับเป็นซ้ำเมื่อลอก ILM อยู่ที่ 0-2.6% และเมื่อไม่ลอกอยู่ที่ 8.6-21% 12) หากตรวจพบข้อบกพร่องของ ILM ในการตรวจ OCT en face ก่อนผ่าตัด (พบใน 22.7% ของกรณี) จำเป็นต้องใช้เทคนิคการลอกจากขอบข้อบกพร่อง 1) อย่างไรก็ตาม ความยากทางเทคนิคสูง และต้องตัดสินใจโดยพิจารณาสมดุลกับความเสี่ยงของภาวะแทรกซ้อน เช่น การฝ่อของ RPE ในกลุ่มที่ลอก ILM แบบ active การฟื้นตัวของการมองเห็น อาจล่าช้าเล็กน้อย 18)
Q
หลังผ่าตัด การมองเห็นจะฟื้นตัวเมื่อใด?
A
การฟื้นตัวของการมองเห็น จะค่อยเป็นค่อยไปในช่วง 3-6 เดือนหลังผ่าตัด และอาจดีขึ้นต่อเนื่องจนถึง 12 เดือนหลังผ่าตัด แม้ใน 1 ปีหลังผ่าตัด อาจยังมีความหนาของจอประสาทตา และความผิดปกติของการมองเห็น ที่เกี่ยวข้อง ดังนั้นการติดตามผลระยะยาวจึงสำคัญ ในผลลัพธ์ระยะยาว การฟื้นตัวจะดำเนินต่อไปจนถึง 3 ปีหลังผ่าตัด และคงที่นานถึง 10 ปี 17) ระดับความผิดรูปของจอประสาทตา ก่อนผ่าตัดและความสมบูรณ์ของโซน ellipsoid (EZ ) ส่งผลต่อแนวโน้มการฟื้นตัว
การเกิดเยื่อเหนือจอตาเป็นที่เข้าใจกันว่าเป็นปฏิกิริยาคล้ายการสมานแผลที่ผ่านขั้นตอนต่อไปนี้ 11)
PVD และวุ้นตา ส่วนคอร์เทกซ์ที่เหลือPVD วุ้นตา ส่วนคอร์เทกซ์บางส่วนจะยังคงอยู่บน ILM รอยฉีกขาดขนาดเล็กของ ILM (สมมติฐานดั้งเดิม) : การดึงรั้งของวุ้นตา ส่วนคอร์เทกซ์ที่เหลือทำให้เกิดรอยฉีกขาดขนาดเล็กบน ILM การย้ายที่ของเซลล์ : เซลล์เกลียจอตา (เซลล์มุลเลอร์, แอสโตรไซต์), เซลล์ RPE และมาโครฟาจย้ายที่ผ่านรอยฉีกขาดของ ILM เข้าสู่ช่องวุ้นตา การเพิ่มจำนวนและการแยกตัวเป็นไฟโบรบลาสต์ : เซลล์ที่ย้ายที่มาเพิ่มจำนวนและแยกตัวเป็นเซลล์หดตัวคล้ายไฟโบรบลาสต์ ก่อตัวเป็นเยื่อเหนือจอตา
ลามิโนไซต์ (ไฮยาโลไซต์ที่มาจากเยื่อวุ้นตา ส่วนหลัง) ถือเป็นองค์ประกอบเซลล์หลักใน ERM ที่ไม่ทราบสาเหตุ 12) ไฮยาโลไซต์มีต้นกำเนิดจากเซลล์ไขกระดูกและมีการสร้างใหม่ต่อเนื่อง เซลล์เกลียและไฮยาโลไซต์แยกตัวเป็นไฟโบรบลาสต์/ไมโอไฟโบรบลาสต์ ทำให้เกิดการสร้างเมทริกซ์นอกเซลล์และพังผืด นำไปสู่การเกิด ERM องค์ประกอบของ ERM มีความหลากหลาย โดยมีต้นกำเนิดและสาเหตุหลายประการ
ในสมมติฐานใหม่ที่ไม่ต้องอาศัยรอยฉีกขาดของ ILM เชื่อว่าไฮยาโลไซต์ในวุ้นตา ส่วนคอร์เทกซ์ที่เหลือบน ILM ถูกกระตุ้นให้เป็นไมโอไฟโบรบลาสต์ ซึ่งสร้างและหดรัด ERM โดยตรง 12)
ในกรณี ไม่ทราบสาเหตุ การเพิ่มจำนวนของไฟโบรบลาสต์, ไมโอไฟโบรบลาสต์, เซลล์เกลีย, มาโครฟาจ, เซลล์อักเสบ, ไฮยาโลไซต์ และเซลล์เยื่อบุผิวเม็ดสีจอตาในวุ้นตา ส่วนคอร์เทกซ์ ร่วมกับการเปลี่ยนแปลงของเมทริกซ์นอกเซลล์ มีส่วนในการสร้างเนื้อเยื่อเยื่อ
ในกรณีทุติยภูมิ การแตกของสิ่งกีดขวางเลือด-จอประสาทตา ทำให้เกิดการปล่อยไซโตไคน์ ส่งผลให้เซลล์เยื่อบุผิวรงควัตถุจอประสาทตา และเซลล์เกลียเพิ่มจำนวนบนคอร์เทกซ์วุ้นตา และเยื่อลิมิตันภายใน เกิดเป็นเยื่อ
ผลต่อหลอดเลือด : การดึงรั้งโดยเยื่อเหนือจอประสาทตา ทำให้พื้นที่บริเวณหลอดเลือดว่าง (FA Z) ลดลง และความหนาแน่นของหลอดเลือด (VAD) ในข่ายเส้นเลือดฝอยผิว (SCP) เพิ่มขึ้นอย่างมีนัยสำคัญ2) มีความสัมพันธ์ผกผันอย่างมีนัยสำคัญระหว่างพื้นที่ FA Z และค่าสายตาที่ดีที่สุดที่แก้ไขแล้ว (BCVA) (r = −0.683)2) ทำให้สัณฐานวิทยาของ FA Z เป็นตัวบ่งชี้สำคัญของการทำงานทางการมองเห็น
ในเยื่อเหนือจอประสาทตา ที่เกี่ยวข้องกับ NF 2 การสูญเสียการทำงานของยีนยับยั้งเนื้องอกทำให้เกิดการเพิ่มจำนวนผิดปกติของส่วนประกอบเกลียคล้ายเซลล์มุลเลอร์ เกิดเป็นเยื่อเหนือจอประสาทตา การย้อมอิมมูโนแสดงรูปแบบ GFA P บวกเล็กน้อย และ nestin บวกปานกลาง9)
ในการทดลองแบบสุ่มมีกลุ่มควบคุมของ Ducloyer และคณะ (2024) ใน 213 ตา (101 ตาลอกเอง, 51 ตาลอก ILM แบบ active, 49 ตาไม่ลอก) อัตราการกลับเป็นซ้ำคือ 0% ในกลุ่มลอก active เทียบกับ 19.6% ในกลุ่มไม่ลอก ซึ่งแตกต่างอย่างมีนัยสำคัญ18) อย่างไรก็ตาม การฟื้นตัวของ BCVA และไมโครเพอริเมทรี หลังผ่าตัดล่าช้าเล็กน้อยในกลุ่มลอก ILM แบบ active จำเป็นต้องประเมินผลระยะยาวเพื่อพิจารณาข้อแลกเปลี่ยนระหว่างการป้องกันการกลับเป็นซ้ำและการฟื้นฟูการทำงานทางการมองเห็น
รายงานของ Elhusseiny และคณะ (2020) ใน 49 ตา โดยติดตามเฉลี่ย 111 เดือน (ประมาณ 9.3 ปี) แสดงให้เห็นว่า BCVA ดีขึ้นจาก 0.56 ก่อนผ่าตัดเป็น 0.33 ที่ 1 ปี, 0.25 ที่ 3 ปี และคงที่ที่ 0.28 ที่ 10 ปี แสดงให้เห็นถึงการปรับปรุงอย่างต่อเนื่องถึง 3 ปีและคงที่เป็นเวลา 10 ปี17) ซึ่งสนับสนุนการผ่าตัดตั้งแต่เนิ่นๆ ในแง่ของการรักษาการทำงานทางการมองเห็น ในระยะยาว
Frisina และคณะ (2023) ยืนยันด้วย OCTA ว่าพื้นที่ FA Z ในตาที่มีเยื่อเหนือจอประสาทตา ไม่ทราบสาเหตุหดตัวเหลือประมาณครึ่งหนึ่งของตาปกติ (0.11 มม.² เทียบกับ 0.24 มม.²) โดยมี VAD ใน SCP เพิ่มขึ้นอย่างมีนัยสำคัญ2) พวกเขายังรายงานความสัมพันธ์ผกผันอย่างมีนัยสำคัญระหว่างพื้นที่ FA Z และ BCVA (r = −0.683) ซึ่งบ่งชี้ว่า OCTA เป็นเครื่องมือที่มีแนวโน้มสำหรับการพยากรณ์โรคก่อนผ่าตัด ค่าสายตา logMAR ดีขึ้นอย่างมีนัยสำคัญจาก 0.4 เป็น 0.1 หลังผ่าตัด
Sasajima และ Zako (2023) รายงานว่า OCT en face ก่อนผ่าตัดพบข้อบกพร่องของ ILM ใน 22.7% ของกรณี และเทคนิคการลอกจากขอบข้อบกพร่อง (defect-edge technique) ปลอดภัยและมีประสิทธิภาพ 1) การระบุตำแหน่งข้อบกพร่องก่อนผ่าตัดคาดว่าจะช่วยเพิ่มความแม่นยำในการวางแผนการผ่าตัด
การวินิจฉัย ERM ด้วย AI จากภาพถ่ายจอประสาทตา หรือการตรวจด้วยกล้องตรวจตา อยู่ในขั้นตอนการประเมิน 12) มีข้อชี้ให้เห็นว่ามีข้อดีในด้านต้นทุนและการเข้าถึง และคาดว่าจะนำมาใช้ในการคัดกรอง อย่างไรก็ตาม การตรวจสอบความแม่นยำในการวินิจฉัยยังคงดำเนินอยู่ และ OCT ยังคงเป็นมาตรฐานโดยพฤตินัยสำหรับการวินิจฉัย ERM
Giachos และคณะ (2021) รายงานกรณีที่แรงดึงของเยื่อเหนือจอประสาทตา กระตุ้นให้เกิดเส้นเลือดใหม่ในจอประสาทตา ในผู้ป่วยที่ไม่มีโรคเบาหวาน 6) OCTA ช่วยให้ประเมินหลอดเลือดได้อย่างละเอียด และพบว่าเส้นเลือดใหม่มีการหดตัวหลังการผ่าตัดเยื่อเหนือจอประสาทตา
Venkatesh และคณะ (2022) รายงานกรณีจอประสาทตา เสื่อมจากการใช้สีย้อม BBG ร่วมกับแสงส่องภายในตา 10) ซึ่งแสดงให้เห็นถึงความสำคัญของการจำกัดเวลาในการสัมผัสแสงและการจัดการความเข้มของแสงที่เหมาะสมเมื่อใช้ BBG การกำหนดระเบียบปฏิบัติการย้อมสีที่ปลอดภัยเป็นความท้าทายในอนาคต
Koiwa และคณะ (2024) รายงานกรณีจอประสาทตา ขาดเลือดบริเวณรอบรอยบุ๋มคล้าย PAMM หลังการผ่าตัดวุ้นตา เพื่อรักษาเยื่อเหนือจอประสาทตา 5) และชี้ให้เห็นว่าการประเมินการไหลเวียนเลือดก่อนผ่าตัดและการจัดการความดันลูกตา ระหว่างผ่าตัดมีความสำคัญต่อการป้องกันภาวะแทรกซ้อน
Sasajima H, Zako M. Internal limiting membrane peeling technique from internal limiting membrane defect edge. Clin Case Rep. 2023;11(5):e7279. doi:10.1002/ccr3.7279. PMID: 37155426.
Frisina R, De Salvo G, Tozzi L, et al. Effects of physiological fluctuations on the estimation of vascular flow in eyes with idiopathic macular pucker. Eye (Lond). 2023;37(7):1470-1478. doi:10.1038/s41433-022-02158-4. PMID: 35794376.
Mashayekhi A, Shields CL, Shields JA, et al. Malignant epiretinal membrane after proton beam radiation. J Ophthalmic Vis Res. 2023;18(4):445-451. doi:10.18502/jovr.v18i4.14558.
Munoz-Solano J, Preziosa C, Staurenghi G, Pellegrini M. Resolution of epiretinal membrane after anti-VEGF and photodynamic therapy of retinal hemangioblastoma. Am J Ophthalmol Case Rep. 2024;33:101994. doi:10.1016/j.ajoc.2024.101994. PMID: 38303898. PMCI D: PMC10831802.
Koiwa C, Chi P, Yamamoto S, Nakao S. Extramacular paracentral acute middle maculopathy-like retinal ischemia after vitrectomy for epiretinal membrane. Am J Ophthalmol Case Rep. 2024;36:102221. doi:10.1016/j.ajoc.2024.102221. PMID: 39634097. PMCI D: PMC11615521.
Giachos I, et al. ERM -induced intraretinal neovascularization. Am J Ophthalmol Case Rep. 2021;23:101180.
Alshahrani ST, Al Zoba A, Uwaydah Z. Epiretinal membrane separation following dexamethasone intravitreal implant in diabetic macular edema: a case report. Ophthalmol Ther. 2022;11(2):737-742. doi:10.1007/s40123-022-00472-4. PMID: 35362248.
Rivera-Valdivia N, et al. RPE atrophy after ERM /ILM peeling. Rom J Ophthalmol. 2022;66(1):79-83.
Kunikata H, Nishiguchi KM, Watanabe M, Nakazawa T. Surgical outcome and pathological findings in macular epiretinal membrane caused by neurofibromatosis type 2. Digit J Ophthalmol. 2022;28(1):12-16. doi:10.5693/djo.02.2021.06.001. PMID: 35573141.
Venkatesh R, Yadav NK , Pereira A, et al. Phototoxic maculopathy following brilliant blue G-assisted internal limiting membrane peeling. J Curr Ophthalmol. 2022;34(2):267-270. doi:10.4103/joco.joco_46_22.
Flaxel CJ, Adelman RA, Bailey ST, et al. Idiopathic Epiretinal Membrane and Vitreomacular Traction Preferred Practice Pattern. Ophthalmology. 2020;127(2):P145-P183.
Bailey ST, Vemulakonda GA, et al. Idiopathic Epiretinal Membrane and Vitreomacular Traction Preferred Practice Pattern. Ophthalmology. 2025;132(2):P203-P237.
Xiao W, Chen X, Yan W, et al. Prevalence and risk factors of epiretinal membranes: a systematic review and meta-analysis of population-based studies. BMJ Open. 2017;7:e014644. doi:10.1136/bmjopen-2016-014644. PMID: 28951399.
Fraser-Bell S, Guzowski M, Rochtchina E, et al. Five-year cumulative incidence and progression of epiretinal membranes: the Blue Mountains Eye Study. Ophthalmology. 2003;110(1):34-40. PMID: 12511343.
Meuer SM, Myers CE, Klein BE, et al. The epidemiology of vitreoretinal interface abnormalities as detected by spectral-domain optical coherence tomography: the Beaver Dam Eye Study. Ophthalmology. 2015;122(4):787-795.
Ng CH, Cheung N, Wang JJ, et al. Prevalence and risk factors for epiretinal membranes in a multi-ethnic United States population. Ophthalmology. 2011;118(4):694-699. doi:10.1016/j.ophtha.2010.08.009.
Elhusseiny AM, Smiddy WE, Flynn HW Jr, et al. Long-term visual and anatomical outcomes after epiretinal membrane peeling. Retina. 2020;40(10):1952-1959. doi:10.1097/IAE.0000000000002705. PMID: 31764264.
Ducloyer JB, et al. Pros and cons of internal limiting membrane peeling during epiretinal membrane surgery: a randomised clinical trial with microperimetry (PEELING). Br J Ophthalmol. 2024. doi:10.1136/bjo-2023-324990. PMID: 38901960.
Chang WC, Lin C, Lee CH, et al. Vitrectomy with or without internal limiting membrane peeling for idiopathic epiretinal membrane: a meta-analysis. PLoS One. 2017;12(6):e0179105. doi:10.1371/journal.pone.0179105. PMID: 28622372. PMCI D: PMC5476241.