รูจุดรับภาพ (Macular hole) คือความบกพร่องของจอตาทุกชั้นที่เกิดขึ้นที่รอยบุ๋มจอตา (fovea) แบ่งเป็น 4 ชนิด: ไม่ทราบสาเหตุ, สายตาสั้น , จากอุบัติเหตุ, และทุติยภูมิ
ชนิดไม่ทราบสาเหตุพบมากในผู้หญิงอายุ 60-70 ปี โดยผู้หญิงเป็นประมาณ 3.3 เท่าของผู้ชาย ผู้ป่วย 72% เป็นผู้หญิง มากกว่า 50% เริ่มมีอาการในช่วงอายุ 65-74 ปี
อาการหลักคือ การมองเห็น ส่วนกลางลดลงและภาพบิดเบี้ยว (การบิดเบี้ยวแบบเหวี่ยงออกจากศูนย์กลาง) หากไม่รักษา การมองเห็น จะลดลงเหลือ 0.1 หรือน้อยกว่า
OCT เป็นมาตรฐานทองคำในการวินิจฉัยและจำแนกระยะ การวัดเส้นผ่านศูนย์กลางรูที่เล็กที่สุด (MLD) มีความสำคัญในการกำหนดแผนการรักษาการผ่าตัดมาตรฐาน (การตัดน้ำวุ้นตา + การลอก ILM + การอัดแก๊ส) ทำให้รูปิดได้ 91-98% ข้อมูลทางคลินิกจากสหราชอาณาจักร (1,483 ตา) แสดงอัตราการปิด 95.7% การมองเห็น ดีขึ้นจาก 0.78 เป็น 0.42 logMAR (ประมาณ 4 บรรทัด) 2) 3)
ในกรณีรูขนาดใหญ่หรือดื้อต่อการรักษา สามารถใช้เทคนิค inverted ILM flap หรือ ILM flap โดยไม่ใช้แก๊ส (Szeto 2025) การมองเห็น ดีขึ้นนานถึง 3 ปีหลังผ่าตัดและคงอยู่นาน 5-10 ปี 3)
ในรูจากอุบัติเหตุ มีโอกาสปิดเองได้ (10-67%) ดังนั้นการสังเกตอาการหลังได้รับบาดเจ็บจึงเป็นแนวทางเริ่มต้น
รูจุดรับภาพ (macular hole; MH) เป็นโรคที่มีความบกพร่องของจอตาทุกชั้นบริเวณจุดรับภาพ รูไม่ได้เกิดจากการสูญเสียเนื้อจอตา แต่เกิดจากรอยแยกเล็กๆ จากการดึงรั้งของน้ำวุ้นตา ส่วนหลัง ซึ่งขยายใหญ่ขึ้นกลายเป็นรู การปิดเองนั้นพบได้น้อย และเมื่อเวลาผ่านไปรูจะขยายใหญ่ขึ้นและเกิดการเสื่อมของเซลล์เยื่อบุผิวรงควัตถุจอตา
ในปี 1988 Gass ได้บรรยายกระบวนการดำเนินโรคของรูจุดรับภาพชนิดไม่ทราบสาเหตุเป็น 4 ระยะเป็นครั้งแรก ในปี 1991 Kelly และ Wendel รายงานประสิทธิภาพของการผ่าตัดน้ำวุ้นตา และในปี 1995 Brooks รายงานการเพิ่มอัตราการปิดรูด้วยการลอกเยื่อหุ้มชั้นใน ปัจจุบัน การตัดน้ำวุ้นตา + การลอก ILM + การอัดแก๊สเป็นวิธีการผ่าตัดมาตรฐาน
รูพรุนจอตา (macular hole) แบ่งออกเป็น 4 ชนิดตามสาเหตุ
ชนิด ชั้นที่พบบ่อย สาเหตุหลัก ไม่ทราบสาเหตุ ผู้หญิงอายุ 60-70 ปี การดึงรั้งของวุ้นตา -จอตาจากอายุ สายตาสั้น ผู้หญิงที่มีสายตาสั้น มาก สตาฟิโลมาส่วนหลัง / จอตาพร่า จากอุบัติเหตุ ชายหนุ่ม (อายุ 20-30 ปี) การบาดเจ็บที่ตาจากของทื่อ ทุติยภูมิ หลากหลาย จอตาลอก / การอักเสบ / ยา (เช่น ทามอกซิเฟน) 4)
รอยยุบจอตาชั้นใน (Lamellar macular hole; LMH) ไม่ใช่การขาดแบบเต็มความหนา แต่เป็นโรคที่ทำให้เกิดการขาดบางส่วนในชั้นในของจอตา ในขณะที่ชั้นนอกยังคงอยู่ ความชุกอยู่ที่ 1.1–3.6% และพบบ่อยในช่วงอายุ 50–70 ปี 12) เป็นรอยโรคที่เกี่ยวข้องที่สำคัญที่ต้องแยกให้ออก
ส่วนรอยยุบจอตาเทียม (pseudohole) เป็นภาวะที่ส่วนกลางบุ๋มลงเนื่องจากเยื่อเหนือจอตาที่อยู่รอบข้าง ซึ่งแตกต่างจากรอยยุบจอตาไม่ทราบสาเหตุตรงที่ไม่ใช่การขาดแบบเต็มความหนา
อุบัติการณ์ของรอยยุบจอตาไม่ทราบสาเหตุรายงานอยู่ที่ 3.14–7.8 ต่อประชากร 100,000 คนต่อปี 2) ในการศึกษาประชากรในสหรัฐฯ อุบัติการณ์อยู่ที่ 7.8 ต่อ 100,000 คนต่อปี (8.7 ตา) อัตราส่วนหญิงต่อชาย 3.3:1 3) อายุที่พบบ่อยที่สุดคือ 60–70 ปี โดยสูงสุดในทศวรรษที่ 7 ผู้ป่วย 72% เป็นหญิง มากกว่า 50% เกิดในช่วงอายุ 65–74 ปี และเพียง 3% อายุต่ำกว่า 55 ปี 3)
โดยปกติเป็นข้างเดียว แต่ความถี่ในตาอีกข้างคือ 10–20% ความเสี่ยง 5 ปีในตาอีกข้างคือ 10–15% และสูงถึง 28% หากไม่มีภาวะวุ้นตา หลุดตัวสมบูรณ์ 2) มีรายงานว่าชาวเอเชียมีความเสี่ยง iFTMH สูงกว่าชาวผิวขาว 177% 2) รอยยุบจากอุบัติเหตุพบบ่อยในชายหนุ่ม ซึ่งตรงกันข้ามกับชนิดไม่ทราบสาเหตุ
จอตาลอกจากรอยยุบจอตาพบบ่อยในหญิงที่มีสายตาสั้น มาก และในญี่ปุ่นคิดเป็นประมาณ 5% ของผู้ป่วยจอตาลอก ซึ่งสูงกว่า 0.5–2.0% ในยุโรปและอเมริกา
Q
รอยยุบจอตาเกิดขึ้นทั้งสองตาหรือไม่?
A
ความเสี่ยงในตาอีกข้างหลังจากเกิดข้างเดียวอยู่ในระดับปานกลาง ในผู้ป่วยที่ไม่มีภาวะวุ้นตา หลุดตัวในตาอีกข้าง ความเสี่ยงสูงถึง 28% ใน 5 ปี 2) หากมีภาวะวุ้นตา หลุดตัวสมบูรณ์ในตาอีกข้าง ความเสี่ยงต่ำ เวลาที่เกิดไม่จำเป็นต้องพร้อมกัน แต่ประมาณ 10–20% ของผู้ป่วยเกิดในทั้งสองตา
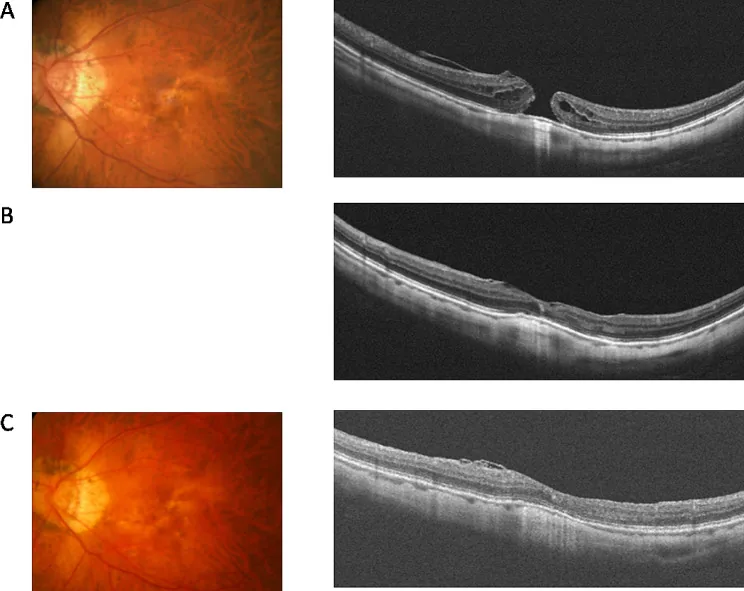
ภาพถ่ายจอตาและภาพ OCT ของรอยยุบจอตา Wu TT, et al. Inverted flap technique versus internal limiting membrane insertion for macular hole in eyes with extremely high myopia. BMC Ophthalmol. 2024. Figure 1. PM
CI D: PMC11251341. License: CC BY.
OCT ก่อนผ่าตัดแสดงรอยยุบแบบเต็มความหนาที่จอตาส่วนกลางอย่างชัดเจน OCT หลังผ่าตัดแสดงการปิดของรอยยุบ ทำให้เข้าใจภาพลักษณะเฉพาะของรอยยุบจอตาได้ง่าย
อาการหลักที่ผู้ป่วยรับรู้ของรอยยุบจอตาไม่ทราบสาเหตุมีดังนี้:
การมองเห็น ส่วนกลางลดลงการมองเห็น ประมาณ 0.4–1.0 ลดลงเหลือประมาณ 0.1 เมื่อโรคดำเนินไปภาพบิดเบี้ยว (metamorphopsia)จุดบอดกลาง (Central scotoma)จุดบอดกลาง ภาพเล็ก (Micropsia) : ไม่ค่อยมีผู้ป่วยบ่นว่ามองเห็นวัตถุเล็กกว่าขนาดจริง
อาการจะค่อยๆ ดำเนินไปเป็นเวลาหลายสัปดาห์ถึงหลายเดือน แต่มักรับรู้ได้ค่อนข้างฉับพลัน3)
ในรอยรั่วจอประสาทตา ชนิดทะลุตลอดชั้น (full-thickness macular hole) ที่ไม่ได้รับการรักษา การพยากรณ์โรคมักไม่ดี ประมาณ 40-50% ของระยะที่ 1 ดำเนินไปเป็นรอยรั่วทะลุตลอดชั้น และประมาณ 50% ดีขึ้นเองเมื่อมีการหลุดของวุ้นตา ส่วนหลัง3) ประมาณ 75% ของระยะที่ 2 ดำเนินไปเป็นระยะที่ 3-43) ในรอยรั่วจอประสาทตา ชนิดทะลุตลอดชั้นที่ไม่ได้รับการรักษา มีเพียง 5% ที่คงความชัดเจนในการมองเห็น 20/50 หรือดีกว่า 55% มีค่า 20/100 หรือแย่กว่า และ 40% มีค่า 20/200 หรือแย่กว่า3) อัตราการปิดเองโดยการสังเกตเพียงอย่างเดียวอยู่ที่ 2.5-27% (ขึ้นอยู่กับขนาดและระยะเวลา) และไม่มีการปิดเองในรอยรั่วขนาดใหญ่ (>400 μm)2)
การจำแนกระยะที่ Gass บรรยายไว้ในปี 1995 ยังคงใช้กันอย่างแพร่หลายเป็นมาตรฐาน ด้วยความก้าวหน้าของ OCT ทำให้เข้าใจพยาธิสภาพของแต่ละระยะได้ละเอียดมากขึ้น
ระยะที่ 1 (ใกล้เกิด/แฝง)
ระยะที่ 1A (รอยรั่วใกล้เกิด) : ระยะที่เกิดการผิดรูปของ fovea เนื่องจากการหลุดของวุ้นตา ส่วนหลัง พบการหายไปของรอยบุ๋ม fovea และจุดสีเหลือง (100-200 μm)3) เกิดโพรงถุงน้ำใน fovea หรือจอประสาทตา หลุดที่ fovea
ระยะที่ 1B (รอยรั่วแฝง) : พบวงแหวนสีเหลือง (200-350 μm)3) เกิดการแยกชั้นของเซลล์รับแสง แต่ยังไม่ถึงขั้นทะลุตลอดชั้น (occult hole)
การดำเนินโรคตามธรรมชาติ : ประมาณ 50% ของระยะที่ 1 ดีขึ้นเอง
ระยะที่ 2-4 (รอยรั่วทะลุตลอดชั้น)
ระยะที่ 2 : รอยรั่วทะลุตลอดชั้นขนาด <400 μm อาจอยู่เยื้องศูนย์และมีแผ่นเนื้อเยื่อยกขึ้น3) วุ้นตา ส่วนหลังเชื่อมต่อกับ fovea ผ่านแผ่นเนื้อเยื่อนี้
ระยะที่ 3 : รอยรั่วทะลุตลอดชั้นขนาด ≥400 μm มี pseudo-operculum หลุดลอย การหลุดของวุ้นตา ส่วนหลังยังไม่สมบูรณ์
ระยะที่ 4 : ระยะที่การหลุดของวุ้นตา ส่วนหลังสมบูรณ์แล้ว ตรวจพบวงแหวน glial ด้วย ophthalmoscope พบวงแหวน Weiss
ในปี 2013 กลุ่มศึกษาแรงดึงแก้วตา-จอประสาทตา ระหว่างประเทศ (IVTS) ได้กำหนดการจำแนกประเภทตามผลการตรวจ OCT รูจอประสาทตา ชนิดทะลุตลอดความหนาจะถูกจำแนกตามเส้นผ่านศูนย์กลางที่เล็กที่สุด 2)
ประเภท เส้นผ่านศูนย์กลางที่เล็กที่สุด เล็ก (S) < 250 ไมโครเมตร ปานกลาง (M) 250–400 ไมโครเมตร ใหญ่ (L) > 400 ไมโครเมตร
โดยทั่วไป รูในระยะที่ 2 ขึ้นไปและขนาดปานกลางหรือใหญ่เป็นข้อบ่งชี้ในการผ่าตัด กลุ่มศึกษา CLOSE เสนอให้แบ่งย่อยรูขนาดใหญ่เป็น L (>400–≤550 ไมโครเมตร), XL (>550–≤800 ไมโครเมตร), XXL (>800–≤1000 ไมโครเมตร) และ Giant (>1000 ไมโครเมตร) มีรายงานว่าอัตราการปิดลดลงต่ำกว่า 90% เมื่อเส้นผ่านศูนย์กลางเกิน 500 ไมโครเมตร 2)
รูจอประสาทตา จากการบาดเจ็บถูกจำแนกตามผลการตรวจ OCT เป็นประเภทต่อไปนี้ 14)
ประเภท ผลการตรวจ OCT ลักษณะเฉพาะ ชนิดที่ I จอประสาทตา บวมน้ำและการเปลี่ยนแปลงแบบถุงน้ำรูที่ยังไม่ก่อตัวเต็มที่ ชนิดที่ II รูแบบชั้นบาง ความบกพร่องของชั้นบางส่วน ชนิดที่ III รูทะลุทุกชั้น (ขนาดเล็กถึงกลาง) การจำแนก IVTS S/M ชนิดที่ IV รูทะลุทุกชั้น (ขนาดใหญ่) การจำแนก IVTS L ชนิดที่ V รูร่วมกับจอประสาทตาลอก ข้อบ่งชี้ในการผ่าตัดฉุกเฉิน
รอยรั่วชั้นจอประสาทตา ชั้นในแบ่งตามการจำแนกของ Govetto ออกเป็นสองประเภทหลัก: “ชนิดเสื่อม” และ “ชนิดดึงรั้ง” 13) Hubschman และคณะได้นิยามชนิดเสื่อมใหม่เป็น “LMH” และชนิดดึงรั้งเป็น “ERM foveoschisis (ERM F)” 12)
ชนิดเสื่อมมีลักษณะเฉพาะคือโพรงที่ไม่เป็นเส้นตรงในจอประสาทตา ชั้นใน การสูญเสียเนื้อเยื่อรอยบุ๋มจอประสาทตา และการเจริญเกินของเยื่อเหนือจอประสาทตา (LHEP) ชนิดดึงรั้งมีลักษณะเฉพาะคือการมีเยื่อเหนือจอประสาทตา ที่หดตัวและการแยกชั้นจอประสาทตา ในระดับเส้นใยเฮนเล 13) ชนิดเสื่อมมักเกิดร่วมกับการทำลายบริเวณรูปไข่ (EZ ) และมีการพยากรณ์โรคด้านการมองเห็น ที่แย่กว่า
ในตาที่เป็นรอยรั่วจอประสาทตา อาจมีการดึงรั้งของวุ้นตา -จอประสาทตา ที่แฝงอยู่ในตาข้างตรงข้าม แนะนำให้ตรวจอวัยวะรับภาพของตาข้างตรงข้ามเป็นประจำ อาจมีจอประสาทตาฉีกขาด บริเวณรอบนอกหรือจอประสาทตา เสื่อมแบบตาข่ายร่วมด้วย ดังนั้นจำเป็นต้องสังเกตบริเวณรอบนอกอย่างเพียงพอก่อนการผ่าตัด
Q
รอยรั่วจอประสาทตาระยะที่ 1 จำเป็นต้องรักษาหรือไม่?
A
ระยะที่ 1 คือรอยรั่วที่กำลังจะเกิดขึ้นซึ่งยังไม่เป็นรอยรั่วตลอดความหนา และประมาณ 50% จะดีขึ้นเอง 3) โดยทั่วไปแนะนำให้สังเกตอาการ อย่างไรก็ตาม เนื่องจากมีความเสี่ยงที่จะลุกลาม การติดตามผลด้วย OCT เป็นประจำจึงเป็นสิ่งสำคัญ
สาเหตุหลักของรอยรั่วจอประสาทตา โดยไม่ทราบสาเหตุคือการดึงรั้งของวุ้นตา -จอประสาทตา ในระยะเริ่มต้นของภาวะวุ้นตาหลุดจากจอประสาทตาส่วนหลัง (PVD ) ที่เกี่ยวข้องกับอายุ 2)
ในวุ้นตา ของตามนุษย์ มีโพรงเหลวทางสรีรวิทยาด้านหน้ารอยบุ๋มจอประสาทตา (ถุงหน้ารอยบุ๋ม: ถุงคิชิ) เมื่ออายุมากขึ้น เปลือกที่ก่อตัวเป็นผนังด้านหลังของถุงจะดึงรอยบุ๋มจอประสาทตา และมีส่วนทำให้เกิดรอยรั่วจอประสาทตา
กระบวนการเกิดมีดังนี้:
เมื่ออายุมากขึ้น วุ้นตา จะกลายเป็นของเหลวและเกิดโพรงเหลว (ถุง) ขึ้นด้านหน้าเปลือกวุ้นตา ส่วนหลัง
เยื่อวุ้นตา ส่วนหลังหลุดออกจากจอประสาทตา รอบรอยบุ๋มจอประสาทตา (PVD รอบรอยบุ๋ม)
ที่รอยบุ๋มจอประสาทตา การยึดเกาะของวุ้นตา แข็งแรงตามสรีรวิทยา ดังนั้นการยึดเกาะจึงคงอยู่
แรงดึงในแนวหน้าหลังรวมตัวที่โฟเวีย
เกิดการแยกตัวระหว่างกรวยมุลเลอร์และเซลล์รับแสง ทำให้เกิดถุงน้ำในจอประสาทตา 2)
หากแรงดึงยังคงอยู่ ILM และ ELM จะฉีกขาด นำไปสู่รูทะลุทุกชั้น 2)
ขอบเขตของความบกพร่องของจอประสาทตา ชั้นนอกสัมพันธ์กับขอบเขตและความรุนแรงของแรงดึงวุ้นตา -จอประสาทตา การยึดเกาะที่กว้างขึ้นทำให้เซลล์รับแสง บกพร่องเป็นบริเวณกว้างขึ้น 2) เมื่อความพยายามซ่อมแซมของเซลล์เกลียล้มเหลว เซลล์เกลียจะเคลื่อนที่และหดตัวบน ILM ที่ขอบรู ทำให้รูขยายใหญ่ขึ้นด้วยแรงดึงในแนวสัมผัส 2)
เมื่อมีการบาดเจ็บแบบทื่อต่อลูกตา จะเกิดการกดในแนวหน้าหลังและการขยายในแนวเส้นศูนย์สูตรพร้อมกัน การเสียรูปนี้ทำให้แรงดึงในแนวสัมผัสรวมตัวที่จอประสาทตา ฉีกขาดเนื้อเยื่อโฟเวียและเกิดเป็นรู ในคนหนุ่มสาว วุ้นตา จะยึดติดแน่นกับจอประสาทตา (ไม่มี PVD ) ทำให้แรงภายนอกถ่ายทอดโดยตรงไปยังจอประสาทตา ผ่านวุ้นตา ได้ง่าย 14) ประมาณ 85% ของกรณี TMH ไม่พบการหลุดลอกของวุ้นตา ส่วนหลัง
เลเซอร์กำลังสูง เช่น การฉายเลเซอร์พอยน์เตอร์ผิดทิศทาง ก็สามารถทำให้เกิดรูจอประสาทตา ได้เช่นกัน
อายุ : ความเสี่ยงเพิ่มขึ้นหลังจากอายุ 60 ปี หลังจากอายุ 70 ปี มีการเพิ่มขึ้นแบบไม่เป็นเส้นตรง 2) เพศหญิง : อุบัติการณ์สูงกว่าผู้ชาย 2–3.3 เท่า 2) สายตาสั้น สูงแกนตา ที่เพิ่มขึ้นเป็นปัจจัยเสี่ยง ยิ่งระดับสายตาสั้น มาก อายุที่เริ่มเป็นก็ยิ่งน้อยลง 2) ประวัติการคลอดบุตร : จำนวนครั้งที่คลอดบุตรสัมพันธ์กับความเสี่ยงของ iFTMH (การศึกษาแบบกลุ่มในเกาหลี) 3) การดำเนินไปไม่สมบูรณ์ของการหลุดลอกของวุ้นตา ส่วนหลัง : การยึดเกาะของวุ้นตา เฉพาะที่บริเวณโฟเวียเป็นสาเหตุการบาดเจ็บ : การเสียรูปของลูกตาและการยืดของจอประสาทตา จากการบาดเจ็บแบบทื่อเป็นสาเหตุ แตกต่างจากชนิดไม่ทราบสาเหตุ พบมากในชายหนุ่ม
ไม่มีวิธีการป้องกันที่พิสูจน์แล้วสำหรับรอยรั่วที่จอประสาทตา ชนิดไม่ทราบสาเหตุ หากตาข้างหนึ่งเกิดรอยรั่วที่จอประสาทตา ตาอีกข้างก็อาจเกิดได้เช่นกัน ดังนั้นควรตรวจอวัยวะรับภาพเป็นประจำ หากจู่ๆ การมองเห็น ส่วนกลางบิดเบี้ยวหรือมืดลง ควรไปพบจักษุแพทย์แต่เนิ่นๆ เพื่อป้องกันการบาดเจ็บที่ดวงตาขณะเล่นกีฬา ควรใช้แผ่นปิดหน้าหรือแว่นตาป้องกันตามชนิดของกีฬา
OCT เป็นมาตรฐานทองคำในการวินิจฉัยและจัดการรอยรั่วที่จอประสาทตา 3) สามารถประเมินรายละเอียดโครงสร้างจอประสาทตา บริเวณรอยรั่วได้ ข้อมูลต่อไปนี้สามารถหาได้:
การยืนยันรอยรั่วแบบทะลุทุกชั้นและการวัดเส้นผ่านศูนย์กลางน้อยที่สุด (MLD): เลือกภาพตัดขวาง OCT ที่กว้างที่สุดและวัดความกว้างน้อยที่สุดตรงกลางรอยรั่ว มีความสามารถในการทำซ้ำได้ดีและเป็นมาตรฐานทางคลินิกและการวิจัย 2)
การมีหรือไม่มีแรงดึงของวุ้นตา -จอประสาทตา (VMT )
การมีหรือไม่มีเยื่อเหนือจอประสาทตา (ERM )
การประเมินของเหลวใต้จอประสาทตา หรือการเปลี่ยนแปลงแบบถุงน้ำ
สถานะของบริเวณ ellipsoid (EZ )
เพื่อแยกแยะรอยรั่วที่จอประสาทตา เทียม ต้องแน่ใจว่าไม่มีข้อบกพร่องทะลุทุกชั้นของจอประสาทตา ในส่วนบุ๋มด้วย OCT การสแกนแบบปริมาตรก็สำคัญเพื่อตรวจสอบอย่างต่อเนื่อง
เป็นการตรวจพื้นฐานในการมาพบครั้งแรก นอกเหนือจาก OCT ควรตรวจวัดสายตาที่ดีที่สุดที่แก้ไขแล้ว (BCVA) ความดันลูกตา (IOP ) และตรวจจอประสาทตา ส่วนปลาย (คัดกรองรอยฉีกขาด) 3)
การตรวจอวัยวะรับภาพอย่างละเอียดภายใต้การขยายม่านตา เป็นพื้นฐาน ในรอยรั่วแบบทะลุทุกชั้น จะเห็นขอบจอประสาทตา สีเทา (สะท้อนการสะสมของของเหลวใต้จอประสาทตา ) ตะกอนสีเหลืองที่ก้นรอยรั่ว และการเปลี่ยนแปลงของ RPE
การทดสอบ Watzke-Allen (สัญญาณลำแสงกรีด) : เมื่อฉายลำแสงแคบไปที่รอยรั่วที่จอประสาทตา ผู้ป่วยจะรู้สึกลำแสงบิดเข้าด้านในที่จุดตรึง หากลำแสงดูเหมือนคอดตรงกลางหรือขาดตอน มีแนวโน้มเป็นรอยรั่วที่จอประสาทตา หากเพียงบิดเบี้ยว มีแนวโน้มเป็นรอยรั่วเทียม ให้ผลบวกในรอยรั่วทะลุทุกชั้น ให้ผลลบในรอยรั่วเทียมแผนภูมิ Amsler : ใช้ในการตรวจหาภาพบิดเบี้ยว (metamorphopsia)การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน (FA ) : มีประโยชน์ในการยืนยันภาวะแทรกซ้อน (จอประสาทตาลอก , ความเสียหายของคอรอยด์ ) ในกรณีที่เกิดจากการบาดเจ็บการตรวจลานสายตา จุดบอดกลาง
วิธีการตรวจ บทบาทหลัก ลักษณะเฉพาะ OCT การวินิจฉัยที่แน่นอน, การจำแนกระยะ, การแยกโรค มาตรฐานทองคำ กล้องจุลทรรศน์ชนิดกรีด (Slit lamp) การวินิจฉัยทางคลินิก สังเกตรูโดยตรงภายใต้การขยายม่านตา การทดสอบ Watzke-Allen ยืนยันรูทะลุตลอดความหนา มีประโยชน์ในการแยกจากรูปลอม แผนภูมิ Amsler การตรวจหาภาพบิดเบี้ยว (metamorphopsia) การประเมินเชิงคุณภาพของอาการที่ผู้ป่วยรับรู้
จำเป็นต้องแยกจากโรคต่อไปนี้ ทั้งหมดนี้แตกต่างจากรอยรั่วจอประสาทตา ทะลุตลอดชั้น (full-thickness macular hole) ตรงที่ไม่พบความบกพร่องของจอประสาทตา ตลอดชั้นในการตรวจ OCT
รอยรั่วจอประสาทตา เทียม (pseudohole) : การบุ๋มตัวรูปทรงกระบอกของรอยบุ๋มจอประสาทตา (fovea) เนื่องจากการหดรัดของเยื่อเหนือจอประสาทตา (epiretinal membrane) การมองเห็น ค่อนข้างดี และการทดสอบ Watzke-Allen ให้ผลลบ หากการมองเห็น ดีและไม่มีอาการที่ผู้ป่วยรับรู้ โดยทั่วไปจะไม่ผ่าตัดและติดตามอาการรอยรั่วจอประสาทตา ชั้นใน (LMH) : ความบกพร่องบางส่วนของชั้นในของจอประสาทตา ชั้นนอกของจอประสาทตา ยังคงอยู่จอประสาทตา บวมน้ำแบบถุงน้ำ (cystoid macular edema)จอประสาทตา กลุ่มอาการดึงรั้งวุ้นตา -จอประสาทตา (vitreomacular traction syndrome) : จอประสาทตา บวมน้ำเนื่องจากการดึงรั้งของวุ้นตา ในแนวหน้า-หลัง 5) ไม่มีรอยรั่วตลอดชั้นการแยกชั้นของรอยบุ๋มจอประสาทตา ที่สัมพันธ์กับ ERM (ERM F) : การแยกชั้นที่ระดับเส้นใย Henle เนื่องจาก ERM ที่หดรัด เป็นแนวคิดใหม่ที่ควรแยกจาก pseudohole และ LMH 12)
Q
จะแยกรอยรั่วจอประสาทตาเทียมกับรอยรั่วจอประสาทตาทะลุตลอดชั้นได้อย่างไร?
A
สามารถแยกได้ง่ายด้วย OCT ในรอยรั่วจอประสาทตา เทียม ไม่มีความบกพร่องของจอประสาทตา ตลอดชั้น แต่มีการบุ๋มของรอยบุ๋มจอประสาทตา เนื่องจากเยื่อเหนือจอประสาทตา การทดสอบ Watzke-Allen ให้ผลลบใน pseudohole และให้ผลบวกในรอยรั่วตลอดชั้น สิ่งสำคัญคือต้องยืนยันว่าไม่มีความบกพร่องของจอประสาทตา ตลอดชั้นในบริเวณที่บุ๋มด้วย OCT และตรวจสอบอย่างต่อเนื่องด้วยการสแกนแบบปริมาตร (volume scan)
การรักษารอยรั่วจอประสาทตา คือการผ่าตัดวุ้นตา (vitrectomy) ไม่มีการรักษาทางยา หากอายุ 50 ปีขึ้นไป มักจะผ่าตัดต้อกระจก พร้อมกัน
การตัดแก้วตา : ทำการตัดแก้วตาผ่านพาร์สพลานา (PPV )การลอกเยื่อหุ้มชั้นใน (ILM ) : ทำให้เห็น ILM ด้วย Brilliant Blue G (BBG) หรือ triamcinolone แล้วลอกด้วยคีม BBG เป็นส่วนผสมของ 0.025% BBG และ 4% polyethylene glycol มีความถ่วงจำเพาะสูง ตกตะกอนเมื่อฉีดจากขวดและย้อมผิว ILM 3) นอกจากนี้ยังใช้ ICG (Indocyanine Green) แต่ควรหลีกเลี่ยงความเข้มข้นสูงและการสัมผัสนาน3) .การเปลี่ยนของเหลวเป็นอากาศ : แทนที่ของเหลวในลูกตาด้วยอากาศการอัดแก๊ส : ใช้อากาศ (คงอยู่ไม่กี่วัน), SF₆ (2-3 สัปดาห์), C₂F₆ (4-5 สัปดาห์), C₃F₈ (6-8 สัปดาห์), ซิลิโคนออยล์ (ต้องเอาออก)3) การสำรวจในสหราชอาณาจักร (2018) พบว่าแก๊สที่ใช้มากที่สุดคือ C₂F₆ (47%), รองลงมา SF₆ (33%), C₃F₈ (19%) และอากาศ (1%)2) .ท่าทางหลังผ่าตัด : รักษาท่านอนคว่ำประมาณ 3 วันเพื่อให้แก๊สสัมผัสรู
การวิเคราะห์อภิมาน 5,480 ราย (Rahimy 2016) พบอัตราการปิดรู 98.82% ในกลุ่มลอก ILM เทียบกับ 92.88% ในกลุ่มไม่ลอก (P<0.0001) และอัตราการเปิดซ้ำลดลงอย่างมาก (25% → 0%)3) การวิเคราะห์อภิมานของ RCT 4 เรื่อง (317 ราย, ระยะที่ 2-4) ก็พบว่าการลอก ILM ลดความจำเป็นในการผ่าตัดเพิ่ม และมีรายงานว่าพื้นที่ลอกที่กว้างขึ้นช่วยลดภาพบิดเบี้ยว 3) การลอก ILM มีความคุ้มค่า และการวิเคราะห์ต้นทุนประสิทธิผลจาก RCT แสดงให้เห็นว่าการลอก ILM ดีกว่าไม่ลอกในช่วง 6 เดือน3) .
อัตราการปิดรูด้วยวิธีการมาตรฐานคือ 91-98% 3) ในการวิเคราะห์อภิมานของ RCOphth กลุ่มผ่าตัดมีค่าการมองเห็น ดีกว่า 0.16 logMAR (95% CI −0.23 ถึง −0.09) เมื่อเทียบกับกลุ่มสังเกต และอัตราส่วนออดส์ของการปิดรูคือ 31.4 (95% CI 14.9-66.3) แสดงให้เห็นประสิทธิผลของการผ่าตัดอย่างชัดเจน2) ข้อมูลทางคลินิกในสหราชอาณาจักร (1,483 ตา) พบอัตราการปิดรู 95.7%, การมองเห็น ดีขึ้นจาก 0.78 เป็น 0.42 logMAR (ดีขึ้นประมาณ 4 บรรทัด) และ 64.2% ดีขึ้น ≥0.3 logMAR2) .
ค่ามัธยฐานของสายตาหลังผ่าตัดประมาณ 20/40 (0.5) และการมองเห็น ที่ดีขึ้นคงอยู่นานถึง 3 ปีหลังผ่าตัด และคงอยู่ต่อไปอีก 5–10 ปี 3) ทุกๆ 1 เดือนที่เพิ่มขึ้นของระยะเวลาอาการจะทำให้ BCVA แย่ลง 0.008 logMAR (≈ ลดลง 1 ตัวอักษร ETDRS ทุก 2 เดือน) ดังนั้นการผ่าตัดตั้งแต่เนิ่นๆ จึงมีความสำคัญ 3) (การวิเคราะห์อภิมาน IPD จาก 12 RCT, 940 ตา) เมื่อระยะเวลาของโรคเกิน 2–3 ปี อัตราการปิดจะลดลงเหลือ 63% และพยากรณ์โรคทางสายตาไม่ดี 3) ยิ่งระยะเวลาของโรคสั้นลงและรูเล็กลง อัตราการปิดก็จะสูงขึ้นและพยากรณ์โรคทางสายตาก็ดีขึ้น
ในการทบทวน Cochrane ของ 8 RCT ที่รวม 709 ตา ไม่พบความแตกต่างที่มีนัยสำคัญในอัตราการปิดรูระหว่างกลุ่มที่นอนคว่ำและกลุ่มที่ไม่นอนคว่ำ แม้ในรูขนาดใหญ่ (≥400 μm) อัตราการปิดคือ 94% ในกลุ่มนอนคว่ำเทียบกับ 84% ในกลุ่มไม่นอนคว่ำ และในรูขนาดเล็กคือ 100% เทียบกับ 96% การวิเคราะห์อภิมาน (251 ราย, 5 RCT) ชี้ให้เห็นว่าไม่จำเป็นต้องนอนคว่ำสำหรับรู <400 μm แต่มีประโยชน์สำหรับรู ≥400 μm 3) การสำรวจในสหราชอาณาจักร (2018) รายงานว่า 82% ของแพทย์ยังคงแนะนำให้จำกัดท่าทาง โดยระยะเวลาแตกต่างกันไป: 1 วัน (19%), 2–4 วัน (30%), 5–6 วัน (23%) และ ≥1 สัปดาห์ (9%) 2)
รูจอประสาทตา ขนาดใหญ่ (>400 μm), กรณีที่มีระยะเวลานาน, และรูทุติยภูมิที่เกี่ยวข้องกับสายตาสั้น มาก, การบาดเจ็บ หรือการอักเสบ ถือว่าดื้อต่อการรักษา
เทคนิค inverted ILM flap (การพลิกแผ่นเยื่อหุ้มชั้นใน) : ใช้กับรูขนาดใหญ่ที่มีเส้นผ่านศูนย์กลาง ≥1/3 ของจานประสาทตา หรือกรณีที่ไม่ปิดในการผ่าตัดครั้งแรก ILM ที่ลอกจนถึงขอบรูจะถูกพลิกและปิดทับรู หรืออุดเข้าไปในรู ในการผ่าตัดซ้ำ สามารถอุดรูด้วยแผ่น ILM อิสระที่ลอกจากนอกจอประสาทตา เพื่อส่งเสริมการปิด ในการทบทวนอย่างเป็นระบบของ RCT ขนาดเล็ก 4 เรื่อง เทคนิคนี้อาจทำให้ BCVA ดีขึ้นกว่าการลอก ILM ทั่วไป (หลักฐานระดับต่ำ) และอัตราการปิดดีกว่าด้วยหลักฐานระดับปานกลาง 3)
ILM flap + การผ่าตัดแบบไม่ใช้แก๊ส (Szeto 2025)ILM ด้านขมับ (92.9% ของกรณี) และเทคนิคไม่ใช้แก๊สโดยใช้ของเหลว PFCL เพื่อกางและทำให้แผ่นคงที่ 16)
Szeto และคณะ (2025) รายงานการผ่าตัดแบบไม่ใช้แก๊สสำหรับรูขนาดใหญ่ (รวมถึง >30% ที่มีสายตาสั้น มาก) โดยมีเส้นผ่านศูนย์กลางรูน้อยที่สุด ≥500 μm 16) อัตราการปิดใกล้เคียงกันระหว่างกลุ่มไม่ใช้แก๊ส (94.1%) และกลุ่มดั้งเดิม (95.2%) (P=0.812) สายตาหลังผ่าตัดระยะแรกดีกว่าอย่างมีนัยสำคัญในกลุ่มไม่ใช้แก๊ส (1 สัปดาห์และ 1 เดือนหลังผ่าตัด) อัตราการเกิด gliosis ที่รอยบุ๋มจอประสาทตา ต่ำกว่าในกลุ่มไม่ใช้แก๊ส (4.9% เทียบกับ 20.0%, P=0.043) สามารถประเมิน OCT ได้ในวันถัดไปหลังผ่าตัด และไม่มีภาระในการจำกัดท่าทางสำหรับผู้ป่วย 16)
เทคนิคการผ่าตัดโดยใช้วัสดุชีวภาพอื่นๆ (Romano 2025)1) :
เยื่อหุ้มน้ำคร่ำมนุษย์ (hAM): ใช้เป็นโครงร่าง การวิเคราะห์อภิมานพบว่ามีประโยชน์ใน MH ที่ดื้อต่อการรักษา อัตราการปิด 57-100%
พลาสมาที่มีเกล็ดเลือดสูงด้วยปัจจัยการเจริญเติบโต (PRGF): ให้ปัจจัยการเจริญเติบโต อัตราการปิด 57-91%
แผ่นพับแคปซูลเลนส์: ใช้แคปซูลส่วนเกินระหว่างการผ่าตัดต้อกระจก อัตราการปิด 75-100%
การปลูกถ่ายจอประสาทตา ตัวเองแบบเต็มความหนา (ART): ปลูกถ่ายจอประสาทตา ส่วนรอบข้าง การวิเคราะห์อภิมานของ Hanai 2024 พบอัตราการปิด 94% ใช้ในรูที่เกิดซ้ำหรือขนาดใหญ่
เซลล์ต้นกำเนิดมีเซนไคม์ (MS C): ปิดใน 6 จาก 7 ราย
ปัจจัยการเจริญเติบโตของเส้นประสาท (NGF): อัตราการปิด MH 100% การฟื้นตัวของ EZ /ELM ก็ดีกว่าในกลุ่ม NGF
Song และคณะ (2024) รายงานผลการผ่าตัดในตา 8 ข้างที่มีรูจอประสาทตา ร่วมกับจอประสาทตา เสื่อมชนิดสี6) การปิดรูเกิดขึ้นในทุกตาที่ได้รับการลอก ILM และใช้การปลูกถ่ายแผ่นพับ ILM อิสระสำหรับรูขนาดใหญ่ หลังผ่าตัด การมองเห็น ดีขึ้นใน 1 ตา และคงที่ใน 7 ตา
ในทางธรรมชาติ การมองเห็น ลดลงเหลือ 0.1 หรือน้อยกว่าในกรณีส่วนใหญ่ การผ่าตัดทำให้ปิดรูได้มากกว่า 90% และการมองเห็น ดีขึ้น อย่างไรก็ตาม อาการภาพบิดเบือนมักยังคงอยู่ หากไม่ปิดในการผ่าตัดครั้งแรก ให้พิจารณาขยายบริเวณลอก ILM หรือผ่าตัดซ้ำด้วยการปลูกถ่าย ILM ตัวเอง
เนื่องจากมีความเป็นไปได้ที่จะปิดเอง (10-67%) การสังเกตอาการเป็นระยะเวลาหนึ่งหลังการบาดเจ็บจึงเป็นแนวทางเริ่มต้น การปิดเองเชื่อว่าเกิดจากเซลล์เกลียสร้างสะพานเชื่อมข้ามบริเวณที่ขาด ผู้ป่วยอายุน้อยมีความสามารถในการเพิ่มจำนวนเซลล์เกลียสูงกว่า ดังนั้นอัตราการปิดเองจึงค่อนข้างสูงกว่า
หากไม่เกิดการปิดเอง การตัดน้ำวุ้นตา (PPV ) ร่วมกับการลอกเยื่อหุ้มขอบใน (ILM ) เป็นมาตรฐานทองคำ14) มีรายงานอัตราการปิด 82-96%14) ประสิทธิภาพของการลอก ILM ยังไม่ชัดเจนในบางแง่มุม แต่ใช้เทคนิคเดียวกับรูไม่ทราบสาเหตุ หลังผ่าตัด จะมีการอัดแก๊ส (SF₆ หรือ C₃F₈) และต้องนอนคว่ำ สำหรับกรณีขนาดใหญ่หรือปิดยาก เทคนิคแผ่นพับ ILM หรือการปลูกถ่ายเยื่อหุ้มน้ำคร่ำเป็นทางเลือก14)
การวิเคราะห์อภิมานโดย Zhou และคณะ (2021) แสดงให้เห็นว่าอัตราการปิดรูด้วย PPV สูงกว่าอัตราการปิดเองอย่างมีนัยสำคัญ 15) การรอเป็นเวลานานอาจทำให้อัตราการปิดลดลง และแม้จะปิด การฟื้นฟูการมองเห็น อาจไม่เพียงพอ
สถานการณ์ แนวทาง ทันทีหลังได้รับบาดเจ็บ / ขนาดเล็ก สังเกตก่อน ไม่มีการปิดเอง PPV + ลอก ILM ขนาดใหญ่ / ปิดยาก แผ่นปิด ILM / การปลูกถ่ายเยื่อหุ้มน้ำคร่ำ
รายงานอัตราการปิดรูจอประสาทตา จากการบาดเจ็บแบบทื่อด้วยการผ่าตัดน้ำวุ้นตา สูงกว่า 90% การมองเห็น ที่ดีขึ้นขึ้นอยู่กับการปิดรูและการบาดเจ็บอื่นๆ ที่จอประสาทตา และตำแหน่งที่บาดเจ็บ
ในสายตาสั้น มาก รูจอประสาทตา อาจพัฒนาไปสู่จอประสาทตาลอก วิธีการมาตรฐานคือการผ่าตัดน้ำวุ้นตา + ลอกเยื่อหุ้มขอบใน + การอุดด้วยแก๊ส (ซิลิโคน) แม้ว่าจะดูเหมือนมีการลอกของน้ำวุ้นตา ส่วนหลัง แต่ชั้นคอร์เทกซ์ของน้ำวุ้นตา ยังคงยึดติดกับจอประสาทตา เป็นบริเวณกว้าง ชั้นคอร์เทกซ์ที่เหลือจะถูกกำจัดภายใต้การนำของ triamcinolone และเยื่อหุ้มขอบในจะถูกลอกออกประมาณ 2-3 เท่าของเส้นผ่านศูนย์กลางหัวประสาทตาโดยใช้สีย้อมชีวภาพ อัตราการกลับเข้าที่ประมาณ 70% ซึ่งต่ำกว่าจอประสาทตาลอก แบบรอยฉีกขาดทั่วไป (>90%)
การสังเกต :
LMH จำนวนมากคงที่เมื่อเวลาผ่านไป และกรณีที่ไม่แสดงอาการโดยไม่ทราบสาเหตุไม่มีข้อบ่งชี้ในการรักษา ติดตามการเปลี่ยนแปลงโครงสร้างด้วย OCT เป็นระยะ
การผ่าตัดสงวน LHEP :
พิจารณาการผ่าตัดในกรณีที่มีการมองเห็น ลดลงตามอาการ ภาพบิดเบี้ยว ที่แย่ลง หรือลักษณะของรอยบุ๋มจอประสาทตา แย่ลง เมื่อเร็วๆ นี้ เทคนิคการสงวนหรือฝัง LHEP โดยไม่ลอกออกได้รับความสนใจ
ในการวิเคราะห์อภิมาน (8 การศึกษา) โดย Yu และคณะ (2025) การปรับปรุงค่า BCVA หลังผ่าตัดในกลุ่มผ่าตัดแบบสงวน LHEP คือ −0.25 logMAR (95% CI −0.30 ถึง −0.21, P<0.00001) ซึ่งมีนัยสำคัญ11) เมื่อเทียบกับการลอกแบบดั้งเดิม ความแตกต่างของการปรับปรุง BCVA คือ −0.19 logMAR (P<0.0001) โดยกลุ่มสงวนดีกว่า สัดส่วนของผู้ป่วยที่มีการซ่อมแซม EZ หลังผ่าตัดก็สูงกว่าอย่างมีนัยสำคัญในกลุ่มสงวน (OR 2.55; 95% CI 1.48 ถึง 4.38)11) ไม่มีรายงานการเกิด FTMH หลังผ่าตัดในกลุ่มสงวน LHEP11)
หากการมองเห็น ดีและไม่มีอาการ主观 มักไม่ต้องผ่าตัดและติดตามอาการ หากมีอาการ主观 เช่น การมองเห็น ลดลงหรือภาพบิดเบี้ยว รุนแรง ให้พิจารณาการตัดน้ำวุ้นตา เช่นเดียวกับการรักษาเยื่อเหนือจอประสาทตา ในการตัดน้ำวุ้นตา จะลอกเยื่อเหนือจอประสาทตา และเยื่อลิมิตติ้งชั้นในออก
อาจเกิดภาวะแทรกซ้อนทั่วไปของการตัดน้ำวุ้นตา ได้
จอประสาทตาฉีกขาด 3–17% มักเกิดทางด้านล่าง3) จอประสาทตาลอก 1–5% หลังผ่าตัด มักเกิดจากรอยฉีกขาดเล็กๆ ด้านล่าง ส่วนใหญ่สามารถซ่อมแซมได้โดยไม่ต้องเปิดรูอีก3) ต้อกระจก มากกว่า 80% ของตาที่ยังมีเลนส์แก้วตา เกิดต้อกระจก ภายในไม่กี่ปีหลังผ่าตัด ค่ามัธยฐาน 14 เดือนต้องผ่าตัดต้อกระจก และ 98% ต้องผ่าตัดในระยะติดตามเฉลี่ย 91 เดือน3) หลังผ่าตัดต้อกระจก 11% ของรูที่ปิดแล้วเปิดอีก และความเสี่ยงในการเปิดอีกเพิ่มขึ้น 7 เท่าเมื่อเกิด CME 3) DONF L (ชั้นใยประสาทตาที่แยกออก) : อาจพบลักษณะคล้ายข้อบกพร่องตามแนวใยประสาทตาหลังลอก ILM หลายเดือน ไม่ใช่ข้อบ่งชี้ของข้อบกพร่องลานสายตาการเปิดอีก : สูงถึง 10% ของรูที่ปิดสำเร็จอาจเปิดอีก แต่การลอก ILM ช่วยลดความเสี่ยง3) ข้อบกพร่องลานสายตา : เดิมเกิดใน 20% แต่ลดลงด้วยการใช้เกจเล็กและการให้สารน้ำความดันต่ำ3) เยื่อบุตาอักเสบ หลังผ่าตัด3) พบได้ยากแต่รุนแรง
ในขณะที่มีแก๊สอยู่ในตา ห้ามขึ้นเครื่องบินหรือเดินทางไปที่สูง ความดันในตาที่เพิ่มขึ้นอาจทำให้เกิดภาวะแทรกซ้อนรุนแรง
การใช้ยาสลบไนตรัสออกไซด์ (แก๊สหัวเราะ) ก็เป็นข้อห้ามในขณะที่มีแก๊สในตา
จำเป็นต้องมาตรวจติดตามเป็นระยะหลังการผ่าตัด มีรายงานการเปิดซ้ำอีกหลังปิดรูได้น้อยมาก
ในรูจอประสาทตา ที่เกี่ยวข้องกับสายตาสั้น สูง เนื่องจากการดึงรั้งจากสตาฟิโลมาส่วนหลัง ยังคงอยู่ การผ่าตัดวุ้นตา เพียงอย่างเดียวอาจปิดรูได้ยาก
ในกรณีที่เกิดจากอุบัติเหตุร่วมกับจอประสาทตาลอก จำเป็นต้องผ่าตัดฉุกเฉิน
Q
หลังผ่าตัดต้องใช้เวลานานเท่าใดการมองเห็นจึงจะฟื้นตัว?
A
การมองเห็น ก่อนผ่าตัด ขนาดของรู และระยะเวลาที่เป็นโรค ส่งผลต่อพยากรณ์โรคด้านการมองเห็น ค่ามัธยฐานของการมองเห็น หลังผ่าตัดประมาณ 20/40 (0.5) การมองเห็น ดีขึ้นต่อเนื่องนานถึง 3 ปีหลังผ่าตัด และคงอยู่นาน 5-10 ปี 3) อาการภาพบิดเบือนมักยังคงอยู่ ระยะเวลาที่เป็นโรคนานขึ้น พยากรณ์โรคยิ่งแย่ลง หากเกิน 2-3 ปี อัตราการปิดรูจะลดลงเหลือ 63% 3) ในกรณีที่เกิดจากอุบัติเหตุ การบาดเจ็บอื่นๆ ที่ร่วมกับรูจอประสาทตา ก็ส่งผลต่อพยากรณ์โรคด้านการมองเห็น เช่นกัน
การเกิดรูจอประสาทตา โดยไม่ทราบสาเหตุมีความเกี่ยวข้องอย่างมากกับระยะเริ่มต้นของการหลุดของวุ้นตา ส่วนหลัง (PVD ) 2) ในกระบวนการสูงอายุปกติ PVD จะเริ่มจากบริเวณรอบรอยบุ๋มจอประสาทตา และดำเนินไป 4 ระยะ ในระยะที่ 1 วุ้นตา จะหลุดบริเวณรอบรอยบุ๋มแต่ยังคงยึดติดที่รอยบุ๋ม และในที่สุดระยะที่ 4 จะหลุดจากหัวประสาทตาด้วยจนสมบูรณ์ 2)
รูจอประสาทตา เกิดขึ้นเป็นภาวะทางพยาธิวิทยาของ PVD ระยะที่ 1 มีการยึดติดของวุ้นตา ผิดปกติที่รอยบุ๋ม และด้วยแรงดึงรั้งแบบพลวัตที่เกี่ยวข้องกับการเคลื่อนไหวของลูกตา ทำให้เกิดการแยกตัวระหว่างกรวยเซลล์มุลเลอร์และเซลล์รับแสง 2) ในการตรวจ OCT กระบวนการนี้จะสังเกตเห็นเป็นถุงน้ำในจอประสาทตา
หากการดึงรั้งในแนวหน้า-หลังยังคงอยู่ เยื่อลิมิตติ้งชั้นใน (ILM ) และเยื่อลิมิตติ้งชั้นนอก (ELM) จะแตกออก ทำให้เกิดการฉีกขาดของจอประสาทตา และนำไปสู่รูตลอดความหนา 2)
กลไกที่การลอก ILM และการอัดแก๊สในการผ่าตัดวุ้นตา ทำให้รูปิดยังไม่เป็นที่เข้าใจอย่างสมบูรณ์ หลังการลอก ILM ในระยะแรกหลังผ่าตัด พบว่าจุดรับภาพจะเคลื่อนตัวเล็กน้อยไปทางด้านจมูกและรอยบุ๋มตามแนวกลุ่มเส้นใยประสาท การเคลื่อนที่ของจอประสาทตา นี้เชื่อว่าช่วยให้ขอบรูเข้ามาใกล้กัน
การศึกษา OCT ล่าสุดพบว่าการดึงรั้งมีส่วนเกี่ยวข้องอย่างสม่ำเสมอในการเกิด LMH ในการศึกษาของ Hsia และคณะ (2023) ในตา 50 ตาที่มีสายตาสั้น สูง พบการดึงรั้งในทุกกระบวนการเกิด LMH 9) มีการระบุกระบวนการเกิดที่เกี่ยวข้องกับการดึงรั้ง 4 แบบ
ชนิดที่ 1 : การฉีกขาดของเนื้อเยื่อรอยบุ๋มเนื่องจากการดึงรั้งระหว่างวุ้นตา กับจอประสาทตา สอดคล้องกับรูปแบบที่ล้มเหลวของการเกิด FTMH 9) ชนิดที่ 2 : การแตกของผนังด้านในของถุงน้ำพาราฟอฟเวียลเนื่องจากเยื่อเหนือจอประสาทตา หรือจอประสาทตา หลุดลอก พบบ่อยที่สุด (64%) 9) .ชนิดที่ 3 : การเปิดหลังคาของถุงน้ำฟอฟเวียลที่เกิดจากเยื่อเหนือจอประสาทตา หรือแรงดึงของวุ้นตา 9) .ชนิดที่ 4 : การบางลงของฟอฟเวียลแบบก้าวหน้าเนื่องจากแรงดึงอย่างต่อเนื่องของเยื่อเหนือจอประสาทตา โดยไม่มีการสร้างถุงน้ำ ทุกรายดำเนินไปเป็น FTMH และมีการพยากรณ์โรคที่แย่ที่สุด 9) .
มีรายงานว่า LMH บางส่วนสามารถปิดได้เอง Catania และคณะ (2024) รายงานการปิดเองใน 11 จาก 187 รายชนิดเสื่อม (5.9%) และ 10 จาก 200 รายชนิดผสม (5.0%) 10) ค่ามัธยฐานของระยะเวลาการปิดคือ 4 ปี 10) .
ในกลุ่มที่ปิด ความถี่ของขอบด้านในสะท้อนแสงสูง (HIB) และเส้นสะท้อนแสงสูงในชั้นพลีซิฟอร์มนอก (LHOP) สูงกว่ากลุ่มที่คงที่อย่างมีนัยสำคัญ 10) การค้นพบเหล่านี้อาจสะท้อนถึงการกระตุ้นร่วมกันของไมโครเกลียและเซลล์มุลเลอร์ 10) .
สายตาสั้น สตาฟิโลมา หลังและจอประสาทตา หลุดลอกแบบแมคคูลาร์มีส่วนเกี่ยวข้อง 1) การตัดวุ้นตา เพียงอย่างเดียวอาจไม่เพียงพอ และพิจารณาการใช้แถบรัดจอประสาทตา ร่วมด้วยจากอุบัติเหตุ : การเสียรูปของลูกตาและการยืดของจอประสาทตา จากการบาดเจ็บ รวมถึงการยึดเกาะที่แน่นของวุ้นตา กับจอประสาทตา ในคนหนุ่มสาวมีส่วนเกี่ยวข้อง 14) .จากยา : รอยรั่วจอประสาทตา จากทามอกซิเฟนสันนิษฐานว่าเกี่ยวข้องกับความเสื่อมของเซลล์ประสาทของเซลล์มุลเลอร์ 4) มีลักษณะเฉพาะคือข้อบกพร่องของชั้นนอก ในขณะที่ชั้นในมักจะคงอยู่กลุ่มอาการอัลพอร์ต 7) การขาดหายไปโดยสมบูรณ์ของเยื่อหุ้มลิมิตติงชั้นในเป็นปัจจัยที่ทำให้การผ่าตัดรอยรั่วจอประสาทตา ทำได้ยากไม่ใช่จากอุบัติเหตุในเด็ก : แรงดึงจากการเจริญเหนือจอประสาทตา อาจเป็นสาเหตุ มีรายงานเด็กหญิงอายุ 9 ปีที่รอยรั่วปิดภายใน 1 เดือนหลังการลอกเยื่อหุ้มลิมิตติงชั้นในและการอัดแก๊ส C₃F₈ การมองเห็น ดีขึ้นเป็น 20/40 หลัง 1 ปี 8) .
เนื้อหาต่อไปนี้อยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิกในปัจจุบัน และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับการพัฒนาทางการแพทย์ในอนาคต
Ocriplasmin (ocriplasmin) เป็น serine protease ขนาด 27 kDa ที่ย่อยสลายการยึดเกาะระหว่างวุ้นตา และจอประสาทตา ด้วยเอนไซม์ 1) ขนาดยาคือการฉีดเข้าในวุ้นตา ครั้งเดียว 0.125 mcg/0.1 mL 2) ข้อบ่งชี้จำกัดเฉพาะกรณี “VMT แบบต่อเนื่อง + iFTMH <400 μm + ไม่มี ERM ” 2)
ในการทดลอง MIVI -TRUST 28 วันหลังฉีด การปลดการยึดเกาะวุ้นตา จุดรับภาพเกิดขึ้นใน 26.5% ของกลุ่ม ocriplasmin (เทียบกับ 10.1% ในกลุ่มยาหลอก) และอัตราการปิดรูคือ 40.6% ในกลุ่ม ocriplasmin (เทียบกับ 10.6% ในกลุ่มยาหลอก) ในการวิเคราะห์อภิมาน IPD ของ RCOphth (1,067 ราย) อัตราการปิด iFTMH คือ 36.8% (กลุ่มควบคุม 9.3%, OR 6.1) การมองเห็น ดีขึ้น +5.97 ตัวอักษร (กลุ่มควบคุม +3.33 ตัวอักษร, ความแตกต่าง +2.32 ตัวอักษร) 2)
ผลข้างเคียงรวมถึงการเปลี่ยนแปลงของ ERG (ความกว้างลดลง 40%, 81.3% ฟื้นตัวระหว่างการติดตามผล), ภาวะบกพร่องการมองเห็น สี (4.5% เทียบกับกลุ่มควบคุม 0.6%) และเลนส์ตาย่อยหลุด 2) ในทางปฏิบัติทางคลินิกจริง ประสิทธิภาพมีแนวโน้มต่ำกว่า RCT และอัตราการนำไปใช้กำลังลดลง 2)
ในการทดลอง DRCR Retina Network Protocol AH ได้ทำการฉีด C₃F₈ 100% ปริมาตร 0.3 mL เข้าในวุ้นตา ในรูจอประสาทตา ขนาดเล็ก (มัธยฐาน 79 μm) อัตราการปิดคือ 29% (ช่วงความเชื่อมั่น 95% 16-45%) แต่ เกิดการฉีกขาดและจอประสาทตาลอก ใน 12% (7/59 ตา, ช่วงความเชื่อมั่น 95% 6-23%) ทำให้ต้องหยุดการทดลอง 2) ห้ามใช้ในผู้ป่วยที่มีความเปราะบางของจอประสาทตา ส่วนปลาย 2)
สำหรับรูจอประสาทตา ชนิดดื้อหรือเป็นซ้ำ กำลังมีการทดลองใช้วัสดุชีวภาพชนิดใหม่ 1)
เยื่อหุ้มน้ำคร่ำมนุษย์ (human amniotic membrane) : วางเป็นโครงยึดภายในรูเพื่อส่งเสริมการเคลื่อนที่และการเพิ่มจำนวนของเซลล์เกลีย 1) การปลูกถ่ายจอประสาทตา ตนเองแบบเต็มความหนา (ART) : การปลูกถ่ายจอประสาทตา จากส่วนปลาย ในการวิเคราะห์อภิมานของ Hanai 2024 อัตราการปิด 94% 1) เซลล์ต้นกำเนิดมีเซนไคม์ (MS C) : มีรายงานการปิดรูใน 6 จาก 7 ราย 1) ปัจจัยการเจริญเติบโตของเส้นประสาท (NGF) : อัตราการปิดรูจอประสาทตา 100% การฟื้นตัวของ EZ /ELM ก็ดีกว่าในกลุ่ม NGF 1)
การผ่าตัดสงวน LHEP ได้รับการพัฒนาอย่างรวดเร็วในช่วงไม่กี่ปีที่ผ่านมา มีรายงานเทคนิคการฝังแผ่นพับคู่ของ ILM ที่ลอกออกและ LHEP เข้าไปในรู 11) จำเป็นต้องมีการทดลองแบบสุ่มที่มีกลุ่มควบคุมไปข้างหน้าในอนาคต 11)
HIB และ LHOP ที่ตรวจพบโดยการประมวลผลภาพอาจเป็นตัวทำนายการปิดเองของ LMH 10) การตรวจสอบตัวบ่งชี้เหล่านี้ในการศึกษาไปข้างหน้าเป็นที่คาดหวังในอนาคต
การบำบัดฟื้นฟูจอประสาทตา โดยใช้สเต็มเซลล์ยังอยู่ในขั้นทดลอง 1) คาดว่าจะนำไปใช้ในการสร้างเซลล์รับแสง ใหม่และการฟื้นฟูการทำงานหลังการปิดรูจอประสาทตา
Grieco G, Carla MM, Di Stefano G, Scampoli A, Governatori L, Tombolini B, et al. Updates on surgical and nonsurgical innovations for macular hole treatment. Surv Ophthalmol. 2025 Nov 12:S0039-6257(25)00215-2. doi:10.1016/j.survophthal.2025.11.008.
Macular Hole Guidelines Group, The Royal College of Ophthalmologists. Idiopathic Full Thickness Macular Holes: Clinical Guideline. London: Royal College of Ophthalmologists; 2025. https://www.rcophth.ac.uk/resources-listing/idiopathic-full-thickness-macular-holes/
Kim SJ, Lim JI, Bailey ST, Kovach JL, Vemulakonda GA, Ying GS, et al; American Academy of Ophthalmology Preferred Practice Pattern Retina/Vitreous Committee. Idiopathic Macular Hole Preferred Practice Pattern. Ophthalmology. 2025 Feb 7:S0161-6420(24)00785-1. PMID:39918525. doi:10.1016/j.ophtha.2024.12.021.
Sohn A, Sanchez G, Mantopoulos D. Partial thickness subfoveal hole in a patient treated with tamoxifen: a case report and review of the literature. J Med Case Rep. 2022;16:471.
American Academy of Ophthalmology. Idiopathic epiretinal membrane and vitreomacular traction preferred practice pattern. 2024.
Song Y, Zhang Y, Si Y, et al. Pre- and postoperative OCT features and surgical outcomes of advanced retinitis pigmentosa with macular hole: case series and literature review. BMC Ophthalmol. 2024;24:370.
Chaudhry SG, Liew G, Fung AT. Missing internal limiting membrane during macular hole repair in Alport syndrome. Case Rep Ophthalmol. 2021;12:320-323.
Bou Said R, Kraker JA, Trejo-Lopez J, et al. Pediatric macular hole associated with vitreoretinal traction on epiretinal lesions: a case report and literature review. Retinal Cases Brief Reports. 2025;19:730-735.
Hsia Y, Lee CY, Ho TC, Yang CH, Yang CM. The development and evolution of lamellar macular hole in highly myopic eyes. Eye (Lond). 2023;37:1170-1177.
Catania F, Romano MR, Crincoli E, et al. Phenomenology of spontaneous closure in degenerative and mixed type lamellar macular hole. Eye (Lond). 2024;38:315-320.
Yu Y, Wang YY, Tian M, Yu XH. Surgical outcomes of lamellar macular hole eyes with or without preservation of lamellar hole-associated epiretinal proliferation technique: a meta-analysis. Retina. 2025;45:1996-2002.
Hubschman JP, Govetto A, Spaide RF, et al. Optical coherence tomography-based consensus definition for lamellar macular hole. Br J Ophthalmol. 2020;104:1741-1747.
Govetto A, Dacquay Y, Farajzadeh M, et al. Lamellar macular hole: two distinct clinical entities? Am J Ophthalmol. 2016;164:99-109.
Liu W, Grzybowski A. Current management of traumatic macular holes. J Ophthalmol. 2017;2017:1748135. PMID:28250720. PMCI D:PMC5292388. doi:10.1155/2017/1748135.
Zhou Q, Feng H, Lv H, et al. Vitrectomy vs. Spontaneous Closure for Traumatic Macular Hole: A Systematic Review and Meta-Analysis. Front Med. 2021;8:735968.
Szeto SKH, Lam JTW, Yu AHY, et al. Macular hole closure by internal limiting membrane flap without gas tamponade versus conventional surgery: a comparative study. Ophthalmol Retina. 2025 (in press).