จุดลอย
ลักษณะ: สิ่งลอยคล้ายแมลง เส้นด้าย หรือจุด เคลื่อนที่ในลานสายตา
สาเหตุ: การรวมตัวของคอลลาเจนในน้ำวุ้นตา การเกิดวงแหวน Weiss (วงแหวนเกลียก่อนหัวประสาทตา)
การดำเนินโรค: มักลดลงตามความรู้สึกภายในประมาณ 3 เดือน

ภาวะวุ้นตาหลุดจากจอประสาทตาส่วนหลัง (PVD) คือภาวะที่ชั้นคอร์เทกซ์วุ้นตาส่วนหลังหลุดออกจากจอประสาทตาเนื่องจากการเปลี่ยนแปลงที่เกี่ยวข้องกับอายุหรือพยาธิสภาพ หมายถึงการแยกตัวของชั้นคอร์เทกซ์วุ้นตาส่วนหลังออกจากเยื่อลิมิตันส์ชั้นในของจอประสาทตา (ILM) และการวินิจฉัย PVD ที่แม่นยำมีความสำคัญต่อการพยากรณ์โรคจอประสาทตาและวุ้นตาและการตัดสินใจผ่าตัด
เป็นที่ยอมรับอย่างกว้างขวางว่าเป็นปรากฏการณ์ทางสรีรวิทยาที่เกี่ยวข้องกับอายุ และเป็นสาเหตุที่พบบ่อยที่สุดของภาพลอย ซึ่งเป็นหนึ่งในอาการหลักที่พบบ่อยที่สุดในคลินิกจักษุ
PVD ที่เกี่ยวข้องกับอายุเพิ่มขึ้นหลังจากอายุ 40 ปี และพบได้บ่อยในผู้สูงอายุ ในตาสายตาสั้น ความถี่จะสูงกว่า และในตาสายตาสั้นมาก PVD บางส่วนเกิดขึ้นตั้งแต่อายุน้อยกว่าตาปกติ และอาจพัฒนาเป็น PVD เต็มที่1,6)
ในดวงตาที่มีสายตาสั้น PVD มักเกิดขึ้นเร็วขึ้นและสามารถเกิดขึ้นในตาอีกข้างได้ภายในระยะเวลาหนึ่ง 1,6) นอกจากนี้ยังมี PVD ที่พบโดยบังเอิญโดยไม่มีอาการ 6)
อุบัติการณ์รายปีของจอประสาทตาลอกชนิดมีรอยฉีกขาด (RRD) คือ 10-18 คนต่อ 100,000 คน 6) และการดึงรั้งของวุ้นตาเนื่องจาก PVD เป็นกลไกการเกิดที่พบบ่อยที่สุด
เมื่อ PVD สมบูรณ์ จะเกิดความขุ่นเป็นวงแหวนของคอลลาเจน (วง Weiss, วงเกลียก่อนประสาทตา) ซึ่งเกิดขึ้นเมื่อวุ้นตาหลุดจากหัวประสาทตา จะถูกรับรู้เป็นภาพลอย
โดยพื้นฐานแล้วเป็นการเปลี่ยนแปลงทางสรีรวิทยาที่เกี่ยวข้องกับอายุ และไม่ใช่โรคในตัวมันเอง อย่างไรก็ตาม การเกิด PVD อาจนำไปสู่ภาวะแทรกซ้อนร้ายแรง เช่น จอประสาทตาฉีกขาดหรือจอประสาทตาลอก ดังนั้นจึงจำเป็นต้องได้รับการตรวจตาโดยละเอียดและการติดตามผลอย่างเหมาะสม
ด้านล่างนี้คืออาการหลักที่ผู้ป่วยรับรู้เมื่อเกิด PVD ภาพลอยและเห็นแสงวาบเป็นอาการที่พบบ่อยของ PVD และส่วนใหญ่มีสาเหตุจาก PVD 17)
ยิ่งมีจำนวนจุดลอยในน้ำวุ้นตามากเท่าใด ความเสี่ยงของภาวะแทรกซ้อนก็ยิ่งสูงขึ้น เมื่อมีจุดลอยตั้งแต่ 10 จุดขึ้นไป ความเสี่ยงของการฉีกขาดของจอประสาทตาจะสูงที่สุด1)17) นอกจากนี้ จุดลอยมักจะลดลงตามความรู้สึกภายในประมาณ 3 เดือน1) มีรายงานว่าผลกระทบของจุดลอยต่อคุณภาพชีวิตเทียบเท่ากับค่า utility ก่อนการผ่าตัดต้อกระจก13) ดังนั้นจึงเป็นสิ่งสำคัญที่จะไม่มองข้ามข้อร้องเรียนของผู้ป่วย
จุดลอย
ลักษณะ: สิ่งลอยคล้ายแมลง เส้นด้าย หรือจุด เคลื่อนที่ในลานสายตา
สาเหตุ: การรวมตัวของคอลลาเจนในน้ำวุ้นตา การเกิดวงแหวน Weiss (วงแหวนเกลียก่อนหัวประสาทตา)
การดำเนินโรค: มักลดลงตามความรู้สึกภายในประมาณ 3 เดือน
แสงวาบ
ลักษณะ: แสงวาบสีขาวบริเวณรอบนอกของลานสายตา มักเกิดขึ้นในที่มืดหรือเมื่อขยับตา
สาเหตุ: น้ำวุ้นตาดึงเยื่อลิมิตติ้งชั้นใน กระตุ้นจอประสาทตาให้เกิดแสง
ความสำคัญ: แสงวาบที่เกิดขึ้นใหม่เป็นสัญญาณของการดึงรั้งที่เพิ่มขึ้นและความเสี่ยงต่อการฉีกขาด
แสงวาบเชิงลบ
ลักษณะ: แสงวาบสีดำ (แตกต่างจากแสงวาบ)
สาเหตุ: การดึงรั้งของน้ำวุ้นตาที่หัวประสาทตา → การรบกวนการขนส่งตามแนวแกน
ลักษณะพิเศษ: อาจเกิดขึ้นก่อนแสงวาบแบบคลาสสิก
มีการยืนยันอาการแสดงที่จอประสาทตาและน้ำวุ้นตาดังต่อไปนี้
อาการเห็นจุดลอยและแสงวาบที่มาพร้อมกับ PVD ต้องให้ความสนใจ ใน PVD ที่มีฝุ่นยาสูบหรือเลือดออกในวุ้นตา ควรถือว่ามีจอประสาทตาฉีกขาดและดำเนินการตรวจต่อไป
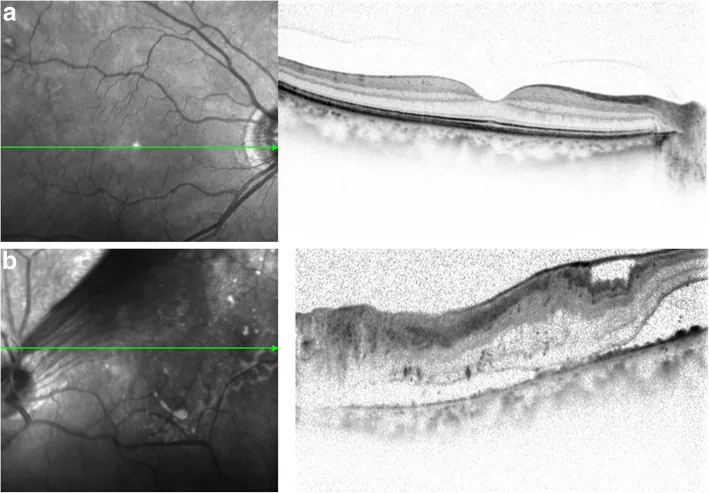
นอกจากนี้ยังสังเกตการเปลี่ยนแปลงของไฮยาโลไซต์ (เซลล์แมคโครฟาจประจำถิ่นที่รอยต่อของคอร์เทกซ์วุ้นตาส่วนหลัง) ในรายงานผู้ป่วยโดยใช้ en face OCT มีรายงานการเพิ่มขึ้นของจุดสะท้อนแสงสูงที่ถือว่าเป็นไฮยาโลไซต์ภายในคอร์เทกซ์วุ้นตาส่วนหลังของตา PVD โดยมีการเปลี่ยนแปลงรูปร่าง2) ใน PVD ที่ผิดปกติ ปฏิกิริยาของเซลล์ที่รอยต่อวุ้นตา-จอประสาทตาอาจมีส่วนในการสร้างเยื่อดึงรั้ง
เลือดออกในวุ้นตาอาจเป็นสัญญาณของจอประสาทตาฉีกขาด ในกรณีที่มีเลือดออก ความเสี่ยงของการฉีกขาดสูงถึง 50-70% ดังนั้นควรรีบไปพบจักษุแพทย์เพื่อตรวจอย่างละเอียดด้วยจอประสาทตาทางอ้อมหรืออัลตราซาวนด์ B-scan หลังจากเลือดถูกดูดซึมแล้วจะมองเห็นจอประสาทตาได้ แต่ควรพักผ่อนจนกว่าจะถึงเวลานั้น
PVD จำแนกตามผลการตรวจด้วยกล้องจุลทรรศน์ชนิดกรีดดังนี้
| การจำแนก | เนื้อหา | ความสำคัญทางคลินิก |
|---|---|---|
| PVD สมบูรณ์ (ชนิดยุบตัว) | ไม่มีความต่อเนื่องระหว่างคอร์เทกซ์วุ้นตาส่วนหลังกับจอประสาทตา วุ้นตายุบตัว | อาการค่อยๆ ลดลง |
| PVD สมบูรณ์ (ชนิดไม่ยุบตัว) | วุ้นตาเสื่อมชั้นหลังหลุดลอกแต่ไม่ยุบตัว | สังเกตอาการ |
| PVD บางส่วนที่มีการหดรัดตัว | ไม่เคลื่อนไหว (ชนิดหดรัดตัว) | แรงดึงสูง → เสี่ยงต่อการฉีกขาด |
| PVD บางส่วนที่ไม่มีการหดรัดตัว | เคลื่อนไหวได้ (ชนิดไม่หดรัดตัว) | แรงดึงค่อนข้างน้อย |
| PVD บางส่วนที่ไม่มีการหดรัดตัว (M) | วุ้นตาเกาะติดกับจอประสาทตาส่วนกลางผ่านวงแหวนก่อนจอประสาทตาส่วนกลาง | ชนิดย่อยสำคัญที่ทำให้พยากรณ์โรค ERM และ DME แย่ลง |
นอกจากนี้ ในการจำแนกระยะโดย OCT จะพบการดำเนินไปอย่างค่อยเป็นค่อยไปจากระยะ 1 (PVD รอบจอประสาทตาส่วนกลาง) ไปจนถึงระยะ 4 (PVD สมบูรณ์) การดำเนินจาก PVD บางส่วน (ระยะ 1-3) ไปสู่ PVD สมบูรณ์จะถึงจุดสูงสุดในช่วงอายุ 50-60 ปี AAO PPP 2024 ก็ใช้การจำแนก 4 ระยะที่ใกล้เคียงกัน โดยกำหนดระยะ 1 = การแยกรอบจอประสาทตาส่วนกลางที่ยังคงยึดติดกับรอยบุ๋มจอประสาทตา ระยะ 2 = การแยกจอประสาทตาส่วนกลางอย่างสมบูรณ์ ระยะ 3 = การแยกเป็นบริเวณกว้างที่ยังคงยึดติดกับหัวประสาทตา ระยะ 4 = PVD สมบูรณ์ 6) ระยะเหล่านี้ไม่ได้ดำเนินไปเป็นเส้นตรงเสมอไป 6)
PVD ตื้นแบ่งออกเป็นสองชนิด: ชนิดที่มีและไม่มีชั้นวุ้นตาชั้นหลังหนาและหดรัดตัว PVD ตื้นที่มีการหนาและหดรัดตัวพบในกลุ่มอาการดึงรั้งวุ้นตา-จอประสาทตาส่วนกลาง (VMT) และจอประสาทตาเสื่อมจากเบาหวาน และมักเกิดร่วมกับ ERM ชนิดที่ไม่มีการหนาและหดรัดตัวจัดเป็นระยะเริ่มต้นของ PVD ตามอายุ หรือ PVD ตื้นรอบรอยบุ๋มจอประสาทตาที่สัมพันธ์กับรูจอประสาทตาส่วนกลาง
สถานะของ PVD (สมบูรณ์/บางส่วน/ไม่มี) มีผลอย่างมากต่อการพยากรณ์โรคที่เกี่ยวข้อง
การเกิด PVD เกี่ยวข้องกับกลไกคู่: «การกลายเป็นของเหลว» ของวุ้นตา และ «การอ่อนแรงของการยึดเกาะ» ระหว่าง皮质วุ้นตาส่วนหลังและเยื่อ ILM 1)
ผนังด้านหลังของถุงก่อน皮质วุ้นตาส่วนหลัง (ถุง Kishi) จะค่อยๆ หลุดออกจากบริเวณรอบจุดรับภาพเมื่ออายุมากขึ้น (ระยะที่ 1) จากนั้นกลายเป็น PVD รอบรอยบุ๋มจอตา (ระยะที่ 2) ต่อมาถุงทั้งหมดจะแยกออกจากรอยบุ๋มจอตา (ระยะที่ 3) และสุดท้ายหลุดออกจากจานประสาทตา กลายเป็น PVD สมบูรณ์ (ระยะที่ 4)
การวินิจฉัย PVD ต้องใช้การตรวจหลายอย่างร่วมกัน การตรวจอวัยวะภายในตาอย่างละเอียดเพื่อดูว่ามีรอยฉีกขาดหรือไม่นั้นสำคัญที่สุด
นี่เป็นขั้นตอนแรกในการวินิจฉัยว่าอาการเห็นจุดลอยเป็นทางสรีรวิทยาหรือพยาธิสภาพ สังเกตน้ำวุ้นตาโดยใช้กล้องจุลทรรศน์ชนิดกรีดและเลนส์นูนสองด้านแบบไม่สัมผัส ปรับความกว้างของลำแสงให้แคบและความเข้มของแสงให้สูงสุด ทำการสังเกตแบบไดนามิกโดยคำนึงถึงการเคลื่อนไหวของน้ำวุ้นตา
การมีวงแหวนเกลียลก่อนหัวประสาทตา (Weiss ring) ใช้เป็นตัวบ่งชี้ว่ามี PVD หรือไม่ และจำแนกชนิดของ PVD (สมบูรณ์/บางส่วน) โดยพิจารณาจากความต่อเนื่องของคอร์เทกซ์น้ำวุ้นตาส่วนหลังกับจอประสาทตา
วงแหวนเกลียลก่อนหัวประสาทตามักไม่เป็นวงแหวนที่สมบูรณ์ และบางครั้ง PVD เกิดขึ้นโดยทิ้งวงแหวนเกลียลไว้ที่หัวประสาทตา
ในผู้ป่วยที่มีอาการเห็นจุดลอยและแสงวาบ ควรซักประวัติอย่างเป็นระบบดังนี้ 6):
แสดงการจำแนกระยะของ PVD ตามผล OCT
| ระยะ | สภาพ |
|---|---|
| ระยะ 0 | ไม่มีการแยกของผิวด้านหลังวุ้นตา |
| ระยะ 1 | การแยกบางส่วนบริเวณจอประสาทตาส่วนกลาง |
| ระยะ 2 | การแยกของขั้วหลังรวมถึงจานประสาทตา |
| ระยะ 3 | การแยกสมบูรณ์ยกเว้นฐานวุ้นตา |
| ระยะ 4 | การแยกสมบูรณ์รวมถึงฐานวุ้นตา |
ในผู้ป่วยที่มีอาการหลักคือ ภาพลอย (floaters) และแสงวาบ (photopsia) การแยกความแตกต่างระหว่างการเปลี่ยนแปลงทางสรีรวิทยาและโรคทางพยาธิวิทยาเป็นสิ่งสำคัญที่สุด
ภาพลอยที่เกิดจากความขุ่นของวุ้นตาแบบเส้นใยเล็กน้อยหรือ PVD ตามอายุ เรียกว่า ภาพลอยทางสรีรวิทยา และไม่จำเป็นต้องรักษา ในทางกลับกัน ภาพลอยที่เกิดร่วมกับจอประสาทตาฉีกขาด จอประสาทตาลอก เลือดออกในวุ้นตา หรือม่านตาอักเสบ เป็น ภาพลอยทางพยาธิวิทยา ซึ่งต้องได้รับการรักษาอย่างจริงจัง
หากพบฝุ่นบุหรี่ (tobacco dust) เลือดออก หรือ flare ควรถือว่าเป็นพยาธิสภาพและตรวจดูจอประสาทตาอย่างละเอียด ในกรณีที่มี PVD ร่วมกับแสงวาบ ควรพิจารณาถึงความเป็นไปได้ของการดึงรั้งจอประสาทตาอย่างรุนแรง และทำการตรวจจอประสาทตาอย่างละเอียด ใน PVD ที่มีฝุ่นบุหรี่หรือเลือดออกในวุ้นตา ควรสันนิษฐานว่า “มีจอประสาทตาฉีกขาดอยู่ที่ใดที่หนึ่ง” และดำเนินการตรวจต่อไป
โปรดทราบว่าปรากฏการณ์ entoptic แบบสนามสีน้ำเงิน (blue-field entoptic phenomenon) ซึ่งเห็นจุดสว่างเล็กๆ เคลื่อนที่แบบสุ่มในลานสายตาเมื่อมองแสงสีฟ้าสว่าง เช่น ท้องฟ้าสีคราม แตกต่างจากภาพลอย เกิดจากการไหลของเม็ดเลือดขาวในเส้นเลือดฝอยจอประสาทตา และไม่จำเป็นต้องรักษา
| โรคที่ต้องแยก | ลักษณะเฉพาะและจุดแยก |
|---|---|
| จอประสาทตาฉีกขาดและจอประสาทตาลอก | เครื่องหมาย Shafer’s sign บวก, ความบกพร่องของลานสายตา, เลือดออกในวุ้นตา ยืนยันด้วยจักษุแพทย์ทางอ้อม |
| เลือดออกในวุ้นตา | การมองเห็นลดลงอย่างรวดเร็ว, ภาพลอยแย่ลง แยกจอประสาทตาลอกด้วย B-scan |
| ม่านตาอักเสบ | ความขุ่นของวุ้นตา, flare มักมีอาการอักเสบในช่องหน้าม่านตาร่วมด้วย |
| เยื่อเหนือจอตา (ERM) | ภาพบิดเบี้ยวและการมองเห็นลดลง OCT แสดงการสร้างเยื่อที่จุดรับภาพ |
| กลุ่มอาการดึงรั้งวุ้นตา-จุดรับภาพ (VMT) | OCT แสดงการดึงรั้งที่จุดรับภาพ เกี่ยวข้องกับ PVD ที่ไม่สมบูรณ์ (ระยะ 1-3) |
| รูที่จุดรับภาพ | จุดบอดกลางและภาพบิดเบี้ยว OCT แสดงข้อบกพร่องตลอดความหนา |
| ประกายไฟ (aura ไมเกรน) | แสงซิกแซกในสองตา หายไปใน 15-30 นาที |
| การอุดตันของสาขาหลอดเลือดแดงจอตา | ข้อบกพร่องลานสายตาเฉียบพลัน จอตาขุ่นในภาพถ่ายจอตา |
อาการเห็นจุดลอยที่เกี่ยวข้องกับ PVD ตามอายุไม่จำเป็นต้องรักษาเชิงรุก การสังเกต เป็นพื้นฐาน 1)18) จุดลอยทางสรีรวิทยาไม่จำเป็นต้องรักษา อาการเห็นจุดลอยมักดีขึ้นตามความรู้สึกภายใน 3 เดือน และผู้ป่วยปรับตัวได้
ในกรณีจุดลอยทางพยาธิวิทยา (เกิดจากจอตาฉีกขาด จอตาลอก เลือดออกในวุ้นตา ม่านตาอักเสบ ฯลฯ) จำเป็นต้องรักษาโรคที่เป็นสาเหตุ ไม่มีวิธีป้องกัน PVD ที่พิสูจน์ได้ ไม่มีวิธีที่มีประสิทธิภาพในการป้องกันการเหลวของวุ้นตา PVD หรือ RRD 6)
แสดงนโยบายการจัดการตามประเภทของรอยโรคตาม AAO PPP 2024 6)
| ประเภทของรอยโรค | นโยบายการจัดการ |
|---|---|
| รอยฉีกขาดรูปเกือกม้าเฉียบพลันที่มีอาการ | รักษาทันที |
| รูกลมเฉียบพลันที่มีอาการพร้อมฝาปิด | อาจไม่ต้องรักษา |
| จอประสาทตาฉีกขาดแบบ dialysis เฉียบพลันที่มีอาการ | รักษาทันที |
| รอยฉีกขาดของจอประสาทตาจากการบาดเจ็บ | มักรักษา |
| รอยฉีกขาดรูปเกือกม้าไม่มีอาการ (ไม่มี RRD ระยะก่อนแสดงอาการ) | พิจารณารักษาหากไม่มีสัญญาณของภาวะเรื้อรัง |
| รูกลมไม่มีอาการพร้อมฝาปิด | ไม่ค่อยแนะนำให้รักษา |
| รอยทะลุฝ่อที่ไม่แสดงอาการ | ไม่ค่อยแนะนำให้รักษา |
| จอประสาทตาเสื่อมแบบแลตทิซที่ไม่แสดงอาการ (ไม่มีฉีกขาด) | ไม่รักษาเว้นแต่ PVD จะทำให้เกิดฉีกขาดรูปเกือกม้า |
| จุดลอยในตา | ไม่มีฉันทามติในการจัดการ หลักฐานไม่เพียงพอ |
ตารางต่อไปนี้แสดงแนวทางการติดตามผลตามภาวะต่างๆ ตาม AAO PPP 20246)
| ภาวะ | ระยะเวลาการติดตามผล |
|---|---|
| PVD ที่ไม่แสดงอาการ | ตรวจตามปกติเท่านั้น เว้นแต่มีอาการ |
| PVD ที่แสดงอาการ (ไม่มีฉีกขาด ไม่มีผลตรวจความเสี่ยงสูง) | หลังจาก 4-6 สัปดาห์ จากนั้นเมื่ออาการเปลี่ยนไป |
| PVD ที่แสดงอาการ (ไม่มีฉีกขาด มีเลือดออกในวุ้นตา/จอประสาทตา) | 1-2 สัปดาห์ขึ้นอยู่กับความรุนแรงของเลือดออกในจอประสาทตา เลือดออกในวุ้นตาทุกสัปดาห์จนกว่าจะดูดซึม อัลตราซาวนด์ B-scan หากจำเป็น |
| รอยฉีกขาดรูปเกือกม้าเฉียบพลันที่มีอาการ (หลังการรักษา) | 1-2 สัปดาห์ → 4-6 สัปดาห์ → 3-6 เดือน → หลังจากนั้นปีละครั้ง |
| รูฝาปิดเฉียบพลันที่มีอาการ | 1-4 สัปดาห์ → 1-3 เดือน → 6-12 เดือน → ปีละครั้ง |
| รอยฉีกขาดรูปเกือกม้าที่ไม่มีอาการ | 1-4 สัปดาห์ → 2-4 เดือน → 6-12 เดือน → ปีละครั้ง |
| รูฝ่อที่ไม่มีอาการ | ทุก 1-2 ปี |
| จอประสาทตาเสื่อมแบบแลตทิซ (ไม่มีรอยฉีกขาด) | ปีละครั้ง |
| รูฝ่อหรือจอประสาทตาเสื่อมแบบแลตทิซที่มีประวัติ RRD ในตาอีกข้าง | ทุก 6-12 เดือน |
เมื่อยืนยันว่ามีรอยฉีกขาด จำเป็นต้องปิดรอยฉีกขาดโดยเร็ว โรคจอประสาทตา-วุ้นตาที่เกี่ยวข้องกับ PVD เป็นข้อบ่งชี้ในการรักษาโดยการผ่าตัด เช่น การจี้จอประสาทตาด้วยแสง การผ่าตัดแบบบัคกลิง หรือการตัดวุ้นตา
การผ่าตัดน้ำวุ้นตา (PPV): เลือกใช้เมื่ออาการรบกวนคุณภาพชีวิตอย่างมีนัยสำคัญ สามารถกำจัดวงแหวนไวส์และความขุ่นในน้ำวุ้นตาได้ 1) การศึกษาไปข้างหน้าโดย Sebag และคณะ (2014) ยืนยันความปลอดภัยและประสิทธิภาพ 11) Nguyen และคณะ (2022) รายงานว่า PPV ช่วยเพิ่มความไวต่อคอนทราสต์ในตาเทียมแบบหลายจุดที่มีอาการเห็นจุดลอยตัว 19) อย่างไรก็ตาม ต้องระวังความเสี่ยงของภาวะแทรกซ้อน เช่น การติดเชื้อ จอตาลอก และการลุกลามของต้อกระจก
การตัดน้ำวุ้นตาด้วยเลเซอร์ YAG: ในการทดลองแบบสุ่มมีกลุ่มควบคุมโดย Shah และคณะ (2017) (JAMA Ophthalmol) กลุ่มที่ได้รับการตัดน้ำวุ้นตาด้วย YAG มีอัตราการดีขึ้นของอาการสูงกว่ากลุ่มหลอกอย่างมีนัยสำคัญ 10) อย่างไรก็ตาม โดยรวมสำหรับการรักษาอาการเห็นจุดลอยตัว ยังไม่มีฉันทามติในการจัดการและหลักฐานไม่เพียงพอ (AAO PPP 2024) 6) และการทบทวนอย่างเป็นระบบของ Cochrane (Kokavec และคณะ 2017) สรุปว่าหลักฐานเชิงเปรียบเทียบไม่เพียงพอ 14)
ผลกระทบต่อคุณภาพชีวิต: Wagle และคณะ (2011) รายงานว่าค่าอรรถประโยชน์ของอาการเห็นจุดลอยตัวเทียบเท่ากับก่อนผ่าตัดต้อกระจก 13) Garcia และคณะ (2016) รายงานการลดลงของความไวต่อคอนทราสต์หลัง PVD 12)
หากอาการรุนแรงและส่งผลกระทบต่อคุณภาพชีวิตอย่างมีนัยสำคัญ การผ่าตัดวุ้นตา (PPV) หรือการเลเซอร์วุ้นตาด้วย YAG (vitreolysis) เป็นทางเลือก PPV สามารถกำจัด Weiss ring และความขุ่นในวุ้นตาได้ และการศึกษาไปข้างหน้ายืนยันความปลอดภัยและประสิทธิภาพ 11) สำหรับ YAG vitreolysis การทดลองแบบสุ่มมีกลุ่มควบคุม (Shah 2017) แสดงให้เห็นการปรับปรุงอย่างมีนัยสำคัญเมื่อเทียบกับ sham 10) แต่ทั้งสองวิธียังอยู่ในระหว่างการพัฒนาเป็นมาตรฐานการรักษา และควรพิจารณาข้อบ่งชี้อย่างรอบคอบ ผลกระทบของจุดลอยต่อคุณภาพชีวิตรายงานว่าสามารถเทียบได้กับผลกระทบของต้อกระจกก่อนการผ่าตัด 13) ดังนั้นจึงเป็นสิ่งสำคัญที่จะไม่มองข้ามข้อร้องเรียนของผู้ป่วย
วุ้นตาเป็นเนื้อเยื่อโปร่งใสคล้ายวุ้นที่ครอบครองประมาณ 80% ของปริมาตรลูกตา ประกอบด้วยน้ำ 98-99% 1) ส่วนที่เหลือ 1-2% ประกอบด้วยกรดไฮยาลูโรนิก (HA) และเส้นใยคอลลาเจนชนิดที่ 2 เป็นหลัก ซึ่งสร้างโครงสร้างตาข่ายเพื่อรักษาสถานะวุ้น กรดไฮยาลูโรนิกกักเก็บน้ำปริมาณมากเพื่อเพิ่มความหนืดและรักษาโครงสร้างวุ้นของวุ้นตา เปลือกวุ้นตาส่วนหลังยึดติดกับเยื่อลิมิตติ้งชั้นใน (ILM) และมีชั้นยึดติดระหว่างกันซึ่งประกอบด้วยโปรตีนเชื่อมเส้นใย (เช่น ไฟโบรเนกติน)
จอประสาทตาและวุ้นตายึดติดแน่นเป็นพิเศษในบริเวณต่อไปนี้:
PVD ปกติเกิดขึ้นผ่านกระบวนการ “การกลายเป็นของเหลวเกิดขึ้นก่อนการอ่อนกำลังของการยึดติดอย่างสม่ำเสมอ” ในทางตรงกันข้าม ใน PVD ที่ผิดปกติ (vitreoretinal traction) แม้ว่าการกลายเป็นของเหลวจะดำเนินไป แต่การอ่อนกำลังของการยึดติดไม่สม่ำเสมอ ทำให้วุ้นตายังคงดึง ILM เฉพาะที่อย่างแรง 1)
Alsahaf และคณะ (2025) รายงานผู้ป่วย 3 รายที่มี negative dysphotopsia 4) การดึงรั้งของหัวประสาทตาโดยแก้วตาเสมือนทำให้เยื่อ Elschnig และ ILM ถูกดึง ขัดขวางการขนส่งตามแอกซอนของเซลล์ปมประสาท ทำให้เกิดจุดบอดทางประสาท (negative dysphotopsia; ND) ในกรณีที่ 1 หลังจาก ND เป็นเวลา 6 เดือน พบ PVD สมบูรณ์และจอประสาทตาฉีกขาด ได้รับการรักษาด้วยเลเซอร์ กรณีที่ 2 หลังจาก ND เป็นเวลา 5 เดือน ลุกลามเป็นจอประสาทตาลอกชนิดมีรอยฉีกขาด และต้องผ่าตัดน้ำวุ้นตา
PVD ทางสรีรวิทยาและอาการเห็นจุดลอยทางสรีรวิทยาไม่จำเป็นต้องรักษา ทันทีหลังจากเกิด PVD อาการจะรุนแรง แต่หลังจาก PVD สมบูรณ์ วงแหวน Weiss จะเคลื่อนห่างจากจอประสาทตาและอาการลดลง อาการเห็นจุดลอยมักจะลดลงตามความรู้สึกภายในประมาณ 3 เดือน 1) แม้ในการติดตามระยะยาว การจัดการตั้งแต่เนิ่นๆ เมื่อตรวจพบ PVD เป็นแนวป้องกันด่านแรกต่อ RRD 18)
เนื่องจากประมาณ 2% ที่ไม่มีการฉีกขาดครั้งแรกเกิดการฉีกขาดช้าภายในไม่กี่สัปดาห์ จึงแนะนำให้นัดตรวจซ้ำหลังจาก 4-6 สัปดาห์ 6) โดยเฉพาะอย่างยิ่งหากมีเลือดออกในน้ำวุ้นตาหรือเม็ดสี (ฝุ่นยาสูบ) จำเป็นต้องติดตามทุก 1-2 สัปดาห์ หลังจากนั้น หลักการคือมาตรวจเมื่อมีอาการเปลี่ยนแปลง หากมีอาการเห็นจุดลอยเพิ่มขึ้นใหม่ แสงวาบเพิ่มขึ้น จุดบอดในลานสายตา หรือรู้สึกเหมือนมีม่านบัง ให้รีบไปพบแพทย์ทันที
หลังจาก PVD สมบูรณ์ ส่วนประกอบของคอร์เทกซ์วุ้นตาที่เหลืออยู่บน ILM และไฮยาโลไซต์ที่ถูกกระตุ้นเป็นพื้นฐานสำหรับการสร้างเยื่อเหนือจอประสาทตา มีรายงานว่า 80-95% ของเยื่อเหนือจอประสาทตาเกิดขึ้นหลัง PVD7) และการประเมิน OCT บริเวณจุดรับภาพระหว่างการติดตาม PVD ช่วยในการตรวจพบโรคตั้งแต่ระยะแรก
การประเมินเชิงปริมาณของไฮยาโลไซต์โดยใช้ en face OCT อาจมีประโยชน์ในการทำนายความเสี่ยงของโรคที่รอยต่อระหว่างวุ้นตาและจอประสาทตา (เยื่อเหนือจอประสาทตา, VMT, รูจอประสาทตาชั้นใน) มีรายงานว่าเซลล์ที่เชื่อว่าเป็นไฮยาโลไซต์ในตาที่มี PVD สามารถมองเห็นและวัดปริมาณได้ด้วย en face OCT 2) และปฏิกิริยาของเซลล์ที่รอยต่อระหว่างวุ้นตาและจอประสาทตากำลังได้รับความสนใจในฐานะหัวข้อวิจัยใหม่
Matsui และคณะ (2025) รายงานผู้หญิงอายุ 53 ปีที่มีการหลุดลอกเองของเยื่อเหนือจอประสาทตาระยะที่ 3 ร่วมกับตาที่ไม่มี PVD 5) แม้ว่าอัตราการหลุดลอกเองของเยื่อเหนือจอประสาทตาโดยทั่วไปจะอยู่ที่ 1-3% แต่ในตาที่ไม่มี PVD อัตรานี้สูงถึง 13.4% ซึ่งสูงกว่าอัตรา 0.47-1.5% ในตาที่มี PVD อย่างมาก ผล OCT แสดงให้เห็นความหนาของเยื่อเหนือจอประสาทตาลดลงจาก 408 ไมครอนเหลือ 267 ไมครอน มีการเสนอว่าการเกิดวุ้นตาฉีกขาด (vitreoschisis) บริเวณที่ยึดเกาะระหว่างเยื่อเหนือจอประสาทตากับ ILM ในตาที่ไม่มี PVD อาจเกี่ยวข้องกับกลไกการหลุดลอกเอง
ภาพแสงลบ (แสงวาบสีดำ) มักไม่ถูกแยกความแตกต่างจากภาพแสงแบบคลาสสิก ทำให้การวินิจฉัยล่าช้า 4) ในรายงานผู้ป่วยโดย Alsahaf และคณะ (2025) ได้แสดงตัวอย่างผู้ป่วยที่มีอาการภาพแสงลบก่อนการดำเนินของ PVD จากนั้นพัฒนาเป็นจอประสาทตาฉีกขาดและจอประสาทตาลอกชนิดรีกมาโตจีนัส 4) ได้มีการเน้นย้ำถึงความสำคัญทางคลินิกของการรับรู้ภาพแสงลบว่าเป็นอาการเฉพาะ
Chen และคณะ (2023) รายงานกรณีการปิดเองของรูจอประสาทตาชั้นในในตาสายตาสั้นที่ไม่มี PVD 3) อัตราการปิดเองของรูจอประสาทตาชั้นในในสายตาสั้นรายงานไว้ประมาณ 6.2% (3.5% ในบางรายงาน) และการทำความเข้าใจกลไกที่เกิดการปิดเองแม้จะมีการดึงรั้งของวุ้นตาอย่างต่อเนื่องในกรณีที่ไม่มี PVD เป็นความท้าทายในอนาคต
ความพยายามในการฉีดสารเตรียมเอนไซม์ เช่น ออคริพลาสมิน (ocriplasmin) เข้าไปในช่องวุ้นตาเพื่อตัดการยึดเกาะระหว่างวุ้นตากับ ILM ด้วยยายังคงดำเนินต่อไป 1) ข้อบ่งใช้สำหรับกลุ่มอาการดึงรั้งวุ้นตาจุดรับภาพ (VMT) ได้รับการอนุมัติในบางประเทศ แต่ตำแหน่งของการรักษานี้ในฐานะการรักษามาตรฐานยังไม่ได้รับการกำหนด
RCT โดย Shah และคณะ (2017) ตีพิมพ์ใน JAMA Ophthalmol แสดงให้เห็นว่ากลุ่มที่ได้รับการสลายวุ้นตาด้วย YAG มีอัตราการดีขึ้นของอาการสูงกว่ากลุ่มหลอกอย่างมีนัยสำคัญ 10) ในทางกลับกัน การทบทวนวรรณกรรมอย่างเป็นระบบของ Cochrane (Kokavec และคณะ 2017) สรุปว่าหลักฐานเปรียบเทียบระหว่างการสลายวุ้นตาด้วย YAG และ PPV ยังไม่เพียงพอ 14) และการสร้างฉันทามติเกี่ยวกับการรักษาภาพลอยตา (myodesopsia) ยังคงเป็นความท้าทายในอนาคต
Garcia และคณะ (2016) รายงานว่าความไวต่อคอนทราสต์ความถี่สูงลดลงอย่างมีนัยสำคัญหลัง PVD 12) Nguyen และคณะ (2022) แสดงให้เห็นว่าความไวต่อคอนทราสต์ดีขึ้นหลัง PPV ในผู้ป่วยที่มีอาการเห็นจุดลอยในตาปลอมแบบหลายจุด 19) และการประเมินเชิงปริมาณของผลกระทบเชิงหน้าที่ของจุดลอยกำลังได้รับความสนใจ