مگسپران (فلوتر)
ویژگی: اجسام شناور به شکل حشره، نخ یا نقطه که در میدان دید حرکت میکنند.
علت: تجمع کلاژن زجاجیه، تشکیل حلقه وایس (حلقه گلیال پیشپاپیلاری).
سیر: معمولاً پس از حدود ۳ ماه به طور خودبهخودی کاهش مییابد.

جداشدگی زجاجیه خلفی (PVD) وضعیتی است که در آن قشر زجاجیه خلفی به دلیل تغییرات سالخوردگی یا پاتولوژیک از شبکیه جدا میشود. این به جدایی قشر زجاجیه خلفی از ILM (غشای محدود کننده داخلی شبکیه) اشاره دارد و تشخیص دقیق PVD برای پیشآگهی بیماریهای زجاجیه-شبکیه و تعیین اندیکاسیون جراحی مهم است.
این پدیده به عنوان یک پدیده فیزیولوژیک وابسته به سن شناخته میشود و شایعترین علت «مگسپرانی» است که یکی از شایعترین شکایات در کلینیکهای چشم پزشکی است.
PVD سالخوردگی پس از 40 سالگی افزایش مییابد و در افراد مسن بسیار شایع است. در چشمهای نزدیکبین، بروز آن بیشتر است و در نزدیکبینی شدید، PVD جزئی زودتر از چشمهای طبیعی رخ میدهد و ممکن است به PVD کامل پیشرفت کند1,6).
در چشمهای نزدیکبین، PVD زودتر رخ میدهد و ممکن است در مدت زمان مشخصی در چشم مقابل نیز ایجاد شود1,6). برخی موارد PVD به صورت تصادفی و بدون علامت کشف میشوند6).
بروز سالانه جداشدگی شبکیه رگماتوژن (RRD) ۱۰ تا ۱۸ نفر در هر ۱۰۰٬۰۰۰ نفر است6) و کشش زجاجیه ناشی از PVD شایعترین مکانیسم ایجاد آن است.
پس از تکمیل PVD، کدورت حلقوی کلاژن (حلقه وایس، حلقه گلیال پیشپاپیلاری) که هنگام جداشدن زجاجیه از سر عصب بینایی ایجاد میشود، به صورت مگسپران احساس میشود.
اساساً یک تغییر فیزیولوژیک مرتبط با افزایش سن است و به خودی خود بیماری محسوب نمیشود. با این حال، با شروع PVD ممکن است عوارض جدی مانند پارگی شبکیه یا جداشدگی شبکیه ایجاد شود، بنابراین معاینه دقیق چشمپزشکی و پیگیری در زمان مناسب ضروری است.
علائم ذهنی اصلی که در شروع PVD ایجاد میشوند در زیر آورده شده است. مگسپران و فتوپسی شکایات شایع PVD هستند و اکثر موارد منشأ PVD دارند17).
هرچه تعداد مگسپران (فلوتر) بیشتر باشد، خطر عوارض افزایش مییابد. اگر تعداد مگسپران ۱۰ یا بیشتر باشد، خطر پارگی شبکیه به حداکثر میرسد 1)17). همچنین، مگسپران معمولاً پس از حدود ۳ ماه به طور خودبهخودی کاهش مییابند 1). تأثیر مگسپران بر کیفیت زندگی (QOL) با مقدار utility value قبل از جراحی آب مروارید قابل مقایسه گزارش شده است 13)، بنابراین نباید شکایت بیمار را نادیده گرفت.
مگسپران (فلوتر)
ویژگی: اجسام شناور به شکل حشره، نخ یا نقطه که در میدان دید حرکت میکنند.
علت: تجمع کلاژن زجاجیه، تشکیل حلقه وایس (حلقه گلیال پیشپاپیلاری).
سیر: معمولاً پس از حدود ۳ ماه به طور خودبهخودی کاهش مییابد.
فوتوپسی (جرقههای نوری)
ویژگی: جرقههای سفید در محیط میدان دید. معمولاً در تاریکی یا هنگام حرکت چشم ظاهر میشوند.
علت: کشش زجاجیه بر روی غشای محدود کننده داخلی (ILM) که باعث تحریک نوری شبکیه میشود.
اهمیت: فوتوپسی جدید نشانه افزایش کشش و خطر پارگی است.
فوتوپسی منفی
ویژگی: جرقههای سیاه (متفاوت از فوتوپسی).
علت: کشش زجاجیه بر روی سر عصب بینایی → اختلال در انتقال آکسونی.
ویژگی: ممکن است قبل از فوتوپسی کلاسیک ظاهر شود.
یافتههای فوندوس و زجاجیه شامل موارد زیر است.
مگسپران و فتوپسی همراه با PVD باید جدی گرفته شوند. در PVD همراه با گرد و غبار تنباکو یا خونریزی در ژل زجاجیه، باید به وجود پارگی شبکیه مشکوک شد و معاینه را بر این اساس پیش برد.
تغییرات هیالوسیتها (سلولهای ماکروفاژ ساکن در سطح قشر خلفی زجاجیه) نیز مشاهده میشود. در گزارشهای موردی OCT en face، افزایش نقاط بازتابی بالا که احتمالاً هیالوسیت هستند در قشر خلفی زجاجیه چشمهای مبتلا به PVD و تغییر شکل آنها گزارش شده است 2). در PVD غیرطبیعی، واکنش سلولی در سطح مشترک زجاجیه-شبکیه ممکن است در تشکیل غشاهای کششی نقش داشته باشد.
خونریزی زجاجیه به احتمال زیاد نشانه وجود پارگی شبکیه است. از آنجایی که در موارد همراه با خونریزی زجاجیه، خطر پارگی به 50-70٪ میرسد، سریعاً به چشمپزشک مراجعه کرده و با افتالموسکوپی غیرمستقیم یا سونوگرافی B-scan بررسی شوید. پس از جذب خون، فوندوس قابل مشاهده خواهد بود، اما در این فاصله استراحت توصیه میشود.
PVD بر اساس یافتههای لامپ شکاف به شرح زیر طبقهبندی میشود.
| طبقهبندی | شرح | اهمیت بالینی |
|---|---|---|
| PVD کامل (نوع فروپاشیده) | عدم تداوم قشر خلفی زجاجیه با شبکیه. زجاجیه فروپاشیده است | علائم به تدریج کاهش مییابند |
| PVD کامل (نوع غیر فروپاشیده) | قشر زجاجیه خلفی جدا شده اما فروپاشیده نشده است | پیگیری |
| PVD جزئی با انقباض | بدون تحرک (نوع انقباضی) | کشش قوی → خطر پارگی |
| PVD جزئی بدون انقباض | با تحرک (نوع غیر انقباضی) | کشش نسبتاً ضعیف |
| PVD جزئی بدون انقباض (M) | ژل زجاجیه از طریق حلقه پیشماکولار به ناحیه ماکولا چسبیده است | زیرگروه مهمی که پیشآگهی ERM و DME را بدتر میکند |
همچنین، در طبقهبندی مرحلهای بر اساس OCT، پیشرفت تدریجی از مرحله 1 (PVD پاراماگولار) به مرحله 4 (PVD کامل) تأیید میشود. پیشرفت از PVD جزئی (مراحل 1 تا 3) به PVD کامل در دهه 50 تا 60 سالگی به اوج خود میرسد. AAO PPP 2024 نیز تقریباً همان طبقهبندی چهار مرحلهای را اتخاذ کرده است: مرحله 1 = جداشدگی پارافووئال با چسبندگی فووئال باقیمانده، مرحله 2 = جداشدگی کامل ماکولا، مرحله 3 = جداشدگی گسترده با چسبندگی پاپیلاری باقیمانده، مرحله 4 = PVD کامل 6). این مراحل لزوماً به صورت خطی پیشرفت نمیکنند 6).
PVD سطحی به دو دسته اصلی تقسیم میشود: آنهایی که ضخیمشدگی و انقباض قشر زجاجیه خلفی دارند و آنهایی که ندارند. PVD سطحی همراه با ضخیمشدگی و انقباض در سندرم کشش زجاجیه-ماکولا (VMT) و رتینوپاتی دیابتی دیده میشود و اغلب با ERM همراه است. موارد بدون ضخیمشدگی و انقباض یا به عنوان مراحل اولیه PVD مرتبط با سن یا به عنوان PVD سطحی پریفووئال مرتبط با سوراخ ماکولا طبقهبندی میشوند.
وضعیت PVD (کامل/جزئی/عدم PVD) به طور قابل توجهی بر پیشآگهی بیماریهای مرتبط تأثیر میگذارد.
ایجاد PVD شامل یک مکانیسم دوگانه است: «مایعشدن» زجاجیه و «تضعیف چسبندگی» بین کورتکس خلفی زجاجیه و غشای محدودکننده داخلی (ILM)1).
دیواره خلفی پاکت قدامی کورتکس خلفی زجاجیه (پاکت کیشی) با افزایش سن به تدریج از ناحیه اطراف ماکولا جدا میشود (مرحله 1) و سپس به PVD پارافووهآ (مرحله 2) تبدیل میشود. سپس پاکت به طور کامل از فووهآ جدا میشود (مرحله 3) و در نهایت از دیسک بینایی جدا شده و به PVD کامل (مرحله 4) میرسد.
تشخیص PVD نیاز به ترکیبی از چندین آزمایش دارد. به ویژه، معاینه دقیق فوندوس برای تأیید وجود یا عدم وجود پارگی بسیار مهم است.
این اولین گام برای تشخیص فیزیولوژیک یا پاتولوژیک بودن مگسپران است. زجاجیه با استفاده از لامپ شکافی و یک لنز دو محدب غیرتماسی مشاهده میشود. عرض نور شکاف را باریک و شدت نور را حداکثر تنظیم کنید و با توجه به حرکت زجاجیه، به صورت پویا مشاهده کنید.
وجود حلقه گلیال پیشپاپیلاری (Weiss ring) به عنوان نشانهای برای وجود PVD استفاده میشود و نوع PVD (کامل/ناقص) بر اساس تداوم قشر خلفی زجاجیه با شبکیه طبقهبندی میشود.
حلقه گلیال پیشپاپیلاری اغلب یک حلقه کامل نیست و گاهی PVD در حالی رخ میدهد که حلقه گلیال روی پاپیلا باقی میماند.
در بیماران با مگسپران و فوتوپسی، موارد زیر را به طور سیستماتیک بپرسید6):
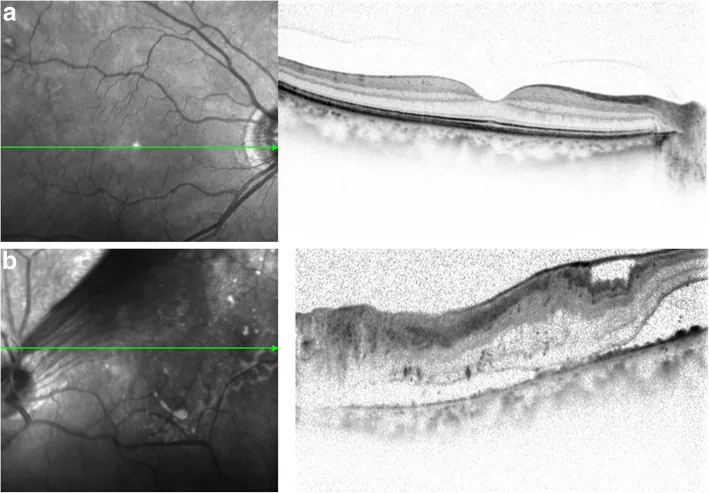
مراحل جداسازی خلفی زجاجیه بر اساس یافتههای OCT را نشان میدهد.
| مرحله | وضعیت |
|---|---|
| مرحله 0 | بدون جداشدگی سطح خلفی زجاجیه |
| مرحله 1 | جداشدگی جزئی در ناحیه ماکولا |
| مرحله 2 | جداشدگی قطب خلفی شامل دیسک بینایی |
| مرحله 3 | جداشدگی کامل به جز قاعده زجاجیه |
| مرحله 4 | جداشدگی کامل شامل قاعده زجاجیه |
در بیمارانی که با شکایت اصلی مگسپران (floaters) و فوتوپسی (photopsia) مراجعه میکنند، مهمترین نکته تمایز بین تغییرات فیزیولوژیک و بیماریهای پاتولوژیک است.
کدورتهای خفیف فیبری زجاجیه یا مگسپران ناشی از جداشدگی خلفی زجاجیه (PVD) مرتبط با افزایش سن، مگسپران فیزیولوژیک نامیده میشوند و نیاز به درمان ندارند. در مقابل، مگسپران ناشی از پارگی شبکیه، جداشدگی شبکیه، خونریزی زجاجیه، یووئیت و غیره مگسپران پاتولوژیک بوده و نیاز به درمان فعال دارند.
در صورت مشاهده گرد و غبار تنباکو (tobacco dust)، خونریزی یا فلیر (flare)، باید پاتولوژیک تلقی شده و فوندوس به طور کامل بررسی شود. در ترکیب PVD با فوتوپسی، باید احتمال کشش شدید بر شبکیه را در نظر گرفت و معاینه دقیق فوندوس انجام داد. در PVD همراه با گرد و غبار تنباکو یا خونریزی در ژل زجاجیه، باید با این فرض پیش رفت که «یک پارگی شبکیه در جایی وجود دارد» و معاینه را ادامه داد.
لازم به ذکر است که پدیده درونمیدانی آبی (blue field entoptic phenomenon) که در آن هنگام نگاه به نور آبی روشن مانند آسمان، نقاط کوچک روشنی به طور تصادفی در میدان بینایی حرکت میکنند، با مگسپران متفاوت است و ناشی از جریان گلبولهای سفید در مویرگهای شبکیه است و نیازی به درمان ندارد.
| بیماری افتراقی | ویژگیها / نکات افتراقی |
|---|---|
| پارگی شبکیه / جداشدگی شبکیه | علامت شیفر (Shafer’s sign) مثبت، نقص میدان بینایی، خونریزی زجاجیه. تأیید با افتالموسکوپی غیرمستقیم |
| خونریزی زجاجیه | کاهش ناگهانی بینایی و تشدید مگسپران. رد جداشدگی شبکیه با اسکن B |
| یووئیت | کدورت زجاجیه، فلیر. اغلب همراه با یافتههای التهابی اتاق قدامی |
| غشای اپیرتینال (ERM) | دگرگونیبینی و کاهش بینایی. OCT تشکیل غشای ماکولا را تأیید میکند |
| سندرم کشش زجاجیه-ماکولا (VMT) | OCT نشانههای کشش ماکولا را نشان میدهد. همراه با جداشدگی ناقص زجاجیه خلفی (مراحل ۱ تا ۳) |
| سوراخ ماکولا | اسکوتوم مرکزی و دگرگونیبینی. OCT نقص تمامضخامت را تأیید میکند |
| اسکوتوم سوسوزن (پیشدرآمد میگرن) | نورهای زیگزاگی دوچشمی که در ۱۵ تا ۳۰ دقیقه ناپدید میشوند |
| انسداد شاخه شریان شبکیه | نقص میدان بینایی حاد. سفیدشدگی شبکیه در فوندوس |
مگسپران ناشی از PVD مرتبط با سن نیازی به درمان فعال ندارد و پیگیری اساس کار است1)18). مگسپران فیزیولوژیک نیازی به درمان ندارند. مگسپران اغلب در عرض ۳ ماه به طور ذهنی کاهش مییابند و بیمار تطابق پیدا میکند.
در مگسپران پاتولوژیک (ناشی از پارگی شبکیه، جداشدگی شبکیه، خونریزی زجاجیه، یووئیت و غیره)، درمان بیماری زمینهای ضروری است. روش پیشگیری از PVD ثابت نشده است. هیچ روش مؤثری برای جلوگیری از مایعشدن زجاجیه، PVD و RRD وجود ندارد6).
مدیریت بر اساس نوع ضایعه بر اساس AAO PPP 2024 نشان داده شده است6).
| نوع ضایعه | مدیریت |
|---|---|
| پارگی نعل اسبی حاد علامتدار | درمان فوری |
| سوراخ گرد با درپوش حاد علامتدار | ممکن است نیازی به درمان نباشد |
| دیالیز شبکیه حاد علامتدار | درمان فوری |
| پارگی شبکیه تروماتیک | معمولاً درمان میشود |
| پارگی نعل اسبی بدون علامت (بدون RRD تحت بالینی) | در صورت عدم وجود علائم مزمن، درمان را در نظر بگیرید |
| سوراخ گرد با درپوش بدون علامت | درمان به ندرت توصیه میشود |
| سوراخ آتروفیک بدون علامت | درمان به ندرت توصیه میشود |
| دژنراسیون شبکهای بدون علامت (بدون پارگی) | تا زمانی که PVD باعث پارگی نعل اسبی نشود، درمان نمیشود |
| مگسپران (فلوتر) | هیچ اجماعی در مورد مدیریت وجود ندارد - شواهد ناکافی است |
بر اساس AAO PPP 2024، راهنمای پیگیری بر اساس وضعیت بیماری ارائه شده است6).
| وضعیت | فاصله پیگیری |
|---|---|
| PVD بدون علامت | فقط معاینات منظم مگر اینکه علائم ظاهر شوند |
| PVD علامتدار (بدون پارگی، بدون یافته پرخطر) | ۴ تا ۶ هفته بعد. سپس در صورت تغییر علائم |
| PVD علامتدار (بدون پارگی، با خونریزی زجاجیه/شبکیه) | ۱ تا ۲ هفته بعد بسته به میزان خونریزی شبکیه. خونریزی زجاجیه هفتگی تا جذب. در صورت نیاز سونوگرافی B |
| پارگی نعل اسبی حاد علامتدار (پس از درمان) | ۱-۲ هفته → ۴-۶ هفته → ۳-۶ ماه → سپس سالانه |
| سوراخ گرد با درپوش حاد علامتدار | ۱-۴ هفته → ۱-۳ ماه → ۶-۱۲ ماه → سالانه |
| پارگی نعل اسبی بدون علامت | ۱-۴ هفته → ۲-۴ ماه → ۶-۱۲ ماه → سالانه |
| سوراخ آتروفیک بدون علامت | هر ۱-۲ سال |
| دژنراسیون شبکهای (بدون پارگی) | سالانه |
| سوراخ آتروفیک یا دژنراسیون شبکهای با سابقه RRD در چشم مقابل | هر ۶-۱۲ ماه |
در صورت تأیید پارگی، بستن سریع پارگی ضروری است. بیماریهای ویترهرتینال همراه با PVD نیاز به درمان جراحی مانند فوتوکوآگولاسیون شبکیه، جراحی باکینگ یا ویترکتومی دارند.
جراحی زجاجیه (PPV): در مواردی که علائم به طور قابل توجهی کیفیت زندگی را مختل میکنند انتخاب میشود. میتواند حلقه وایس و کدورتهای زجاجیه را برطرف کند 1). مطالعه آیندهنگر Sebag و همکاران (2014) ایمنی و اثربخشی آن را تأیید کرده است 11). Nguyen و همکاران (2022) گزارش کردند که PPV حساسیت کنتراست را در چشمهای شبهفاکیک چندکانونی همراه با مگسپران بهبود میبخشد 19). با این حال، باید به خطرات عوارضی مانند عفونت، جداشدگی شبکیه و پیشرفت آب مروارید توجه کرد.
ویترئولیز با لیزر YAG: در کارآزمایی بالینی تصادفی شده Shah و همکاران (2017) (JAMA Ophthalmol)، گروه ویترئولیز YAG بهبود علائم معنیداری نسبت به گروه شم داشت 10). با این حال، در مورد درمان کلی مگسپران «هیچ اجماعی در مدیریت وجود ندارد و شواهد ناکافی است» (AAO PPP 2024) 6) و مرور کاکرین (Kokavec و همکاران 2017) نیز شواهد مقایسهای را ناکافی نتیجهگیری کرده است 14).
تأثیر بر کیفیت زندگی: Wagle و همکاران (2011) گزارش کردند که ارزش مطلوبیت مگسپران در سطح مشابهی با قبل از جراحی آب مروارید است 13). Garcia و همکاران (2016) کاهش حساسیت کنتراست پس از PVD را گزارش کردند 12).
اگر علائم به طور قابل توجهی کیفیت زندگی را مختل کنند، ویترکتومی (PPV) یا لیزر ویترئولیز YAG (vitreolysis) گزینههای درمانی هستند. PPV میتواند حلقه وایس و کدورتهای زجاجیه را برطرف کند و مطالعات آیندهنگر ایمنی و اثربخشی آن را تأیید کردهاند 11). در مورد ویترئولیز YAG، یک کارآزمایی بالینی تصادفیشده (شاه ۲۰۱۷) بهبود قابل توجهی را نسبت به گروه شم نشان داده است 10)، اما هر دو روش هنوز به عنوان درمان استاندارد تثبیت نشدهاند و اندیکاسیون آنها باید با احتیاط ارزیابی شود. گزارش شده است که تأثیر مگسپران بر کیفیت زندگی با تأثیر قبل از عمل آب مروارید قابل مقایسه است 13)، بنابراین نباید شکایت بیماران را نادیده گرفت.
زجاجیه یک بافت ژلهای شفاف است که حدود ۸۰٪ حجم چشم را تشکیل میدهد و ۹۸-۹۹٪ آن از آب تشکیل شده است 1). ۱-۲٪ باقیمانده عمدتاً از اسید هیالورونیک (HA) و فیبرهای کلاژن نوع II تشکیل شده است که یک شبکه ایجاد کرده و حالت ژلهای را حفظ میکنند. اسید هیالورونیک مقدار زیادی آب را نگه میدارد و ویسکوزیته را افزایش میدهد و ساختار ژلهای زجاجیه را حفظ میکند. قشر خلفی زجاجیه به غشای محدود کننده داخلی (ILM) چسبیده است و یک لایه چسبندگی از پروتئینهای اتصال فیبری (مانند فیبرونکتین) بین آنها وجود دارد.
شبکیه و زجاجیه در نواحی زیر به طور ویژهای محکم به هم چسبیدهاند:
PVD طبیعی با فرآیند «مایعشدن اولیه و تضعیف یکنواخت چسبندگی» رخ میدهد. در مقابل، در PVD غیرطبیعی (کشش زجاجیهای-شبکیهای)، با وجود پیشرفت مایعشدن، تضعیف چسبندگی ناهموار است و زجاجیه به صورت موضعی ILM را به شدت میکشد 1).
الساهف و همکاران (2025) سه مورد از دیسفوتوپسی منفی را گزارش کردند 4). فرض بر این است که کشش سر عصب بینایی توسط زجاجیه، غشای السنیگ و لایه محدود کننده داخلی را کشیده و با اختلال در انتقال آکسونی سلولهای گانگلیونی، اسکوتوم نوروپاتیک (دیسفوتوپسی منفی) ایجاد میکند. در مورد اول، پس از ۶ ماه دیسفوتوپسی منفی، جداشدگی کامل زجاجیه خلفی و پارگی شبکیه تشخیص داده شد و لیزر درمانی انجام شد. در مورد دوم، پس از ۵ ماه دیسفوتوپسی منفی، به جداشدگی رگماتوژن شبکیه پیشرفت کرد و نیاز به ویترکتومی شد.
جداشدگی فیزیولوژیک زجاجیه خلفی و مگسپرانی فیزیولوژیک نیاز به درمان ندارند. بلافاصله پس از وقوع جداشدگی زجاجیه خلفی، علائم شدیدتر احساس میشوند، اما پس از جداشدگی کامل، حلقه وایس از شبکیه دور شده و علائم کاهش مییابند. مگسپرانی معمولاً در عرض حدود ۳ ماه به طور ذهنی کاهش مییابد 1). مطالعات طولی نشان داده است که مدیریت زودهنگام در مرحله تشخیص جداشدگی زجاجیه خلفی، اولین خط دفاعی در برابر جداشدگی رگماتوژن شبکیه است 18).
حتی در صورت عدم وجود پارگی اولیه، حدود ۲٪ در عرض چند هفته دچار پارگی دیررس میشوند، بنابراین ویزیت مجدد پس از ۴ تا ۶ هفته توصیه میشود 6). به ویژه در صورت وجود خونریزی زجاجیه یا سلولهای رنگدانهای (گرد و غبار تنباکو)، پیگیری هر ۱ تا ۲ هفته ضروری است. پس از آن، مراجعه در صورت تغییر علائم اساس کار است. در صورت افزایش جدید مگسپرانی، تشدید فوتوپسی، نقص میدان بینایی یا احساس پردهای، سریعاً مراجعه کنید.
اجزای قشر زجاجیه باقیمانده روی غشای محدود کننده داخلی (ILM) پس از تکمیل PVD و هیالوسیتهای فعال شده، بستری برای تشکیل غشای اپیرتینال (ERM) فراهم میکنند. گزارش شده است که ۸۰ تا ۹۵٪ موارد ERM پس از PVD رخ میدهد7) و ارزیابی OCT ماکولا در طی پیگیری PVD به تشخیص زودهنگام بیماری کمک میکند.
ارزیابی کمی هیالوسیتها با استفاده از en face OCT ممکن است در پیشبینی خطر بیماریهای سطح مشترک زجاجیه-شبکیه (اپیرتینال ممبران، VMT، سوراخ ماکولا) مفید باشد. گزارش شده است که در چشمهای دارای PVD، سلولهایی که تصور میشود هیالوسیت هستند را میتوان با en face OCT تجسم و کمّی کرد2) و واکنش سلولی در سطح مشترک زجاجیه-شبکیه به عنوان یک موضوع تحقیقاتی جدید مورد توجه قرار گرفته است.
Matsui و همکاران (2025) زنی 53 ساله را گزارش کردند که اپیرتینال ممبران مرحله 3 همراه با چشم بدون PVD به طور خودبهخود جدا شد5). میزان جداشدگی خودبهخودی اپیرتینال ممبران معمولاً 1-3٪ است، اما در چشمهای بدون PVD این میزان 13.4٪ است که به طور قابل توجهی بیشتر از 0.47-1.5٪ در چشمهای دارای PVD است. یافتههای OCT نشان داد که ضخامت اپیرتینال ممبران از 408 میکرومتر به 267 میکرومتر کاهش یافته است. در چشمهای بدون PVD، وتروشیز در محل اتصال اپیرتینال ممبران و ILM رخ میدهد که ممکن است در مکانیسم جداشدگی خودبهخودی نقش داشته باشد.
فتوپسی منفی (فلاشهای سیاه) اغلب از فتوپسی کلاسیک متمایز نمیشود و تشخیص آن به تأخیر میافتد4). در گزارش موردی Alsahaf و همکاران (2025)، بیمار قبل از پیشرفت PVD فتوپسی منفی را تجربه کرد و سپس به پارگی و جداشدگی رگماتوژن شبکیه پیشرفت کرد4). اهمیت بالینی تشخیص فتوپسی منفی به عنوان یک شکایت خاص مورد تأکید قرار گرفته است.
Chen و همکاران (2023) موردی از بسته شدن خودبهخودی سوراخ ماکولا در نزدیکبینی بدون PVD را گزارش کردند3). میزان بسته شدن خودبهخودی سوراخ ماکولا در نزدیکبینی 6.2٪ (در برخی گزارشها 3.5٪) است و روشن شدن مکانیسم بسته شدن خودبهخودی با وجود کشش مداوم زجاجیه در موارد بدون PVD یک چالش آینده است.
تلاش برای تزریق داخل زجاجیهای آمادههای آنزیمی مانند اوکریپلاسمین (ocriplasmin) برای قطع دارویی اتصال بین زجاجیه و ILM در حال پیشرفت است1). این روش برای نشانگان کشش زجاجیه (VMT) در برخی کشورها تأیید شده است، اما جایگاه آن به عنوان درمان استاندارد هنوز تثبیت نشده است.
کارآزمایی بالینی تصادفی شده Shah و همکاران (2017) (JAMA Ophthalmol) نشان داد که گروه زجاجیهکافت با YAG به طور معنیداری نرخ بهبود علائم بیشتری نسبت به گروه شم داشت10). از سوی دیگر، مرور کاکرین (Kokavec و همکاران 2017) نتیجه گرفت که شواهد مقایسهای برای زجاجیهکافت با YAG در مقابل PPV ناکافی است14) و ایجاد اجماع در مورد درمان مگسپران یک چالش آینده است.
گارسیا و همکاران (2016) گزارش کردند که حساسیت کنتراست با فرکانس بالا پس از جداشدگی زجاجیه خلفی (PVD) به طور قابل توجهی کاهش مییابد 12). نگوین و همکاران (2022) نشان دادند که در بیماران مبتلا به مگسپران چشم با لنزهای داخل چشمی چندکانونی، حساسیت کنتراست پس از ویترکتومی (PPV) بهبود مییابد 19)، و ارزیابی کمی تأثیر عملکردی مگسپران چشم مورد توجه قرار گرفته است.