العوائم
الخصائص: أجسام طافية تشبه الحشرات أو الخيوط أو النقاط تتحرك في مجال الرؤية.
السبب: تجمع الكولاجين الزجاجي، تكوين حلقة فايس (حلقة الدبق أمام الحليمة).
المسار: غالبًا ما تتحسن ذاتيًا في غضون 3 أشهر.

انفصال الجسم الزجاجي الخلفي (PVD) هو حالة ينفصل فيها القشر الزجاجي الخلفي عن الشبكية بسبب تغيرات مرتبطة بالعمر أو مرضية. يشير إلى انفصال القشر الزجاجي الخلفي عن الغشاء الداخلي المحدد للشبكية (ILM)، والتشخيص الدقيق لـ PVD مهم لتحديد تشخيص أمراض الشبكية والجسم الزجاجي وتحديد مؤشرات الجراحة.
يُعرف على نطاق واسع كظاهرة فسيولوجية مرتبطة بالعمر، وهو السبب الأكثر شيوعًا للعوائم، وهي واحدة من أكثر الشكاوى ترددًا في عيادات العيون.
يزداد PVD المرتبط بالعمر بعد سن الأربعين، ويوجد بشكل متكرر لدى كبار السن. في العيون قصيرة النظر، يكون التواتر أعلى، وفي حالات قصر النظر الشديد، يحدث PVD جزئي في سن مبكر مقارنة بالعيون الطبيعية، وقد يتطور إلى PVD كامل1,6).
في العيون قصيرة النظر، يحدث انفصال الجسم الزجاجي الخلفي (PVD) في وقت مبكر، وقد يحدث في العين المقابلة خلال فترة زمنية معينة 1,6). هناك أيضًا حالات PVD تُكتشف عرضيًا بدون أعراض 6).
معدل الإصابة السنوي بانفصال الشبكية الناتج عن تمزق (RRD) هو 10-18 شخصًا لكل 100,000 شخص 6)، ويعتبر الجر الزجاجي الناتج عن PVD أكثر آليات الحدوث شيوعًا.
عند اكتمال PVD، يُلاحظ عتامة حلقية من الكولاجين (حلقة فايس، الحلقة الدبقية أمام الحليمة) تنشأ عند انفصال الجسم الزجاجي عن رأس العصب البصري، وتُرى كعوائم.
بشكل أساسي، هو تغير فسيولوجي مرتبط بالشيخوخة وليس مرضًا بحد ذاته. ومع ذلك، قد يؤدي حدوث PVD إلى مضاعفات خطيرة مثل تمزق الشبكية أو انفصال الشبكية، لذلك من الضروري إجراء فحص عيون شامل ومتابعة في الوقت المناسب.
فيما يلي الأعراض الذاتية الرئيسية التي تحدث عند ظهور PVD. العوائم وميض الضوء هي شكاوى نموذجية لـ PVD، ومعظمها ينشأ من PVD 17).
كلما زاد عدد العوائم، زاد خطر المضاعفات. عندما يكون هناك 10 عوائم أو أكثر، يكون خطر تمزق الشبكية في أقصى حالاته1)17). كما أن العوائم تتحسن ذاتيًا عادةً في غضون 3 أشهر1). تم الإبلاغ عن أن تأثير العوائم على جودة الحياة يعادل قيمة المنفعة قبل جراحة إعتام عدسة العين13)، لذا من المهم عدم الاستهانة بشكوى المريض.
العوائم
الخصائص: أجسام طافية تشبه الحشرات أو الخيوط أو النقاط تتحرك في مجال الرؤية.
السبب: تجمع الكولاجين الزجاجي، تكوين حلقة فايس (حلقة الدبق أمام الحليمة).
المسار: غالبًا ما تتحسن ذاتيًا في غضون 3 أشهر.
وميض الضوء
الخصائص: وميض أبيض في محيط مجال الرؤية. يظهر غالبًا في الظلام أو مع حركة العين.
السبب: سحب الجسم الزجاجي للغشاء الداخلي المحدد مما يحفز الشبكية ضوئيًا.
الأهمية: الوميض الجديد هو علامة على زيادة السحب وخطر التمزق.
وميض الضوء السلبي
الخصائص: وميض أسود (يختلف عن وميض الضوء).
السبب: سحب زجاجي حليمي → اضطراب النقل المحوري.
الميزات: قد يظهر قبل وميض الضوء الكلاسيكي.
يتم تأكيد النتائج التالية في قاع العين والجسم الزجاجي.
يجب الانتباه إلى العوائم والوميض الضوئي المصاحب لانفصال الجسم الزجاجي الخلفي، وفي حالة وجود غبار التبغ أو نزيف في الجسم الزجاجي، يجب اعتبار أن هناك تمزقًا في الشبكية والمضي قدمًا في الفحص.
كما تُلاحظ تغيرات في الخلايا الزجاجية (خلايا بلعمية مقيمة في واجهة القشرة الزجاجية الخلفية). في تقارير حالة باستخدام التصوير المقطعي التوافقي البصري السطحي، تم الإبلاغ عن زيادة في النقاط عالية الانعكاس التي يُعتقد أنها خلايا زجاجية داخل القشرة الزجاجية الخلفية للعين المصابة بانفصال الجسم الزجاجي الخلفي، مع تغيرات شكلية2). في حالات الانفصال غير الطبيعي، قد تشارك التفاعلات الخلوية في واجهة الشبكية الزجاجية في تكوين الأغشية الجاذبة.
نزيف الجسم الزجاجي قد يكون علامة على وجود تمزق في الشبكية. في الحالات المصحوبة بنزيف، يصل خطر التمزق إلى 50-70%، لذا يجب مراجعة طبيب العيون فورًا لإجراء فحص شامل باستخدام منظار العين غير المباشر أو الموجات فوق الصوتية (B-scan). بعد امتصاص النزيف، يمكن رؤية قاع العين، ولكن يُنصح بالراحة حتى ذلك الحين.
يصنف انفصال الجسم الزجاجي الخلفي بناءً على نتائج الفحص بالمصباح الشقي كما يلي.
| التصنيف | المحتوى | الأهمية السريرية |
|---|---|---|
| انفصال كامل (نوع الانهيار) | لا يوجد اتصال بين القشرة الزجاجية الخلفية والشبكية. انهيار الجسم الزجاجي | تخفف الأعراض تدريجيًا |
| انفصال زجاجي كامل (غير منكمش) | انفصال القشرة الزجاجية الخلفية دون انكماش | مراقبة |
| انفصال زجاجي جزئي مع انكماش | غير متحرك (نوع منكمش) | قوة جر عالية → خطر التمزق |
| انفصال زجاجي جزئي بدون انكماش | متحرك (نوع غير منكمش) | جر ضعيف نسبيًا |
| انفصال زجاجي جزئي بدون انكماش (M) | التصاق الهلام الزجاجي بالبقعة عبر الحلقة أمام البقعية | نوع فرعي مهم يؤدي إلى سوء تشخيص ERM و DME |
بالإضافة إلى ذلك، في التصنيف المرحلي باستخدام التصوير المقطعي البصري (OCT)، يُلاحظ تطور تدريجي من المرحلة 1 (انفصال زجاجي خلفي مجاور للبقعة) إلى المرحلة 4 (انفصال زجاجي خلفي كامل). يبلغ تطور الانفصال الزجاجي الجزئي (المراحل 1-3) إلى الانفصال الكامل ذروته في العقدين الخامس والسادس من العمر. تعتمد AAO PPP 2024 أيضًا تصنيفًا مشابهًا من 4 مراحل، حيث تُعرف المرحلة 1 بأنها انفصال مجاور للبقعة مع بقاء التصاق النقرة، والمرحلة 2 بأنها انفصال كامل للبقعة، والمرحلة 3 بأنها انفصال واسع النطاق مع بقاء التصاق القرص، والمرحلة 4 بأنها انفصال زجاجي خلفي كامل 6). هذه المراحل لا تتقدم بالضرورة بشكل خطي 6).
ينقسم الانفصال الزجاجي الخلفي الضحل إلى نوعين: مع أو بدون سماكة وانكماش القشرة الزجاجية الخلفية. يُلاحظ الانفصال الزجاجي الخلفي الضحل المصحوب بالسماكة والانكماش في متلازمة الجر الزجاجي البقعي (VMT) واعتلال الشبكية السكري، وغالبًا ما يكون مصحوبًا بغشاء فوق البقعة (ERM). أما النوع غير المصحوب بالسماكة والانكماش فيُصنف إما كمرحلة مبكرة من الانفصال الزجاجي الخلفي المرتبط بالعمر أو انفصال زجاجي خلفي ضحل حول النقرة مرتبط بثقب البقعة.
تؤثر حالة انفصال الجسم الزجاجي الخلفي (كامل/جزئي/لا يوجد) بشكل كبير على تشخيص الأمراض المرتبطة.
تتضمن نشأة انفصال الجسم الزجاجي الخلفي آلية مزدوجة: «التميع» في الجسم الزجاجي و«ضعف الالتصاق» بين القشرة الزجاجية الخلفية والغشاء الداخلي المحدد 1).
ينفصل الجدار الخلفي للجيب الأمامي للقشرة الزجاجية الخلفية (جيب كيشي) تدريجيًا من حول البقعة مع التقدم في العمر (المرحلة 1)، ثم يصبح انفصالًا جزئيًا حول النقرة (المرحلة 2). ثم يبتعد الجيب بأكمله عن النقرة (المرحلة 3)، وأخيرًا ينفصل عن القرص البصري ليصبح انفصالًا كاملاً (المرحلة 4).
لتشخيص انفصال الجسم الزجاجي الخلفي، يتم الجمع بين عدة فحوصات. الفحص الدقيق لقاع العين للتحقق من وجود تمزقات هو الأكثر أهمية.
هذه هي الخطوة الأولى لتشخيص ما إذا كانت العوائم فسيولوجية أم مرضية. يتم ملاحظة الجسم الزجاجي باستخدام المصباح الشقي وعدسة محدبة ثنائية غير ملامسة. يتم ضبط عرض شعاع الضوء على ضيق وشدة الإضاءة على الحد الأقصى، ويتم إجراء الملاحظة الديناميكية مع الانتباه إلى حركة الجسم الزجاجي.
يتم التحقق من وجود انفصال الجسم الزجاجي الخلفي من خلال وجود حلقة فايس (Weiss ring) أمام القرص البصري، ويتم تصنيف نوع انفصال الجسم الزجاجي الخلفي (كامل/جزئي) بناءً على استمرارية القشرة الزجاجية الخلفية مع الشبكية.
غالبًا لا تكون حلقة فايس حلقة كاملة، وأحيانًا يحدث انفصال الجسم الزجاجي الخلفي مع ترك حلقة فايس على القرص البصري.
بالنسبة للمرضى الذين يعانون من العوائم والوميض الضوئي، يجب أخذ التاريخ المرضي بشكل منهجي وفقًا لما يلي 6):
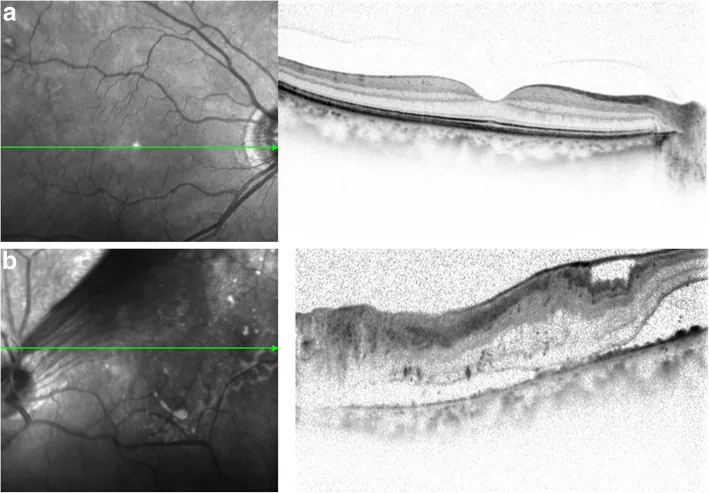
يوضح التصنيف المرحلي لانفصال الجسم الزجاجي الخلفي (PVD) بناءً على نتائج التصوير المقطعي التوافقي البصري (OCT).
| المرحلة | الحالة |
|---|---|
| المرحلة 0 | لا انفصال للسطح الخلفي للجسم الزجاجي |
| المرحلة 1 | انفصال جزئي في منطقة البقعة |
| المرحلة 2 | انفصال القطب الخلفي بما في ذلك القرص البصري |
| المرحلة 3 | انفصال كامل باستثناء قاعدة الجسم الزجاجي |
| المرحلة 4 | انفصال كامل يشمل قاعدة الجسم الزجاجي |
في المرضى الذين يشكون من العوائم والوميض الضوئي، يكون التمييز بين التغيرات الفسيولوجية والأمراض المرضية هو الأكثر أهمية.
العوائم الناتجة عن عتامات زجاجية ليفية طفيفة أو انفصال زجاجي خلفي مرتبط بالعمر تُسمى العوائم الفسيولوجية ولا تحتاج إلى علاج. بينما العوائم المصاحبة لتمزق الشبكية، انفصال الشبكية، نزف زجاجي، أو التهاب العنبية تُسمى العوائم المرضية وتتطلب علاجًا فعالًا.
إذا لوحظ وجود غبار التبغ، نزف، أو وهج، فيجب اعتبار الحالة مرضية وفحص قاع العين بدقة. في حالة انفصال زجاجي خلفي مع وميض ضوئي، يجب التفكير في إمكانية وجود جر قوي على الشبكية وإجراء فحص مفصل لقاع العين. في انفصال زجاجي خلفي مصحوب بغبار التبغ أو نزف داخل الهلام الزجاجي، يجب افتراض وجود تمزق شبكي في مكان ما والمضي قدمًا في الفحص.
تجدر الإشارة إلى أن ظاهرة الحقل الأزرق الداخلي، حيث تتحرك نقاط صغيرة مضيئة عشوائيًا في مجال الرؤية عند النظر إلى ضوء أزرق ساطع مثل السماء الزرقاء، تختلف عن العوائم، وهي ناتجة عن تدفق خلايا الدم البيضاء في الشعيرات الدموية الشبكية، ولا تحتاج إلى علاج.
| الأمراض التفريقية | الخصائص ونقاط التمييز |
|---|---|
| تمزق الشبكية وانفصال الشبكية | علامة شيفر إيجابية، عيوب في مجال الرؤية، نزف زجاجي. التأكيد بمنظار العين غير المباشر |
| نزف زجاجي | انخفاض حاد في الرؤية، تفاقم العوائم. استبعاد انفصال الشبكية بواسطة المسح بالموجات فوق الصوتية (B-scan) |
| التهاب العنبية | عتامة زجاجية، وهج. غالبًا ما يصاحبه علامات التهاب في الغرفة الأمامية |
| الغشاء فوق الشبكي (ERM) | تشوه الرؤية وانخفاض حدة البصر. يُظهر التصوير المقطعي التوافقي البصري (OCT) تشكل غشاء في النقرة. |
| متلازمة الجر الزجاجي النقري (VMT) | يُظهر التصوير المقطعي التوافقي البصري (OCT) علامات جر في النقرة. يحدث بسبب انفصال زجاجي خلفي غير كامل (المراحل 1-3). |
| الثقب النقري | عتمة مركزية وتشوه الرؤية. يُظهر التصوير المقطعي التوافقي البصري (OCT) عيبًا كامل السماكة. |
| الوميض العتمي (هالة الصداع النصفي) | ضوء متعرج في كلتا العينين، يختفي خلال 15-30 دقيقة. |
| انسداد الشريان الشبكي الفرعي | فقدان حاد في المجال البصري. يُظهر قاع العين بياضًا في الشبكية. |
لا تتطلب العوائم المرتبطة بانفصال الزجاجي الخلفي المرتبط بالعمر علاجًا نشطًا، وتكون المراقبة هي الأساس 1)18). لا تحتاج العوائم الفسيولوجية إلى علاج. غالبًا ما تتحسن العوائم ذاتيًا في غضون 3 أشهر، ويتكيف المريض معها.
في حالة العوائم المرضية (الناتجة عن تمزق الشبكية، انفصال الشبكية، نزيف الزجاجي، التهاب العنبية، إلخ)، يلزم علاج السبب الأساسي. لا توجد طرق مثبتة للوقاية من انفصال الزجاجي الخلفي. لا توجد طرق فعالة لمنع تسييل الزجاجي أو انفصال الزجاجي الخلفي أو انفصال الشبكية الروماتويدي 6).
يُظهر إرشادات الإدارة حسب نوع الآفة بناءً على AAO PPP 2024 6).
| نوع الآفة | سياسة الإدارة |
|---|---|
| تمزق حدوة الحصان الحاد المصحوب بأعراض | علاج فوري |
| ثقب دائري حاد مصحوب بأعراض مع غطاء | قد لا يحتاج إلى علاج |
| انفصال الشبكية الحاد المصحوب بأعراض | علاج فوري |
| تمزق الشبكية الرضحي | يعالج عادةً |
| تمزق حدوة الحصان غير المصحوب بأعراض (بدون انفصال شبكي تحت سريري) | النظر في العلاج إذا لم تكن هناك علامات على المزمنة |
| ثقب دائري غير مصحوب بأعراض مع غطاء | نادرًا ما يُوصى بالعلاج |
| ثقب ضموري لا عرضي | نادرًا ما يُوصى بالعلاج |
| تنكس شبكي شبكي لا عرضي (بدون تمزق) | لا تعالج ما لم يسبب انفصال الجسم الزجاجي الخلفي تمزقًا على شكل حدوة حصان |
| العوائم | لا يوجد إجماع على الإدارة، أدلة غير كافية |
يوضح الجدول التالي إرشادات المتابعة حسب الحالة بناءً على AAO PPP 20246).
| الحالة | فترة المتابعة |
|---|---|
| انفصال الجسم الزجاجي الخلفي لا عرضي | فحوصات دورية فقط ما لم تظهر أعراض |
| انفصال الجسم الزجاجي الخلفي عرضي (بدون تمزق، بدون علامات عالية الخطورة) | بعد 4-6 أسابيع، ثم عند تغير الأعراض |
| انفصال الجسم الزجاجي الخلفي عرضي (بدون تمزق، مع نزيف زجاجي/شبكي) | بعد 1-2 أسبوع حسب شدة النزيف الشبكي. النزيف الزجاجي أسبوعيًا حتى الامتصاص. تصوير بموجات فوق الصوتية (B-scan) عند الحاجة |
| تمزق حدوة الحصان الحاد المصحوب بأعراض (بعد العلاج) | 1-2 أسبوع → 4-6 أسابيع → 3-6 أشهر → ثم سنويًا |
| ثقب الغطاء الحاد المصحوب بأعراض | 1-4 أسابيع → 1-3 أشهر → 6-12 شهرًا → سنويًا |
| تمزق حدوة الحصان غير المصحوب بأعراض | 1-4 أسابيع → 2-4 أشهر → 6-12 شهرًا → سنويًا |
| ثقب ضموري غير مصحوب بأعراض | كل 1-2 سنة |
| تنكس شبكي شبيه بالشبكة (بدون تمزق) | سنويًا |
| ثقب ضموري أو تنكس شبكي شبيه بالشبكة مع تاريخ سابق لانفصال الشبكية في العين المقابلة | كل 6-12 شهرًا |
عند تأكيد وجود تمزق، يجب إغلاق التمزق فورًا. أمراض الشبكية والجسم الزجاجي المرتبطة بانفصال الجسم الزجاجي الخلفي تستدعي علاجًا جراحيًا مثل التخثير الضوئي للشبكية، جراحة الانبعاج، أو استئصال الزجاجية.
جراحة الزجاجية (استئصال الزجاجية): تُختار عندما تؤثر الأعراض بشكل كبير على جودة الحياة. يمكنها إزالة حلقة فايس وعتامات الزجاجية 1). أكدت دراسة مستقبلية أجراها سيباغ وآخرون (2014) سلامتها وفعاليتها 11). أبلغ نغوين وآخرون (2022) أن استئصال الزجاجية يحسن حساسية التباين في العيون متعددة البؤر المصابة بعوامات العين 19). ومع ذلك، يجب الانتباه إلى مخاطر المضاعفات مثل العدوى وانفصال الشبكية وتطور إعتام عدسة العين.
استئصال الزجاجية بالليزر YAG: في تجربة عشوائية محكومة أجراها شاه وآخرون (2017) (JAMA Ophthalmol)، كانت مجموعة الـ YAG vitreolysis أفضل بشكل ملحوظ من المجموعة الوهمية من حيث تحسن الأعراض 10). ومع ذلك، بالنسبة لعلاج عوامات العين بشكل عام، لا يوجد إجماع على الإدارة والأدلة غير كافية (AAO PPP 2024) 6)، وخلصت مراجعة كوكرين المنهجية (كوكافيتش وآخرون 2017) إلى أن الأدلة المقارنة غير كافية 14).
تأثير جودة الحياة: أبلغ واغل وآخرون (2011) أن قيمة المنفعة لعوامات العين مماثلة لتلك قبل جراحة إعتام عدسة العين 13). أبلغ غارسيا وآخرون (2016) عن انخفاض حساسية التباين بعد انفصال الجسم الزجاجي الخلفي 12).
إذا كانت الأعراض شديدة وتؤثر بشكل كبير على جودة الحياة، فإن جراحة الجسم الزجاجي (PPV) أو استئصال الزجاجي بالليزر YAG (vitreolysis) تكون خيارات متاحة. يمكن لـ PPV إزالة حلقة Weiss وعتامات الجسم الزجاجي، وقد أكدت الدراسات المستقبلية سلامتها وفعاليتها 11). أما بالنسبة لـ YAG vitreolysis، فقد أظهرت تجربة عشوائية محكومة (Shah 2017) تحسنًا ملحوظًا مقارنة بالعلاج الوهمي 10)، ولكن كلا الإجراءين لا يزالان في مرحلة التطوير كعلاج قياسي، ويجب تقييم المؤشرات بحذر. تشير التقارير إلى أن تأثير العوائم على جودة الحياة يمكن مقارنته بتأثير جراحة الساد قبل العملية 13)، لذا من المهم عدم التقليل من شكاوى المرضى.
الجسم الزجاجي هو نسيج هلامي شفاف يشغل حوالي 80% من حجم العين، ويتكون من 98-99% ماء 1). أما النسبة المتبقية 1-2% فتتكون أساسًا من حمض الهيالورونيك (HA) وألياف الكولاجين من النوع الثاني، والتي تشكل بنية شبكية تحافظ على الحالة الهلامية. يحتفظ حمض الهيالورونيك بكميات كبيرة من الماء لزيادة اللزوجة والحفاظ على البنية الهلامية للجسم الزجاجي. تلتصق القشرة الزجاجية الخلفية بالغشاء الداخلي المحدد (ILM)، وتوجد طبقة التصاق بينهما تتكون من بروتينات رابطة للألياف (مثل الفيبرونيكتين).
ترتبط الشبكية والجسم الزجاجي بقوة خاصة في المناطق التالية:
يحدث الانفصال الزجاجي الخلفي الطبيعي (PVD) من خلال عملية “تسييل يسبق ضعف التصاق متساوٍ”. في المقابل، في الانفصال الزجاجي الخلفي غير الطبيعي (vitreoretinal traction)، على الرغم من تقدم التسييل، يكون ضعف الالتصاق غير متساوٍ، مما يؤدي إلى استمرار سحب الجسم الزجاجي موضعيًا بقوة على ILM 1).
أبلغ ألسهف وآخرون (2025) عن 3 حالات من عسر الرؤية السلبي 4). وُجد أن جر الحليمة البصرية بواسطة الجسم الزجاجي يسحب غشاء إلشنغ والغشاء المحدد الداخلي، مما يعيق النقل المحوري للخلايا العقدية، مما يؤدي إلى عتمة عصبية (عسر الرؤية السلبي). في الحالة الأولى، بعد 6 أشهر من عسر الرؤية السلبي، تم اكتشاف انفصال زجاجي خلفي كامل وتمزق شبكي، وعولج بالليزر. في الحالة الثانية، بعد 5 أشهر من عسر الرؤية السلبي، تطور إلى انفصال شبكي انشقاقي وتطلب جراحة زجاجية.
لا يحتاج الانفصال الزجاجي الخلفي الفسيولوجي والعوامات الفسيولوجية إلى علاج. بعد حدوث الانفصال الزجاجي الخلفي مباشرة، تكون الأعراض شديدة، ولكن بعد اكتمال الانفصال، تبتعد حلقة فايس عن الشبكية وتخف الأعراض. عادةً ما تتحسن العوامات ذاتيًا في غضون 3 أشهر 1). حتى في المتابعة الطولية، تبين أن الإدارة المبكرة عند التعرف على الانفصال الزجاجي الخلفي هي خط الدفاع الأول ضد انفصال الشبكية الانشقاقي 18).
نظرًا لأن حوالي 2% من الحالات بدون تمزق أولي يصابون بتمزق متأخر في غضون أسابيع، يُوصى بإعادة الفحص بعد 4-6 أسابيع 6). خاصة إذا كان هناك نزيف زجاجي أو خلايا صبغية (غبار التبغ)، فإن المتابعة كل 1-2 أسبوع ضرورية. بعد ذلك، يكون الأساس هو الزيارة عند تغير الأعراض. إذا ظهرت زيادة جديدة في العوامات، أو زيادة في وميض الضوء، أو عيوب في المجال البصري، أو إحساس بستارة، فيجب مراجعة الطبيب فورًا.
بعد اكتمال انفصال الجسم الزجاجي الخلفي، تشكل مكونات القشرة الزجاجية المتبقية على الغشاء الداخلي للشبكية والخلايا الهيالوسية المنشطة أساسًا لتكوين الغشاء فوق الشبكي. يُذكر أن 80-95% من الأغشية فوق الشبكية تحدث بعد انفصال الجسم الزجاجي الخلفي7)، ويساهم تقييم التصوير المقطعي التوافقي البقعي أثناء متابعة انفصال الجسم الزجاجي الخلفي في الكشف المبكر عن المرض.
قد يكون التقييم الكمي للخلايا الزجاجية باستخدام التصوير المقطعي التوافقي البصري (en face OCT) مفيدًا في التنبؤ بمخاطر أمراض الواجهة الزجاجية الشبكية (الغشاء فوق الشبكي، والالتصاق الزجاجي البقعي، والثقب البقعي). تم الإبلاغ عن إمكانية تصور وقياس الخلايا التي يُعتقد أنها خلايا زجاجية في العيون المصابة بانفصال الجسم الزجاجي الخلفي (PVD) باستخدام en face OCT 2)، ويجذب التفاعل الخلوي في الواجهة الزجاجية الشبكية الاهتمام كموضوع بحثي جديد.
أبلغ ماتسوي وآخرون (2025) عن حالة لامرأة تبلغ من العمر 53 عامًا تعاني من انفصال تلقائي للغشاء فوق الشبكي من المرحلة 3 المصاحب لعين بدون انفصال الجسم الزجاجي الخلفي 5). على الرغم من أن معدل الانفصال التلقائي للغشاء فوق الشبكي يتراوح عادةً بين 1-3%، إلا أنه في العيون بدون PVD يصل إلى 13.4%، وهو أعلى بكثير من 0.47-1.5% في العيون المصابة بـ PVD. أظهرت نتائج التصوير المقطعي التوافقي البصري انخفاض سمك الغشاء فوق الشبكي من 408 ميكرومتر إلى 267 ميكرومتر. تم اقتراح أن حدوث انشقاق زجاجي (vitreoschisis) في موقع التصاق الغشاء فوق الشبكي بالغشاء الداخلي المحدد (ILM) في العيون بدون PVD قد يشارك في آلية الانفصال التلقائي.
غالبًا لا يتم تمييز الظاهرة الضوئية السلبية (الوميض الأسود) عن الظاهرة الضوئية الكلاسيكية، مما يؤدي إلى تأخير التشخيص 4). في تقرير حالة لآلسهف وآخرين (2025)، تم عرض حالة مريض عانى من الظاهرة الضوئية السلبية قبل تقدم PVD، ثم تطور إلى تمزق وانفصال شبكي انشقاقي 4). تم التأكيد على الأهمية السريرية للتعرف على الظاهرة الضوئية السلبية كشكوى محددة.
أبلغ تشن وآخرون (2023) عن حالة إغلاق تلقائي للثقب البقعي في عين قصر نظر بدون PVD 3). يبلغ معدل الإغلاق التلقائي للثقب البقعي في قصر النظر حوالي 6.2% (3.5% في بعض التقارير)، ويظل فهم الآلية التي يحدث بها الإغلاق التلقائي على الرغم من استمرار الجر الزجاجي في الحالات بدون PVD تحديًا للمستقبل.
تتقدم محاولات حقن المستحضرات الإنزيمية مثل أوكريبلازمين (ocriplasmin) في التجويف الزجاجي لقطع الالتصاق بين الجسم الزجاجي والغشاء الداخلي المحدد دوائيًا 1). تمت الموافقة على استخدامه لمتلازمة الجر الزجاجي البقعي (VMT) في بعض البلدان، لكن مكانته كعلاج قياسي لم يتم تأسيسها بعد.
أظهرت تجربة عشوائية محكومة (RCT) أجراها شاه وآخرون (2017) ونشرت في JAMA Ophthalmol أن مجموعة تحلل الزجاجية بالـ YAG كانت ذات معدل تحسن أعراض أعلى بشكل ملحوظ من المجموعة الوهمية 10). من ناحية أخرى، خلصت مراجعة كوكرين المنهجية (Kokavec وآخرون 2017) إلى أن الأدلة المقارنة بين تحلل الزجاجية بالـ YAG واستئصال الزجاجية عبر القناة (PPV) غير كافية 14)، ويظل تشكيل توافق في الآراء حول علاج العوائم (myodesopsia) تحديًا للمستقبل.
ذكر Garcia وآخرون (2016) أن حساسية التباين عالية التردد تنخفض بشكل ملحوظ بعد انفصال الجسم الزجاجي الخلفي 12). وأظهر Nguyen وآخرون (2022) تحسن حساسية التباين بعد استئصال الزجاجية لدى مرضى العوامات الزجاجية في العيون متعددة البؤر الاصطناعية 19)، مما يلفت الانتباه إلى التقييم الكمي للتأثير الوظيفي للعوامات.